My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Anales de Medicina Interna
Print version ISSN 0212-7199
An. Med. Interna (Madrid) vol.24 n.12 Dec. 2007
Tratamiento del linfoma cutáneo de células T con ligandos selectivos del receptor retinoide X: alteraciones endocrinológicas y metabólicas
Treatment of cutaneous T-cell lymphoma with retinoid receptor X-selective ligands: endocrine and metabolic disorders
M. D. Avilés Pérez, V. Luna López, I. Rodríguez Nevado1, D. de Argila Fernández-Durán1, J. Díaz Pérez de Madrid
Servicios de Endocrinología y 1Dermatología. Complejo Hospitalario Universitario. Badajoz
Dirección para correspondencia
RESUMEN
Los ligandos selectivos del receptor retinoide X se utilizan actualmente en el tratamiento de estadios avanzados del linfoma cutáneo de células T resistentes a otros tratamientos sistémicos, siendo el bexaroteno el primer fármaco de este grupo aprobado en Europa. Se han descrito numerosos efectos adversos asociados a su utilización, entre los que destacan las alteraciones endocrino-metabólicas. Presentamos a 2 pacientes con linfoma cutáneo de células T, tratados con bexaroteno, que desarrollaron hipotiroidismo central y dislipemia de forma precoz tras su inicio. Se describen también la respuesta de estas alteraciones al tratamiento y su remisión completa tras suspender el bexaroteno.
Palabras clave: Linfoma cutáneo de células B. Ligando selectivo del receptor retinoide X. Bexaroteno. Hipotiroidismo central.
ABSTRACT
The retinoid X receptor-selective ligands has been used for advanced stages of cutaneous T-cell lymphoma refractory to previous systemic therapy, being bexarotene the first drug in this group approved in Europe. Multiple drug-related adverse events has been reported such as endocrine-metabolic disorders. We report 2 patients with cutaneous T-cell lymphoma, treated with bexarotene, that developed central hypothyroidism and dislipidaemia inmediately after the begining of this treatment. We also showed the successfully treatment response of these alterations and the total clinical remission after discontinuing the drug.
Key words: Cutaneous T-cell lymphoma. Retinoid X receptor agonist. Bexarotene. Central hypothiroidism.
Introducción
Los ligandos selectivos del receptor retinoide X (RXR) son compuestos que se unen a receptores retinoides nucleares modulando la expresión génica, y de esta forma regulando la proliferación y la diferenciación celular e induciendo la apoptosis celular (1).
El bexaroteno es el primer agonista sintético selectivo de los receptores de retinoide X aprobado en Europa para el tratamiento sistémico de pacientes adultos con linfoma cutáneo de células T que han fracasado a terapias previas tales como psoralenos con ultravioleta (PUVA), mostaza nitrogenada (BNCU) o interferón alfa (2). El bexaroteno, también denominado rexinoide, se administra por vía oral, se transporta unido en alta proporción a proteinas plasmáticas, tiene metabolismo hepático por el citocromo P450 y posterior eliminación biliar. El uso del bexaroteno ha sido también propuesto, con esperanzadores resultados, para el tratamiento de otros tumores como el carcinoma pulmonar no microcítico, el cáncer de tiroides, el cáncer de próstata, mama y algunos tumores digestivos (3,4).
Las formas clínicas más frecuentes del Linfoma cutáneo de células T (LCCT) son la micosis fungoide y el síndrome de Sézary, con una incidencia anual de 3-4 casos/1.000.000 habitantes. La micosis fungoide es una enfermedad de larga evolución que habitualmente cursa con numerosas recaídas y requiere frecuentes sesiones de tratamiento con psoraleno y radiación ultravioleta (PUVA), conllevando para los pacientes un elevado riesgo de tumores dermatológicos. Por este motivo, la introducción del bexaroteno como alternativa terapéutica en estos pacientes, ha supuesto una mejoría en su pronóstico y su calidad de vida, aunque no exenta de efectos secundarios. Los efectos adversos descritos más frecuentemente con agonistas selectivos del receptor retinoide X, son la hipertrigliceridemia, el hipotiroidismo, la neutropenia y la descamación cutánea generalizada (5).
A continuación se presentan 2 casos clínicos de pacientes con LCCT tipo micosis fungoide tratados con bexaroteno. Se describe su evolución, las alteraciones hormonales y metabólicas presentadas y la respuesta al tratamiento de las mismas.
Casos aportados
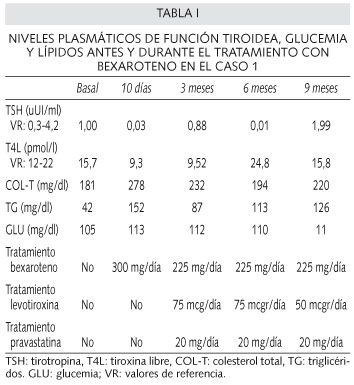
Caso 1. Mujer de 47 años con antecedentes personales de síndrome depresivo, sobrepeso (índice masa corporal: 28,6 kg/m2) y LCCT, tipo micosis fungoide estadío IB, diagnosticado 6 años antes. Inicialmente fue tratada con varios ciclos de PUVA, corticoides y mostaza nitrogenada, sin remisión completa de su enfermedad, por lo que se inicia tratamiento con bexaroteno a dosis de 300 mg/día. Se midieron los niveles de tirotropina (TSH), tiroxina libre (T4L), colesterol, triglicéridos y glucemia antes y después del inicio del tratamiento con bexaroteno (Tabla I). La paciente presentó ya a los 10 días del inicio un descenso de los niveles de TSH y T4L compatibles con hipotiroidismo central. Por otra parte, los niveles plasmáticos de glucemia y colesterol se elevaron, permaneciendo normales los parámetros de función renal y hepática, los niveles de triglicéridos y de leucocitos. Se instauró tratamiento de estas alteraciones con 75 microgramos de Levotiroxina sódica y 20 mg de Pravastatina. Se realizó estudio de función de ejes hipófiso-suprarrenal (ACTH y cortisol) e hipófiso-gonadal (LH, FSH y estradiol) siendo siempre normales. A los 3 meses, la paciente presentó mejoría de sus lesiones cutáneas por lo que se redujo la dosis de bexaroteno a 225 mg/día; esto produjo una elevación de las hormonas tiroideas que obligó a realizar un ajuste de la medicación sustitutiva.
Caso 2. Varón de 55 años diagnosticado hacía 7 años de LCCT tipo micosis fungoide estadio IVA asociado a linfoma anaplásico de células grandes (CD 30+) y sin otros antecedentes de interés. Había recibido varios ciclos de tratamiento con PUVA, corticoides sistémicos, interferón alfa y radioterapia, presentando siempre recidivas tras la suspensión de los mismos. Incluso había sido sometido a un transplante autólogo de médula ósea asociado a poliquimioterapia sin remisión completa de su enfermedad. Hacía unos 6 años y coincidiendo con el inicio del tratamiento de interferón alfa, había sido diagnosticado de hipotiroidismo primario (enfermedad tiroidea autoinmune) y desde entonces tomaba 100 microgramos diarios de Levotiroxina sódica con total normalización de la función tiroidea. Se inició tratamiento con 525 mg/día de bexaroteno asociado a PUVA, presentando en la analítica realizada a los 3 meses un descenso de los niveles de TSH y T4L que requirió aumentar la dosis sustitutiva de hormona tiroidea a 150 mcgr/día (Tabla II). Así mismo, presentó aumentó de los valores de triglicéridos y colesterol total que precisaron asociar tratamiento con fluvastatina, 20 mg/día y fenofibrato, 300 mg/día. A los 9 meses y tras suspender el bexaroteno por mejoría clínica, presentó analítica compatible con hipertiroidismo y normalización de las cifras de colesterol y triglicéridos. Al año, el paciente tuvo una nueva recidiva de la micosis fungoide y se reintrodujo el bexaroteno a dosis de 450 mg/día, volviendo a presentar descenso de los niveles de hormonas tiroideas y marcada elevación del colesterol total y los triglicéridos. La glucemia, los parámetros de función renal y hepática y las determinaciones de leucocitos permanecieron siempre dentro de la normalidad.
Discusión
El bexaroteno o rexinoide es un retinoide sintético de tipo aromático con acción selectiva sobre receptores intracelulares X (RXR) y que tiene capacidad de inhibir la proliferación de las células neoplásicas y una acción más específica sobre los mecanismos de apoptosis que los receptores de retinoides-R. Fue aprobado en Europa en 2001 para el tratamiento sistémico del linfoma cutáneo de células T en adultos que son refractarios o intolerantes a otros tratamientos. Estudios publicados previamente han demostrado que el bexaroteno es muy eficaz en la mejora de las lesiones dermatológicas, sin embargo, no está exento de importantes efectos secundarios, que mal diagnosticados o no tratados pueden empeorar la calidad de vida de estos sujetos y desencadenar otras patologías no relacionadas con su enfermedad de base. Por otra parte, novedosos ensayos clínicos han demostrado la no desdeñable utilidad en el tratamiento coadyuvante de otros tumores sólidos resistentes a tratamientos quimioterápicos convencionales, por su efecto en inhibir la angiogénesis y disminuir la formación de metástasis a distancia (6). Esto augura un futuro prometedor a los fármacos retinoides con un probable aumento de sus indicaciones terapéuticas, y por tanto, resulta importante que se conozcan bien las posibles complicaciones derivadas de su uso y la prevención y manejo de las mismas.
El hipotiroidismo es uno de los efectos secundarios más frecuentes en los pacientes tratados con bexaroteno. Se trata de un hipotiroidismo central porque hay un descenso de los niveles de TSH y una disminución secundaria de la producción de hormonas tiroideas. Aunque no se conoce a ciencia cierta cual es el mecanismo por el que esto ocurre, se cree que hay una disminución de la respuesta de la TSH hipofisaria al estímulo con hormona liberadora de tirotropina (TRH) y una disminución de la transcripción del gen de la TSHbeta en las células tirotropas. Este hipotiroidismo secundario ocurre también en sujetos sanos, es de aparición muy precoz, dosis dependiente y reversible tras la suspensión del fármaco. La capacidad de producir una disminución de la síntesis de TSH sugiere que en un futuro podrían emplearse estos fármacos como una alternativa terapéutica en adenomas productores de TSH o en síndromes de resistencia a las hormonas tiroideas con manifestaciones clínicas de hipertiroidismo. Por otra parte, y como se ha descrito en el caso 1 de nuestro trabajo, el bexaroteno no se asocia a disminución de la síntesis de otras hormonas hipofisarias (7).
Para la normalización de los niveles de hormonas tiroideas de estos pacientes se requiere habitualmente la administración de elevadas dosis de tiroxina. El segundo de los pacientes descrito en este trabajo presentaba ya un hipotiroidismo primario antes de comenzar el tratamiento con bexaroteno y con el inicio de éste requirió un incremento moderado de la dosis sustitutiva de tiroxina. Esto hace sospechar que el bexaroteno, además de suprimir la liberación hipofisaria de TSH, induce hipotiroidismo por otros mecanismos como podrían ser una exacerbación del aclaramiento periférico de las T4 y T3 circulantes. Algunos autores han demostrado que los ligandos selectivos del receptor retinoide X tienen la capacidad de incrementar la síntesis de las enzimas deiodinasa tipo 1 y deiodinasa tipo 3 y de esta forma disminuir los niveles plasmáticos de hormonas tiroideas (8). Por otra parte, otros autores han propuesto que el bexaroteno podría aumentar la actividad metabólica de enzimas del complejo cytocromo P450 (CYP3A, CYP4A) (9). No obstante, no se pueden descartar otros mecanismos por los que el bexaroteno podría inducir aumento de los requerimientos de hormonas tiroideas, tales como el dificultar una correcta absorción intestinal de la tiroxina administrada por vía oral, mecanismo ampliamente descrito con otros fármacos.
Los niveles de triglicéridos suelen elevarse también de forma precoz y pueden alcanzar valores tan altos que conlleven un riesgo de pancreatitis para el sujeto. La hipertrigliceridemia es dosis dependiente y reversible y podría deberse a que el bexaroteno aumenta la transcripción y expresión hepática de la apolipoproteína C-III (10). Al igual que ocurre con el hipotiroidismo, debe existir una predisposición individual a presentar este trastorno metabólico, pudiéndose apreciar cómo la hipertrigliceridemia ocurrió sólo en el paciente descrito en nuestro caso clínico 2. El problema generado por la hipertrigliceridemia puede ser aún mayor si ocurre en poblaciones de elevado riesgo cardiovascular como son los diabéticos y debe realizarse en ellos un tratamiento más enérgico. Así mismo, la importancia de este efecto secundario ha hecho que algunos autores recomienden el tratamiento preventivo con fibratos simultáneo al inicio con el bexaroteno (11). Este tratamiento no debe realizarse con gemfibrozilo, ya que éste es capaz de inhibir una de las enzimas responsables de la metabolización oxidativa del bexaroteno (CYP3A4), aumentar sus concentraciones plasmáticas y secundariamente su potencial toxicidad.
La hipercolesterolemia es otro posible efecto secundario favorecido por el uso del bexaroteno. Ésta, suele ser más leve y responde muy bien a dosis moderadas de estatinas. Además, en algunas ocasiones, el leve efecto que el fenofibrato tiene sobre la reducción de las cifras de LDL-colesterol es suficiente para normalizarlas. Así mismo, el hipotiroidismo inducido por estos compuestos también ejerce un papel coadyuvante en la elevación plasmática del colesterol, por lo que el simple tratamiento de éste es a veces suficiente para su normalización.
Por otra parte, algunos estudios demuestran que el bexaroteno, a través de su acción sobre receptores PPAR del tejido graso, mejora la sensibilidad a la insulina y puede llegar en sujetos diabéticos a disminuir sus necesidades de insulina exógena (12). Incluso, algunos autores han propuesto, que podrían emplearse estos fármacos en el tratamiento de la diabetes mellitus tipo 2 (7). Sin embargo, en el primer paciente descrito en este trabajo existió una discreta elevación de los niveles de glucemia basales cuando se inició el tratamiento con este análogo retinoide, sin que podamos relacionarlo con un aumento ponderal, con la asociación concomitante a otro fármaco, ni a ningún otro mecanismo etiopatogénico conocido.
Concluímos que los ligandos selectivos del receptor retinoide X, entre los que destaca el bexaroteno, son compuestos eficaces en el tratamiento del linfoma cutáneo de células T y que tienen un futuro prometedor como alternativa terapéutica en otras patologías tales como la diabetes mellitus y algunas neoplasias sólidas. El bexaroteno presenta efectos secundarios importantes y frecuentes, entre los que destacan el hipotiroidismo central y alteraciones metabólicas como la hipertrigliceridemia. No obstante, consideramos que estos efectos adversos diagnosticados y tratados precozmente no tienen por qué limitar su uso ni mermar la calidad de vida de los pacientes y coincidimos con los autores que proponen realizar una prevención de los mismos mediante la instauración desde el inicio de tratamiento con tiroxina y fibratos.
Bibliografía
1. Zhang C, Hazarika P, Ni X, Weidner DA, Duvic M. Induction of apoptosis by bexarotene in cutaneous T-cell lymphoma cells: relevante to mechanism of therapeutic action. Clin Cancer Res 2002; 8: 1234-40. [ Links ]
2. Huber MA, Staib G, Pehamberger H, Scharffetter-Kochanek K. Management of refractory early-stage cutaneous T-cell lymphoma. Am J Clin Dermatol 2006; 7: 155-69. [ Links ]
3. Esteva FJ, Glaspy J, Baidas S, Laufman L, Hutchins L, Dickler M, et al. Multicenter phase II study of oral bexarotene for patients with metastatic breast cancer. J Clin Oncol 2003; 21: 999-1006. [ Links ]
4. Haugen BR, Larson LL, Pugazhenthi U, Hays WR, Klopper JP, Kramer CA et al. Retinoic acid and retinoid X receptors are differentially expressed in thyroid cancer and thyroid carcinoma cell lines and predict response to treatment with retinoids. J Clin Endocrinol Metab 2004; 89: 272-80. [ Links ]
5. Ortiz-Romero PL, Sánchez-Largo ME, Sanz H, García-Romero D, Rosales D, Valverde R, et al. Tratamiento de micosis fungoide con PUVA más bexaroteno. Actas Dermosifiliogr 2006; 97: 311-8. [ Links ]
6. Yen WC, Prudente RY, Corpuz MR, Negro-Vilar A, Lamph WW. A selective retinoid X receptor agonist bexarotene (LGD1069, targretin) inhibits angiogenesis and metastasis in solid tumours. Br J Cancer 2006; 94: 654-60. [ Links ]
7. Golden WM, Weber KB, Hernández TL, Sherman SI, Woodmansee WW, Haugen BR. Single-dose rexinoid rapidly and specifically suppresses serum thyrotropin in normal subjects. J Clin Endocrinol Metab 2007; 92:124-30. [ Links ]
8. Sharma V, Hays W, Wood W, Pugazhenthi U, Germain D, Bianco A, et al. Effects of rexinoides on thyrotrope function and the hypothalamic-Pituitary-thyroid axis. Endocrinology 2006; 147: 1438-51. [ Links ]
9. Howell SR, Shirley MA, Ulm EH. Effects of retinoid treatment of rats on hepatic microsomal metabolism and cytochromes P450. Correlation between retinoic and acid receptor/retinoid X receptor selectivity and effects on metabolic enzymes. Drug Metab Dispos 1998; 26: 234-9. [ Links ]
10. Marco A, Familiar C, Sastre J, Cánovas B, Vicente A, López J. Alteraciones endocrino-metabólicas inducidas por bexaroteno en el tratamiento del linfoma cutáneo de células T. Endocrinol Nutr 2006; 53: 430-4. [ Links ]
11. Assaf C, Bagot M, Dummer R, Duvic M, Gniadecki R, Knobler R et al. Minimizing adverse side-effects of oral bexarotene in cutaneous T-cell lymphoma: an expert opinion. Br J Dermatol 2006; 155: 261-6. [ Links ]
12. Shen Q, Cline GW, Shulman GI, Leibowitz MD, Davies PJ. Effects of rexinoids on glucose transport and insulin-mediated signaling in skeletal muscles of diabetic (db/db) mice. J Biol Chem 2004; 279: 19721-31. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
María Dolores Avilés Pérez.
C/ Francisco Ruiz de la Mota, 32.
06011 Badajoz.
e-mail: vlunal@yahoo.es
Trabajo aceptado: 27 de julio de 2007