My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Avances en Odontoestomatología
On-line version ISSN 2340-3152Print version ISSN 0213-1285
Av Odontoestomatol vol.27 n.1 Madrid Jan./Feb. 2011
Herpesvirus
Bascones-Martínez A.**, Pousa-Castro X.*
* Alumna del Postgrado de Periodoncia de la Universidad Complutense de Madrid.
** Director del Postgrado de Periodoncia de la Universidad Complutense de Madrid.
Dirección para correspondencia
RESUMEN
El Herpesvirus (HSV) destaca por ser el principal responsable de un gran número de infecciones de la región orofacial, así como de la región genital. El virus del herpes simple es el prototipo de una gran familia de virus de doble cadena de ADN, los herpesviridiae, que causan una gran morbilidad en humanos.
La infección en las células de la mucosa epitelial da lugar a una serie de signos clínicos y a la infección latente a nivel de las neuronas sensoriales. Durante la fase de infección productiva se expresan múltiples proteínas virales mientras que en fases latentes apenas se expresan dichas proteínas. La reactivación del virus da lugar a infecciones recurrentes, desencadenando en lisis celular y múltiples cuadros con manifestaciones clínicas bien definidas y que desarrollaremos en esta revisión.
Por otro lado analizaremos la evidencia disponible que relaciona ciertos virus de esta familia con la progresión de la enfermedad periodontal tanto en adultos como en niños.
Palabras clave: Herpesvirus, periodontitis, infección orofacial.
SUMMARY
The HSV is a virus that causes of a great number of infections both in the orofacial and in the genital area.
The herpes simple virus is the prototype of a big family of double DNA strand viruses, the herpesviridiae, which causes a great morbidity in humans.
The infection of epithelial cells of the oral mucosa gives rise to a series of clinical signs and symptoms and to a latent infection of the sensitive neurons.
During the active phase of infection, multiple viral proteins are expressed while in the latent phase they are barely expressed.
When the virus is reactivated, recurrent infection starts, producing cell lisis and different clinical manifestations that we are will reviewed in this article. We will explain the.
The fact that certain virus of the herpesvirus family might be related with the progression of periodontal diseases in adults and children which is gaining interest lately.
Key words: Herpesvirus, periodontitis, orofacial infection.
Introducción
La mayoría de los virus humanos responsables de los principales cuadros de afectación orofacial son virus de tipo ADN contraídos durante la infancia o en la adolescencia a través del contacto con sangre, saliva o secreciones genitales (1).
Los herpesvirus son los virus tipo ADN más importantes en la patología oral y adquieren especial relevancia cuando infectan a sujetos con VIH o a sujetos con cuadros de inmunodepresión.
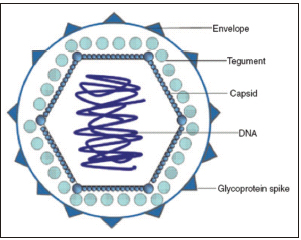
Los herpesvirus están constituidos por una estructura bien definida, con una cadena de ADN rodeada por una cápside icosaédrica. Ésta, a su vez, se rodea de un tegumento que contiene entre 15 y 20 proteínas y que esta en contacto directo con una envuelta que contiene numerosas glicoproteínas.
Clasificación de los virus
Clasificaremos los virus distinguiendo entre aquellos que pertenecen a la familia de los herpesvirus y todos los demás virus no pertenecientes a dicha familia pero que pueden dar lugar a lesiones orofaciales.
Dentro de los herpesvirus, en los cuales nos vamos a centrar, se han podido identificar ocho especies diferentes.
Se han atribuído lesiones orales al virus del herpes simple tipo I (HSV tipo I), al tipo II (HSV tipo II), al virus de la varicela zóster (VZV), al virus de Epstein-Barr (EBV), al citomegalovirus (HCMV) y al virus herpes 6, 7 y 8 (HHV-6, -7, -8) (2).
Además de los herpesvirus existen otros virus responsables de un gran número de lesiones bucales como el virus Coxsakie, el togavirus, el paramyxovirus, el virus del papiloma humano, el retrovirus VIH o el virus de la hepatitis, pero no serán objeto de nuestra revisión.
Características generales de los herpesvirus
La familia Herpesviridiae, contiene únicamente el género Herpesvirus.
Éstos tiene en común que poseen, al menos, cuatro características:
1. Una morfología típica con una cápsula icosaédrica de 162 capsómeros, recubiertos de una envuelta viral.
2. El genoma comprende una única molécula de ADN, de 120 a 250 kbp.
3. La infección viral exhibe cierta tendencia hacia el tropismo, siendo altamente recurrente en las superficies u órganos que infectan.
4. La fase productiva de la infección, donde el virus libera múltiples proteínas virales, es seguida por una fase de latencia en la cual el genoma viral permanece a salvo dentro de las células del huésped durante toda la vida del individuo infectado. De forma ocasional los herpesvirus en estado latente pueden sufrir procesos de reactivación y dar lugar de nuevo a una fase productiva en la cual, se liberan numerosas proteínas virales (3).
La tabla 1 muestra que dentro de las 8 especies de herpesvirus existen tres subgrupos: α, β; y γ.
El subgrupo alfa, conocido como la subfamilia alphaherpesvirinae, incluye los virus HVS-1, HVS-2 y VZV.
El grupo beta o subfamilia betaherpesvirinae, incluye HCMV, el herpesvirus tipo 6 y el herpesvirus tipo 7.
La subfamilia gammaherpesvirinae incluye el EBV y el HHV-8 o Sarcoma de Kaposi.
En estados de latencia, HSV-1, HSV-2 y VZV residen en los ganglios de los nervios sensitivos y en los monocitos.(4)
El EBV reside en los linfocitos B y en el tejido de la glándula salivar. (5-9)
HHV-6 permanece latente en los linfocitos y el epitelio ductal de las glándulas salivares.
HHV-7 en los linfocitos y el tejido glandular y el HHV-8 en linfocitos y macrófagos (10).
La activación de infecciones latentes pueden causar infección recurrente sintomática o asintomática (11, 12).
Un trauma físico, el estrés, periodos de inmunosupresión y radioterapia pueden desencadenar dicha reactivación (5).
Estructura y organización de su genoma
Existe bastante información acerca de la estructura molecular de los herpesvirus, se ha llegado incluso a secuenciar completamente el genoma en siete de ellos.
Los herpesvirus comparten genes homólogos e incluso bloques de secuencias conservadas que les permiten traducir proteínas, las cuales les caracterizan como miembros de dicha familia.
Se han descrito siete bloques de genes conservados que se localizan en el centro del genoma.
A pesar de que la latencia es una característica que comparten todos los herpesvirus, los genes responsables de dicha capacidad no se encuentran dentro de los núcleos de genes conservados.
Cualquiera de las especies de virus puede diferenciarse entre sí por el tamaño de su genoma y la distinta composición en cuanto a pares de bases.
Así, el tamaño molecularvaría desde los 125 kbp del virus varicela-zóster (13) hasta los 230 kbp del citomegalovirus. Incluso dentro de la misma especie pueden encontrarse diferencias de hasta 10 kp de tamaño molecular en función del número de secuencias repetidas del extremo terminal o internas.
La composición nucleotídica de los herpes virus varía entre ellos, así el contenido de Guanina-cytosina de los herpesvirus tipo alfa y VSV es del 68% y 46% respectivamente (13, 14).
Los herpesvirus traducen muchas proteínas necesarias para la replicación viral, se han identificado los genes responsables de la DNA polimerasa y del complejo helicasa-primasa, necesarios para la replicación viral huésped dependiente, así como los genes responsables del metabolismo del los nucleótidos, de la reparación del ADN, de la traducción de las glicoproteínas que expresan los virus en la superficie de la célula infectada o incluso de la cápside viral.
A pesar del gran conocimiento al que hemos llegado, gracias a los avances de la genética molecular, todavía no se ha podido identificar la función de aquellos genes que no están conservados entre las 3 familias, los cuales son responsables de la diversidad biológica de los herpesvirus.
Mecanismo y fases de la infección viral
Podemos dividir el ciclo viral en distintas fases
1. Fase de entrada
Consiste en 2 eventos principales, la unión del virus a la superficie celular y la fusión con la membrana plasmática.
La unión a la superficie celular tiene lugar a través de receptores celulares específicos, como gB y gC que se unen a un residuo de heparán sulfato que es un proteoglicano de la superficie celular, gD también parece tener cierta importancia a este nivel. A continuación se produce la fusión de la envuelta viral con la membrana plasmática de la célula, implicándose las glicoproteínas gB, gD, gH y gL.
Actualmente se conocen hasta 3 tipos diferentes de receptores celulares para la familia de los herpesvirus: uno perteneciente a la familia del TNF (tumor necrosis factor) denominado HveA (herpesvirus entry mediator A) y dos moléculas denominadas HveB y C, o más recientemente PRR1 y PRR2.
2. Expresión de los genes virales
Además de las glicoproteínas implicadas en la entrada, hay otros componentes del virión implicados en el desarrollo de la infección: vhs (UL41), que está implicado en la inducción de la inhibición de la síntesis de proteínas del huésped, destruyendo la mayoría de los ARNm mensajeros para permitir a HSV hacerse totalmente cargo de la maquinaria de síntesis de proteínas y aumentar la eficiencia en la producción de virus.
Para impedir la degradación de los ARNm virales, VP16 podría unirse a vhs a tiempos tardíos de infección, cuando ya se hayan eliminado los ARNm celulares. Otra proteína importante es la proteína quinasa UL13, con función no del todo conocida, pero cuya ausencia bloquea la infección.
Una vez en la célula, la cápside atraviesa los poros nucleares y libera el ADN en el nucleoplasma. Probablemente, el citoesqueleto celular colabora con el transporte hacia el núcleo.
Dentro de la célula infectada, la RNA polimerasa celular tipo II puede producir hasta 50 tipos diferentes de mRNA que están organizados en 3 bloques: Inmediatamente tempranos (alfa), tempranos (beta) y tardíos (gamma):
Alfa HSV-1 codifica para 5 genes inmediatamente tempranos que producen 5 proteínas denominadas ICP (Infected Cell Protein): La 0, 4, 22, 27 y 47. Suelen codificar para proteínas reguladoras e implicadas en la transcripción del resto de los bloques genéticos (beta y gamma). Entre estas proteínas, la ICP 4 y 27 se necesitan para la replicación viral en la célula infectada, así como la ICP 0. La ICP 47 está implicada en inhibir la presentación de los antígenos víricos por el complejo mayor de histocompatibilidad. La proteína del tegumento viral VP16 está implicada en la transactivación inicial de estos genes.
Beta y Gamma. Entre los mensajeros Beta se encuentran la polimerasa viral y la timidina quinasa (UL23), así como algunas proteínas estructurales menores. Los genes Gamma codifican para las glicoproteínas de la envuelta, proteínas de la cápside, tegumento (VP16), la vhs y la proteasa viral (VP22).
Replicación
El hecho de que se necesiten proteínas celulares para la replicación convierte a los herpesvirus en virus nucleares. Una característica de estos virus es el enorme número de enzimas involucradas en la síntesis de su ADN. En células infectadas, se detecta síntesis de ADN a las 3 horas postinfección, la cual continúa durante otras 12 horas. Esta síntesis se realiza en el núcleo celular. Sólo un porcentaje pequeño de las cadenas de ADN del input es replicado. Para ello, el ADN viral se vuelve circular y la replicación se lleva a cabo mediante el proceso del círculo rodante. En el genoma de HSV existen 3 orígenes de replicación, uno ori y dos ori. Uno de ellos podría estar implicado en la replicación del genoma de herpes durante la fase de latencia por parte de la ADN polimerasa celular. Con este mecanismo de replicación, se forman grandes concatámeros, los cuales son cortados para la encapsidación. Sólo alrededor del 25% del DNA/proteínas sintetizados acabarán formando viriones. El resto se acumula dentro de la célula.
Combinación, encapsulación y salida
El ensamblaje se produce en el núcleo. El DNA viral se empaqueta en una cápside preformada que contiene la proteasa viral. Para el ensamblaje se necesita la colaboración de un gran número de proteínas no capsídicas. Al empaquetar el ADN, éste sufre un proceso por el cual vuelve a ser lineal. La cápside con el ADN se une a la membrana interna nuclear y antes de pasar al espacio perinuclear, el virión adquiere la envuelta para luego perderla en la membrana externa nuclear. A partir de entonces el virus pasa al retículo endoplasmático, adquiriendo, de nuevo, la membrana. Unos autores apuntan a que el virión va al citoplasma atravesando la membrana plasmática, otros proponen que el virus maduro pasa al aparato de Golgi y de aquí sale como si se tratara de una proteína que se secreta.
Infección activa y latencia
El herpesvirus puede actuar como patógeno humano, con un ciclo lítico rápido y con la capacidad de invadir neuronas sensoriales. En este sistema se produce una restricción de la expresión del genoma viral y se establece la fase de latencia.
Estos periodos de latencia pueden alternarse con otros periodos de reactivación, en los cuales el virus puede ser transportado a través del axón hasta la periferia, produciendo una infección lítica a nivel de las células epiteliales.
Patogénesis
La infección primaria ocurre a través los ojos o de alguna pequeña herida en el epitelio nasal, bucal, o incluso la piel. Por su distribución universal, la mayoría de los niños entre 1-2 años han sido ya infectados. Inicialmente, esta infección es asintomática, aunque podrían producirse algunas lesiones vesiculares menores y locales.
A partir de la infección primaria, el virus llega a las terminales nerviosas sensoriales periféricas para, mediante transporte retrógrado a través del axón, llegar a los ganglios sensoriales e infectar el Sistema Nervioso Central donde permanece de forma latente una vez desaparecida la expresión proteica viral. Sólo se detecta un producto de transcripción denominado LAT (latency associated transcripts), que no codifica para ninguna proteína conocida, pero queda más o menos clara su participación en el control de la latencia. Durante este periodo, el ADN viral se mantiene como epítima, no estando integrado en el celular. Con la inducción de latencia, el virus podría escapar más fácilmente de la vigilancia inmune.
Cuando se produce una reactivación, el virus puede viajar de forma anterógrada hasta la periferia dando lugar a lesiones recurrentes. Normalmente, éstas son autolimitantes y desaparecen espontáneamente.
Manifestaciones clínicas de la infección
Virus herpes simple tipo 1 y 2
El HSV-1 es un virus de gran tamaño y neurotrópico que causa principalmente infecciones orales, desde leves como el herpes labial hasta graves como la meningoencefalitis. El HSV tipo 2 es muy similar pero da lugar a infecciones ano-genitales o herpes neonatal.
En España, más del 90% de la población expresa anticuerpos contra el VSH-1 y cerca de un 40% sufre infecciones recurrentes.
A pesar de que la mayoría de los casos de primoinfección herpética ocurren de forma asintomática, un 1 % cursa con un cuadro clínico de gingivoestomatitis herpética primaria.
La gingivoestomatitis herpética primaria (GHPA), ocurre generalmente en niños de entre 6 meses y 5 años de edad. Muy ocasionalmente podría afectar a adolescentes o adultos.
Cursa con fiebre, linfadenopatía y mialgia. Clínicamente aparecen úlceras puntiformes superficiales a nivel de encía y peribucal. A los 3 o 4 días, puede encontrarse una gingivitis con encías tumefactas y hemorrágicas e importante odinofagia con múltiples vesículas distribuidas por la cavidad bucal. Dichas vesículas poseen un contenido claro amarillento y se rompen con facilidad dejando erosiones muy dolorosas que curan de forma espontánea en un periodo de 10 o 14 días.
Las formas graves se caracterizan por úlceras blanquecinas con bordes festoneados y halo eritematoso. En pacientes inmunodeprimidos podría tener una duración más prolongada.
El herpes labial es la lesión más común y suele reactivarse con estímulos como el estrés, la ansiedad, luz solar prolongada o traumatismos.
Afecta a la unión mucocutánea del labio y se comienza con síntomas de escozor, picor y sensación de parestesias muy localizadas, a los 2 días pueden observarse vesículas en ramillete de contenido claro amarillento con un tamaño que oscila entre 1 y 10 mm. Tras su rotura aparecen costras que curan sin dejar cicatriz entre los 8 y los 15 días.
El tratamiento con sulfato de zinc puede reducir el numero de episodios y el tiempo de aparición del herpes labial.
El herpes intraoral recidivante se manifiesta con vesículas en ramillete a nivel de la mucosa masticatoria, que se ulceran rápidamente originando una erosión única con bordes estrellados y eritematosos, ligeramente dolorosa y que cura sin dejar cicatriz en 8 o 10 días.
En pacientes inmunodeprimidos el herpes se caracteriza por una rápida progresión o por cursar con formas extensas e incluso presentaciones atípicas. Puede llegar a afectar hasta el 40% de los pacientes con leucemia.
El HSV esta presente en un 30 % en úlceras orales persistentes de pacientes HIV positivos (15), también puede detectarse HCMV (53%) en este tipo de lesiones e incluso la coinfección de ambos virus en un 28%.
El HSV 1 y 2 están implicados también en el eritema multiforme recurrente, así como en el Síndrome de Behcet y en algunos casos de úlceras orales o como posible agente etiológico del carcinoma oral escamoso (1, 16, 44).

El diagnóstico del herpes puede realizarse por numerosos métodos: biopsia, citología exfoliativa, cultivo, microscopía electrónica, pruebas serológicas o bien por detección de antígenos virales empleando técnicas más sofisticadas como ELISA, PCR, etc.
El tratamiento con aciclovir sistémico resulta ser bastante efectivo, incluso en pacientes inmunodeprimidos.
En pacientes con cuadro de gingivoestomatitis herpética, el tratamiento de elección es aciclovir 200 mg, 5 veces al día mientras existan lesiones.
Es muy importante la hidratación oral y pueden emplearse anestésicos tópicos en forma de colutorios y/o analgésicos sistémicos.
Se recomienda mantener una buena higiene oral para evitar posibles sobreinfecciones.

Para el herpes labial recurrente el tratamiento ideal es Aciclovir en crema al 5%,5 veces al día, durante 5 días. Su utilización puede abortar las lesiones y acelerar la curación siempre que sea administrado antes de la aparición de vesículas.
Otra alternativa es el Penciclovir tópico en crema al 1%, cada dos horas durante el día, durante 4 días y éste se ha mostrado más efectivo que el Aciclovir.
Para el herpes intraoral se recomienda el empleo de anestésicos de lidocaína al 2%, junto con Aciclovir en suspensión 2,5 ml, 5 veces al día sobre la lesión.
En el caso de pacientes inmunodeprimidos, es recomendable emplear
Aciclovir intravenoso 5 mg por cada Kg de peso en infusión durante 1 hora cada 8-12 horas durante 7 días o bien Aciclovir vía oral 400 mg 5 veces al día (2.000 mg/día) durante 10-21 días.
Este tratamiento disminuye el dolor, el contagio y la formación de nuevas lesiones acelerando la curación, sin modificar las recurrencias.
Como podemos comprobar, hoy en día, no disponemos de un fármaco eficaz para combatir el herpes simple, sobre todo en lo que se refiere a evitar las recurrencias. Los fármacos que disponemos actúan positivamente en las situaciones de infección clínica, pero no han dado resultados a la hora de combatir al virus en el estado de latencia en los ganglios nerviosos, con lo que el paciente seguirá expuesto a nuevas recidivas.

Virus de la varicela-zóster (VZV)
Es un virus neurodermatotropo, cuyo modo de contacto inicial es por inhalación de gotitas que penetran en el organismo a través del aparato respiratorio, con un periodo de incubación de 1 a 3 semanas.
El virus varicela-zóster es el causante de la varicela como infección primaria, afectando principalmente a niños, mientras que su reactivación en adultos da lugar al herpes zóster.
La varicela es altamente contagiosa, en niños es más leve pero en adultos tiende a ser algo más severa. Las lesiones orales incluyen la presencia de vesículas en los labios y el paladar tanto duro como blando (4, 11, 17).
Tanto la infección primaria como la secundaria puede dar lugar a lesiones gingivales (11). Tras la infección primaria el virus permanece latente a nivel de la raíz dorsal de las células ganglionares.
El herpes zóster resulta de la reactivación del mismo virus latente.
A nivel oral las vesículas se rompen para formar lesiones ulceradas con bordes rosados prominentes que semejan úlceras aftosas.
En la piel aparecen erupciones de vesículas intraepiteliales que causan un dolor constante o intermitente y que se describe con carácter quemante.
Las lesiones se distribuyen de forma unilateral a lo largo del nervio infectado
Existe cierta preferencia por las ramas maxilar y mandibular del nervio cuando la reactivación ocurre desde el ganglio trigeminal.
Si hablamos del ganglio geniculado puede producir el Síndrome de Ramsay Hunt que cursa con parálisis facial unilateral, dolor, vesículas en el pabellón auditivo.
El herpes zóster en su manifestación oral podría incluso dar lugar a necrosis del periodonto y alteraciones óseas maxilares produciendo secuestros y pérdidas dentarias.
En individuos inmunosuprimidos, éstos podrían experimentar una mayor incidencia y recurrencia de infecciones por herpes zóster, convirtiéndose en un dolor crónico que podría afectar al sistema nervioso central e incluso provocar la muerte. Cuando aparece en individuos de la tercera edad puede ser indicador de afectación sistémica.
El diagnóstico puede realizarse empleando los mismos métodos que para el herpes simple, citología exfoliativa, cultivo, serología
El tratamiento es sistémico, empleando Aciclovir a dosis altas de 800 mg, 5 veces al día, durante 15 días, Famciclovir 500 mg 3 al día o Valaciclovir 1.000 mg 3 veces al día durante 10 días.
Para el control del dolor suele recetarse paracetamol con codeína e incluso antidepresivos como la amitriptilina y/o anticonvulsionantes.
El tratamiento antiviral es obligatorio en pacientes mayores de 50 años, ante el riesgo de desarrollar una neuralgia postherpética. En jóvenes, sólo, si el dolor es moderado o severo o si hay un compromiso del área oftálmica. El tratamiento es más efectivo si se inicia en las 72 horas tras el comienzo del rash.
El tratamiento intravenoso con aciclovir y foscarnet, ha sido efectivo a la hora de controlar los herpes zóster en pacientes VIH positivos (17).
Virus de Epstein-Barr
El virus EBV infecta y se replica en el epitelio oral y en la orofaringe, así como en los linfocitos B (16, 18-20).
Se transmite por la saliva y la sangre y en países en desarrollo infecta a la mayoría de los niños, generalmente de forma asintomática y antes de los dos años de edad. En países desarrollados, sin embargo, afecta generalmente a adolescentes causando la mononucleosis infecciosa, que se caracteriza por fiebre, linfadenopatías, astenia y faringitis (21).
Se han descrito úlceras orales, petequias palatales y de forma menos frecuente también pericoronaritis, gingivitis necrotizante o úlceras gingivales. En este caso el aciclovir es inefectivo para el tratamiento de la mononucleosis.
Existen al menos dos tipos de EBV: El tipo 1 y 2. El primero es el más predominante en el hemisferio oeste mientras que el 2 es más frecuente en Africa (12, 22). En individuos con VIH, la infección por EBV tanto 1 como 2, o incluso ambos, es muy frecuente.
La infección latente puede reactivarse y manifestarse a nivel de la mucosa oral, en pacientes VIH positivos dando lugar a leucoplasia vellosa.
La aparición de ésta puede ser indicativa de sida. No obstante, existen lesiones orales muy similares a la leucoplasia vellosa que no están relacionadas con la infección por el virus de Epstein Barr.
La infección por este virus podría derivar en una lesión maligna como el carcinoma nasofaríngeo, (22, 23), linfoma de Burkitt (22), linfoma de células B (24) o carcinoma oral.
El diagnóstico se realiza gracias a la combinación de los hallazgos clínicos, y una prueba de anticuerpo heterófilo positiva y/o antígenos de la cápside viral del virus.
El tejido de las amígdalas o ganglios linfáticos se muestra aumentado de tamaño con hiperplasia germinal y linfocitos T también aumentados.
Citomegalovirus (HCMV)
El HCMV se detecta en sangre y en secreciones orales como semen, saliva o leche materna. Es un virus muy frecuente, generalmente adquirido en la infancia, su infección primaria es sintomática cursando con faringitis, malestar, fiebre y linfadenopatías y el lugar de latencia es desconocido. Puede encontrase a nivel de las glándulas salivares (5) y puede infectar monocitos gingivales, macrófagos y linfocitos T (25, 26).
Este virus ha surgido como un patógeno oportunista de especial importancia en pacientes inmunodeprimidos, ya sean transplantados o pacientes con sida. Estos últimos pueden infectarse con diferentes cepas y se someten a riesgo de infección diseminada por HCMV.
Existen tres entidades clínicas diferentes producidas por este virus:
La enfermedad perinatal (27, 28), la infección aguda adquirida por HCMV y la enfermedad en el huésped inmunodeficiente (28).
La enfermedad perinatal por HCMV se da en niños cuyas madres sufren una primoinfección durante el embarazo y pueden presentar microcefalia asociada a retraso mental y sordera. La infección adquirida en neonatos es muy similar a una mononucleosis o puede cursar de forma asintomática.
El segundo síndrome relacionado con HCMV es también similar a la mononucleosis pero cursa sin faringitis ni anticuerpos heterofílicos
El tercer síndrome se observa en aquellos pacientes inmunodeprimidos como infectados por VIH o transplantados, ya que la infección por HCMV puede aumentar la inmunosupresión y agravar las infecciones oportunistas (17, 29, 30).
Las úlceras orales en pacientes inmunodeprimidos están frecuentemente relacionados con este virus (31). Dichas úlceras podrían ocasionalmente afectar a encías y periodonto dando lugar a destrucción ósea subyacente u osteomielitis (32). Se han descrito también casos de hiperplasia gingival (30).
El diagnóstico puede hacerse por hibridación in situ de ADN.
En pacientes inmunodeprimidos, pacientes con linfomas o leucemias, pueden verse células parenquimatosas de gran tamaño (2 a 4 veces lo normal) y cuerpos de inclusión intranucleares.
No hay un tratamiento claro ni una vacuna fiable, podrían emplearse ganciclovir y foscarnet durante periodos prolongados.
Herpesvirus tipo 6
El HHV-6 fue originalmente llamado virus B linfotrópico, pero ha sido recientemente reclasificado como herpesvirus.
Se han identificado dos variantes, A y B, con afinidad por los linfocitos CD4.
Este virus infecta el epitelio ductal de las glándulas salivares y se aísla en la saliva de la mayoría de los individuos, puede encontrarse también a nivel de encía de lesiones periodontales (33).
En niños, el HHV-6, puede causar exantema súbito o incluso mononucleosis, neumonía, meningitis, encefalitis. Se le ha identificado como un cofactor para acelerar la inmunodepresión en pacientes infectados por VIH (10).
El HHV-6 también podría ser responsable de algunos casos de mononucleosis no asociados a EBV o a HCMV. La coinfección por HHV-6 y EBV también ha sido relacionada con la mononucleosis.
Se ha encontrado en alto porcentaje en lesiones malignas, de modo que también se ha barajado su posible papel como factor causal del cáncer.
En pacientes con esclerosis múltiple se han encontrado niveles elevados de anticuerpos antiHHV-6 comparado con controles, de modo que también podría estar implicado en la patogénesis de dicha enfermedad.
A pesar de que el virus HHV-6 esta presente en el cerebro de casi todos los adultos (34), especialmente en las neuronas y en las células gliales, también ha sido encontrado en el núcleo de los oligodendrocitos asociados con placas de esclerosis múltiple (35).
Herpes virus 7
Éste es un virus muy frecuente, muy relacionado con el HHV-6.
Se adquiere durante la infancia y la mayoría de los adultos son HHV-7 seropositivos. Este virus se encuentra en la saliva y ésta resulta la mayor vía de transmisión, de padres a hijos y así sucesivamente.
Las glándulas salivares menores muchas veces albergan al virus y pueden ser el lugar de replicación de éste.
En un estudio de más de 100 individuos se ha detectado el virus en el 100% en la glándula submaxilar, en un 85% en la parótida y en el 59% en las glándulas salivares menores labiales (36). También ha sido detectado en encías inflamadas (33).
Parece estar asociado con al menos dos condiciones patológicas: la roséola y la pitiriasis rosácea. La pitiriasis es un exantema caracterizado por lesiones ovales cutáneas que pueden durar hasta dos semanas, pudiendo aparecer en lengua y mejillas (37).
Herpes virus 8
Ha sido recientemente descubierto y se cree que es el agente clave del sarcoma de Kaposi, se ha identificado en numerosas lesiones, incluso en lesiones periodontales de pacientes VIH positivos (33).
Estudios serológicos refieren una prevalencia del 25% del virus HHV-8 en la población adulta estadounidense y de un 8% en los niños (38).
El sarcoma de Kaposi fue originalmente descrito como un tumor vascular maligno que se presentaba en sujetos adultos de la región mediterránea.
Con el aumento del sida, la prevalencia de este tumor ha aumentado (45).
Aparentemente, la inmunosupresión actúa como activador del virus HHV-8 latente, con el consecuente desarrollo del tumor maligno.
El sarcoma de Kaposi aparece en la cavidad oral en un 60% de los pacientes y puede progresar a localizaciones extraorales. La localización más frecuente es el paladar seguido de la encía queratinizada, pudiendo llegar a afectar al hueso alveolar.
En el 25% de los pacientes son lesiones sintomáticas (39).
Asociación entre herpesvirus y periodontitis
La posible relación entre la infección por herpesvirus y la enfermedad periodontal ha suscitado la atención de muchos investigadores ya que se ha encontrado evidencia suficiente como para atribuir a determinados herpesvirus un papel importante en la etiología y la patogénesis de los procesos destructivos del periodonto (40).
Así, autores como Contreras & Slots, entre otros, han intentado esclarecer esta posible asociación y han descrito cinco mecanismos que pueden explicar el carácter periodontopatógeno de los herpesvirus, así:
1. Los herpesvirus tienen la capacidad de causar daños citopáticos en fibroblastos, queratinocitos, células endoteliales e inflamatorias.
2. Estos virus tienen la capacidad de actuar negativamente sobre las células de defensa del huésped, predisponiendo al sujeto a una sobreinfección bacteriana.
3. La infección gingival por herpesvirus puede facilitar la colonización subgingival por bacterias periodontopatógenas.
4. Las infecciones virales podrían alterar la respuesta inflamatoria, aumentando la producción de mediadores proinflamatorios.
5. Por último, pueden producir daño directo sobre los tejidos como consecuencia de la respuesta inmunopatológica a las células infectadas por el virus.
Al revisar la literatura podemos encontrar estudios que demuestran la presencia de virus en lesiones periodontales.
Kamma y cols 2001, examinaron 16 pacientes con periodontitis agresiva y encontraron una relación significativa con los virus CMVH y EBV tanto de forma individual como asociados.
La coinfección por CMVH-EBV se asoció siempre a aquellas localizaciones que sangraban al sondaje y un ritmo de progresión más rápido que aquellas localizaciones en las que únicamente se aisló a uno de los dos virus.
Ting y cols asociaron la forma activa del virus con aquellas localizaciones donde radiográficamente no se observaba la lámina dura de la cresta alveolar, siendo indicativo de progresión (41).
Yapar y cols 2003 encontraron cierta relación entre periodontitis agresiva y los virus CMVH y EBV sobretodo si los dos virus se hallaban asociados (42).
Kubar 2004, empleando PCR cuantitativa no pudo observar la presencia de CMVH en ninguna de las localizaciones sanas que examinó (43).
Slots y Contreras resumen en una serie de puntos, la evidencia disponible para implicar a los virus en la etiología y patogénesis de la enfermedad periodontal:
1. El hallazgo de secuencias de ácido nucleico de EBV-1 y HCMV y otros herpesvirus en lesiones de periodontitis juvenil y del adulto.
2. La asociación entre los herpesvirus y la gingivitis necrotizante en una población de niños nigerianos.
3. La demostración de ARN mensajero de HCMV en lesiones periodontales y su aparente relación con la progresión de las mismas.
4. La mayor prevalencia de bacterias periodontopatogénicas en lesiones periodontales positivas para herpesvirus.
5. El probable efecto negativo de la infección por herpesvirus en las células de defensa del periodonto.
6. La detección de secuencias de ADN viral en células inflamatorias del periodonto.
7. La habilidad de los herpesvirus para aumentar la producción de citoquinas en las células inflamatorias del periodonto.
Estos autores concluyen que la frecuencia con la que se encuentran virus en lesiones periodontales, junto con el conocimiento de su naturaleza infecciosa sobre las células encargadas del proceso inflamatorio así como del regenerativo hacen posible la creencia que exista una periodontitis asociada a herpesvirus. Si se demostrara que determinados tipos de lesiones periodontales son el resultado de una infección bacteriana oportunista mediada por la infección herpética, el manejo y tratamiento de estos pacientes deberá centrarse más en el intento de controlar los herpesvirus que permiten el sobrecrecimiento bacteriano, mediante el desarrollo de vacunas efectivas (33).
No obstante, aunque los datos hasta ahora examinados sean claros, aún queda por demostrar que existe una clara relación causa-efecto, capaz de aclarar si la infección periodontal por HCMV puede desencadenar una lesión periodontal destructiva o si, por el contrario, es la enfermedad periodontal la responsable de reactivar la infección por HCMV latente.
Bibliografía
1. Scott DA, Coulter WA, Lamey PJ. Oral shedding of herpes simplex virus type 1: a review. J Oral Pathol Med. 1997 Nov;26(10):441-7. [ Links ]
2. Drew WL, Buhles W, Erlich KS. Herpesvirus infections (cytomegalovirus, herpes simplex virus, varicella-zóster virus). How to use ganciclovir (DHPG) and acyclovir. Infectious disease clinics of North America. 1988 Jun;2(2):495-509. [ Links ]
3. Roizman B. The function of herpes simplex virus genes: a primer for genetic engineering of novel vectors. Proceedings of the National Academy of Sciences of the United States of America. 1996 Oct 15;93(21):11307-12. [ Links ]
4. Millar EP, Troulis MJ. Herpes zoster of the trigeminal nerve: the dentistís role in diagnosis and management. Journal (Canadian Dental Association). 1994 May;60(5):450-3. [ Links ]
5. Mocarski ES, Stinski MF. Persistence of the cytomegalovirus genome in human cells. Journal of virology. 1979 Sep;31(3):761-75. [ Links ]
6. Drew WL. Cytomegalovirus infection in patients with AIDS. The Journal of infectious diseases. 1988 Aug;158(2):449-56. [ Links ]
7. Lang DJ, Drew WL. Cytomegalovirus and other herpes viruses. Transfusion medicine reviews. 1988 Dec;2(4):294-5. [ Links ]
8. Stinski MF, Mocarski ES, Thomsen DR. DNA of human cytomegalovirus: size heterogeneity and defectiveness resulting from serial undiluted passage. Journal of virology. 1979 Jul;31(1):231-9. [ Links ]
9. Stinski MF, Mocarski ES, Thomsen DR, Urbanowski ML. Membrane glycoproteins and antigens induced by human cytomegalovirus. The Journal of general virology. 1979 Apr;43 (1): 119-29. [ Links ]
10. Lusso P, Markham PD, Tschachler E, di Marzo Veronese F, Salahuddin SZ, Ablashi DV, et al. In vitro cellular tropism of human B-lymphotropic virus (human herpesvirus-6). The Journal of experimental medicine. 1988 May 1;167(5):1659-70. [ Links ]
11. Scully C. New aspects of oral viral diseases. Current topics in pathology. 1996;90:29-96. [ Links ]
12. Scully C, Epstein J, Porter S, Cox M. Viruses and chronic disorders involving the human oral mucosa. Oral surgery, oral medicine, and oral pathology. 1991 Nov;72(5):537-44. [ Links ]
13. Davison AJ, Taylor P. Genetic relations between varicella-zoster virus and Epstein-Barr virus. The Journal of general virology. 1987 Apr;68 ( Pt 4):1067-79. [ Links ]
14. Davison AJ, Scott JE. DNA sequence of the major capsid protein gene of herpes simplex virus type 1. The Journal of general virology. 1986 Oct;67 (Pt 10):2279-86. [ Links ]
15. Smith S, Ross JW, Scully C. An unusual oral complication of herpes zoster infection. Oral surgery, oral medicine, and oral pathology. 1984 Apr;57(4):388-9. [ Links ]
16. Scully C, Laskaris G, Pindborg J, Porter SR, Reichart P. Oral manifestations of HIV infection and their management. II. Less common lesions. Oral surgery, oral medicine, and oral pathology. 1991 Feb;71(2):167-71. [ Links ]
17. Miller CS. Viral infections in the immunocompetent patient. Dermatologic clinics. 1996 Apr;14(2):225-41. [ Links ]
18. Klein G. Viral latency and transformation: the strategy of Epstein-Barr virus. Cell. 1989 Jul 14;58(1):5-8. [ Links ]
19. Flaitz CM, Jin YT, Hicks MJ, Nichols CM, Wang YW, Su IJ. Kaposiís sarcoma-associated herpesvirus-like DNA sequences (KSHV/HHV-8) in oral AIDS-Kaposiís sarcoma: a PCR and clinicopathologic study. Oral surgery, oral medicine, oral pathology, oral radiology, and endodontics. 1997 Feb;83(2):259-64. [ Links ]
20. Sixbey JW, Vesterinen EH, Nedrud JG, Raab-Traub N, Walton LA, Pagano JS. Replication of Epstein-Barr virus in human epithelial cells infected in vitro. Nature. 1983 Dec 1-7;306(5942):480-3. [ Links ]
21. Khanna R, Burrows SR, Moss DJ. Immune regulation in Epstein-Barr virus-associated diseases. Microbiological reviews. 1995 Sep;59(3):387-405. [ Links ]
22. Rickinson AB, Lee SP,Steven NM. Cytotoxic T lymphocyte responses to Epstein-Barr virus. Current opinion in immunology. 1996 Aug;8(4): 492-7. [ Links ]
23. Tao Q, Ho FC, Loke SL, Srivastava G. Epstein-Barr virus is localized in the tumour cells of nasal lymphomas of NK, T or B cell type. International journal of cancer. 1995 Jan 27;60(3):315-20. [ Links ]
24. Boulter A, Johnson NW, Birnbaum W, Teo CG. Epstein-Barr virus (EBV) associated lesions of the head and neck. Oral diseases. 1996 Jun;2(2):117-24. [ Links ]
25. Contreras A, Slots J. Active cytomegalovirus infection in human periodontitis. Oral microbiology and immunology. 1998 Aug;13 (4):225-30. [ Links ]
26. Grundy JE. Virologic and pathogenetic aspects of cytomegalovirus infection. Reviews of infectious diseases. 1990 Sep-Oct;12 Suppl 7:S711-9. [ Links ]
27. Britt WJ. Vaccines against human cytomegalovirus: time to test. Trends in microbiology. 1996 Jan;4(1):34-8. [ Links ]
28. Ho M. Epidemiology of cytomegalovirus infections. Reviews of infectious diseases. 1990 Sep-Oct;12 Suppl 7:S701-10. [ Links ]
29. Ficarra G, Eversole LE. HIV-related tumors of the oral cavity. Crit Rev Oral Biol Med. 1994;5(2):159-85. [ Links ]
30. Epstein JB, Scully C. Herpes simplex virus in immunocompromised patients: growing evidence of drug resistance. Oral surgery, oral medicine, and oral pathology. 1991 Jul;72(1):47-50. [ Links ]
31. Regezi JA, Eversole LR, Barker BF, Rick GM, Silverman S, Jr. Herpes simplex and cytomegalovirus coinfected oral ulcers in HIV-positive patients. Oral surgery, oral medicine, oral pathology, oral radiology, and endodontics. 1996 Jan;81(1):55-62. [ Links ]
32. Glick M, Cleveland DB, Salkin LM, Alfaro-Miranda M, Fielding AF. Intraoral cytomegalovirus lesion and HIV-associated periodontitis in a patient with acquired immunodeficiency syndrome. Oral surgery, oral medicine, and oral pathology. 1991 Dec;72(6):716-20. [ Links ]
33. Contreras A, Nowzari H, Slots J. Herpesviruses in periodontal pocket and gingival tissue specimens. Oral microbiology and immunology. 2000 Feb;15(1):15-8. [ Links ]
34. Luppi M, Barozzi P, Maiorana A, Marasca R, Torelli G. Human herpesvirus 6 infection in normal human brain tissue. The Journal of infectious diseases. 1994 Apr;169(4):943-4. [ Links ]
35. Challoner PB, Smith KT, Parker JD, MacLeod DL, Coulter SN, Rose TM, et al. Plaque-associated expression of human herpesvirus 6 in multiple sclerosis. Proceedings of the National Academy of Sciences of the United States of America. 1995 Aug 1;92(16):7440-4. [ Links ]
36. Sada E, Yasukawa M, Ito C, Takeda A, Shiosaka T, Tanioka H, et al. Detection of human herpesvirus 6 and human herpesvirus 7 in the submandibular gland, parotid gland, and lip salivary gland by PCR. Journal of clinical microbiology. 1996 Sep;34(9):2320-1. [ Links ]
37. Vidimos AT, Camisa C. Tongue and cheek: oral lesions in pityriasis rosea. Cutis; cutaneous medicine for the practitioner. 1992 Oct;50(4):276-80. [ Links ]
38. Lennette ET, Blackbourn DJ, Levy JA. Antibodies to human herpesvirus type 8 in the general population and in Kaposiís sarcoma patients. Lancet. 1996 Sep 28;348(9031):858-61. [ Links ]
39. DiAlberti L, Teo CG, Porter S, Zakrzewska J, Scully C. Kaposiís sarcoma herpesvirus in oral Kaposiís sarcoma. European journal of cancer. 1996 Jan; 32B(1):68-9. [ Links ]
40. Contreras A, Slots J. Herpesviruses in human periodontal disease. Journal of periodontal research. 2000 Feb;35(1):3-16. [ Links ]
41. Ting M, Contreras A, Slots J. Herpesvirus in localized juvenile periodontitis. Journal of periodontal research. 2000 Feb;35(1):17-25. [ Links ]
42. Yapar M, Saygun I, Ozdemir A, Kubar A, Sahin S. Prevalence of human herpesviruses in patients with aggressive periodontitis. Journal of periodontology. 2003 Nov;74(11):1634-40. [ Links ]
43. Kubar A, Saygun I, Yapar M, Ozdemir A, Slots J. Real-time PCR quantification of cytomegalovirus in aggressive periodontitis lesions using TaqMan technology. Journal of periodontal research. 2004 Apr;39(2):81-6. [ Links ]
44. Nunes R, Lauro Gilberto, Moresco V, Raquel G, Marley et al. Síndrome de Behcet. Av Odontoestomatol 2005; 21(4): 183-7. [ Links ]
45. Casariego, Zulema, Fonio S, Micinquevich S. Lesiones estomatológicas en pacientes VIH-1 ractivos. Comparación de proporción en dos poblaciones independientes. Av Odontoestomatol 2006;22(4): 217-22. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
X. Pousa-Castro
xianaxiana@hotmail.com
Fecha de recepción: 9 de octubre de 2009.
Aceptado para publicación: 14 de octubre de 2009.