Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO  Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.79 no.12 dic. 2004
ARTÍCULO ORIGINAL
TRATAMIENTO DIGITAL DE RETINOGRAFÍAS PARA DETECTAR AUTOMÁTICAMENTE
LESIONES ASOCIADAS CON LA RETINOPATÍA DIABÉTICA
RETINAL IMAGE ANALYSIS TO DETECT LESIONS ASSOCIATED WITH DIABETIC RETINOPATHY
SÁNCHEZ GUTIÉRREZ CI 1, LÓPEZ GÁLVEZ MI 2, HORNERO SÁNCHEZ R 3, POZA CRESPO J 1
| RESUMEN Objetivos: La retinopatía diabética es la causa más frecuente de ceguera en la población activa de los países industrializados. Para retrasar su evolución y evitar así la pérdida de visión, el mejor método de prevención es un seguimiento regular médico. Para ello, se utilizan las imágenes de fondo de ojo o retinografías. Sin embargo, debido al gran número de pacientes, se requiere mucho esfuerzo y tiempo para revisar todas las imágenes. El objetivo de este trabajo es desarrollar un método automático que ayude a detectar los primeros síntomas de la retinopatía diabética mediante un tratamiento digital de las retinografías. Palabras claves: Exudados duros, procesado digital, retinografía, retinopatía diabética. | SUMMARY Purpose: Diabetic retinopathy is a leading cause of vision loss in developed countries. Regular diabetic retinal eye screenings are needed to detect early signs of retinopathy, so that appropriate treatments can be rendered to prevent blindness. Digital imaging is becoming available as a means of screening for diabetic retinopathy. However, with the large number of patients undergoing screenings, medical professionals require a tremendous amount of time and effort in order to analyse and diagnose the fundus photographs. Our aim is to develop an automatic algorithm using digital image analysis for detecting these early lesions from retinal images. Key words: Diabetic retinopathy, digital processing, hard exudates, retinal images.
|
Recibido: 31/5/04. Aceptado: 22/12/04.
Instituto de Oftalmobiología (IOBA). Universidad de Valladolid. Valladolid. Epaña.
1 Licenciado en Ingeniería de Telecomunicación.
2 Doctor en Medicina.
3 Doctor en Ingeniería de Telecomunicaciones. E.T.S. Ingenieros de Telecomunicación. Universidad de Valladolid. Valladolid.
Comunicación presentada parcialmente en el LXXIX Congreso de la S.E.O. (Valencia 2003).
Proyecto Subencionado Agencia de Desarrollo Económico. Junta de Castilla y León.
Correspondencia:
Clara Isabel Sánchez
IOBA. Facultad de Ciencias de la Salud
Avda. Ramón y Cajal, 7
47005 Valladolid
España
E-mail: csangut@telefonica.net
INTRODUCCIÓN
La Diabetes Mellitus es una enfermedad metabólica que se caracteriza por la presencia de niveles elevados de glucosa en sangre. La diabetes por sí misma provoca otras complicaciones crónicas, entre ellas una enfermedad ocular conocida como Retinopatía Diabética (RD). Hoy en día, la RD es la causa más frecuente de ceguera entre la población activa de los países desarrollados. Los principios que producen esta enfermedad no se conocen completamente y todavía no puede ser prevenida. Sin embargo, existen tratamientos efectivos que retrasan su evolución siempre que sea diagnosticada con suficiente antelación (1). El problema de la RD es que es una enfermedad asintomática y sólo aparecen defectos en la visión en una etapa avanzada de la enfermedad. Por lo tanto, los pacientes diabéticos no se dan cuenta de que padecen la enfermedad y no se someten a un examen ocular. Algunas veces se examina al paciente cuando ya es demasiado tarde para un tratamiento adecuado y ya se han causado severos daños a la retina (1).
Con la idea de evitar estos daños, lo que se ha propuesto es realizar un despistaje regular de la retina de todos los pacientes diabéticos para garantizar una detección a tiempo y un tratamiento adecuado. De esta manera, cada persona con diabetes se debería someter a una exploración oftalmológica al menos una vez al año (2). Debido a que la diabetes es una enfermedad de elevada prevalencia (superior a un 6% de la población mundial según la Organización Mundial de la Salud), son muchos los exámenes que se tienen que llevar a cabo. Por lo tanto, la realización de este despistaje supone unos costes muy elevados y requiere personal altamente cualificado (1). Para reducir tanto los costes como el número de especialistas, sería de gran utilidad desarrollar un método automático para detectar la enfermedad en sus primeras etapas.
Existen un gran conjunto de técnicas que ayudan a realizar este despistaje. Varían desde la observación directa con un oftalmoscopio hasta la revisión de fotografías del fondo de ojo y más recientemente de imágenes digitales (retinografías). Estas últimas están adquiriendo un protagonismo cada vez mayor, ya que resultan un modo económico y eficaz de mantener almacenada la información del fondo de ojo (2). Además, tienen la capacidad de ser procesadas por sistemas automáticos.
Basándose en esto, el objetivo a largo plazo de este trabajo es automatizar el despistaje de la RD usando imágenes digitales a color de la retina. De esta manera, se podría discriminar entre pacientes diabéticos que necesitan un examen más detenido por un oftalmólogo de aquellos que no lo necesitan. Este artículo se centra en el análisis automático de una de las lesiones asociadas a la RD: los exudados duros, como un primer paso para esa automatización completa. Anteriormente se han realizado otros trabajos que han identificado los exudados duros utilizando su nivel de gris (3,4), su contraste (4-7) o su color (8,9). Debido a que la iluminación, contraste y color de los exudados varía mucho entre imágenes de diferentes pacientes, estos métodos no funcionan con todos los tipos de imágenes que se producen en un entorno clínico normal. La mejora principal que se introduce en el presente artículo es su robustez ante la apariencia variable de las retinografías para obtener un rendimiento óptimo con todos los tipos de imágenes posibles.
MÉTODOS
El método desarrollado intenta detectar los exudados duros usando dos de las características principales que los diferencia del resto de lesiones: su color blanco-amarillento y sus bordes definidos. La idea del algoritmo se presenta de manera gráfica en el diagrama de la figura 1. En una primera etapa, se detecta elementos comunes de las mayorías de las retinografías, como son la papila y los vasos sanguíneos. Posteriormente, por una parte, se consigue una imagen con aquellos elementos que posean una coloración blanco-amarillenta y, por otra parte, otra imagen con todos los objetos que presenten unos bordes bien definidos. Seleccionando los elementos que se encuentren en ambas imágenes a la vez, se detectan regiones de color blanquecino con bordes definidos. Finalmente, eliminando posibles falsos positivos (como la papila), se conseguirá detectar los exudados duros presentes en la imagen. Una explicación más detallada de cada una de estas etapas se lleva a cabo en los siguientes apartados.
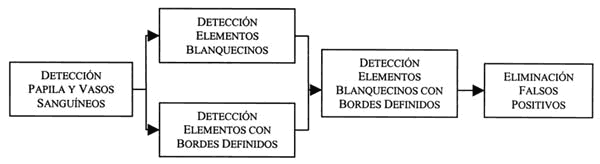
Fig. 1. Esquema del método diseñado para la detección de exudados duros.
Detección de la papila y de los vasos sanguíneos
Primeramente se localiza la papila buscando los conjuntos de píxeles con mayor intensidad y aplicando sobre estos el modelo Principal Component Analysis (PCA) para seleccionar la que va a ser la posición final del centro de la papila (7). También detectamos su borde usando un contorno activo o snake conducido por un campo exterior conocido como Gradient Vector Field (GVF) (10) sobre la imagen e inicializado automáticamente (fig. 2 a).
Los vasos sanguíneos se realzan mediante el filtrado adaptado descrito en (11) y posteriormente se detectan poniendo un umbral a la imagen obtenida (fig. 2 b).

Fig. 2. A. Imagen en la que se puede ver en color negro el perfil de la papila que se ha detectado;
B. Detección de la red vascular.
Detección de regiones blanco amarillentas
La detección de este tipo de elementos se lleva a cabo mediante una segmentación de color basado en el método de clasificación estadística expuesto en (8,9). Este método consiste en dividir la imagen en diferentes clases. Cada una de estas clases viene definida por un patrón de color que es necesario conocer. En nuestro caso, estas clases son dos: la clase 1 que la forman las regiones de color blanquecino y la clase 2 compuesta por el resto de regiones que presentan otro color. De esta manera, un píxel de la imagen pertenece a la clase 1 si su color se acerca más al patrón de color de la clase 1 que al de la clase 2 y viceversa. Al finalizar el algoritmo se obtendría una imagen en blanco y negro, donde las regiones en color blanco representan los elementos de la clase 1. De esta manera se conseguirá una imagen en la que sólo aparecen los elementos blanco-amarillentos. Un esquema de este método se puede observar en la figura 3.

Fig. 3. Esquema del método seguido para la detección de regiones blanco amarillentas.
Primeramente, se realiza un preprocesado para conseguir una uniformidad del color y una mejora del contraste de la imagen. Esta etapa es necesaria porque debido a la variación de iluminación, la disminución de la saturación del color, la pigmentación de la piel,... el color y la iluminación de los exudados en algunas regiones pueden aparecer menos nítidos que en otras, pudiendo así ser clasificados incorrectamente (fig. 4 a). El preprocesado consiste en la combinación aritmética de las componentes de color del modelo YCbCr de la imagen. De esta manera, se mejora tanto el contraste de las lesiones como la saturación del color de la imagen (fig. 4 b).

Fig. 4. A. Imagen original en la que se puede ver como los exudados cercanos a la papila aparecen con menos contraste
y más débiles que aquellos que están más alejados de ella; B. Imagen realzada en la que los exudados aparecen
con el mismo color independientemente del lugar en el que se encuentren.
Para la elección de los patrones de color, aprovechamos que, tras la primera etapa, la papila y los exudados presenta la misma coloración independientemente de la posición en la que se encuentren los exudados. Así tomamos como patrón de color de la clase 1 (los objetos blanco-amarillentos de la imagen) la coloración que presenta la papila en la imagen y para la clase 2 el color de la zona que rodea este elemento.
Aplicando finalmente el algoritmo descrito en (8,9), obtenemos todos los elementos blanco-amarillentos de la imagen (fig. 5). A la vez que los exudados duros, otras regiones también se detectan, como la papila, los exudados algodonosos, drusas,...

Fig. 5. Detección de las zonas blanco-amarillentas, en las que
además de los exudados se incluyen la zona cercana a la papila.
Detección de elementos con bordes definidos
La detección de estos elementos se lleva a cabo mediante la aplicación de un filtro detector de borde: el filtro Kirsch, y la imposición de un umbral T a la imagen obtenida (fig. 6). T es un parámetro del algoritmo. Si disminuimos T, se detectaría bordes cada vez menos abruptos, aumentando así la sensibilidad pero disminuyendo la especificidad. Otros objetos con bordes fuertemente definidos son detectados, como la papila, los vasos sanguíneos, las hemorragias,...

Fig. 6. Detección de los bordes de los elementos con mayor contraste,
entre ellos los exudados, hemorragias, vasos sanguíneos, papila,...
Combinación de las etapas anteriores y eliminación de falsos positivos
Para detectar únicamente los exudados duros, se combinan las dos imágenes obtenidas en las etapas previas (elementos blanco-amarillentos y elementos con bordes definidos) mediante un AND lógico.
Tras ello, además de los exudados duros se obtienen algunos falsos positivos localizados en la región papilar y cerca de los vasos. Su eliminación se lleva a cabo mediante la substracción a la imagen obtenida de una versión dilatada de la detección de la papila y de los vasos sanguíneos. En la figura 7 se muestra el resultado final de nuestro algoritmo.

Fig. 7. Imagen que presenta en verde los exudados duros
detectados automáticamente sobre la figura.
RESULTADOS
El algoritmo se probó en una base de datos de 20 retinografías tomadas con una TopCon TRC-NW6S (Topcon Medical Co., Ltd. Hongo, Bukyo-ku, Tokyo, Japan) y se compararon los resultados obtenidos con la opinión de un especialista en la materia.
Para evaluar la calidad del sistema se determinan el número de aciertos y el de falsos positivos (FP) en cada imagen a la vez que se varía T. Así se puede representar en una gráfica la tasa de aciertos frente al número de FP por imagen usando las curvas Free Response Operating Characteristic (FROC). Es un método muy apropiado para medir la calidad del sistema y encontrar un compromiso entre la tasa de aciertos y la de fallos. Cada umbral de decisión T produce un punto de operación en la curva.
Un exudado se considera que ha sido detectado cuando se ha localizado al menos el 50% de su área. La curva obtenida se muestra en figura 8. El mejor resultado se alcanza en el punto de operación T=0,8 con una sensibilidad del 79,62% con una media del 2.2 FP por imagen.

Fig. 8. Curva FROC en la que se representa distintos puntos de operación (T=1,3, 1, 0,8 y 0,6).
DISCUSIÓN
La evaluación del método se ha llevado a cabo en una base de datos de retinografías independiente y personal, caracterizada por tener un conjunto de imágenes muy variables en cuanto iluminación y color. Debido a la falta de una base de datos común y un método fiable de medida del rendimiento, es difícil comparar los resultados de este método con los propuestos por otros autores. Así, por ejemplo, se puede observar una discrepancia con los resultados presentados por otros autores (5,7).
La principal contribución del trabajo expuesto en este artículo es que se obtiene una detección aceptable de manera global en la mayoría de las imágenes independientemente de su color, iluminación, tamaño,... manteniendo el número de FP pequeño. Esta independencia en el aspecto se consigue usando un método particular para cada imagen (para realzarlas, para la segmentación de color,...) en contraposición a otros autores que utilizan técnicas generales para todas ellas. Particularizar el algoritmo para cada imagen es muy importante ya que el color de las retinografías varía mucho de unas a otras, y el color que presenta los exudados en una de ellas puede ser muy distinto, aunque dentro de la misma gama, que el que presenta en otra imagen. Por lo tanto, el comportamiento que muestra el algoritmo es más adecuado para un entorno clínico en el que la variabilidad de las imágenes es algo común. Aunque algunos exudados no son detectados debido a su proximidad a los vasos sanguíneos o porque aparecen muy pálidos incluso después del realzado propuesto.
El método descrito, sin embargo, presenta una serie de problemas que tienen que ser mejorados. Primero, el algoritmo depende de otras tareas de detección como es la detección de la papila y de los vasos, provocando que los resultados sean dependientes del éxito o fracaso de estas tareas. Sería, por lo tanto, necesario mejorar estas tareas de detección para mejorar el resultado global. Por otra parte, se usa el color de la papila para caracterizar las regiones blanco-amarillentas pero así no se representa su color real. Una buena idea consistiría localizar un conjunto de exudados y, a partir de su color, localizar el resto. Finalmente la detección de los exudados duros puede verse distorsionada por lesiones de apariencia semejante en cuanto al color y las dimensiones, como sucede con las drusas duras, incrementando así el número de falsos positivos y presentando un problema difícil de resolver. Ahora bien, la coexistencia de otras alteraciones en el fondo de ojo de los pacientes diabéticos, como los microaneurismas, las hemorragias o las alteraciones del calibre venoso, y su consiguiente detección sería imprescindible para el diagnóstico.
Este artículo presenta principalmente la detección de exudados duros en retinografías. Pero las primeras etapas de la RD están caracterizadas también por otros signos clínicos, como son los microaneurismas, las hemorragias y los exudados algodonosos. El trabajo futuro de este grupo de trabajo se centrará, por lo tanto, en detectar el resto de lesiones para así poder discriminar con mayor exactitud un paciente con retinopatía diabética de uno que no la posee.
BIBLIOGRAFÍA
1. Pastor JC. Guiones de Oftalmología. 3.ª edición. Madrid: McGraw-Hill; 2002. [ Links ]
2. Aiello LP, Gardner TW, King GL, Blankenship G, Cavallerano JD, Ferris FL 3rd, et al. Diabetic retinopathy. Diabetes Care 1998; 21: 143-156. [ Links ]
3. Ward NP, Tomlinson S, Taylor CJ. Image analysis of fundus photographs. The detection and measurement of exudates associated with diabetic retinopathy. Ophthalmology 1989; 96: 80-86. [ Links ]
4. Philips R, Forrester J, Sharp P. Automated detection and quantification of retinal exudates. Graefes Arch Clin Exp Ophthalmol 1993; 231: 90-94. [ Links ]
5. Walter T, Klein JC, Massin P, Erginay A. A contribution of image processing to the diagnosis of diabetic retinopathy--detection of exudates in color fundus images of the human retina. IEEE Trans Med Imaging 2002; 21: 1236-1243. [ Links ]
6. Li H, Chutatape O. Fundus image features extraction. Proc 22nd Annual Int Conf of the IEEE Engin Med Biol Soc (EMBS00) 2000: 3071-3073. [ Links ]
7. Li H, Chutatape O. A model-base approach for automated feature extraction in fundus images. Proc 9th Int Conf of the IEEE Comp Vision, (ICCV 03) 2003: 50-53. [ Links ]
8. Goh KG, Hsu W, Lee ML, Wang H. ADRIS: an automatic diabetic retinal image screening system. In: Cios. KJ Medical Data Mining and Knowledge Discovery. New York: Physica Verlag; 2000; 181-210. [ Links ]
9. Wang H, Hsu W, Goh KG, Lee M. An effective approach to detect lesions in color retinal images. IEEE Conf on Comp Vision and Patt Recogn 2000; 2: 181-186. [ Links ]
10. Xu C, Prince JL. Snake, shapes and gradient vector flow. IEEE Trans Imag Process 1998; 7: 359-369. [ Links ]
11. Chaudhuri S, Chatterjee S, Katz N, Nelson M, Goldbaum M. Detection of blood vessels in retinal images using two-dimensional matched filters. IEEE Trans Med Imaging 1989; 8: 263-269. [ Links ]














