Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.81 no.10 oct. 2006
ARTÍCULO ORIGINAL
Resultados de la cirugía del agujero macular con diferentes técnicas de tratamiento
Outcomes of macular hole surgery using three different surgical techniques
Villota-Deleu E. 1, Castro-Navarro J. 2, González-Castaño C. 1 , Pérez-Carro G. 1
Hospital Universitario Central de Asturias. Sección de Vítreo y Retina. Universidad de Oviedo. Asturias. España.
1 Licenciado en Medicina
2 Doctor en Medicina
Dirección para correspondencia
RESUMEN
Objetivo: Comparar la efectividad, eficiencia y complicaciones de las tres técnicas quirúrgicas empleadas en el tratamiento del agujero macular en el período 1998-2004 en nuestro centro.
Métodos: Estudio retrospectivo, comparativo, intervencionista y no aleatorizado de 131 ojos con agujero macular idiopático en estadío III y IV, operados con tres técnicas. En 25 ojos se realizó vitrectomía simple (grupo 1), en 19 ojos se asoció rexis de la membrana limitante interna (MLI) (grupo 2), y en 87 ojos esta rexis se llevó a cabo previa tinción con verde de indocianina (ICG) (grupo 3). Las concentraciones de ICG empleadas fueron del 5%, 2,5% y 0,5%. Se compararon la recuperación anatómica y funcional y las complicaciones en los distintos grupos.
Resultados: El 88,4% (114 ojos) lograron la resolución anatómica, siendo superior en el grupo 3 (90,6%). La recuperación funcional se consiguió en el 63,6%. En ambos casos no existieron diferencias entre grupos. Las complicaciones más importantes fueron: cataratas post-cirugía (51,9%), aumento de PIO (37,2%), desprendimientos de retina (7,8%) y alteraciones del epitelio pigmentario (7%). Esta última se relacionó con el uso de ICG (p<0,05), sin encontrarse diferencias en las concentraciones empleadas. El tamaño del agujero tuvo una correlación inversa con la agudeza visual (AV) inicial y post-quirúrgica. La presencia de membrana epirretiniana se asoció a mejores AV y a un mayor éxito anatómico.
Conclusiones: En nuestra experiencia, la cirugía mejora la AV, siendo más efectiva si se asocia ICG para la rexis de la MLI. Sin embargo, esta tinción podría estar relacionada con las alteraciones del EPR encontradas.
Palabras clave: Agujero macular, vitrectomía, liberación de la membrana limitante interna, verde de indocianina.
ABSTRACT
Purpose: To compare the effectiveness, efficiency and complications of three different surgical techniques employed for the treatment of macular holes between 1998 -2004 in our health care centre.
Methods: A retrospective, comparative, and non-randomized study of 131 eyes with macular holes, stage III and IV, treated with three different surgical techniques was performed. Vitrectomy was performed in 25 eyes (group 1). Vitrectomy was associated with internal limiting membrane peeling in 19 eyes (group 2), and in the remaining 87 eyes, the peeling of the retinal internal limiting membrane was assisted with indocyanine green (ICG) (group 3). The concentrations of ICG used were 5%, 2.5% and 0.5%. We compared the anatomic and functional results, and the complications which occurred.
Results: The overall anatomic success rate was 88.4% (114 eyes), and it was higher in group 3 (90.6%). A visual acuity improvement was achieved in 63.6% of eyes; however there were no significant differences between the groups studied. The most important complications included cataracts (51.9%), increase in intra-ocular pressure (37.2%), retinal detachment (7.8%) and retinal pigment epithelial changes (7%). These pigment epithelial changes were associated with the use of ICG-assisted peeling (p<0.05), but there was no correlation between the changes and the concentration of ICG employed. The hole size had an inverse correlation with initial and final visual acuity. An epi-retinal membrane was associated with better visual acuities and higher anatomic success.
Conclusions: In our experience, the use of ICG-assisted internal limiting membrane peeling in macular hole surgery improves the anatomic success, but may lead to retinal pigment epithelial changes (Arch Soc Esp Oftalmol 2006; 81: 581-590).
Key Words: Macular hole, vitrectomy, internal limiting membrane peeling, indocyanine green.
Introducción
El agujero macular (AM) idiopático o senil es la causa más frecuente de agujero macular (1) y una causa importante de pérdida de visión central. La primera descripción de esta patología la realizó Knapp en 1869. En 1991, Kelly y Wendel publicaron el primer cierre con éxito de un agujero macular idiopático completo con vitrectomía vía pars plana y posterior intercambio gaseoso (2). Desde entonces, se ha desarrollado la técnica quirúrgica. Se introdujeron las terapias adyuvantes en un esfuerzo de inducir el crecimiento de células gliales (3-8). Posteriormente se procedió a la liberación de la membrana limitante interna (MLI) perifoveal con el fin de eliminar cualquier membrana epirretiniana (MER) que pudiera estar presente, promover la liberación de citoquinas estimulantes de la proliferación glial que facilitasen el cierre del agujero y conseguir unos márgenes más móviles, reduciéndose el tamaño del AM (7,9-12). Dado que la MLI es muy fina y transparente, su liberación no resulta siempre fácil, de ahí que surgiese la tinción de la misma. Se utilizó en primer lugar el verde de indocianina (ICG o VID) (13-20). Las técnicas, volumen y concentraciones de ICG varían mucho en las distintas series, y todavía no se ha establecido un protocolo internacional al respecto (21). A pesar de que el ICG es comúnmente empleado para la tinción de la MLI, la sospecha de su toxicidad sobre la retina y el epitelio pigmentario de la retina (EPR) ha reabierto el debate sobre su uso (22-27). A fin de evitar esta toxicidad han surgido nuevas tinciones, como el verde de infracianina (28), el azul tripán (29,30) y la triamcinolona (31). Aceptado el uso de la cirugía para el tratamiento de los agujeros maculares en estadío II, III y IV, los cirujanos buscan ahora nuevas técnicas quirúrgicas que mantengan los porcentajes actuales de éxito anatómico y funcional, reduciendo al máximo las complicaciones. Así, se plantea la creación de un desprendimiento de vítreo posterior durante la vitrectomía sin necesidad de retirar la MLI (32) o la realización de una vitrectomía reducida (33).
La cirugía del AM en nuestro centro ha evolucionado de forma paralela al desarrollo de estos conocimientos. El objetivo de este estudio es comparar la efectividad, eficiencia y complicaciones de las tres técnicas quirúrgicas empleadas en el tratamiento del agujero macular, en el período 1998-2004 en nuestro hospital, tanto entre sí como con los resultados recogidos en la literatura al respecto.
Sujetos, material y métodos
Se ha realizado un estudio retrospectivo, comparativo, intervencionista y no aleatorizado de 131 ojos con agujeros maculares idiopáticos en estadío III y IV de Gass intervenidos en el Hospital Universitario Central de Asturias entre los años 1998 y 2004. Fueron excluidos del estudio los agujeros maculares secundarios a traumatismos, los pacientes con retinopatía diabética, degeneración macular asociada a la edad o miópica y aquellos con antecedente de cirugía de retina. En todos los individuos se obtuvo el consentimiento informado aceptado por el comité ético hospitalario.
En función de la técnica quirúrgica utilizada se dividen los ojos operados en tres grupos: grupo 1, grupo 2 y grupo 3. En el grupo 1 se incluyen 25 ojos en los que se realizó vitrectomía sin liberación de la MLI; de éstos, 8 correspondían a varones y 17 a mujeres, con edades comprendidas entre los 62 y 76 años, media de 70,3, desviación estándar (D.E.: 4,09). La agudeza visual previa a la cirugía en este grupo oscilaba entre 0,02 y 0,3, media 0,14 (D.E.: 0,11). En el grupo 2 fueron incluidos 19 ojos en los que se realizó la técnica anterior asociada a la liberación de la MLI; de éstos, 9 correspondían a varones y 10 a mujeres, con edades comprendidas entre los 61 y 80 años, media de 72,0 años (D.E.: 4,42). La agudeza visual previa a la cirugía en este grupo fluctúo entre 0,02 y 0,2, media 0,09 (D.E.: 0,11). El grupo 3 reunió a 87 ojos en los que se realizó la rexis de la MLI previa tinción con diferentes concentraciones de ICG, 33 pertenecían a varones y 54 a mujeres, con edades entre los 51 y 84 años, media de 68,9 años (D.E.: 7,77). La agudeza visual previa se situaba entre 0,02 y 0,55, media de 0,12 (D.E.: 0,11). Las características basales eran equiparables en todos los grupos.

Fig. 1.Agujero macular idiopático antes de la cirugía.

Fig. 2.Agujero macular cerrado después de la cirugía.
Los pacientes incluidos en el grupo 3 recibieron concentraciones decrecientes de ICG: 5,0 mg/ml (48,4%), 2,5 mg/ml (27,4%) y 0,5 mg/ml (24,2%), en función de la evolución de las técnicas quirúrgicas y los conocimientos científicos.
El tiempo de evolución del agujero macular fue recogido en 94 ojos, estando comprendido entre 1 y 120 meses, media de 12,8 (D.E.: 16,8) y no existiendo diferencias estadísticamente significativas entre los 3 grupos.
El porcentaje de afectación bilateral fue de: seis casos en el grupo 1 (24%); tres casos en el grupo 2 (15,8%) y doce casos en el grupo 3 (13,8%). Con respecto al total, 21 casos (16%) desarrollaron un agujero macular bilateral.
En todos los casos se realizó, antes y después de la cirugía, una exploración oftalmológica completa que incluía: agudeza visual (AV) mediante escala de Snellen, exploración del segmento anterior, tensión ocular, visualización del fondo de ojo mediante oftalmoscopia indirecta y estudio biomicroscópico de la mácula. En casos seleccionados se realizaron retinografías, estudios angiográficos o campos visuales.
Preoperatoriamente se recogieron datos de: edad, género, ojo afectado, mejor agudeza visual corregida preoperatoria, tiempo de evolución, presencia de metamorfopsias, estado del cristalino y tamaño del agujero.
Entre los 130 ojos en los que se recogió el estado del cristalino previamente a la cirugía, en 15 (11,5%) se realizó una cirugía combinada, 9 de ellos en el año 2004. La técnica quirúrgica consistió en una facoemulsificación, con implante de lente intraocular en saco capsular, seguida de vitrectomía.
La cirugía fue siempre realizada por los mismos cirujanos (JCN y CGC). Todos los pacientes fueron intervenidos bajo anestesia peribulbar con una mezcla de Lidocaína al 5% (B. Braun Medical S.A Barcelona) y Bupivacaína al 0,75% (Inibsa, S.A Laboratorios Barcelona) y sedación cuando precisaban. Se realizó una vitrectomía por tres vías, vía pars plana, seguida de liberación, en todos los pacientes, del cortex vítreo. Si existía una membrana epirretiniana (MER) ésta se retiraba con unas pinzas de membrana. Durante la cirugía se utilizó un sistema de visualización de campo amplio y una lente de polo posterior.
La rexis de la MLI se llevó a cabo a partir de febrero del 2000. Se realizaba una pequeña incisión en la MLI con una pinza vitreorretiniana. Posteriormente se llevaba a cabo la liberación de la membrana alrededor de la fóvea con un tamaño aproximado de tres diámetros de disco mediante una maniobra de membranorrexis circular.
La ICG se utilizó desde marzo del 2001. Las soluciones fueron preparadas reconstituyendo el vial de 25 mg de verde de indocianina (ICG-PULSION. Medical Systems AG. München) con 0,5 mL de agua destilada estéril. Una vez disuelto totalmente se añadía a la solución 4,5 ml de solución salina balanceada (BSS) para obtener una concentración final de 5 mg/ml, y 9,5 ml de BSS para obtener una concentración de 2,5 mg/ml. En el caso de la disolución de menor concentración (0,5 mg/ml) se añadió, en vez de BSS, 9,5 ml de suero glucosado al 5%. Un ml de esta disolución (2,5 mg) se diluye con 4 ml de suero glucosado para obtener la concentración final deseada. Se aplicaba una pequeña cantidad de esta solución (0,1-0,2 ml) directamente sobre la retina a nivel de la mácula, al tiempo que se cerraba la infusión. Se mantenía durante 2 minutos, en el caso del ICG al 5% y al 2,5%, y 30 segundos para la concentración al 0,5% antes de proceder a su lavado y aspiración.
Finalmente se llevaba a cabo un intercambio fluido-gas (C3F8 o SF6 —utilizado en 17,6% de los ojos—) a concentraciones discretamente expansibles (15% y 25% respectivamente), y tratamiento postural específico durante 7 días.
Todos los pacientes fueron evaluados al día siguiente de la intervención, a la semana, al mes, y a los 3 y 6 meses. Sólo los pacientes de nuestra Área Sanitaria pudieron ser seguidos durante un período máximo de 48 meses, pues el resto de pacientes se derivaron progresivamente a sus respectivos centros de atención. El período de seguimiento pues fue de 6 a 48 meses (media de 10,8 meses). Se comprobó la agudeza visual, la tensión intraocular, el estado del cristalino, las complicaciones surgidas durante y después de la cirugía y el estado macular.
El éxito anatómico se define como la completa desaparición del líquido subrretiniano y los bordes de agujero. Éste se evaluó tras la completa desaparición del gas intraocular. La imposibilidad de cierre inicial del agujero así como su reapertura, se consideraron fracasos de la cirugía.
La recuperación funcional se considera cuando la agudeza visual mejora una o más líneas de Snellen.
Los resultados fueron analizados mediante pruebas no paramétricas considerando p<0,05 como estadísticamente significativo. El análisis estadístico se llevó a cabo con el programa SPSS 12.0 para Windows (SPSS for Windows, SPSS Inc, Chicago, USA).
Resultados
Se recogieron 131 ojos, 81 eran mujeres (61,8%) y 50 varones (38,2%), con una edad media de 69,6 años (intervalo de 51 a 84 años). El 16% de los pacientes presentaban agujero macular bilateral a lo largo del seguimiento. Según los grupos, la afectación bilateral fue de: 6 casos en el grupo 1 (24%); 3 casos en el grupo 2 (15,8%) y 12 casos en el grupo 3 (13,8%).
Se pudo evaluar la resolución anatómica en 129 ojos. De éstos, en 16 (12,2%) fracasó la primera cirugía. En la mitad de los mismos (6,1%), se llevo a cabo una segunda cirugía. Se consiguió la resolución anatómica en 114 ojos (88,4%). Analizando los resultados por grupos, encontramos resolución anatómica en el 80% (20 casos) de los pacientes del grupo 1, en el 89,5% (17 casos) de los pacientes del grupo 2 y en el 90,6% (77 casos) de los pacientes del grupo 3. A pesar del éxito creciente, no se encontraron diferencias significativas en el porcentaje de resolución entre los diferentes grupos. La recuperación funcional con mejoría de la agudeza visual de una o más líneas se consiguió en 82 casos (63,6%), 26 ojos (20,3%) mantuvieron una agudeza visual idéntica a la prequirúrgica y 20 empeoraron (15,6%) (fig. 3). Tampoco se encontraron diferencias estadísticamente significativas entre los distintos grupos (fig. 4).

Fig. 3.Comparación de la agudeza visual pre y post-cirugía.

Fig. 4.Comparación de las AV finales en cada tipo de cirugía.
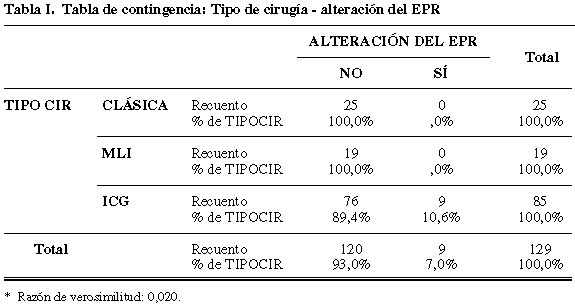
Entre las complicaciones derivadas de la cirugía se produjeron dos desprendimientos de retina (DR) intraoperatorios producidos por pequeñas roturas periféricas próximas a las esclerotomías, dos casos de persistencia de escotoma central posteriormente a la cirugía, un caso de paso de gas a la cámara anterior durante el intercambio y cuatro casos de DR varias semanas después de la intervención quirúrgica. No se pudo realizar el análisis por subgrupos porque sólo se recogieron la existencia o no de complicaciones en ocho pacientes de los grupos 1 y 2. Este escaso número de complicaciones registradas no se debe a la ausencia de las mismas en estos dos grupos o a su acúmulo en el grupo 3, sino a una recogida menos minuciosa de datos clínicos en la historia clínica de los pacientes en los primeros años de revisión, con la consiguiente pérdida de información. Se observó la presencia de catarata post-cirugía en el 51,9% de los ojos intervenidos, sin encontrarse diferencias entre los diferentes grupos. En la primera revisión tras la cirugía, 29 ojos (37,2%) tenían una presión intraocular (PIO) elevada. En todos los casos se resolvió en el transcurso de las 3 primeras semanas. No se encontraron diferencias entre los diferentes grupos ni tampoco en el análisis multivariante entre el gas empleado en el taponamiento y la presencia de PIO elevada post-cirugía. Se registró alteración del epitelio pigmentario de la retina en nueve ojos (7%), todos ellos pertenecientes al grupo 3, siendo este resultado estadísticamente significativo (p<0,05). Sin embargo, no sabemos si esta alteración es debida exclusivamente a la tinción de la MLI con ICG —toxicidad directa— o a la combinación de rexis y tinción, ya que sólo se encontraron diferencias significativas entre uso y no uso de ICG (tablas I y II). Como resumen, las tres complicaciones más frecuentes registradas tras la cirugía del agujero macular fueron las cataratas (51,9 %), la PIO elevada (37,2%) y el desarrollo de DR, intraoperatorio o varias semanas después a la cirugía, (6 ojos –7,8%–); y la única estadísticamente significativa la alteración del EPR con el uso de ICG.
Se realizó un segundo análisis multivariante, empleando la resolución anatómica y la AV inicial y final como variables dependientes, a fin de identificar cualquier factor preoperatorio o intraoperatorio predictivo del éxito quirúrgico. Se encontró una correlación inversa entre el tamaño del agujero y la AV inicial y final (figs. 5 y 6); sin embargo la resolución anatómica fue independiente del tamaño (p=0,56). En cuanto al tiempo de evolución del agujero macular, se recogieron un mayor número de fracasos a mayor tiempo de evolución (los agujeros abiertos tuvieron un tiempo medio de evolución de 19,20 meses, mientras que los cerrados tuvieron una evolución de 11,98 meses), pero las DE son muy amplias para ambos grupos (21,27 y 16,41 respectivamente) y el número de ojos incluido, escaso (92 ojos). La presencia de MER se correlacionó con una mejor agudeza visual preoperatoria (media de 0,18 frente a 0,11 sin MER) y post-cirugía (media de 0,33 frente a 0,20 sin MER), así como con un mayor éxito anatómico (100% frente a 86,5%). Sin embargo, ningún estudio estadístico ha resultado significativo, probablemente por un tamaño muestral insuficiente.

Fig. 5.Comparación del tamaño del agujero macular (micras) con la AV pre-cirugía.

Fig. 6.Comparación del tamaño del agujero macular (micras) con la AV final.
Por último se analizó si el porcentaje de ICG empleado en la tinción de la MLI tenía alguna influencia en los resultados. No se encontraron diferencias en la AV final (p=0,32) ni en la resolución anatómica (p=0,77) entre los distintos grupos. Con respecto a las complicaciones, el grupo que reunió un mayor número de ellas es el que empleó la concentración del 5% (ocho ojos) frente a seis del grupo en el que se empleó la concentración del 2,5% y uno del grupo del 0,5%, sin diferencias significativas entre los mismos. No se encontraron diferencias en cuanto a la aparición de alteraciones del EPR en función de las diferentes concentraciones de ICG.
Discusión
La cirugía del AM continúa siendo tema de debate y de revisiones con el fin de obtener guías terapéuticas óptimas. Parece evidente, en función de los resultados obtenidos en diferentes estudios prospectivos y retrospectivos, que la cirugía es el tratamiento de elección para los agujeros maculares idiopáticos. Sin embargo, no todos los AM idiopáticos son susceptibles de cirugía. La Academia Americana de Oftalmología (34) recomienda el tratamiento quirúrgico sólo en los estadíos II, III y IV, mientras que los AM en estadío I deben vigilarse periódicamente debido a su mayor tasa de cierre espontáneo, ausencia de progresión y mejor AV.
En nuestro trabajo retrospectivo sobre 131 ojos en estadio III y IV se han alcanzado unas cifras totales de éxito anatómico del 88,4% y funcional del 63,6%; valores semejantes a la media de lo publicado (11,12,14,16,18). En nuestra serie, 20 pacientes empeoraron (15,6%) comparable con el 14% de Park (35), algo mejor que Freeman (36) con un 34% y peor en comparación con el 0% de Mester (37) y con el 6% de Haritoglou (38). Encontramos un 16% de afectación bilateral, comparable con el 15,6% de Ezra (39).
Los nuevos conocimientos sobre la patogénesis de los agujeros maculares indican que la MER, presente en ocasiones sobre la retina, no es la causa del AM, sino un intento del organismo de cerrar el agujero. La contracción de esta membrana incrementa el tamaño del agujero (40,41). Si se encuentra una MER, ésta debe eliminarse durante la cirugía a fin de conseguir mejores resultados anatómicos y funcionales. Nuestro trabajo coincide con los datos recogidos en la literatura sobre mejores AV finales en pacientes en los que se retira la MER (12,41).
Muchos artículos recogen el beneficio de la rexis de la MLI (9,10). Sin embargo, son menos los que comparan el resultado de la vitrectomía con y sin rexis de la MLI. Castro y González (11) analizaron retrospectivamente 50 ojos de 48 pacientes con AM idiopático en estadíos III y IV encontrando mejorías anatómicas y funcionales en el grupo en el que se realiza la rexis de la MLI. Al-Abdulla et al (12) recogían una mayor tasa de cierre tras la disección de la MLI, pero no encontraron diferencias en la AV final. Kumagai et al (18) sugieren que el peeling de la MLI incrementa el éxito anatómico y reduce las recurrencias; sin embargo, su beneficio es limitado en AM de larga evolución y gran tamaño; y no encuentran diferencias en la AV final. En nuestro trabajo no se han encontrado diferencias significativas entre los dos tipos de cirugías, tanto en el éxito anatómico como en el funcional, pero sí existe un mayor número de cierres tras realizar la rexis de la MLI (89,5%-90,6% frente al 80%).
Encontramos una correlación inversa entre el tamaño del agujero y AV inicial con la AV final; sin embargo la resolución anatómica fue independiente del tamaño. En cuanto al tiempo de evolución del agujero macular, parece existir un mayor número de fracasos a mayor tiempo de evolución. Resultados similares a Blumenkranz (8) que encuentra significativo el éxito anatómico y funcional en subgrupos de AM de menos de 450 micras y de menos de 6 meses de evolución; al igual que Brooks (9). Kumagai también encontró, a menor tamaño y menos evolución, un mayor éxito significativo en el grupo sin rexis de la MLI, pero no en el grupo con rexis de la MLI. Postula la efectividad de la rexis en AM de más de 6 meses de evolución y el escaso valor de la misma en AM grandes al encontrar cifras semejantes de éxito entre los 2 grupos (18).
Por otra parte, la rexis de la MLI puede dañar la retina subyacente. Haritoglou et al (38) encontraron en el 56% de los pacientes escotomas paracentrales que, aunque asintomáticos, indicarían lesión en la retina subyacente. En nuestro estudio no encontramos diferencias en la alteración del campo visual en los diferentes grupos analizados.
La ICG permite una mejor visualización de la MLI, facilitando la cirugía. Hay series que describen un descenso de éxitos funcionales, controlando otras variables, al usar ICG (19). Otros recogen mejorías tanto anatómicas como funcionales (13,16,17,20). En nuestro estudio no se encuentran diferencias, obteniéndose buenos resultados quirúrgicos y funcionales. Otro aspecto cada vez más importante concerniente al uso de ICG es su toxicidad. Nosotros sólo encontramos una mayor alteración del EPR (7%) en relación con el uso de ICG. Estos datos coinciden con lo publicado por Engelbrecht et al (24) y Ho et al (25). Asimismo se han descrito defectos campimétricos (19,27) por lesión de la capa de fibras nerviosas que se han relacionado con la creación de un plano de clivaje falso por el ICG (22). Nuestra serie sólo recoge dos pacientes con escotomas. No existen muchos estudios que intenten relacionar la toxicidad del ICG con su concentración, pH, osmolaridad o tiempo de contacto con la retina. Kwok et al (21) no encuentran diferencias usando concentraciones entre 0,2% y 1,25%. Tampoco en nuestra serie se encuentran diferencias con concentraciones entre 0,5% y 5%. Sin embargo, los grupos no son comparables pues difieren en el tiempo de exposición de la retina (en las primeras cirugías la exposición era de 2-3 minutos reduciéndose posteriormente a 30 segundos) y en el disolvente empleado (primero BSS y en la actualidad suero glucosado al 5%).
Van de Moere et al (28) describieron la utilización de verde de infracianina, como alternativa al uso de ICG, con éxito anatómico y funcional. Vote et al (29) defienden a su vez el uso de azul tripán, a pesar de no ser éste un colorante selectivo para la MLI. Lee et al (30) compararon el ICG y el azul tripán, y obtuvieron mejores resultados visuales en el grupo en el que se empleó el azul. La cirugía intraocular empleando triamcinolona también se ha utilizado con éxito para el cierre de los AM (31).
Los últimos avances en la cirugía del AM buscan una cirugía individualizada (32) y mínimamente traumática (33).
Nuestros resultados están sometidos a múltiples limitaciones. Se trata de un estudio retrospectivo, consecutivo y no aleatorizado en cada una de las 3 técnicas realizadas. Los resultados de AV final, en algunos casos, son los obtenidos tras haber sido intervenidos de catarata sin poder valorar si la AV posquirúrgica es diferente antes y después de la facoemulsificación y si ésta acentúa alguna complicación. De la misma manera, la posibilidad de obtener resultados estadísticamente significativos es escasa, por el tamaño reducido de las muestras y por la desigual recogida de datos a lo largo del tiempo. Sin embargo, orientan sobre la efectividad, eficacia y seguridad de las técnicas utilizadas y permiten establecer un futuro protocolo de actuación en esta patología.
Podemos concluir que la cirugía mejora la agudeza visual en el 63,6% de los casos. A pesar del incremento, no se han encontrado diferencias significativas en el porcentaje de éxito anatómico y funcional entre los diferentes grupos. La posible causa sería el reducido tamaño de los subgrupos.
Encontramos como factores predictivos del éxito quirúrgico, el tamaño del agujero y la AV inicial. Sin embargo, la resolución anatómica está más relacionada con la evolución del agujero macular que con el tamaño. La presencia de MER se correlaciona con una mejor agudeza visual previa y final, así como con un mayor éxito anatómico. Las alteraciones del EPR se recogen en el grupo de rexis de la MLI con ICG. Aunque se podría apuntar al colorante como posible implicado en la génesis de estas alteraciones por toxicidad directa, no podemos determinar si la propia rexis de la MLI teñida, quizás a través de la creación de un plano de clivaje falso, contribuye a la aparición de las mismas.
Quedan muchas preguntas aún por contestar. Desde el punto de vista quirúrgico sería interesante delimitar si es siempre necesario realizar la rexis de la MLI, clarificar el beneficio real del uso de ICG o de otras tinciones y determinar la etiología de las alteraciones del EPR. Socialmente se debería evaluar el beneficio real de la cirugía en la vida cotidiana de los pacientes.
Agradecimientos
Los autores agradecen a la Dra. Begoña Baamonde Arbaiza, médico adjunto del Servicio de Oftalmología del HUCA y al Dr. Norberto Corral Blanco, catedrático del Departamento de Estadística e I.O y Didáctica de la Matemática, el apoyo constante y la ayuda prestada.
Bibliografía
1. Gass JD. Idiopathic senile macular hole. Its early stages and pathogenesis. Arch Ophthalmol 1988; 106: 629-639. [ Links ]
2. Kelly NE, Wendel RT. Vitreous surgery for idiopathic macular holes. Results of a pilot study. Arch Ophthalmol 1991; 109: 654-659. [ Links ]
3. Glaser BM, Michels RG, Kuppermann BD, Sjaarda RN, Pena RA. Transforming growth factor –beta 2 for the treatment of full-thickness macular holes. A prospective randomized study. Ophthalmology 1992; 99: 1162-1173. [ Links ]
4. García Arumi J, Salvador Rodríguez F, Mateo García C, Corcóstegui Guraya B. Vitrectomía y suero autólogo como tratamiento del agujero macular idiopático. Arch Soc Esp Oftalmol 1996; 71: 415-422. [ Links ]
5. Liggett PE, Skolik DS, Horio B, Saito Y, Alfaro V, Mieler W. Human autologous serum for the treatment of full-thickness macular holes. A preliminary study. Ophthalmology 1995; 102: 1071-1076. [ Links ]
6. Ezra E, Gregor ZJ, Moorfields Macular Hole Study Group Report No. 1. Surgery for idiopathic full-thickness macular hole: two-year results of a randomised clinical trial comparing natural history, vitrectomy, and vitrectomy plus autologous serum: Moorfields Macular Hole Study Group Report No.1. Arch Ophthalmol 2004; 122: 224-236. [ Links ]
7. Olsen TW, Sternberg P Jr, Capone A Jr, Martin DF, Lim JI, Grossniklaus HE, et al. Macular hole surgery using thrombin-activated fibrinogen and selective removal of the internal limiting membrane. Retina 1998; 18: 322-329. [ Links ]
8. Blumenkranz MS, Ohana E, Shaikh S, Chang S, Coll G, Morse LS, et al. Adjuvant methods in macular hole surgery: intraoperative plasma-thrombin mixture and postoperative fluid-gas exchange. Ophthalmic Surg Lasers 2001; 32: 198-207. [ Links ]
9. Brooks HL Jr. Macular hole surgery with and without internal limiting membrane peeling. Ophthalmology 2000; 107: 1939-1949. [ Links ]
10. Haritoglou C, Gass CA, Schaumberger M, Gandorfer A, Ulbig MW, Kampik A. Long-term follow-up after macular hole surgery with internal limiting membrane peeling. Am J Ophthalmol 2002; 134: 661-666. [ Links ]
11. Castro Navarro J, González Castaño C. Cirugía del agujero macular con y sin liberación de la membrana limitante interna. Arch Soc Esp Oftalmol 2003; 78: 159-164. [ Links ]
12. Al-Abdulla NA, Thompson JT, Sjaarda RN. Results of macular hole surgery with and without epiretinal dissection or internal limiting membrane removal. Ophthalmology 2004; 111: 142-149. [ Links ]
13. Da Mata AP, Burk SE, Riemann CD, Rosa RH Jr, Snyder ME, Petersen MR, et al. Indocyanine green-assisted peeling of the retinal internal limiting membrane during vitrectomy surgery for macular hole repair. Ophthalmology 2001; 108: 1187-1192. [ Links ]
14. Sheidow TG, Blinder KJ, Holekamp N, Joseph D, Shah G, Grand MG, et al. Outcome results in macular hole surgery. An evaluation of internal limiting membrane peeling with and without indocyanine green. Ophthalmology 2003; 110: 1697-1701. [ Links ]
15. Haritoglou C, Neubauer A, Gandorfer A, Thiel M, Kampik A. Indocyanine green for successful repair of a long-standing macular hole. Am J Ophthalmol 2003; 136: 389-391. [ Links ]
16. Wolf S, Reichel MB, Wiedemann P, Schnurrbusch UE. Clinical findings in macular hole surgery with indocyanine green-assisted peeling of the internal limiting membrane. Graefes Arch Clin Exp Ophthalmol 2003; 241: 589-592. [ Links ]
17. Kwok AK, Lai TY, Man-Chan W, Woo DC. Indocyanine green assisted retinal internal limiting membrane removal in stage 3 or 4 macular hole surgery. Br J Ophthalmol 2003; 87: 71-74. [ Links ]
18. Kumagai K, Furukawa M, Ogino N, Uemura A, Demizu S, Larson E. Vitreous surgery with and without internal limiting membrane peeling for macular hole repair. Retina 2004; 24: 721-727. [ Links ]
19. Ando F, Sasano K, Ohba N, Hirose H, Yasui O. Anatomic and visual outcomes after indocianine green-assisted peeling of the retinal internal limiting membrane in idiopathic macular hole surgery. Am J Ophthalmol 2004; 137: 609-614. [ Links ]
20. Da Mata AP, Burk SE, Foster RE, Riemann CD, Petersen MR, Nehemy MB, et al. Long-term follow-up of indocyanine green-assisted peeling of the retinal internal limiting membrane during vitrectomy surgery for idiopathic macular hole repair. Ophthalmology 2004; 111: 2246-2253. [ Links ]
21. Kwok AK, Lai TY, Yew DT, Li WW. Internal limiting membrane staining with various concentrations of indocyanine green dye under air macular surgeries. Am J Ophthalmol 2003; 136: 223-230. [ Links ]
22. Gandorfer A, Haritoglou C, Gass CA, Ulbing MW, Kampik A. Indocyanine green-assisted peeling of the internal limiting membrane may cause retinal damage. Am J Ophthalmol 2001; 132: 431-433. [ Links ]
23. Haritoglou C, Gandorfer A, Gass CA, Schaumberger M, Ulbing MW, Kampik A. Indocyanine green-assisted peeling of the internal limiting membrane in macular hole surgery affects visual outcome: a clinicopathologic correlation. Am J Ophthalmol 2002; 134: 836-841. [ Links ]
24. Engelbrecht N, Freeman J, Sternberg P Jr, Aaberg TM Sr, Aaberg TM Jr, Martin DF, et al. Retinal pigment epithelial changes after macular hole surgery with indocyanine green-assisted internal limiting membrane peeling. Am J Ophthalmol 2002; 133: 89-94. [ Links ]
25. Ho JD, Tsai RJ, Chen SN, Chen HC. Cytotoxicity of indocyanine green on retinal pigment epithelium: implications for macular hole surgery. Arch Ophthalmol 2003; 121: 1423-1429. [ Links ]
26. Gass CA, Haritoglou C, Schaumberger M, Kampik A. Functional outcome of macular hole surgery with and without indocyanine green-assisted peeling of the internal limiting membrane. Graefes Arch Clin Exp Ophthalmol 2003; 241: 716-720. [ Links ]
27. Kanda S, Uemura A, Yamashita T, Kita H, Yamakiri K, Sakamoto T. Visual field defects after intravitreous administration of indocyanine green in macular hole surgery. Arch Ophthalmol 2004; 122: 1447-1451. [ Links ]
28. Van De Moere A, Stalmans P. Anatomical and visual outcome of macular hole surgery with infracyanine green-assisted peeling of the internal limiting membrane, endodrainage, and silicone oil tamponade. Am J Ophthalmol 2003; 136: 879-887. [ Links ]
29. Vote BJ, Russell MK, Joondeph BC. Trypan blue-assisted vitrectomy. Retina 2004; 24: 736-738. [ Links ]
30. Lee KL, Dean S, Guest S. A comparison of outcomes after indocyanine green and trypan blue assisted internal limiting membrane peeling during macular hole surgery. Br J Ophthalmol 2005; 89: 420-424. [ Links ]
31. Horio N, Horiguchi M, Yamamoto N. Triamcinolone-assisted internal limiting membrane peeling during idiopathic macular hole surgery. Arch Ophthalmol 2005; 123: 96-99. [ Links ]
32. Kimura T, Takahashi M, Takagi H, Kiryu J, Nishiwaki H, Tanabe T, et al. Is removal of internal limiting membrane always necessary during stage 3 idiophatic macular hole surgery? Retina 2005; 25: 54-58. [ Links ]
33. Spaide RF. Macular hole repair with minimal vitrectomy. Retina 2002; 22: 183-186. [ Links ]
34. Benson WE, Cruickshanks KC, Fong DS, Williams GA, Bloome MA, Frambach DA, et al. Surgical management of macular holes: a report by the American Academy of Ophthalmology. Ophthalmology 2001; 108: 1328-1335. [ Links ]
35. Park DW, Sipperley JO, Sneed SR, Dugel PU, Jacobsen J. Macular hole surgery with internal-limiting membrane peeling and intravitreous air. Ophthalmology 1999; 106: 1392-1398. [ Links ]
36. Freeman WR, Azen SP, Kim JW, el-Haig W, Mishell DR 3rd, Bailey I. Vitrectomy for the treatment of full-thickness stage 3 or 4 macular holes. Results of a multicentered randomized clinical trial. The Vitrectomy for Treatment of Macular Hole Study Group. Arch Ophthalmol 1997; 115: 11-21. [ Links ]
37. Mester V, Kuhn F. Internal limiting membrane removal in the management of full–thickness macular holes. Am J Ophthalmol 2000; 129: 769-777. [ Links ]
38. Haritoglou C, Gass CA, Schaumberger M, Ehrt O, Gandorfer A, Kampik A. Macular changes after peeling of the internal limiting membrane in macular hole surgery. Am J Ophthalmol 2001; 132: 363-368. [ Links ]
39. Ezra E, Wells JA, Gray RH, Kinsella FM, Orr GM, Grego J, et al. Incidence of idiopathic full-thickness macular holes in fellow eyes. A 5-year prospective natural history study. Ophthalmology 1998; 105: 353-359. [ Links ]
40. ooh HS, Brooks HL Jr, Capone A Jr, L´Hernault NL, Grossniklaus HE. Ultrastructural features of tissue removed during idiopathic macular hole surgery. Am J Ophthalmol 1996; 122: 67-75. [ Links ]
41. Smiddy WE, Flynn HW Jr. Pathogenesis of macular holes and therapeutic implications. Am J Ophthalmol 2004; 137: 525-537. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Eva Villota Deleu
C/ Manuel Fernández Avello, 21 - 6º E
33010 Oviedo (Asturias)
España
E-mail: milideleu@yahoo.es
Recibido: 01.06.05
Aceptado: 19.10.06