Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Archivos de la Sociedad Española de Oftalmología
versão impressa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.86 no.9 Set. 2011
Detección automática de microaneurismas en retinografías
Automatic detection of microaneurysms in colour fundus images
S. Jiméneza, P. Alemanya, F. Núñez Benjumeab, C. Serranob, B. Achab, I. Fondónb, F. Carrala y C. Sáncheza
aServicio de Oftalmología, Hospital Universitario Puerta del Mar, Cádiz, España
bDepartamento de Teoría de la Señal y Comunicaciones, Universidad de Sevilla, Sevilla, España
Este proyecto está subvencionado por el Ministerio de Sanidad (ETES-PI07/90373 y ETES-PI07/90379).
Dirección para correspondencia
RESUMEN
Propósito: Presentamos el desarrollo de una herramienta para la detección automática de microaneurismas y su evaluación clínica. El propósito de esta herramienta es facilitar el diagnóstico de lesiones diabéticas en programas generales de detección.
Método: La herramienta diseñada y desarrollada consta de tres etapas de procesamiento: 1) Obtención de la imagen de fondo de ojo con el retinógrafo, inversión del canal verde y filtrado paso de alta de la imagen. Esta fase realza los microaneurismas. 2) Detección de los candidatos a microaneurismas, mediante un filtrado de predicción adaptativo y un crecimiento de regiones. 3) Selección, de entre los candidatos, de los que deben considerarse microaneurismas por cumplir con los criterios de: forma circular, intensidad alta en el canal verde invertido y contraste respecto a los píxeles de alrededor.
Resultados: Se seleccionaron 20 retinografías de buena calidad y dimensiones 600×600 píxeles de pacientes con retinopatía diabética no proliferante. Los oftalmólogos detectaron un total de 297 microaneurismas en estas imágenes. La herramienta de detección automática localizó adecuadamente 252 microaneurismas, con una sensibilidad media del 89% y una tasa de falsos positivos del 93%.
Conclusiones: Los resultados obtenidos parecen indicar que la herramienta desarrollada podría ser muy útil para su potencial utilización en programas de detección en los centros de asistencia primaria. Por otro lado, es necesario seguir trabajando en el algoritmo para disminuir la tasa de falsos positivos.
Palabras clave: Retinopatía diabética. Microaneurismas. Diagnóstico asistido por computador. Procesamiento de datos asistido por computador.
ABSTRACT
Purpose: We present the development of a tool for the automatic detection of microaneurysms and its clinical evaluation. The intention of this tool is to facilitate the diagnosis of diabetic retinopathy in general screening programs.
Method: The designed and developed tool consists of three stages of processing: 1) Obtaining of the basic image of eye with the retinal camera, inverted image on the green channel, and a high-pass filter of the image. This phase enhances the microaneurysms. 2) Detection of the candidates for microaneurysms, by means of an adaptive prediction filter and regions growth. 3) Selection, among the candidates, of whom microaneurysms must be considered to fulfil the criteria of circular shape, high intensity in the inverted green channel and contrasts with respect to the surrounding pixels.
Results: We selected to 20 retinal photographs of good quality and dimensions 600x600 pixels from patients with nonproliferative diabetic retinopathy. The ophthalmologists detected 297 microaneurysms in these images. The tool for automatic detection correctly located 252 microaneurysms, with a mean sensitivity of 89% and a false positives rate of 93%.
Conclusions: The results obtained seem to indicate that the tool developed will be very useful for its potential use in screening programs in primary care centres. On the other hand, more work is needed on the algorithm to decrease the rate of false positives.
Key words: Diabetic retinopathy. Microaneurysm. Computer-aided diagnosis. Computer data processing.
Introducción
La evaluación cuantitativa del número de microaneurismas (MA) es un buen indicador de la progresión de la retinopatía diabética (RD)1. Sin embargo, una comparación manual de las diferentes imágenes temporales del paciente consume mucho tiempo del especialista, con lo que sería deseable disponer de una herramienta que permitiera su detección y cuantificación automáticas. Asimismo esta herramienta sería de gran utilidad para asistir al diagnóstico en Atención Primaria.
Un número importante de publicaciones en el campo de la ingeniería abordan este problema2. La mayoría de ellas se centra en la detección de MA en angiografías de fluoresceína3-7. Øien y Osnes fueron los primeros en detectar MA en imágenes en color8. Tras ellos, varios investigadores han seguido publicando trabajos en esta línea9-11.
En el presente trabajo se propone una nueva técnica para la detección automática de MA. Dicha técnica se basa en el uso de filtros de predicción adaptativos y crecimiento de regiones.
Sujetos, material y métodos
Utilizamos 30 retinografías -con buena calidad de imagen- del Programa de Detección Precoz de Retinopatía Diabética de la Consejería de Salud de la Junta de Andalucía, captadas con retinógrafos no midriáticos, en pacientes con retinopatía diabética no proliferante leve y moderada, sin lesiones diabéticas blancas. Diez retinografías se utilizan para elaborar el algoritmo y veinte para validarlo.
En la Figura 1 se presenta un diagrama de flujo del método. Conforme se muestra en la figura, la herramienta desarrollada consta de tres etapas de procesado: 1) Preprocesado. 2) Detección de los candidatos a MA. 3) Selección, de entre los candidatos, de los que deben considerarse MA. En las siguientes subsecciones se detallan estos tres bloques de procesado.

Fig. 1. Diagrama de flujo del algoritmo
para la detección de microaneurismas.
Bloque de preprocesamiento
El objetivo de este bloque es preparar la imagen para su tratamiento posterior, aislando las imágenes de características no inherentes al fondo de ojo, tales como iluminación y contraste. Este bloque puede dividirse en los pasos siguientes:
1) Inversión del canal verde: según se describe en Walter et al.10, de los tres planos de color el que contiene información más relevante es el canal verde (G). A dicho plano se le aplica una operación de inversión de los niveles de gris, obteniendo el negativo del plano verde. Esta inversión se realiza porque de esta manera se muestran más claramente los MA. Un ejemplo de esta imagen se muestra en la Figura 2.
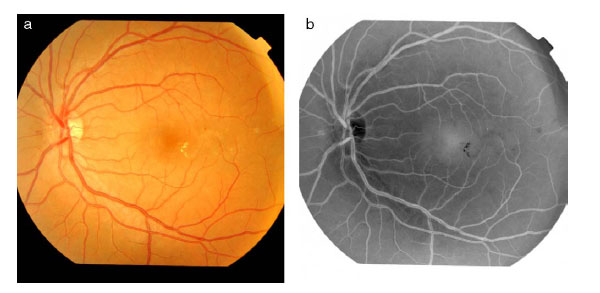
Fig. 2. a) Imagen de retinografía original en color. b) Imagen del negativo del plano verde.
2) Filtrado paso de alta o high pass (HP): este paso consiste en aplicar un filtro paso de alta a la inversión del canal verde. Una vez realizada esta operación se obtiene una nueva imagen en la que se resaltarán aquellos píxeles cuyos valores sean muy diferentes de los de sus vecinos, mientras que los que poseen un valor homogéneo tomarán valores cercanos a cero, es decir, un filtrado paso de alta realza los detalles de la imagen12.
3) Ampliación de contraste: el objetivo de esta operación es ampliar el rango dinámico de la imagen, es decir, aumentar el contraste de la misma mediante la separación de niveles de intensidad parecidos.
4) Filtrado morfológico top-hat: este bloque es el encargado de eliminar el árbol vascular. Para ello, este filtrado depende de la forma (de ahí que sea un filtrado morfológico) y es capaz de diferenciar entre elementos circulares (microaneurismas) y líneas curvas que pueden asimilarse como una sucesión de tramos rectos (árbol vascular)12.
Una vez realizados estos pasos, la imagen es apta para detectar sus microaneurismas.
Bloque de detección
El objetivo de este bloque es la obtención de unos puntos -semillas- a partir de los cuales se aplicará la siguiente fase en la que obtendremos los candidatos a microaneurismas.
Para la detección de las semillas se usa un algoritmo de predicción lineal en 2D (algoritmo de Burg)13,14. Su funcionamiento puede resumirse de la siguiente manera: el algoritmo recorre fila a fila todos los píxeles de la imagen, prediciendo el valor del siguiente píxel que va a examinar a partir del valor de sus píxeles vecinos. El error de predicción superior a un umbral en un determinado píxel indica que este es un punto singular (posible microaneurisma). Junto con la condición de que su error de predicción sea superior a un umbral, para que un píxel sea etiquetado como semilla, este debe tener al menos un vecino con la característica de ser también punto singular. De esta forma se evita que puntos aislados sean considerados microaneurismas15-17.
Bloque de segmentación
El objetivo de la segmentación consiste en obtener el conjunto de píxeles (región) que conforman los candidatos a microaneurismas. El método empleado es el crecimiento de regiones por adición de píxeles con condiciones de parada. Las regiones las haremos crecer a partir de las semillas obtenidas en el bloque anterior.
El bloque de segmentación adquiere gran importancia, ya que de su resultado depende la clasificación posterior de los candidatos, puesto que la forma de las regiones segmentadas es una característica fundamental para la clasificación y además es de gran carga computacional.
El funcionamiento es el siguiente: para cada semilla se comprueba si en un entorno, llamado entorno de búsqueda, los píxeles colindantes son también semillas pertenecientes a la misma región. El propósito de esto es establecer una media y una desviación local de intensidad de los píxeles semilla contiguos. Con estos valores se crea un umbral que se usa para incluir en la región otros píxeles no semillas colindantes que puedan pertenecer a la misma región. Este umbral también se usa como condición de parada. Para agregar píxeles no semillas a la región se usa otro entorno, denominado entorno de agregación, en el que se buscan píxeles cuyo valor de intensidad supere el umbral. Conforme se van agregando píxeles no semillas, eestos se van considerando semillas a efectos de proseguir la búsqueda.
El umbral es totalmente local y además es variable, ya que cada vez que se añade un píxel a la región este se vuelve a calcular.
Bloque de selección final de microaneurisma
Una vez finalizada la segmentación se procede a la clasificación de las regiones resultantes para diferenciar los microaneurismas verdaderos de los simplemente candidatos. Consiste en un clasificador empírico basado en la extracción de tres características o descriptores: intensidad (I), tamaño (T) y forma de la lesión (F). El criterio de intensidad está basado en la diferencia local entre la intensidad promedio de la región global y la intensidad promedio de la región que rodea al píxel que es candidato. El criterio de tamaño no es más que el número de píxeles del candidato. El criterio de forma consiste en ver cómo es de parecida la forma del candidato a una gaussiana en 2D. Cada candidato puede cumplir, o no, cada uno de estos criterios, asignándole un 1 si cumple el criterio y un 0 si no lo cumple. Para decidir si el candidato es un microaneurisma se utiliza la siguiente inecuación:
Se aprecia que la característica de forma adquiere mayor peso a la hora de dilucidar si un candidato es o no un microaneurisma.
Resultados
Se han seleccionado 20 retinografías de buena calidad y dimensiones 600 × 600 píxeles. Las imágenes se seleccionan según la nitidez de los detalles, con predominio de lesiones diabéticas de color rojo (microaneurismas y hemorragias). En total los oftalmólogos detectaron 297 microaneurismas en las 20 imágenes. De entre estos, con la herramienta de detección automática, se localizaron 252 microaneurismas, obteniéndose una sensibilidad media del 89% y una tasa de falsos positivos del 93%. En la Tabla 1 se muestran los resultados obtenidos para las 20 imágenes de la base de datos.
Los parámetros variables del algoritmo han sido fijados a un valor constante para todas las imágenes de la base de datos, lo cual proporciona un método completamente automático al clínico.
Discusión
La inclusión de las nuevas tecnologías en la clínica es una práctica cada vez más extendida. Para el diagnóstico precoz de la retinopatía diabética es necesario un control periódico del fondo de ojo del paciente diabético mediante oftalmoscopía y/o retinografías.
Uno de los factores claves para la detección precoz de la retinopatía diabética es la aparición de los microaneurismas. El control periódico del número de microaneurismas permite evaluar el grado de severidad de la enfermedad. Este conteo es laborioso y consume mucho tiempo del clínico, con lo que una herramienta de ayuda al diagnóstico sería de gran ayuda al médico.
Aunque en los últimos años han surgido publicaciones sobre la detección automática de microaneurismas3-7, son pocas las que se centran en la detección en imágenes de retinografía8-11.
En este artículo se presenta un nuevo algoritmo para la detección de MA en retinografías. El sistema presenta una alta sensibilidad (89%), sin embargo el número de falsos positivos es alto. Como líneas futuras de este trabajo se propone la reducción de la tasa de falsos positivos mediante una mejora del preprocesamiento de la imagen, una detección del árbol vascular más exacta y el uso de una red neuronal para la clasificación final de los candidatos a MA.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Agradecimientos
Los autores muestran su agradecimiento a Alejandro Garzón Camacho por su contribución en la implementación del algoritmo.
Bibliografía
1. Klein R, Meuer SM, Moss SE, Klein BE. Retinal microaneurysm counts and 10-year progression of diabetic retinopathy. Archives of Ophthalmology. 1995; 113:1386-91. [ Links ]
2. Lee SC, Lee ET, Kingsley RM, Wang Y, Russell D, Klein R, et al. Comparison of diagnosis of early retinal lesions of diabetic retinopathy between a computer system and human experts. Arch Ophthalmol. 2001; 119:509-15. [ Links ]
3. Lay B. Analyse automatique des images angiofluorographiques au cours de la rétinopathie diabétique (thesis doctoralis). Paris: School of Mines; 1983. [ Links ]
4. Spencer T, Phillips RP, Sharp PF, Forrester JV. Automated detection and quantification of microaneurysms in fluorescein angiograms. Graefe's Arch Clin Exp Ophthalmol. 1991; 230:36-41. [ Links ]
5. Spencer T, Olson JA, McHardy KC, Sharp PF, Forrester JV. An image processing strategy for the segmentation and quantification of microaneurysms in fluorescein angiograms of the ocular fundus. Computers in Biomedical Research. 1996; 29:284-302. [ Links ]
6. Usher D, Dumsky M, Himaga M, Williamson TH, Nussey S, Boyce J. Automated detection of diabetic retinopathy in digital retinal images: a tool for diabetic retinopathy screening. Diabetic Medicine. 2004; 21:84. [ Links ]
7. Mendoca AM, Campilho AJ, Nunes JM. Automatic segmentation of microaneurysms in retinal angiogram of diabetic patients. Proc Int Conf on Image Analysis and Processing. 1999. 728-33. [ Links ]
8. Øien GE, Osnes P. Automatic detection of early symptoms from retinal images. Proc Norwegian Signal Processing Symposium. 1995. 135-40. [ Links ]
9. Niemeijer M, van Ginneken B, Staal J, Suttorp-Schulten MS, Abramoff MD. Automatic detection of red lesions in digital color fundus photographs. IEEE Trans Medical Imaging. 2005; 24:584-92. [ Links ]
10. Walter T, Massin P, Erginay A, Ordonez R, Jeulin C, Klein J-C. Automatic detection of microaneurysms in color fundus images. Medical Image Analysis. 2007; 11:555-66. [ Links ]
11. Fleming AD, Philip S, Goatman KA, Olson JA, Sharp PF. Automated microaneurysm detection using local contrast normalization and local vessel detection. IEEE Trans Medical Imaging. 2006; 25:1223-32. [ Links ]
12. Gonzalez RC, Woods RE. Digital Image Processing. 2.a ed. New Jersey: Prentice Hall; 2002. [ Links ]
13. Kuduvalli GR, Rangayyan RM. An Algorithm for Direct Computation of 2-D Linear Prediction Coefficients. IEEE Trans Signal Processing. 1993; 4:996-9. [ Links ]
14. Kuduvalli GR, Rangayyan RM. Performance of reversible image compression techniques for high-resolution digital teleradiology. IEEE Trans Medical Imaging. 1992; 11:430-45. [ Links ]
15. Acha B, Serrano C. Automatic detection of microaneurysms in retinal angiograms. Proc of Computer Assisted Radiology and Surgery (CARS). 2003; 17:1328. [ Links ]
16. Serrano C, Acha B, Revuelto S. 2D adaptive filtering and region growing algorithm for the detection of microaneurysms in retinal angiographies. SPIE Int Symp on Medical Imaging. 2004. 1924-31. [ Links ]
17. Acha B, Serrano C, Rangayyan RM, Desautels JEL. Detection of Microcalcifications in Mammograms Using Error of Prediction and Statistical Measures. Journal of Electronic Imaging 2009;18:013011-1-10. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: soledadjimenez@ono.com
(S. Jiménez).
Recibido el 5 de Agosto de 2010
Aceptado el 15 de Abril de 2011















