Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Archivos de la Sociedad Española de Oftalmología
versión impresa ISSN 0365-6691
Arch Soc Esp Oftalmol vol.87 no.4 abr. 2012
Glaucoma de ángulo cerrado secundario a topiramato
Angle-closure glaucoma secondary to topiramate use
M. Rodríguez-Blanco, A. Piñeiro, M. Bande y M.J. López-Valladares
Servicio de Oftalmología, Hospital de Conxo, Complexo Hospitalario Universitario de Santiago de Compostela, La Coruña, España
Dirección para correspondencia
RESUMEN
Caso clínico: Se presenta el caso de una mujer de 42 años que desarrolló un cuadro de miopía aguda y glaucoma de ángulo cerrado bilateral una semana después del inicio del tratamiento con topiramato. La biomicroscopía ultrasónica (BMU) reveló que la paciente presentaba un ángulo cerrado y una efusión coroidea bilateral. Con la retirada del fármaco se resolvió el cuadro.
Discusión: El topiramato puede desencadenar miopía aguda y glaucoma de ángulo cerrado en algunos pacientes debido a una efusión coroidea. La realización de la BMU parece ser una herramienta útil para observar la evolución del cuadro y su resolución tras la suspensión del fármaco.
Palabras clave: Topiramato. Miopía. Glaucoma de ángulo cerrado. Biomicroscopía ultrasónica.
ABSTRACT
Case report: We describe a 42 year-old patient who developed acute myopia and closed-angle glaucoma one week after beginning treatment with topiramate. Ultrasound biomicroscopy revealed a bilateral angle closure and choroidal effusion. The clinical findings resolved with withdrawal of the topiramate.
Discussion: Topiramate may cause acute myopia and closure angle glaucoma in some patients due to a choroidal effusion. Ultrasound biomicroscopy seems to be a useful tool for monitoring the progression of the clinical lesions and their resolution when the drug is withdrawn.
Key words: Topiramate. Myopia. Closed angle glaucoma. Ultrasound biomicroscopy.
Introducción
El topiramato (Topamax®, Janssen-Cilag, Madrid, España) es un monosacárido sulfamato empleado para el tratamiento de algunos tipos de epilepsias, recientemente también se ha comenzado a utilizar para tratar trastornos bipolares, migrañas o incluso para perder peso. Se han descrito efectos secundarios oculares al tratamiento con este fármaco tales como miopía transitoria (MT) o glaucoma por cierre angular (GCA)1-3 así como también alteraciones campimétricas o maculopatías secundarias a este fármaco4.
Presentamos el caso de una paciente con MT y GCA inducido por topiramato en el que se describe el probable mecanismo patogénico mediante biomicroscopía ultrasónica (BMU) así como la evolución del cuadro correlacionando los hallazgos clínicos con las imágenes ecográficas.
Caso clínico
Paciente de 42 años que acude a Urgencias por cuadro de disminución de agudeza visual (AV) de un día de evolución. Como antecedentes personales destaca una depresión en tratamiento. No presentaba antecedentes oftalmológicos de interés y negaba la utilización previa de gafas. Su tratamiento consiste en olanzapina 10mg, lorazepam 2mg y venlafaxina 150mg retard desde hacía varios meses. Una semana antes había comenzado a tomar topiramato para perder peso.
La AV es de contar dedos a un metro en ambos ojos (AO), que mejoraba a 20/40 con estenopeico. Al examen biomicroscópico presenta edema corneal y quemosis conjuntival, una cámara anterior estrecha y cierre angular evidenciado mediante gonioscopia. La presión intraocular (PIO) es de 55mmHg en AO. Se realiza por tanto el diagnóstico de GCA bilateral. Se le administra tratamiento tópico con pilocarpina 2% (Colircusí Pilocarpina 2%®, Alcon-Cusí, Barcelona, España), timolol 0.5% (Cusimolol 0.5%®, Alcon- Cusí, Barcelona, España), brimonidina 0.2% (Alphagan®, Allergan, Madrid, España) así como 1 comprimido de acetazolamida 250 (Edemox®, Chiesi, Barcelona, España). A las dos horas la PIO era de 30 y 32mmHg respectivamente.
A las 24 horas de la primera visita la visión continúa igual. Biomicroscópicamente el edema corneal ha desaparecido (Fig. 1a,b), la PIO es de 28 y 30mmHg respectivamente. Se realiza una BMU de AO mediante el sistema miomicroscopía ultrasónica (AVISO, Quantel, Clermont-Ferrand, France) con sonda de 50 MHz (Fig. 1c) que evidencia un cierre angular, una cámara anterior estrecha (2,18mm medidos desde el epitelio corneal hasta cápsula anterior del cristalino) así como un cuadro de efusión uveal que empuja hacia delante al cuerpo ciliar y diafragma iridocristaliniano en AO. La paciente es diagnosticada de GCA secundario asociado a un desprendimiento ciliocoroideo. La pilocarpina es suspendida en este momento y se continúa el tratamiento con hipotensores oculares. De acuerdo con el médico que lo había recetado se decide suspender el topiramato.
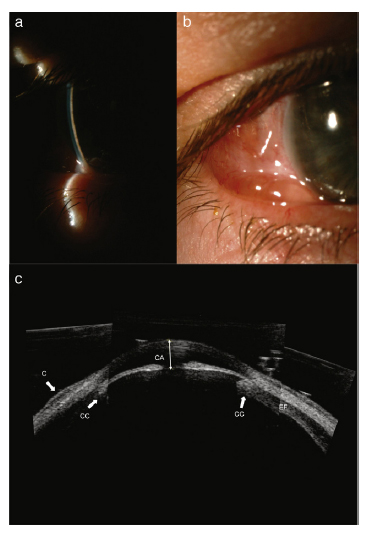
Fig. 1. a y b) fotografías del ojo derecho. Se observa una cámara anterior (CA) estrecha y quemosis conjuntival (C).
c) Biomicroscopía ultrasónica del ojo derecho. Es una composición de tres imágenes en las que se observa un
estrechamiento de la CA, una efusión coroidea (EF), la rotación anterior del cuerpo ciliar (CC), un cierre angular y quemosis.
Cinco días después de la retirada del topiramato la paciente presenta una AV de 20/40 en AO que mejora a 20/20 con una graduación de -2 esférico en AO. La PIO es de 10 y 12mmHg respectivamente. Biomicroscópicamente la amplitud de la cámara anterior se normaliza (fig.2a). Se realiza de nuevo una BMU (Fig. 2b) donde se evidencia una desaparición total de la efusión uveal y de la quemosis conjuntival, la amplitud de la cámara anterior se normaliza (3,54mm) así como también la apertura del ángulo. Las papilas de AO son normales. A los tres meses del inicio del cuadro la paciente continúa estable.
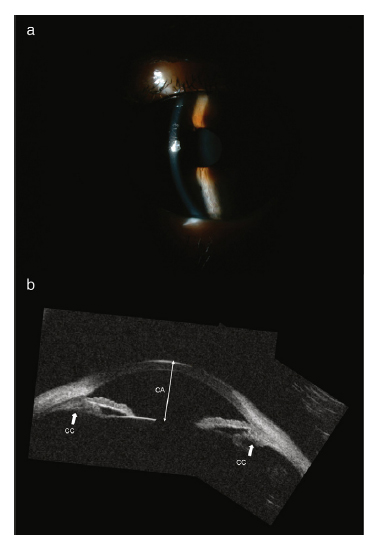
Fig. 2. a) fotografía del ojo derecho, que evidencia el aumento de la amplitud de la cámara anterior (CA).
b) Biomicroscopía ultrasónica del ojo derecho. Es una composición de tres imágenes en la que se
evidencia una profundidad normal de CA, apertura angular con reabsorción del líquido supraciliocoroideo,
reposicionamiento del cuerpo ciliar (CC) y plano cristaliniano. También han desaparecido las bolsas subconjuntivales.
Discusión
El GCA bilateral y los cambios miópicos han sido descritos en la literatura como efectos secundarios del topiramato. El empleo de la BMU ha permitido conocer la etiopatogenia de ambos procesos1,3,5, recientemente también se han empleado las imágenes Scheimpflug para obtener documentación gráfica de dicho fenómeno2. Se sabe que el síndrome de efusión uveal, así como el edema de cuerpo ciliar, provocan un desplazamiento anterior del diafragma iridocristaliniano lo que lleva a la miopización. Como consecuencia de dicho desplazamiento, se produce un estrechamiento de la cámara anterior y una crisis de glaucoma agudo. En nuestro caso podemos confirmar, gracias a la BMU, que la causa de ambos procesos se debe a un síndrome de efusión uveal que se resolvió después de cinco días de la suspensión del topiramato.
Debido a que no existe un bloqueo pupilar, la iridectomía periférica o el tratamiento con pilocarpina no son útiles, incluso se desaconsejan los colirios mióticos ya que estos podrían desencadenar un bloqueo pupilar relativo mediante el desplazamiento del diafragma iridocristaliniano más anteriormente. El tratamiento recomendado es fundamentalmente la retirada del topiramato. Nosotros comenzamos el tratamiento con pilocarpina en el momento inicial ante la duda de la existencia de un bloqueo pupilar, con la realización de la BMU se descarta esa posibilidad y se evidencia un cuadro de efusión uveal, por lo que se retira el tratamiento con mióticos. No está claro si el cuadro de GAC se produjo como consecuencia del inicio del tratamiento con topiramato solo o si la venlafaxina contribuyó en el mecanismo de producción o agravamiento del proceso1.
Como conclusión podemos decir que es necesario el conocimiento de la relación existente entre GAC bilateral y el inicio de medicación reciente con topiramato. El estudio mediante BMU nos ayudará a confirmar el diagnóstico y a seguir la evolución del cuadro.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Sankar PS, Pasquale LR, Grosskreutz CL. Uveal effusion and secondary angle-closure glaucoma associated with topiramate use. Arch Ophthalmol. 2001; 119:1210-1. [ Links ]
2. Kerimoglu H, Tokgoz M, Ozturk B, Gonul S, Pekel H. Topiramate-induced acute-onset myopia and central corneal thickening: Pentacam Scheimpflug imaging findings. Can J Ophthalmol. 2009; 44:222-3. [ Links ]
3. Asensio-Sánchez VM, Torreblanca-Agüera B, Martínez-Calvo S, Calvo MJ, Rodríguez R. Severe ocular side effects with Topamax. Arch Soc Esp Oftalmol. 2006; 81:345-8. [ Links ]
4. Medeiros FA, Zhang XY, Bernd AS, Weinreb RN. Angle-closure glaucoma associated with ciliary body detachment in patients using topiramate. Arch Ophthalmol. 2003; 121:282-5. [ Links ]
5. Guier CP. Elevated intraocular pressure and myopic shift linked to topiramate use. Optom Vis Sci. 2007; 84:1070-3. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
meyerblanco@yahoo.es
(M. Rodríguez-Blanco).
Recibido 28 Febrero 2011
Aceptado 7 Julio 2011














