Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Cirugía Plástica Ibero-Latinoamericana
versión On-line ISSN 1989-2055versión impresa ISSN 0376-7892
Cir. plást. iberolatinoam. vol.37 supl.1 Madrid dic. 2011
https://dx.doi.org/10.4321/S0376-78922011000500003
Aplicación de terapia de vacío en el tratamiento de nevus pigmentario gigante en la infancia
Negative pressure therapy in the treatment of a giant melanocytic nevus in chilhood
Fregenal, J.*, León Llerena, C.**, Revuelta Gómez, M.**
* Jefe de Sección
** Facultativo Especialista de Área
Unidad de Cirugía Plástica, Hospital Universitario Puerta del Mar. Cádiz. España
Dirección para correspondencia
RESUMEN
Los nevus melanocíticos gigantes congénitos son muy infrecuentes. Su incidencia de malignización varía según las series clínicas entre el 2 y el 45%. Este riesgo de malignización y los problemas de adaptación psicosocial que suelen acarrear hacen recomendable el inicio del tratamiento quirúrgico de este tipo de lesiones antes de la edad escolar.
Presentamos el caso de un niño de 7 años de edad con nevus melanocítico congénito gigante que afectaba a la espalda y al flanco derecho, de 30 x 19 cm de diámetro. Desarrollamos un protocolo terapéutico mediante programación de intervenciones quirúrgicas seriadas de mínima morbilidad, con postoperatorio simple y poco doloroso. En un primer tiempo realizamos extirpación de la lesión con bisturí ultrasónico y cobertura temporal del defecto creado con dermis artificial. En un segundo tiempo intentamos cobertura definitiva con piel cultivada autóloga, siendo necesario un tercer tiempo de cobertura con autoinjerto de espesor ultrafino.
En este caso, el sistema de terapia de presión negativa VAC® mostró su eficacia para inmovilizar los apósitos de forma segura, indolora y en régimen ambulatorio.
Palabras clave: Nevus melanocítico congénito gigante, Heridas, Terapia de presión negativa, Terapia asistida por vacío.
Código numérico: 172, 15117, 1526.
ABSTRACT
Giant congenital melanocytic nevi are very uncommon. Malignization incidence varies according to clinical series between 2 and 45%. This risk of malignization and psychosocial adaptation problems make necessary to begin the surgical treatment before school age. We present a 7-year-old child with a giant melanocytic nevus in the back and right flank, 30 x 19 cm in size. A therapeutic protocol using serial surgical interventions with minimal morbidity and an easy and painless postoperative care were developed. In the first surgery we removed the nevus with ultrasonic scalpel and used artificial dermis as a temporary coverage. In the second time we tried to complete the definitive coverage with autologous cultured skin, but we needed a third time to apply definitive ultrathin skin autograft.
In this clinical case, VAC® Therapy System has shown its effectiveness to fix dressings, painless safely and as an outpatient.
Key words: Giant congenital melanocytic nevi, Wounds, Negative pressure therapy, Vacuum assisted therapy.
Numeral Code: 172, 15117, 1526.
Introducción
Los nevus pigmentarios congénitos gigantes son infrecuentes. Su incidencia se ha calculado en 1:20.000 nacidos vivos. Se definen como gigantes aquellos nevus que sobrepasan los 20 cm de diámetro mayor, tanto en el momento de la medición como en su previsión de crecimiento: los nevus crecen proporcionalmente al resto del cuerpo, por lo que en niños se puede predecir que nevus de 9 cm de diámetro mayor en la cabeza y de 6 en el cuerpo, alcanzarán la definición de gigantes en la edad adulta.
Asientan frecuentemente en el tronco, seguido de las extremidades, cabeza y cuello. En principio son manchas más pálidas, planas y glabras que en el transcurso de meses o años aumentan su pigmentación, aunque de forma irregular; además puede aparecer en ellos hipertricosis, erosiones, ulceraciones o volverse hiperqueratósicos y verrucosos. Son frecuentes los nevus satélites solitarios o múltiples asociados, que será necesario mantener bajo vigilancia.
La malignización se manifiesta por crecimiento focal, ulceración, oscurecimiento, prurito, dolor o sangrado. También puede ocurrir depósito de melanocitos extracutáneos, que puede ser sintomático si afecta a las leptomeninges y se denomina melanosis neurocutánea. La incidencia de malignización es muy variada en los estudios publicados al respecto (1, 2), alcanzando en algunos hasta el 45 %, si bien pueden ser más reales las tasas del 2 al 3 % publicadas en estudios prospectivos. Un estudio reciente (3) encuentra un riesgo 51,6 veces superior de malignización en pacientes con nevus gigantes en relación al resto de la población. La malignización suele ocurrir antes de los 13 años de edad y se reconoce como factor de riesgo el diámetro mayor de 20 cm.
El tratamiento quirúrgico suele indicarse antes de la edad escolar, para evitar el riesgo de malignización y por motivos de adaptación psicosocial. En cambio algunos autores creen que el riesgo de una hipotética malignización no compensa la necesidad de múltiples intervenciones quirúrgicas, complejas y a veces mal toleradas por los pacientes, especialmente si se utilizan expansores tisulares.
En este estudio desarrollamos un protocolo quirúrgico adaptado a estos pacientes que simplifica su manejo con cirugías poco agresivas, que minimizan las molestias y el dolor y que por tanto, son fácilmente toleradas, no requieren largas hospitalizaciones y aportan un resultado final muy satisfactorio.
Caso clínico
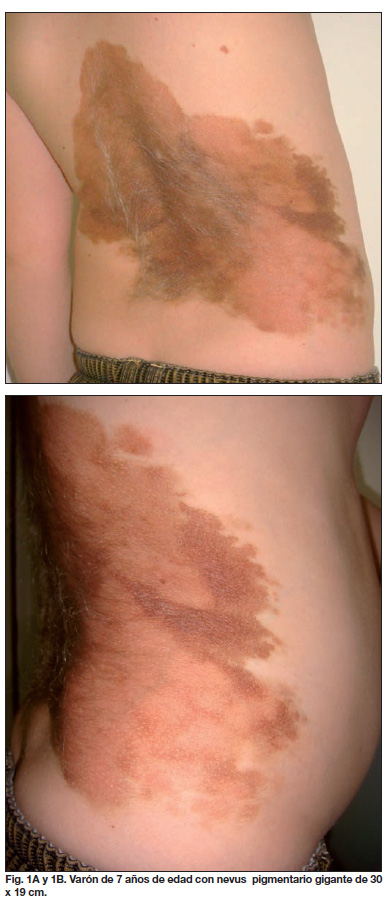
Varón de 7 años de edad, remitido a nuestra consulta por presentar nevus melanocítico congénito gigante en espalda y flanco derecho, con diámetro máximo de 30 x 19 cm, bordes irregulares, zonas de mayor pigmentación y grosor, especialmente en el flanco derecho y recubierto por vello áspero y amelanótico (Fig. 1).
Ante la eventualidad de una posible malignización, decidimos junto con la familia realizar sin demora tratamiento quirúrgico, para lo que obtuvimos los correspondientes consentimientos informados de la familia y la autorización del comité de trasplantes de nuestro hospital. En la primera intervención quirúrgica procedimos a la extirpación completa del nevus mediante bisturí ultrasónico (Harmonic®), lo que permitió la extirpación uniforme en el plano inferior al plexo vascular subdérmico, manteniendo un lecho absolutamente viable (Fig. 2). El defecto resultante se cubrió con Integra® y para asegurar su inmovilidad, utilizamos un sistema de terapia de presión negativa VAC.® (Vacuum Assisted Closure KCl Clinic Spain S.L.) de forma continua, a la presión más baja disponible: -50 mm de Hg (Fig. 3). En la misma intervención se realizó una biopsia de piel sana de uno de los márgenes, que se envió según protocolo al Centro Comunitario de Sangre y Tejidos (CCST) del Principado de Asturias (Oviedo, Asturias, España), para crear una piel artificial mediante cultivo autólogo de queratinocitos y fibroblastos sobre plasma humano (4, 5). El cuidado postoperatorio consistió en curas semanales bajo sedación y el mantenimiento de un sistema VAC® portátil, lo que permitió un alta hospitalaria precoz del paciente (Fig. 3C). La Anatomía Patológica confirmó que se trataba de un nevus melanocítico predominantemente intradérmico, con focos compuestos y junturales (nevus melanocítico congénito gigante), no apreciándose en los cortes estudiados afectación de los bordes laterales ni profundos.
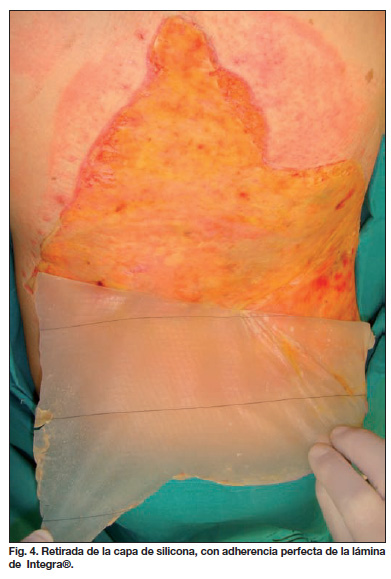
A las 3 semanas, realizamos el segundo tiempo quirúrgico programado para la retirada de la lámina de silicona del Integra® observando un prendimiento casi completo (Fig. 4). Ese mismo día, coordinamos la llegada de las láminas de piel cultivada procedentes del CCST, que se nos remitieron pegadas mediante puntos de histoacryl a un soporte sólido (6), enrolladas sobre sí mismas y envasadas individualmente (Fig. 5A). Cubrimos el defecto completamente con la piel cultivada, inmovilizándola con su propio soporte mediante grapas (Fig. 5B). A su vez, inmovilizamos todo de nuevo con el sistema VAC® , -50mmHg de presión en modo continuo, siguiendo la misma pauta de curas ambulatorias. La piel cultivada prendió en principio en un 90%, proporcionando lo que parecía un epitelio estable y con tendencia a confluir en las zonas cruentas (Fig. 6). Dos semanas después de la primera siembra, cubrimos las zonas cruentas remanentes con una nueva remesa de piel cultivada y con el mismo sistema de fijación. En el postoperatorio inmediato de esta segunda siembra, en la primera cura efectuada a los 4 días, observamos abundante supuración en la herida y en las grapas de fijación, aunque los cultivos sucesivos practicados fueron negativos. A partir de la primera semana, la colaboración del paciente y de la familia nos permitió suspender la terapia de vacío e instaurar de forma ambulatoria curas tópicas oclusivas con gasa vaselinada y compresas impregnadas en cremas antisépticas, sujetas con malla elástica, lo que nos facilitaba el seguimiento y observación frecuentes de la zona. Aproximadamente al mes y medio tuvimos que descartar definitivamente la supervivencia de los cultivos de piel (Fig. 7), por lo que fue necesario realizar cobertura definitiva mediante autoinjertos de espesor ultrafino, sin mallar, tomados con dermatomo eléctrico del muslo derecho. Esta vez la cobertura fue completa, mostrando al año de postoperatorio una cicatriz de calidad y elasticidad excelente y un buen resultado estético, sin evidencia de persistencia de la lesión ni de recidivas (Fig. 8).
Discusión
Los nevus congénitos pigmentarios gigantes son infrecuentes, por lo que la mayor parte de los cirujanos tienen poca experiencia en su tratamiento. Pocos autores publican grandes series (7). Su incidencia de malignización es muy variable según distintos trabajos y oscila entre el 2 y el 45%. Es difícil realizar estudios prospectivos que analicen la tasa de malignización real, porque más de la mitad de los pacientes con nevus gigantes deciden la corrección quirúrgica por motivos de seguridad o simplemente estéticos, aunque probablemente las cifras más aproximadas de riesgo de malignización a lo largo de la vida oscilan entre el 7 y el 9 %. Lo que sí parece demostrado es: 1o) El riesgo superior de estos pacientes en comparación con el resto de la población 2o) Que la mitad de los casos de malignización en nevus melanocíticos congénitos gigantes ocurren durante los 3 primeros años de vida y el 70 % en los primeros 13 años. 3o) El pronóstico de los melanomas que asientan sobre nevus gigantes en la infancia es extremadamente malo, con una alta tasa de mortalidad (8). Todos estos datos hacen recomendable que el tratamiento se inicie en cuanto el paciente pueda tolerarlo, si es posible, antes de los 3 años de edad (1, 2). Pero también hay que señalar que persisten algunas controversias al respecto porque no se ha demostrado que un tratamiento quirúrgico agresivo disminuya el riesgo de malignización local en el lecho del nevus y sobre todo a distancia (9, 10). En nuestro caso, el riesgo de malignización era conocido por la familia y fue el motivo fundamental de consulta, por lo que se decidió realizar un tratamiento quirúrgico inmediato.
Están descritos múltiples tratamientos para el nevus congénito gigante. Se tiende a descartar los métodos no escisionales que no permiten el diagnóstico histológico y dificultan el posterior seguimiento. También se ha asociado la exposición de los melanocitos a la energía laser in vitro con un mayor riesgo de malignización (1).
Cuando se opta por la extirpación quirúrgica, parece existir consenso en que la cobertura mediante expansión de la piel adyacente proporciona los mejores resultados estéticos y funcionales, siempre que sea posible su uso, que se realice a edad temprana y que no se presenten complicaciones. La desventaja de este método radica en la necesidad de realizar procedimientos seriados de expansión en intervalos de 3 a 6 meses, que dificultan progresivamente los resultados y que pueden facilitar la aparición de complicaciones. Esta tasa de complicaciones puede alcanzar el 20% en procedimientos únicos, es mayor en la extremidad inferior, en niños menores de 12 años y cuando se requieren múltiples tiempos de expansión. Si aparecen complicaciones como hematoma, infección, extrusión del expansor, rotura del mismo o isquemia cutánea, pueden hacer fracasar el procedimiento. En niños mayores o en adultos la piel es menos elástica y la expansión se tolera peor, especialmente si se requieren procedimientos seriados (7). Además, cada proceso de expansión precisa tiempo y cuidados complicados, es molesto para el paciente y puede ser doloroso, crea una deformidad estética llamativa que en pacientes de poca edad suele ser mal tolerada y hace necesario contar con la participación de familias muy colaboradoras. En nuestro caso, el paciente acudió a consulta con 7 años de edad y parecía mal candidato a colaborar en procedimientos complejos, molestos o dolorosos, por lo que descartamos el uso de expansores tisulares.
Otros métodos quirúrgicos empleados para este fin han sido las escisiones seriadas, no aplicables en nuestro caso, y el uso de injertos cutáneos de espesor parcial o de espesor completo previa expansión. Bauer (7) sugiere que los resultados obtenidos con injertos de espesor parcial, especialmente si están mallados, hacen preferible dejar el nevus sin tratar. Este autor sólo considera aceptable el resultado si se utilizan grandes segmentos de injertos de espesor parcial sin mallar.
Los sustitutos de piel evitan la morbilidad de las zonas donantes, se pueden utilizar de forma ilimitada y acortan los tiempos quirúrgicos, pero proporcionan una cobertura frágil, menos resistente a la infección y con mayor coste económico. Se asume que el resultado estético final con los sustitutos de piel es inferior al que se consigue con los expansores, aunque esto es difícil de valorar porque existen pocos trabajos con buena iconografía (11). Los trabajos publicados suelen presentar fotos escasas y de mala calidad; además, son confusos en cuanto a la técnica usada (12), por lo que pueden hacer pensar que el resultado es peor incluso de lo que se describe. Tal vez esta sospecha es una de las causas por la que estos métodos, que se llevan utilizando desde hace décadas en experimentación, no han alcanzado un uso clínico habitual, excepto en el tratamiento de quemados críticos.
Existen diversos sustitutos comercializados de los que Integra® es el que más frecuentemente se ha utilizado. Su uso requiere que, al cabo de 3 ó 4 semanas, se complete la cobertura con injertos cutáneos de espesor parcial finos, lo que añade al procedimiento y resultado la morbilidad de las zonas donantes. Otra alternativa son los cultivos autólogos de queratinocitos y fibroblastos en diferentes matrices que intentan reconstruir la piel del paciente. Han demostrado su utilidad para cubrir áreas extensas (13, 14), aunque el resultado estético puede ser poco satisfactorio (15). En España disponemos de una piel desarrollada a partir de plasma humano coagulado en el que se siembran fibroblastos y queratinocitos autólogos tomados de una biopsia de piel del paciente (4). Con estos antecedentes, en nuestro caso, tomamos varias decisiones con el fin de intentar mejorar el resultado estético final:
1o) Extirpación conservadora mediante bisturí ultrasónico (Harmonic®) para crear un lecho uniforme, que se mantuviera a plano con el resto de la piel y con vitalidad y hemostasia perfectas. Las células névicas pueden alcanzar en profundidad el tejido subcutáneo e incluso infiltrar el músculo, el hueso o el cartílago. El margen profundo puede contener células névicas en el 23% de las muestras y el 7% de los pacientes pueden desarrollar recurrencias de pigmentación visibles en las áreas operadas (15). Pero no creemos que el tratamiento de las lesiones benignas requiera una extirpación agresiva hasta fascia muscular. El bisturí ultrasónico nos ha permitido mantener un plano uniforme, inferior al plexo vascular subdérmico y nos ha aportado márgenes suficientes en el estudio anatomopatológico de la pieza de resección.
2o) Reconstrucción de una capa dérmica mediante el uso de Integra® para corregir el desnivel del defecto y aportar resistencia y elasticidad a la cobertura cutánea, evitando la proliferación de tejido de granulación. También nos permitió tiempo suficiente para comprobar en la biopsia que la resección había sido adecuada.
3o) Cobertura con piel cultivada autóloga para evitar la morbilidad de las zonas donantes. La piel sintética autóloga suele cultivarse antes de la intervención y se emplea luego directamente sobre el lecho de extirpación, sola o combinada con injertos mallados (5). A veces, en pacientes quemados, se ha utilizado sobre la dermis de los homoinjertos utilizados como cobertura temporal mientras se obtenían los cultivos. Pensamos que el uso intermedio de Integra® crea una base dérmica que facilita la toma de la piel cultivada y que produce unos resultados estéticos y funcionales superiores al aumentar el grosor y la estabilidad de la piel resultante. En nuestro caso, los cultivos de piel dieron en principio un resultado excelente en el 90% de la superficie tratada, por lo que intentamos completar la cobertura con una nueva remesa de los cultivos disponibles en el CCST del Principado de Asturias. En el postoperatorio inmediato observamos una posible infección local, a pesar de que los cultivos fueron negativos, que respondió favorablemente al tratamiento tópico. Durante algunas semanas la herida, aunque bastante exudativa, mostraba una superficie mate y nacarada, no dolorosa, sin evidencia de tejido de granulación, que presumía la persistencia de epitelio o al menos de la dermis cultivada. Esto demoró bastante la decisión de cobertura definitiva. Incluso nos planteamos la necesidad de tomar alguna biopsia local para confirmar la persistencia de los cultivos, lo que se descartó por la extrema intolerancia al dolor del paciente. La decisión de realizar autoinjertos se tomó 1 mes y medio después de la segunda siembra, cuando por fin apareció un buen tejido de granulación en la herida.
A pesar del fracaso de la piel cultivada, el tratamiento realizado permitió disponer de un lecho uniforme y estable que facilitó después el uso de autoinjertos ultrafinos, con excelente resultado funcional y estético, ausencia de recidivas y mínimas secuelas en la zona donante.
4o) La cobertura de la zona durante todo el proceso con un sistema VAC® aplicado con la mínima presión continua disponible de -50 mmHg que garantiza la inmovilización perfecta, evita por completo el dolor y las molestias y fue perfectamente tolerado por el paciente, lo que permitió su alta hospitalaria precoz.
El sistema VAC® es un método de cierre de heridas que usa la baja presión para favorecer el crecimiento del tejido de granulación. También se ha usado para acelerar la revascularización de la neodermis y acortar el plazo para injertar sobre el Integra® (16, 17). Su uso para asegurar apósitos sobre lechos difíciles se ha publicado esporádicamente y en series cortas, aunque a presiones de -125 mmHg (18, 19). La tolerancia y adhesividad logradas a -50 mmHg hace que no encontremos justificado ni necesario el usar presiones más intensas.
Conclusiones
Pensamos que este protocolo podría convertirse en una alternativa válida al uso de expansores en el tratamiento quirúrgico de los pacientes con nevus pigmentario gigante en la infancia, ya que permite un manejo adecuado mediante intervenciones quirúrgicas poco agresivas y de corta duración, con postoperatorios simples, bien tolerados y no dolorosos y que gracias al uso del sistema VAC® pueden controlarse en régimen ambulatorio.
El resultado obtenido en nuestro caso fue muy satisfactorio, tanto para el paciente y su familia como para nosotros. Al tratarse de un procedimiento secuencial, el método que proponemos es flexible y permite cambiar en cualquier momento a otros planteamientos; por ejemplo, hubiera sido fácil en caso de márgenes afectos durante la resección, ampliar la extirpación en la segunda intervención quirúrgica. En nuestro caso la pérdida de los sustitutos de piel fue suplida con injertos cutáneos de espesor parcial ultrafinos y, en caso de un resultado final insatisfactorio, se podría haber recurridor posteriormente al uso de expansores.
Bibliografía
1. Arneja JS, Gosain AK.: Giant congenital melanocytic nevi. Plast Reconst Surg. 2007; 120(2):26e. [ Links ]
2. Arneja JS, Gosain AK.: Giant congenital melanocytic nevi. Plast Reconst Surg 2009; 124(Suppl.):1e. [ Links ]
3. Zaal LH, Mooi WJ, Klip H, van der Horst CM.: Risk of malignant transformation of congenital melanocytic nevi: A retrospective nationwide study from the Netherlands. Plast Reconst Surg 2005; 116:1902. [ Links ]
4. Llames SG, Del Río M, Larcher, et al: Human plasma as a dermal scaffold for the generation of a completely autologous bioengineered skin. Transplantation 2004; 77: 350. [ Links ]
5. Llames S, García E, García V, et al: Clinical results of an autologous engineered skin. Cell Tissue Bank 2006; 7: 47. [ Links ]
6. Meana A, Iglesias J, Madrigal B, Sánchez J.: Use of cyanoacrylate glue to prepare cultured keratinocyte sheets for grafting. Burns 1997; 23(7/8): 645. [ Links ]
7. Bauer BS, Corcoran J.: Treatment of large and giant nevus. Clin Plastic Surg 2005; 32: 11. [ Links ]
8. Thomas WO, Rayburn S, Le Blanc RT, et al: Artificial skin in the treatment of a large congenital nevus. South Med J 2001; 94(3):325. [ Links ]
9. Watt AJ, Kotsis SV, Chung KC.: Risk of melanoma arising in large congenital melanocytic nevi: A systematic review. Plast Reconstr Surg 2004; 113 (7): 1968. [ Links ]
10. Bett BJ.: Large or multiple congenital melanocytic nevi: Occurrence of cutaneous melanoma in 1008 persons. J Am Acad Dermatol 2005; 52: 793. [ Links ]
11. Abai B, Thayer D, Glat PM.: The use of a dermal regeneration template (Integra) for acute resurfacing and reconstruction of defects created by excision of giant hairy nevi. Plast Reconst Surg 2004; 114(1): 162. [ Links ]
12. Earle SA, Marshall DM.: Management of giant congenital nevi with artificial skin substitutes in children. J Craneofac Surg 2005; 16(5): 904. [ Links ]
13. Pearson GD, Goodman M, Sadove AM.: Congenital nevus: The Indiana University's approach to treatment. J Craneofac Surg 2005; 16(5): 915. [ Links ]
14. Warner PM, Yakuboff KP, Kagan RJ, et al: An 18-year experience in the management of congenital nevomelanocytic nevi. Ann Plast Surg 2008; 60(3): 283. [ Links ]
15. Gosain AK, Santoro TD, Larson DL, Gingrass RP.: Giant congenital nevi: Experience and an algorithm for their management. Plast Reconstr Surg 2001; 108 (3): 622. [ Links ]
16. Molnar JA, DeFranzo AJ, Hadaegh A, et al: Acceleration of Integra incorporation in complex tissue defects with subatmospheric pressure. Plast Reconstr Surg 2004; 113 (5): 1339. [ Links ]
17. Park CA, Defranzo AJ, Marks MW, Molnar JA.: Outpatient reconstruction using Integra and subatmospheric pressure. Ann Plast Surg 2009; 62(2): 164. [ Links ]
18. McEwan W, Brown TH, Mills SM, Muller MJ.: Suction dressings to secure a dermal substitute. Burns 2004; 30: 259. [ Links ]
19. Schneider A, Morykwas M, Argenta L.: A new and reliable method of securing skin grafts to the difficult recipient bed. Plast Reconstr Surg 1998; 102(4): 1195. [ Links ]
 Dirección para correspondencia:
Dirección para correspondencia:
Dr. Javier Fregenal
Unidad de Cirugía Plástica
Hospital Universitario Puerta del Mar.
Av. Ana de Viya no 21.
11009, Cádiz. España
e-mail: correo@javierfregenal.com