Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Cirugía Plástica Ibero-Latinoamericana
versión On-line ISSN 1989-2055versión impresa ISSN 0376-7892
Cir. plást. iberolatinoam. vol.38 no.3 Madrid jul./sep. 2012
https://dx.doi.org/10.4321/S0376-78922012000300012
Terapia fotodinámica (PDT) en piel y estética: procedimiento, materiales y método en base a nuestra experiencia
Photodinamic therapy in skin and aesthetics: procedure, matherials and method based on our experience
Mordon, S.*, Martínez-Carpio, P.A.**, Vélez, M.***, Alves, R.****, Trelles, M.A.*****
* Profesor de Biofísica Médica, Doctor Ciencias Físicas. Universidad de Lille Nord de France, Lille University Hospital, Lille, Francia.
** Especialista en Bioquímica Clínica y Patología Molecular, Experto en Oftalmología Experimental y Clínca. IMC Investiláser. Sabadell, Barcelona, España.
*** Dermatólogo, Servicio de Dermatología Hospital Universitario del Mar, Barcelona. España. Dermatólogo Instituto Médico Vilafortuny, Cambrils, Tarragona, España.
**** Dermatóloga, Servicio de Dermatología. Hospital Central Funchal, Funchal, Portugal.
***** Cirujano Plástico, Instituto Médico Vilafortuny, Cambrils, Tarragona. España.
Dirección para correspondencia
RESUMEN
La terapia fotodinámica (PTD) es un procedimiento cada vez más utilizado para tratar diversas afecciones dermatológicas y dermatoestéticas. Su aplicación obtiene buenos resultados en casos de carcinoma basocelular, enfermedad de Bowen, queratosis actínica, acné, rosácea y fotoenvejecimiento cutáneo. Los fotosensibilizantes y las fuentes de luz que se pueden utilizar son cada vez más variados, pero aún existe poco consenso en su metodología de aplicación, sistemas de irradiación y dosificaciones.
En este artículo describimos los materiales y métodos disponibles en la actualidad y discutimos algunos detalles que, en base a nuestra experiencia, permiten mejorar los resultados. Presentamos también 5 casos clínicos ilustrativos de diferentes patologías.
Palabras clave: Terapia fotodinámica, Fotosensibilizantes, Fuentes de luz, Queratosis actínica, Carcinoma basocelular, Enfermedad de Bowen, Acné, Rosácea, Envejecimiento cutáneo.
Código numérico: 14-17-26.
ABSTRACT
Photo Dynamic Therapy (PTD) is an increasingly used technique in Dermatology and Dermocosmetics. PDT has a wide range of medical applications for the treatment of extended cutaneous cancer, offering also very good results in the treatment of basal cell carcinoma, Bowen's disease, actinic keratosis, acne, rosacea and in cutaneous rejuvenation.
The sensitizers and light sources used for photoactivation are also more and more varied but there is still no consensus regarding methods and energy dosage.
This study describes material and methods which are currently available and discusses a few details, that based on our own experience, can improve results. Five illustrative cases of different conditions are presented.
Key words: Photodynamic therapy, Photosensitizers, Light sources, Actinic keratosis, Basal cell carcinoma, Bowen's disease, Acne, Rosacea, Cutaneous aging.
Numeral Code: 14-17-26.
Introducción
La terapia fotodinámica (PTD), dentro de sus varias aplicaciones en las especialidades médicas, también se utiliza para tratar diversas afecciones dermatoestéticas. La técnica consiste en administrar un compuesto fotosensible que se acumula en las células diana a tratar, y transcurrido un tiempo denominado periodo de incubación, iluminar con una luz de longitud de onda dentro del espectro de absorción del fotosensibilizante. El efecto terapéutico se obtiene con la fotoactivación del producto sensibilizante en el tejido patológico, lo que conduce al daño oxidativo en una amplia variedad de dianas celulares. El resultado final es la destrucción del tejido canceroso o anómalo gracias a la síntesis de oxígeno reactivo monoatómico (singlet) y al daño oxidativo que originan los radicales libres en las células alteradas y en las células endoteliales de los neovasos anómalos (1-4).
La PDT está considerada como un tratamiento no invasivo y selectivo por la mayor capacidad que tienen las células tumorales o alteradas para captar y concentrar el agente fotosensibilizante, con menor velocidad de eliminación.
En la piel se utiliza con éxito en el tratamiento de queratosis actínicas (KA), carcinoma basocelular (BCC), enfermedad de Bowen, acné, rosácea y también para corregir el fotoenvejecimiento cutáneo (2-4). Cada vez existe mayor documentación científica sobre la eficacia y seguridad del procedimiento, así como un mayor conocimiento de los mecanismos bioquímicos y celulares implicados en el mismo (2,3). Posiblemente, la indicación de la PDT en el tratamiento del fotoenvejecimiento cutáneo sea la que más auge ha adquirido en los últimos años; algunos autores apuntan que, bajo protocolos optimizados, los resultados en este campo podrían ser superiores a los que se obtienen con la terapia de luz intensa pulsada (IPL) (2-7). También se ha comprobado que la combinación de PDT e IPL mejora los resultados que logran obtener ambas terapias por separado (8,9).
El objetivo de este trabajo es dar a conocer las características de los fotosensibilizantes y de las fuentes de luz disponibles en el mercado y comercializadas para la PDT cutánea siguiendo las condiciones de uso propuestas por los fabricantes y nuestra experiencia personal sobre los resultados obtenidos.
Fotosensibilizantes
Las características y particularidades de los fotosensibilizantes en PDT son importantes para el resultado del tratamiento. Según Stapleton y Rodes (10) las características que deben reunir los fotosensibilizantes son:
1. Capacidad para localizarse específicamente en el tejido o células a tratar.
2. Distribución homogénea en la diana.
3. Alta lipofilia a fin de que penetren las barreras biológicas.
4. Vida media corta y rápida eliminación en los tejidos no enfermos.
5. Espacio de tiempo lo más breve posible entre la administración y la acumulación máxima en la diana a tratar.
6. Activación frente a longitudes de onda determinadas y penetración óptima en el tejido.
7. Alto rendimiento en la producción de oxigeno reactivo monoatómico (singlet) o, en general, de especies reactivas de oxígeno.
8. Ausencia de toxicidad en un ambiente oscuro.
Los fotosensibilizantes que han demostrado eficacia en PDT cutánea incluyen el ácido 5-aminolevulínico (5-ALA), el metil éster de ácido levulínico (MAL), los derivados de la hematoporfirina, los derivados de la benzoporfirina, y la meta-tetradidroxifenilclorina (4). Entre los que se encuentran comercializados destacan el 5-ALA (Levulan® KerasticTM DUSA Pharmaceuticals, Wilmington, MA, EE.UU.) y el MAL (Metvix® PhotoCure SAS, Oslo, Noruega), con la ventaja, este último, de que es más liposoluble (Tabla I). La mayor liposolubilidad permite una mejor penetración en el tejido empleando dosis menores. Ambos compuestos se consideran óptimos para su aplicación clínica aunque también se dispone de otras moléculas fotosensibilizantes, algunas en fase de investigación, que reaccionan de forma notoria frente a diferentes longitudes de onda (Tabla II). Destaca entre ellas el hexilester 5-aminolevulinato (HAL), utilizado en Urología y que según se ha observado, ofrece ventajas para tratar algunos cánceres cutáneos mediante PDT.
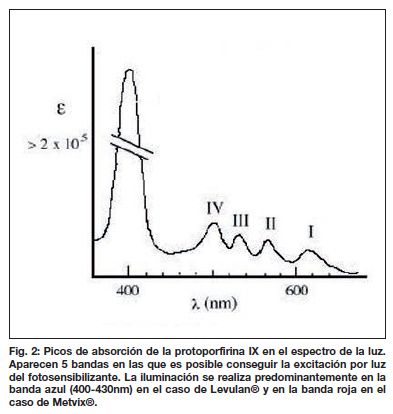
El 5-ALA, MAL y HAL no son fotosensibilizantes efectivos por sí mismos, sino que después de su administración, se transforman en protoporfirina IX (pPIX); es decir, el agente sensibilizante principal sobre el que se actúa durante el tratamiento (Fig. 1). Aunque se conocen las particularidades de reacción y absorción de las porfirinas frente al extenso espectro de longitudes de onda (Fig. 2), no existen suficientes estudios que analicen la farmacocinética de estos tres compuestos a nivel de la producción del pPIX fluorescente que generan, por lo que aún no hay un consenso pleno sobre qué concentraciones y en qué condiciones deben aplicarse. Los laboratorios fabricantes se limitan a dar unas recomendaciones generales de uso, que son las siguientes:
1) Levulan® Kerastic: contiene en cada aplicador de 1.5ml, 354mg de clorhidrato de 5-ALA. Se indica formalmente para el tratamiento de KA de grosor mínimo a moderado, aunque puede emplearse también para otras lesiones cutáneas. El producto sólo debe ser aplicado por un profesional cualificado, nunca por el paciente. La frecuencia de tratamiento recomendada es una aplicación y dosis de irradiación única. Cuando hace falta una segunda sesión se recomienda que transcurran al menos 2 semanas o más, pero en este punto también existen discrepancias. Dependiendo de la indicación se procederá a irradiar con luz azul o roja de 409 ó 635 nm. respectivamente, y como efectos colaterales es frecuente la aparición de prurito, sensación dolorosa, eritema y edema.
2) Metvix® crema: contiene 160mg/g de MAL. Se indica para el tratamiento de KA en cara y cuero cabelludo, en el BCC superficial y nodular y en la Enfermedad de Bowen. Antes de aplicar la crema, deben prepararse las lesiones retirando la descamación cutánea y las costras frotando la superficie donde se localizan. Tras aplicar la crema, se cubre la zona tratada con un vendaje durante aproximadamente unas 3 horas hasta el momento de aplicar la luz terapéutica de 409 a 635 nm. Generalmente se precisan una o dos sesiones de tratamiento. Los efectos adversos (muy frecuentes), son sensación de quemazón, aparición de costras y enrojecimiento de la piel.
Tanto en la aplicación de una sustancia como de otra, la sensación de dolor y el ardor suelen desaparecer hacia las 24 horas del tratamiento lumínico. La PDT está contraindicada en pacientes con fotosensibilidad cutánea, porfiria, alergia a las porfirinas y en pacientes con sensibilidad a cualquiera de los componentes de la formulación.
Levulan® en EE.UU y Metvix® en Europa, son los fotosensibilizantes más empleados y los que cuentan con mayor información y experiencia. Sin embargo, las indicaciones, condiciones de uso y las fuentes de luz aplicables quedan muy limitadas si se tiene en cuenta la aceptación oficial de la Food and Drug Administration (FDA) en EEUU. La mayoría de expertos coinciden en señalar que las indicaciones de los fotosensibilizantes en PDT son mucho más extensas que las que constan en los prospectos de Levulan® y Metvix® , y que los procedimientos y fuentes de luz apropiados pueden ser diferentes y obtener mejores resultados dependiendo de la naturaleza, extensión y profundidad de las lesiones. Lo propio ocurre con el sensibilizante HAL (Hexilester 5 aminolevulinico) que se activa con longitudes de onda de 409 a 635 nm.
Recientemente se han introducido en el mercado tres nuevos productos sensibilizantes que se comienzan a emplear con éxito: Allumera® , Ameluz® y Alacare® (Tabla I)
1) Allumera® (Photocure, Noruega) es una crema de aplicación tópica formulada con la intención de conseguir un mejor efecto en el aspecto de la piel tras el tratamiento. Su principio activo es el hexaminolevulinato.
2) Ameluz® (Biofrontera Bioscience, Alemania), contiene 78 mg de 5-ALA en forma de gel. El fabricante recomienda la iluminación con luz roja (630nm) a una dosis aproximada de 37J/cm2. También puede aplicarse en un espectro más amplio, entre los 570-670nm a dosis de entre 75-200J/cm2.
3) Alacare® (Photonamic, comercializado por Spirig Pharma, AG), se presenta en forma de parches de 5-ALA y se indica formalmente para el tratamiento de la KA empleando luz roja.
Material y método
Método resumido de Aplicación
Podemos analizar la distribución y definición objetiva de las lesiones a tratar mediante luz ultravioleta (UV) o luz de Wood, que permiten ver la fluorescencia que desprende el producto en su forma de porfirina y posibilita el seguimiento iconográfico.
Para sistematizar adecuadamente el tratamiento conviene ordenar los siguientes pasos:
• Limpieza del área a tratar (eliminar maquillajes, etc.). Se recomienda peeling de salicílico, microdermoabrasión, limpieza enérgica con gasa o emplear una cucharilla con maniobras suaves, particularmente en las KA muy elevadas.
• Aplicación del fotosensibilizante.
• Colocar un apósito oclusivo y mantener, dependiendo de la alteración cutánea, entre 30 minutos a 5 horas. En algunos casos, como en los tratamientos de estética cutánea, la oclusión puede sustituirse por aplicaciones del agente sensibilizante cada 10 minutos. Es importante añadir un protector opaco después de su aplicación para evitar que el producto reaccione con la luz ambiental.
• En el caso de emplear ALA, diluido entre el 1 al 20 % , se recomienda mantener tiempos de oclusión entre 30 minutos y 5 horas. Si se utiliza ALA en liposomas al 0,5 % , su aplicación debe ser de una hora con intervalos de 10 minutos, sin necesidad de ocluir el área de tratamiento.
• En el caso de emplear MAL (generalmente al 16 %), se mantiene la oclusión durante 3 horas. Este tiempo es más reducido en los tratamientos de estética cutánea.
• Transcurrido este tiempo, se retira el apósito y los residuos del producto lavando suavemente con agua y jabón no agresivo.
• Se procede al tratamiento con el sistema seleccionado de luz coherente (láser) o no coherente (LED, IPL, luz de banda estrecha, etc.), siguiendo las dosis indicadas para cada sistema y de acuerdo a la lesión a tratar.
Fuentes de luz
La fuente de luz ideal para PDT debe cumplir los siguientes requisitos:
• Ser bien absorbida por el fotosensibilizante.
• Tener capacidad de penetración en la piel para alcanzar las células diana.
• Estar preparada para emitir las dosis (fluencias) adecuadas para generar la reacción tóxica en la célula.
• Poder administrarse en un periodo breve de tiempo y ser capaz de conseguir la reacción terapéutica.
• Producir mínimos efectos secundarios, como poco dolor y eritema y evitar la formación de púrpura, ampollas, costras y discromías.
• Facilitar la recuperación rápida del área tisular lesionada por el tratamiento.
Se considera que la longitud de onda más efectiva para la PDT tras la aplicación de Levulan® o Metvix® corresponde a la luz de 635nm, pero las longitudes de onda y los sistemas de iluminación aplicables varían mucho en función de la patología y de la experiencia del facultativo. Entre las fuentes de luz más utilizadas se incluyen:
- Láser de colorante pulsado, de emisión entre 585 a 595nm.
- Luz azul intensa de 418 nm.
- Luz intensa pulsada (IPL).
- Diodos emisores de luz (LED) próximos a los 630 nm
- Láser de Argón, de emisión multilínea entre 488 a 514 nm.
- Láser de colorante pulsado de emisión en 575 a 595 nm.
- Láser de vapor de oro, de emisión en 628nm.
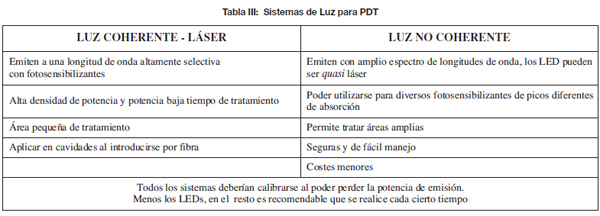
Existen equipos pensados especialmente para la PDT en piel, como el sistema PDT 1200L Waldman® (Herbert Waldmann GmbH & Co. KG Villingen-Schwenningen, Alemania) equipado con una lámpara halógena de 2100W que montando filtros apropiados permite aplicar luz en una banda entre 580 a 740nm, con irradiaciones entre 20 a 200 mW/cm2. También destaca el sistema Blu-U Blue Light® (DUSA Pharmaceuticals, Inc Wilmington, MA, EE.UU.), que emite luz azul de banda ancha a dosis de 10mW/cm2. Cabe tener en cuenta que las dosis bajas de luz producen un daño leve en el tejido y que se repara con facilidad, mientras que las dosis altas inducen hipoxia de la zona iluminada y conllevan riesgo de reducir la eficacia del tratamiento. Por lo tanto, reducir la intensidad o fraccionar la irradiación puede ayudar a obtener mejores resultados (Tabla III).
Indicaciones
En la actualidad, existe acuerdo sobre la eficacia de la PDT en determinadas afecciones dermatológicas y estéticas (Tabla IV); sin embargo, y en tanto que los sensibilizantes reaccionan a cualquier luz visible, queda aún la cuestión sobre las longitudes de onda y las fluencias más adecuadas para tratar cada tipo de afección. Cabe tener en cuenta que la luz visible, y por tanto la luz solar, emiten longitudes de onda capaces de excitar la PpIX que generan Levulan® y Metvix®.
No es el objetivo de este trabajo profundizar en los detalles de cada alteración cutánea susceptible de ser tratada con PDT; sólo pretendemos enumerar las más importantes y destacar algunos aspectos clínicos fundamentales. En nuestra experiencia, en cada una de las siguientes indicaciones existe suficiente respaldo bibliográfico para diseñar protocolos de trabajo que permitan un abordaje bien estructurado.
1) Carcinoma basocelular (BCC) superficial y nodular, carcinoma epidermoide y enfermedad de Bowen: tanto la PDT con 5-ALA como con MAL han demostrado ser eficaces. La luz roja entre 570 y 670nm con una fluencia de 75J/cm2, obtiene buenos resultados.
2) Queratosis Actínica (KA): La PDT con 5-ALA o MAL es claramente eficaz para el tratamiento de estas lesiones hipertróficas localizadas en la cara y en el cuero cabelludo. Se obtienen buenos resultados con una o dos sesiones de tratamiento, con tasas de curación aproximadas del 86 % , 24 % de recurrencias en el primer año y 9 % de transformación maligna. Estas cifras indican que es necesario realizar un seguimiento de la evolución de las lesiones después del tratamiento (2). En nuestra experiencia, se consiguen excelentes resultados con MAL al 16 % y luz roja LED (633nm) para una dosis total de 105J/cm2.
3) Acné y rosácea: el Propionibacterium acnes sintetiza porfirinas cuyo componente principal es la coproporfirina III. La síntesis de porfirinas aumenta cuando las bacterias se exponen a longitudes de onda alrededor de los 420nm (luz color violetaazul). La fotoactivación de las porfirinas bacterianas asocia la formación de oxígeno citotóxico con efecto bactericida. La fototerapia con luz ultravioleta-violeta tiene al menos opciones teóricas de eficacia. Para el tratamiento se utiliza PDT con 5-ALA o MAL iluminado con luz policromática visible o especialmente, luz roja. Recientemente se han obtenido buenos resultados utilizando como fotosensibilizante el ácido 3-indol-acético (IAA) y luz verde de (520nm y 9J/cm2), tras iluminación durante 15 minutos (11). Se trata de un fotosensibilizante muy poco común del que no existe literatura previa. No obstante, en nuestra experiencia se obtienen resultados similares con MAL al 8 % y luz roja LED (633nm), para una dosis total de 105J/cm2.
4) Fotoenvejecimiento: la PDT con 5-ALA o MAL demuestra ser eficaz. El tratamiento tiene especial interés cuando el fotoenvejecimiento se asocia a KA, porque el mismo procedimiento permite tratar ambos procesos. Existe buena experiencia con láser de colorante pulsado de 585nm y en el uso de lámparas de luz IPL. Recientemente se han descrito buenos resultados con MAL y luz roja LED de 633nm empleando energías de 37J/cm2.
Por otro lado, existen también estudios documentados sobre la eficacia de la PDT en casos de psoriasis, queilitis actínica, enfermedad de Paget de la mama, esclerodermia, liquen escleroso y atrófico, herpes virus tipo I, hiperplasia sebácea, verrugas víricas, poroqueratosis actínica diseminada, leishmaniasis cutánea y onicomicosis, entre otros (2,3).
Casos clínicos
Múltiples queratosis (KA) y carcinomas basocelulares (BCC) (Fig. 3): Varón de 76 años de edad, fototipo III, de profesión agricultor. Presenta múltiples lesiones en cabeza de disposición aleatoria. La evolución es crónica, habiendo aumentado en número y gravedad, con sangrado y apilamiento queratósico en la mayor parte de las lesiones. El diagnóstico histológico es de múltiples BCC. Tras ensayar sin resultados varios tratamientos tópicos y crioterapia, las lesiones continuaron apareciendo a pesar del uso de sombrero y protección solar. Se indicó tratamiento con PDT mediante 5-ALA (5 %) diluido hasta el 2 % . Se procedió a curetaje con gasa seca, evitando en lo posible el sangrado. Después del lavado con jabón y secado, se pasó de forma rápida y sistematizada el láser de CO2 en modo fraccionado, lo que que produjo "perforaciones" de la epidermis que facilitaron la penetración del sensibilizante. De esta forma se abrevió el tiempo de incubación que fue de una hora. Se cubrió con apósito de poliuretano y gorro oscuro de algodón durante la incubación. Trascurrido este tiempo se lavó con agua y jabón y se irradió con lámpara IPL (Sciton Joule® BBL, Palo Alto, California, EE.UU.) de longitudes de onda entre 420 a 980 nm, spot de 6.75 cm2 y fluencia de 15J/cm2. Se recomendaron analgésicos y evitar la exposición de la zona tratada a cualquier tipo de luz durante una semana.
Las lesiones evolucionaron con formación y posterior caída de costras y el control realizado un año después no mostró recurrencias.
Enfermedad de Bowen (Fig. 4): Varón de 73 años de edad, fototipo III, de profesión comerciante. Padece lesión en cabeza de larga evolución que ha ido en aumento pese a varios tratamientos tópicos por su dermatólogo y curetajes quirúrgicos. La piel es de aspecto frágil, con erosiones e hiperqueratosis. Parte de la lesión es elevada, descamativa y de fácil sangrado. La histología mostró una acantosis epidérmica con presencia de queratinocitos, alteración de la morfología normal y mitosis, que afectaba al espesor de la epidermis, confirmando carcinoma epidermoide o enfermedad de Bowen.
Empleando el mismo protocolo que en el caso anterior, pero utilizando como sensibilizante MAL al 16 % (Metvix®) e incubación de 3 horas, utilizamos luz de láser de Argón (488-514 nm) focalizando el haz para un diámetro de 12 cm a fin de cubrir la lesión. La iluminación se realizó durante 15 minutos, con emisión láser en continuo a 1W de potencia y con una fluencia total de 54J. No se observaron recurrencias un año después del tratamiento.
Acné inflamatorio (Fig. 5): Mujer de 28 años, fototipo IV/V que padece acné moderado-severo y reacción folicular con evidente eritema focal y pigmentación reactiva. Cursa con pústulas frecuentes de nula respuesta a los tratamientos tópicos y orales con retinoides, antibióticos e isotretinoina (Roacutan®, Roche Farma, S.A., Madrid, España). El tratamiento se realizó con MAL al 8 % aplicado sobre las lesiones. Tras 30 minutos de incubación con oclusivo, se irradió con lámpara LED de 418 nm (Omnilux, PhotoTherapeutics Ltd., Cheshire, UK). Se realizaron dos sesiones de 20 minutos cada una y dosis total de 48 J/cm2 por sesión, separadas 3 semanas entre ellas. No se observaron recidivas tras 6 meses de seguimiento, salvo comedones aislados que reaccionaron bien al tratamiento local con acido fusídico.
Rejuvenecimiento cutáneo (Fig. 6): Mujer de 46 años de edad, fototipo III/IV, que presenta envejecimiento cutáneo avanzado por abuso de exposición solar. Se observan líneas, arrugas y cicatrices residuales de acné juvenil, pigmentación moteada y pequeñas queratosis. Después de abrasión mecánica con polvo de cristales de aluminio (Gentle Peel, Candela, BHC Group, UK) y lavado, se aplicó cada 15 minutos MAL al 8 % durante un periodo de 3 horas. Se realizaron dos tratamientos separados un mes con lámpara de luz roja de LEDs (Omnillux, Phototherapeutics Ltd., Cheshire, UK), durante 16 minutos cada uno para una dosis de 105 J/cm2.
Rosácea (Fig.7): Varón de 64 años, fototipo III. Lesión extensa que ocupa toda la nariz y las mejillas. Reacción principal en la punta, dorso y alas nasales, con inflamación y dermatitis reactiva. Múltiples telangectasias, eritrodermia facial y formación de comedones dolorosos. Aplicamos MAL al 16 % en incubación de una hora con apósito oclusivo. Después del lavado, irradiamos con lámpara de LEDs de 633 nm (Omnilux, Phototherapeutics Ltd., Cheshire, UK) durante 16 minutos para una dosis de 105 J/cm2. Se realizaron dos sesiones, una cada 3 semanas.
Discusión
La queratosis actínica, el carcinoma basocelular, el acné, son las afecciones que junto con los métodos de rejuvenecimiento facial, disponen de mayor información bibliográfica y nuestra experiencia concuerda con las publicaciones actuales. La importancia y objetivo de la PDT en los dos primeros casos que presentamos radica en el potencial de transformación maligna de las patologías que presentaban los pacientes, por lo que el tratamiento en estos casos debe orientarse a erradicar la lesión y evitar recidivas. En el acné vulgar y en el fotorrejuvenecimiento, la finalidad sin embargo es reducir el número de lesiones y conseguir una mejoría estética. No obstante, especialmente en áreas expuestas y visibles, el resultado cosmético siempre es también importante para el paciente.
En el tratamiento de la queratosis actínica se consigue la remisión completa en aproximadamente el 90 % de las lesiones, y además con excelentes resultados cosméticos (12-14). Aunque una sesión única puede ser suficiente, algunos autores sugieren que dos sesiones mejoran los resultados y evitan recidivas (13,14). En el carcinoma basocelular superficial la eficacia del tratamiento también es próxima al 90 % , con escasas tasas de recurrencia. No obstante en los carcinomas basocelulares nodulares de gran tamaño la PTD no es suficiente en el 50 % de los casos. A menudo la remisión se consigue con una sesión única, como sucede en el caso que presentamos, pero al igual que acontece con la queratosis actínica, la doble sesión espaciada una semana parece mejorar los resultados y evitar recidivas (15-17). Un estudio de seguimiento a 10 años indica que la práctica totalidad de recidivas se observan antes del tercer año postratamiento (17).
De acuerdo con las publicaciones consultadas, en los casos de acné vulgar los métodos y resultados de la PTD varían (18). Hongcharu y col. fueron los primeros que aportaron datos clínicos de eficacia aplicando 4 sesiones, 1 por semana y durante 1 mes (19). Trabajos posteriores han demostrado reducciones significativas tanto en el número de lesiones inflamatorias como no inflamatorias, generalmente empleando sesiones múltiples, de 3 a 5, separadas por intervalos de 1 ó 2 semanas (11). De este modo se reduce el número de lesiones más del 50 % (20).
En la indicación de fotorrejuvencimiento, encontramos una revisión muy reciente que indica que tanto los resultados como los efectos adversos de la PTD se sitúan en una posición intermedia entre los obtenidos con los tratamientos láser ablativos y no ablativos (21). Zane y col. demuestran mejorías significativas para la mayoría de signos vinculados al envejecimiento cutáneo (hiperpigmentación, líneas finas, aspereza y color cetrino, entre otros) (15). Issa y col. observan mejoría en arrugas, textura y aspecto global de la piel (16). Se ha planteado la hipótesis de que los efectos sobre el fotoenvejecimiento de la PTD sean retardados al cabo de varios meses de haberse aplicado, por posibles cambios histológicos a largo plazo (21,23).
Conclusiones
La PDT es eficaz y segura y permite tratar diferentes procesos oncológicos y no oncológicos, entre los que destacan las queratosis actínicas, enfermedad de Bowen, carcinoma basocelular superficial, procesos víricos, acné y puede emplearse también para el rejuvenecimiento cutáneo. Numerosos estudios permiten prever que sus aplicaciones se ampliarán en los próximos años gracias a los ensayos con nuevos fotosensibilizantes.
Entre sus limitaciones más importantes en la actualidad están: el coste de los agentes, su producción y formulación. La definición de estos agentes precisa de importantes detalles como son la concentración, tiempo de incubación y dosis de irradiación. Estos parámetros están ligados al tiempo de irradiación preciso según la potencia de emisión de las fuentes de luz empleadas. Es de esperar que en años venideros la PDT ofrezca su justa consideración como tratamiento de relevancia y claras indicaciones en las diferentes especialidades de la Medicina.
Bibliografía
1. Martínez-Carpio PA, Trelles MA.: The role of epidermal growth factor receptor in photodynamic therapy: a review of the literature and proposal for future investigation. Lasers Med Sci 2010; 25: 767. [ Links ]
2. Moreno Arias GA, Eng Luna A, Alvarado A, Camps-Fresneda A.: Terapia fotodinámica. Med Cutan Iber Lat Am 2007; 35: 255. [ Links ]
3. Ruiz J, Rebollo N.: Terapia fotodinámica en dermatología. Dermatología Rev Mex 2009; 53: 178. [ Links ]
4. Uebelhoer NS, Dover JS.: Photodynamic therapy for cosmetic applications. Dermatologic therapy 2005; 18: 242. [ Links ]
5. Ruiz-Rodríguez R, Sanz-Sánchez T, Córdoba S.: Photodynamic photorejuvenation. Dermatol Surg 2002;28:742. [ Links ]
6. Alam M, Dover JS.: Treatment of Photoaging with topical aminolevulínico acid and light. Skin therapy Lett 2004, Dec-2005;9:7. [ Links ]
7. Dover JS, Bhatia AC, Stewart B.: Topical 5 aminolevulinic acid combined with intense pulsed light in the treatment of photoaging. Arch Dermatol 2005; 141: 1247. [ Links ]
8. Ruiz Rodríguez R, Prieto Candelas D.: Resultado cosmético en terapia fotodinámica. Rejuvenecimiento. En: Redondo Bellón P, Sánchez Viera M. Eds. Terapia Fotodinámica. Madrid. Edicomplet-Grupo Saned, 2007, Pp:81-88. [ Links ]
9. Marmur ES, Phelps R, Goldberg DJ.: Ultraestructural changes seen after ALA-IPL photorejuvenation:A pilot study. J Cosmetic Laser Therapy, 2005;7:21. [ Links ]
10. Stapleton M, Rodes LE.: Photosensitizers for photodynamic therapy of cutaneous disease. J Dermatol Treat 2003; 14: 107. [ Links ]
11. Huh SY, Na JI, Huh CH, Park KC.: The effect of photodynamic therapy using indole-3-acetic Acid and green light on acne vulgaris. Ann Dermatol 2012; 24: 56. [ Links ]
12. Tarstedt M, Rosdahl I, Berne B, Svanberg K, Wenberg AM.: A randomized multicenter study to compare two treatment regimens of topical methyl aminolevulinate (Metvix®)-PDT in actinic keratosis of the face and scalp. Acta Derm Venereol 2005; 85: 424. [ Links ]
13. Annemans L, Caekelbergh K, Roelandts R, et al.: Real-life practice study of the clinical outcome and cost-effectiveness of photodynamic therapy using methyl aminolevulinate (MAL-PDT) in the management of actinic keratosis and basal cell carcinoma. Eur J Dermatol 2008;18: 539. [ Links ]
14. Tshen EH, Wong DS, Pariser DM.: Photodynamic therapy using aminolaevulinic acid for patients with nonhyperkeratotic actinic keratoses of the face and scalp: phase IV multicentric clinical trial with 12-mounth follow-up. Br J Dermatol 2006;155:1262. [ Links ]
15. Surrenti T, De Angelis L, Di Cesare A, Fargnoli MC, Peris K.: Efficacy of photodynamic therapy with methyl aminolevulinate in the treatment of superficial and nodular basal cell carcinoma: an open-label trial. Eur J Dermatol 2007; 17: 412. [ Links ]
16. Foley P, Freeman M, Menter A et al.: Photodynamic therapy with methyl aminolevulinate for primary nodular basal cell carcinoma: results of two randomized studies. Int J Dermatol 2009; 48: 1236. [ Links ]
17. Christensen E, Mork C, Skogvoll E.: High and sustained efficacy after two sesions of topical 5-aminolaevulinic acid photodynamic therapy for basal cell carcinoma: a prospective, clinical and histological 10-year followup study. Br J Dermatol 2012; 166: 1342. [ Links ]
18. http://www.skintherapyletter.com/2007/12.10/1.htlm [ Links ]
19. Hongcharu W, Taylor CR, Chang Y, Aghassi D et al.: Topical ALA-photodynamic therapy for the treatment of acné vulgaris. J Invest Dermatol 2000; 115: 183. [ Links ]
20. Horfelt C, Funk J, Frohm-Nilsson M et al.: Topical methyl aminolaevulinate therapy for treatment of facial acne vulgaris: results of a randomized, controlled trial. Br J Dermatol 2006; 155: 608. [ Links ]
21. Kohl EA, Karrer S.: Photodynamic skin rejuvenation. Photon Lasers Med 2012; 1: 27. [ Links ]
22. Zane C, Capezzera R, Sala R, Venturini M, Calzavara-Pinton P.: Clinical and echographic analysis of photodynamic therapy using methylaminolevulinate as sensitizer in the treatment of photodamaged facial skin. Lasers Surg Med 2007; 39: 203. [ Links ]
23. Issa MC, Piñeiro-Maceira J, Vieira MT, Olej B, Mandarim-de-Lacerda CA, Luiz RR, Manela-Azulay M.: Photorejuvenation with topical methyl aminolevulinate and red light: a randomized, prospective, clinical, histopathologic and morphometric study. Dermatol Surg 2010; 36: 39. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Dr. Serge Mordon
INSERM U 703 152, rue du Dr. Yersin 59120
59120 Loos, Francia.
e-mail: serge.mordon@inserm.fr