My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Cirugía Plástica Ibero-Latinoamericana
On-line version ISSN 1989-2055Print version ISSN 0376-7892
Cir. plást. iberolatinoam. vol.40 n.2 Madrid Apr./Jun. 2014
https://dx.doi.org/10.4321/S0376-78922014000200015
Tratamiento de quemaduras mediante plasma rico en plaquetas (PRP). Parte I
Treatment of burns with platelet rich plasma (PRP). Part I
Rossani, G.*; Hernández, I.*; Alcolea, J.M.**; Castro-Sierra, R.***; Pérez-Soto W.**** y Trelles, M.A.*****
*Cirujano Plàstico de INGECEL, Instituto Peruano de Ingeniería Celular y Manufactura Tisular, Lima, Perú
**Licenciado en Medicina y Cirugía. Master en Medicina Estética. Clínica Alcolea, Barcelona, España
***Cirujano Plástico, Jefe del Servicio de Cirugía Plástica, Hospital Nacional Hipólito Unanue (HNHU), Lima, Perú
****Cirujano Plástico, Director del Programa de Investigación y Desarrollo del Servicio de Cirugía Plástica, Hospital Nacional Hipólito Unanue (HNHU), Lima, Perú
*****Cirujano Plástico, Instituto Médico Vilafortuny, Cambrils (Tarragona), España
Dirección para correspondencia
RESUMEN
El objetivo del presente trabajo es determinar la eficacia clínica del plasma rico en plaquetas (PRP) en las quemaduras de segundo grado. Estudiamos el tiempo requerido en la reepitelización del tejido dañado, la estancia hospitalaria asociada a la curación de las lesiones y la satisfacción del paciente.
Realizamos un estudio prospectivo, observacional y longitudinal, en una muestra de 115 pacientes con quemaduras de segundo grado según la clasificación de Converse-Smith. Las lesiones fueron de menos de 48 horas de evolución, en diferentes zonas de cara y cuerpo. A todos los pacientes se les aplicó de forma ambulatoria PRP por goteo, completándose el tratamiento con la aplicación de gasas parafinadas. El estudio se realizó entre marzo de 2011 y agosto de 2013.
Las quemaduras que evolucionaron mejor y de forma más rápida fueron las de cara, seguidas por las de abdomen y, por último, las de extremidades inferiores. En todas, el tiempo de epitelización fue un 30 % inferior que en quemaduras de similar extensión, profundidad y localización, en pacientes anteriormente tratados sin PRP. Los pacientes fueron atendidos ambulatoriamente cuando las lesiones lo permitieron, y si presentaban lesiones más extensas fueron hospitalizados. El tiempo de internamiento en estos casos se redujo como promedio 18 días con respecto al grupo no tratado con PRP. El tiempo de reepitelización, estancia hospitalaria y la satisfacción de los pacientes, alcanzaron significación estadística p< 0,05.
En conclusión, creemos que el uso de PRP acorta el tiempo de recuperación en quemaduras de segundo grado, reduce el tiempo de hospitalización y conlleva un alto grado de satisfacción de los pacientes por los resultados obtenidos.
Palabras clave: Plasma rico en plaquetas, PRP, Factores de crecimiento, Quemaduras de segundo grado, Reparación tisular, Hemoderivados.
Nivel de evidencia científica II
ABSTRACT
The aim of this study is to determine the clinical efficacy of platelet rich plasma (PRP) for second degree burns. The time required for tissue reepithelization of lesions, down time associated with wound healing and patient satisfaction, are studied.
We conduct a prospective, observational and long term study on 115 patients with second degree burns according to Converse-Smith classification. The lesions were of less than 48 hour evolution, located in different areas of the face and body. All patients received outpatient drip PRP, completing the treatment with the application of paraffin wax coated dressing and occlusive bandage. The study was carried out between March 2011 and August 2013.
Lesions wit a better outcome and faster heal were those located on the face, followed by those on the abdomen and lastly those on the legs. In all cases reepithelization time was 30 % less compared to patients with burns of similar size, deepness and location, treated without PRP. Patients were treated as outpatients when lesions permitted. When lesions were more extensive, patients were hospitalized. Hospital stay in these case was decreased an average of 18 days when compared to patients not treated with PRP. Reepitelizatión time, hospital stay and patient satisfaction with the results achieved, reached a statistical value of p < 0,05.
In conclusion, the use of PRP shortens recovery time for second degree burns, reducing hospital stay as well as obtaining a high patient satisfaction with results achieved.
Key words: Platelet rich plasma, PRP, Growth factors, Second degree burns, Tissue repair, Hemoderivatives.
Level of evidence II
Introducción
En nuestro medio, los mecanismos de producción más frecuentes de las quemaduras son: fuego directo (llama) y contacto con líquidos y/o sólidos calientes. La extensión y profundidad de las quemaduras están en relación directa con la intensidad de energía transmitida por unidad de tiempo de contacto con la fuente de origen (1).
La severidad de las quemaduras está determinada por 5 factores, según la escala de Converse-Smith (2):
1. Profundidad de la lesión. A mayor profundidad, peor pronóstico.
2. Extensión de la quemadura, expresada en porcentaje de superficie corporal total lesionada (SCTQ % ).
3. Localización de la quemadura. Peor pronóstico en las que asientan en áreas críticas (parpados, comisura bucal o zonas de flexión articular).
4. Edad del paciente. Peor pronóstico en edades avanzadas.
5. Estado general de salud del individuo afectado.
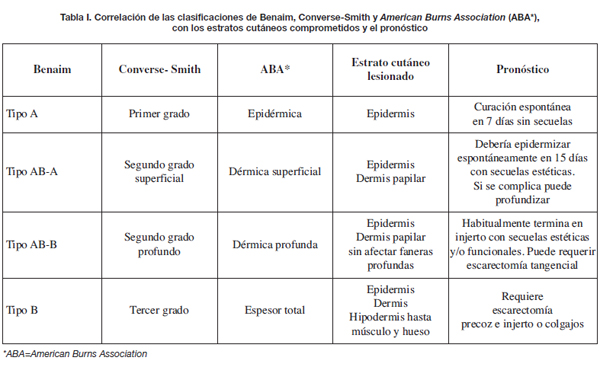
Basamos la asignación del grado de quemadura tratada en la clasificación de Converse-Smith, que junto con la de la American Burns Association (ABA) y la de Benaim, son las habitualmente empleadas (3, 4). Estas clasificaciones se atienen a la profundidad que la quemadura alcanza en el tejido y mostramos sus correlaciones en la Tabla I.
Las quemaduras de segundo grado que presentamos en nuestro estudio, se caracterizaron por estar típicamente ocasionadas por líquidos calientes y fuego directo. Por lo general, en el momento de abordar su tratamiento, eran lesiones exudativas y con flictenas, que al desbridarlas mostraban un fondo de color rojo vivo y altamente sensible al tacto, propio de una localización en dermis papilar. Sin embargo, cuando el fondo aparecía de color blanquecino y de aspecto acartonado, lo consideramos indicativo de afectación de dermis profunda. Según los controles, en condiciones adecuadas de asistencia, estas quemaduras suelen recuperarse en 3 a 4 semanas, aunque sin respetar la arquitectura normal de la epidermis. Pero si alcanzan la dermis profunda, dan lugar a retracciones importantes en las zonas de flexión, dificultando o llegando a impedir la flexo-extensión articular. En aquellos casos en que afectan todo el contorno de las extremidades, pueden inducir un síndrome compartimental.
Cuando se produce una quemadura acontecen dos hechos importantes. En primer lugar disminuye la velocidad del flujo sanguíneo y linfático locales debido al exudado y al edema reactivo acompañantes, lo que afecta de modo inmediato la función de adhesión plaquetaria. En segundo lugar se produce una estasis microcirculatoria que se acompaña de trombosis microvascular. Estos fenómenos, bien conocidos, se suceden en pocos minutos, interfiriendo de modo drástico con el aporte de nutrientes y oxígeno desde la dermis profunda a la zona lesionada, lo que hará que según el tipo de cicatrización, se produzcan secuelas estéticas y/o funcionales (5).
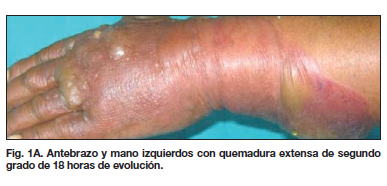
Debido a las alteraciones que induce la quemadura en el tejido, se dificulta la llegada de nutrientes y factores regeneradores capaces de ayudar en la reparación tisular desde el lecho vascular hasta la zona lesionada. Debido a ello, ideamos un método que permite aportar los nutrientes y factores regeneradores a través del propio tejido lesionado, dejando gotear plasma rico en plaquetas (PRP) sobre la lesión convenientemente desbridada (Fig. 1 A-D). El PRP tiene como misión regenerar las zonas quemadas, estimulando su reparación con una arquitectura y funcionalidad de características similares al tejido original. Debido al incremento que el empleo de PRP con distintas finalidades ha experimentado en España, la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) considera al PRP como medicamento de uso humano desde su informe de 23 de mayo de 2013 (6).



El objetivo del presente estudio es comprobar que los pacientes con quemaduras recientes de segundo grado tratados con PRP logran una cicatrización más rápida, con mejor reepitelización y reparación de la arquitectura normal de la piel. Este resultado se traduciría en reducción del tiempo de baja laboral y ventajas para el paciente que repercuten en una mejor calidad de su estado general y un aumento del grado de satisfacción por los resultados obtenidos con el tratamiento. Igualmente, la recuperación más rápida incide sobre el tiempo de estancia hospitalaria y reduce de forma significativa los costos sociosanitarios.
Material y método
Para alcanzar los objetivos de este estudio, elaboramos un protocolo de extracción y preparación de PRP para ser empleado en pacientes ambulatorios con quemaduras de segundo grado. La finalidad de este protocolo debía examinarse como una alternativa terapéutica válida y de bajo costo asistencial.
Diseñamos un estudio prospectivo, observacional en el tiempo, longitudinal y comparativo a casos control anteriormente tratados sin PRP. Los pacientes control habían sido tratados convencionalmente con curas oclusivas tras desbridamiento de flictenas y cobertura de las lesiones expuestas con gasas parafinadas. Las curas se realizaron cada 4 días, con limpieza suave con suero salino y aplicación de povidona iodada en solución al 10 % antes de cubrir con gasas parafinadas. Estos pacientes sirvieron de control para observar la evolución del grupo de estudio de 115 pacientes que presentaban en el momento de su ingreso quemaduras de segundo grado. Todos fueron tratados en el Servicio de Cirugía Plástica del Hospital Nacional Hipólito Unanue (HNHU) de Lima, Perú, en el periodo comprendido entre marzo de 2011 y agosto de 2013.
De la muestra de 115 pacientes, 74 fueron mujeres y 41 varones, con quemaduras de segundo grado y que acudieron al hospital antes de superar las 48 horas de haberse producido las lesiones. Todos presentaban fototipo IV según clasificación de Fitzpatrick. El grupo de edad que padeció más quemaduras fue el comprendido entre los 40 y los 60 años. La muestra para el estudio se seleccionó de un total de 276 pacientes visitados, 161 de los cuales fueron excluidos al no cumplir los criterios de inclusión del presente estudio (Tabla II). De los 115 pacientes seleccionados, 36 recibieron atención hospitalaria y 79 fueron atendidos en consulta ambulatoria externa (Tabla III). Todos firmaron el correspondiente consentimiento informado y fueron tratados bajo los criterios internacionales de Manipulación Mínima de Tejidos Autólogos, respetando los acuerdos y protocolos de investigación de Helsinki.
Como criterios de inclusión empleamos:
• Pacientes con quemaduras de segundo grado en el momento de su admisión.
• Quemaduras producidas en el límite de las 48 horas anteriores a la asistencia médica, con lesiones de similar profundidad y uniformidad del lecho cruento.
• Rango de edad entre 15 y 70 años (media 48,7).
• Superficie corporal total quemada (SCTQ) no superior al 20 % .
• Todos debían ser tratados por el mismo equipo médico del HNHU y con el mismo protocolo.
• Estables desde el punto de vista hemodinámico.
• Con estado físico y nutricional adecuados. A tal fin, determinamos en todos la proteinemia, considerando adecuados valores no inferiores a 3,5 mg/100 ml, y Hemoglobina (Hb) igual o superior a 11 mg/100 ml.
Los criterios de exclusión fueron:
• Quemaduras de primer y tercer grado.
• Quemaduras con evolución superior a 48 horas.
• Quemaduras con signos evidentes de infección.
• Pacientes fuera del rango de edad preestablecido entre 15 a 70 años.
• Quemaduras con SCTQ superior al 20 % .
• Quemaduras con lecho cruento poco uniforme o de profundidad variable, poco definida.
• Pacientes que no pudieran ser tratados por el mismo equipo médico y/o que no siguieran el mismo protocolo de actuación propuesto.
• Hemodinámicamente inestables.
• Con signos de desnutrición y/o estado físico deteriorado, con dificultad para comunicarse verbalmente.
• Proteinemia inferior a 3.5 mg/100 ml y/o Hb inferior a 11 mg/100 ml.
El personal encargado de la admisión de pacientes con quemaduras fue entrenado para incorporar aquellas lesiones que cumplieran los criterios de inclusión del estudio. Con esa finalidad, editamos fichas clínicas para la toma de datos, material fotográfico, e instrucciones para obtener imágenes en similares condiciones de luz. El entrenamiento se realizó mediante formación específica por parte de los 2 primeros autores, a fin de unificar criterios comunes a todo el equipo médico en la selección y en los protocolos de actuación.
Como material empleamos jeringas estériles desechables de diferentes capacidades y tubos estériles de vacío de 3,5 cc para las tomas de sangre, mezcladas con citrato de sodio al 3,2 % como anticoagulante. Una vez obtenidas las muestras, procedimos a su centrifugación empleando una centrifugadora analógica GreedMed GT 119-100T (EE.UU.) de 6 tubos, programable hasta 4000 revoluciones por minuto (rpm). En la posterior activación de las plaquetas utilizamos ampollas de 10 ml de gluconato de calcio al 10 % . Para el tratamiento oclusivo empleamos gasas parafinadas y gasas sin parafina, todas ellas esterilizadas.
Modo de obtención del PRP
El modo de obtención del PRP difiere según el método sea abierto o cerrado. En Perú, mientras se trate de técnica cerrada al vacío, en pequeñas cantidades, autólogo y bajo manipulación nula o mínima, no requiere de seguimiento sanitario, pero es y sería ideal tener la asesoría de un especialista en hematología. En España, en caso de emplear la técnica abierta, debe solicitarse permiso previo al organismo sanitario correspondiente, el cual inspeccionará las instalaciones antes de otorgarlo (6). Si se emplea la técnica cerrada no se precisa el permiso mencionado, aunque el kit empleado en todo el proceso deberá disponer de marcado CE.
En nuestro hospital, el equipo médico de Cirugía Plástica fue el encargado de procesar la sangre que se extrajo mediante técnica cerrada, bajo la autorización y supervisión del Departamento de Hematología y de acuerdo a los protocolos internacionales de manipulación de tejidos autólogos. La extracción de sangre se realizó por venopunción en tubos de 3,5 ml, estériles y cerrados al vacío, que contenían citrato sódico al 3,2 % . Los tubos se colocaron en la centrifugadora que se programó a 3200 rpm durante 12 minutos. El objetivo de la centrifugación es lograr una concentración de plaquetas de entre 3 a 5 veces la concentración basal, que según los análisis realizados, oscilaba entre 143.000 a 247.000 plaquetas, lo que está en el rango normal (7). Por consenso, la cantidad de sangre que se obtuvo de cada paciente no superó los 40 ml, de los que se obtuvieron a su vez entre 8 a 10 ml de PRP, cantidad suficiente para cubrir las zonas de quemaduras que según nuestra experiencia pueden corresponder a un 20 % de SCTQ. La cantidad de sangre extraída no entraña riesgo de producir alteraciones hemodinámicas. El plasma obtenido quedó separado en 3 fracciones: un tercio superior que corresponde a plasma pobre en plaquetas; un tercio medio que tiene una concentración plaquetaria normal; y un tercio inferior que es el que se conoce como PRP. Inmediatamente por debajo de la fracción de PRP y justo por encima de la fracción eritrocitaria, se encuentran los leucocitos. De acuerdo con lo publicado por algunos autores (8), no empleamos la fracción leucocitaria que tiene acción proinflamatoria, considerando que la fracción con PRP posee una adecuada función bacteriostática.
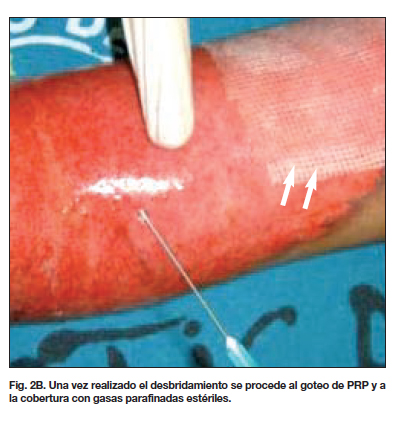
Una vez obtenido por aspiración el PRP del tercio inferior del contenido plasmático del tubo, añadimos 0,1 ml de gluconato de calcio al 10 % por cada ml de PRP, a fin de estimular la liberación de factores de crecimiento. Este proceso deber hacerse con rapidez, ya que la activación plaquetaria y la liberación de factores de crecimiento se inicia tras 8 minutos. Realizamos la aplicación sobre el lecho cruento mediante goteo, antes de que el contenido de la jeringa gelifique como consecuencia de la activación del proceso de coagulación (Fig. 2 A-C). Tratamos de cubrir toda la lesión insistiendo en que el goteo formará una película uniforme sobre la zona quemada. Inmediatamente después, colocamos apósitos parafinados y sobre ellos gasas estériles, manteniéndolos durante 4 días. Pasado este periodo, abrimos y valoramos la evolución, aspecto de las lesiones y resultados. La cura oclusiva se repitió las veces necesarias hasta lograr la reepitelización de la piel en cada uno de los casos (Fig. 3 A-D).




Estudio estadístico
Empleamos el sistema SPSS® v. 21 para Windows. Como test de contraste estadístico utilizamos t de Student para muestras independientes, tomando p < 0,05 como punto de significación.
Resultados
Los 115 pacientes que presentaban quemaduras de segundo grado fueron tratados en 154 unidades distribuidas en abdomen, piernas, manos, cara y otras zonas varias como orejas o párpados. Del total, 53 pacientes sufrieron las lesiones en su domicilio, en 45 ocurrieron en su entorno laboral y en 17 en otros lugares diversos (Tabla III). En su mayoría, las quemaduras se originaron por agua caliente, seguidas con diferencia evidente por las ocasionadas por fuego directo o por agentes químicos. En todos los pacientes dividimos las lesiones por unidades de tratamiento con la finalidad de comparar la evolución y rapidez de las zonas tratadas según las diferentes partes del cuerpo.
La distribución de pacientes, según la localización de las quemaduras que presentaban fue la siguiente:
• Abdomen: 13 pacientes presentaban quemaduras unitarias pero extensas, que correspondieron al 6 % de promedio de SCTQ, con 13 unidades tratadas.
• Brazos: 26 pacientes, con un promedio del 9 % de SCTQ y 36 unidades tratadas.
• Piernas: 29 pacientes, con un promedio del 11 % de SCTQ y 46 unidades tratadas.
• Manos: 24 pacientes, con el 2 % de SCTQ promedio y 30 unidades tratadas.
• Cara: 15 pacientes, con el 3 % de SCTQ promedio y 15 unidades tratadas.
• Otras zonas: 8 pacientes, con 14 unidades tratadas.
La Tabla IV muestra las zonas de las quemaduras y su distribución por sexos. En las mujeres, generalmente ocurrieron durante sus actividades domésticas y fueron más frecuentes en piernas, brazos, abdomen y manos; sin embargo, las producidas en la cara, fueron consecuencia de agresiones. En los hombres, se distribuyeron en brazos, manos y piernas, fueron ocasionadas por accidentes y se originaron durante las actividades ocupacionales. Las quemaduras tratadas en otras zonas se debieron en la mayoría de casos, tanto en hombres como mujeres, a agresiones y a actos de violencia física.
A los 115 pacientes destinados a tratamiento con PRP, con un total de 154 unidades tratadas, se les realizó el primer tratamiento con PRP durante la primera cura. Las curas se realizaron cada 4 días, pero tuvimos en cuenta la disponibilidad de los pacientes para llegar hasta el hospital debido a que 28 de los 115 tratados vivían en regiones apartadas. En estos 28 pacientes, las curas se practicaron cada 6 a 8 días. Lejos de representar este dato un sesgo para el estudio, sirvió para controlar y comparar los datos relativos a la aparición de islotes epidémicos, así como la confluencia y firmeza de las pequeñas islas de crecimiento y escaras, y también el alisamiento y/o uniformidad de la piel.
Las quemaduras de la cara fueron las que más rápidamente evolucionaron, con aparición de los primeros islotes epidérmicos a los 4 días, mostrando islas firmes y confluentes desde el 6o día y consiguiendo una piel de aspecto fino y liso en solo 8 días. Por el contrario, las quemaduras de las piernas fueron las que tardaron más tiempo en reepitelizar, lo que ocurrió aproximadamente en el doble de tiempo que en la cara (Tablas V-VI). El resto de zonas evolucionó de modo similar en cuanto al tiempo, a excepción del alisamiento de la piel de las manos que, en comparación con otras zonas, tardó alrededor de 14 días en completarse, lo que supuso un tiempo proporcionalmente más largo para alcanzar el resultado de reepitelización en comparación al de otras lesiones de las diversas zonas tratadas. Este dato podría relacionarse con el hecho de que, tanto hombres como mujeres, hicieron uso prematuro de las manos que requirió movimiento articular, debido a exigencias laborales y/o domésticas inaplazables.
Las zonas con lesiones varias y extensas como abdomen y cara requirieron 4 a 8 días (promedio de 6 días) de estancia en el hospital. En total el número de pacientes que requirió internamiento fue 28 (15 que presentaban lesiones en cara y 13 en abdomen). En aquellos pacientes tratados de forma convencional, como se explicó con anterioridad, el tiempo de estancia hospitalaria fue de entre 16 a 20 días (promedio de 18 días).
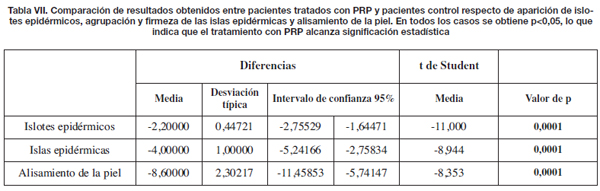
Realizamos análisis de contraste empleando la t de Student para verificar si la diferencia entre medias era estadísticamente significativa en la aparición de los islotes epidérmicos, en la confluencia en islas epidérmicas y en el alisamiento de la piel, tomando para ello los valores promedio obtenidos para las 3 características del estudio. En todos los casos el valor fue de p< 0,05, indicando que la diferencia entre medias era estadísticamente significativa tal y como mostramos en la Tabla VII.
Discusión
Las quemaduras de segundo grado, particularmente las más profundas, pueden derivar en función de su extensión y de las condiciones añadidas que presente el paciente o el agente causante, hacia posibles complicaciones importantes y secuelas físicas que corresponden a la propia cicatrización. También pueden ocurrir retracciones cutáneas, más frecuentemente en las quemaduras que afectan áreas de flexión articular y/o incluso llegar a desarrollarse como complicación un síndrome compartimental. De otro lado, las secuelas emocionales son altamente traumáticas en la psicología de este tipo de pacientes, sobre todo cuando quedan cicatrices residuales y/o las quemaduras se localizan en zonas visibles como la cara o las manos. Asimismo, las secuelas cicatriciales repercuten en absentismo laboral, con tasas difíciles de pronosticar. No hay que olvidar que los sobrecostes hospitalarios, cuando la evolución es tórpida, hacen necesario implementar medidas que acorten la duración del tratamiento y minimicen las secuelas postraumáticas. Sin duda, todo esto se refleja también en el grado de satisfacción por parte del paciente con respecto a los resultados del tratamiento (Fig. 4 A-B).

Actualmente, disponemos de abundante literatura sobre las bondades del empleo de PRP asociadas a los factores de crecimiento que liberan las plaquetas, aunque la mayoría de los estudios disponibles tratan sobre dolor crónico músculo-esquelético, tendinopatías, capsulitis y osteoartritis (9). Estos estudios han arrojado nueva luz sobre los mecanismos de acción con que contribuyen los factores liberados en la degranulación plaquetaria y en la reparación de tejidos previamente lesionados (10); sin olvidar el importante papel que juegan las citoquinas en el proceso de reparación tisular (11). Aunque no tan numerosas, encontramos también desde la década de los 80, referencias sobre la utilización de PRP en la cicatrización de úlceras crónicas en extremidades inferiores (12); pero, a partir de los años 90 se han publicado trabajos sobre el empleo de preparados plaquetarios en solución o gel, como el estudio prospectivo de Frykbert (13), de respuesta estadísticamente significativa para el tratamiento de úlceras crónicas. Posteriormente, Montón (14) comunicó buenos resultados, aunque sin cuantificación analítica, sobre ulceras de etiología diversa de largo tiempo de evolución y algunos casos de reconstrucción mamaria tratados con PRP. En este sentido, también hay informes sobre los buenos resultados de este tratamiento por Anitua (15) y por Driver (16).
Sin embargo, no encontramos tantas referencias sobre la utilización de PRP en el tratamiento de las quemaduras, aunque el trabajo de Poon (17) ayuda a desvelar la relación entre los mecanismos inmunomoduladores moleculares y los factores de crecimiento que intervienen en la reparación del daño tisular. Por otra parte, los trabajos de Eppley (18, 19) dejan clara la importancia que juega la concentración de factores de crecimiento, considerando que es esencial lograr un incremento de hasta 8 veces en el valor basal del número de plaquetas. Aunque los valores obtenidos y verificados por el servicio de Hematología del HNHU donde se efectuó nuestro estudio, se encontraban entre 3 y 5 veces sobre el valor basal con respecto a lo comunicado por Pietrzak (7). Además, los valores constatados en el tratamiento de las quemaduras que presentamos, están en línea con la revisión efectuada por Pallua en 2010 (20). Cabe mencionar también el trabajo de Márquez de Aracena (21) sobre quemaduras conjuntivales, que a pesar recoger un escaso número de pacientes, hecho que puede limitar el estudio analítico, se extrapola bien con los resultados del trabajo que nosotros presentamos. Kazakos (22) habla también sobre los buenos resultados que obtiene al tratar heridas traumáticas y quemaduras por fricción empleando PRP en forma de gel, en tanto que Henderson (23) apunta que las lesiones secundarias a tratamiento con láser ablativo para rejuvenecimiento cutáneo aceleran la angiogénesis si se emplea PRP. El PRP incrementa la proliferación de fibroblastos, y por lo tanto, la formación de colágeno. No obstante, cabe objetar que sus resultados con respecto a la reepitelización no son concluyentes. Igualmente, en este estudio se ha de tener en cuenta el papel del láser ablativo, que preponderantemente contribuye en la neoformación de colágeno, así como que la reepitelización durante el proceso posterior de reparación de las heridas depende de la profundidad que el tratamiento alcanza en la piel, junto al depósito térmico residual. El proceso térmico incide en el grado del proceso inflamatorio que conlleva la intensidad de la respuesta reparativa tisular y la formación de nuevo colágeno.
Como consecuencia de la utilización de PRP en los procesos que requieren fases de regeneración en diversos órganos o tejidos, hemos de plantearnos la posibilidad de utilizar PRP como ocurre en las quemaduras de segundo grado. Es sabido que ante una quemadura de estas proporciones se origina una respuesta inflamatoria con participación de mediadores químicos y enzimáticos, radicales libres y hormonas (24). A esta respuesta se añade la activación sucesiva de macrófagos y otras células entre las que se incluyen las plaquetas, que igualmente liberan mediadores de la reparación del tejido.
En esta situación, el planteamiento que tomamos para el presente estudio fue acelerar el proceso reparativo con el concentrado de plaquetas, previniendo así las complicaciones cicatriciales. Las plaquetas activadas liberan en primer lugar el denominado PDGF o factor de crecimiento derivado de estos elementos formes de la sangre; péptido que tiene un papel importante en la reparación de cualquier tipo de heridas (25). Por este motivo evitamos un posible sesgo en el estudio al fijar el momento máximo de inicio del tratamiento con PRP a las 48 horas después de haber ocurrido las lesiones, teniendo en cuenta que una excesiva activación de las cascada enzimática y celular podría introducir cambios transcurrido este período de tiempo. Por la misma razón, seleccionamos pacientes que no presentaran signos de infección en el momento de su ingreso, cuando se examinaron sus quemaduras por primera vez.
A la vista de los resultados observados, podría plantearse el tratamiento de PRP en quemaduras de tercer grado en tanto que se trata de un producto autólogo, siempre que la extracción hemática se realice en completa asepsia, unido al resto de medidas que son propias del método para tratar este tipo de quemaduras. En este sentido, la propuesta terapéutica que exponemos tiene en cuenta que el PRP se emplea ya como aliado para tratar lesiones que requieren injertos o colgajos (26).
Conclusiones
Atendiendo al número de pacientes presentados en este estudio, y en comparación con los trabajos comentados y con un metanálisis que incluye diversos ensayos clínicos (Martínez-Zapata MJ, Martí-Carvajal AJ, Solá I et al. Autologous platelet-rich plasma for treating chronic wounds. Cochrane Database Syst Rev. 2012 Oct 17; 10:CD006899), estimamos que las observaciones efectuadas en el tratamiento de quemaduras de segundo grado muestran las bondades del tratamiento con PRP.
Evidenciamos un tiempo de recuperación más breve en contraste con las muestras de pacientes tratados sin PRP. La cicatrización, transcurridos 4 meses, fue de mejor calidad, presentando un tejido netamente más uniforme de acuerdo al análisis estadístico, tanto en la aparición de islotes epidérmicos, como en la confluencia y firmeza del tejido neoformado, junto a la homogeneidad de la superficie y al aspecto de la piel. La reincorporación laboral de los pacientes se produjo más rápidamente, y en la economía hospitalaria observamos un menor gasto derivado de que el periodo de internamiento de los pacientes fue más breve. Significativamente, los pacientes manifestaron sentirse muy satisfechos con los resultados obtenidos, a la vez que pudieron reincorporarse más tempranamente a sus actividades gracias a los resultados del tratamiento.
El PRP es un producto autólogo, carente de toxicidad, de bajo coste y su uso se puede considerar como un tratamiento áltamente reproducible.
Declaración
Los autores manifiestan no tener ningún interés comercial en los productos o aparatos reseñados en el presente trabajo. Agradecen al D. Juan Carlos Medina, estadístico, su colaboración en los análisis de los datos.
Bibliografía
1. Ward PA, Till GO.: Pathophysiologic events related to thermal injury of skin. J Trauma. 1990; 30 (12 Suppl): S75-S79. [ Links ]
2. Bendlin A, Linares HA, Benaim F.: Tratado de Quemaduras. Interamericana McGraw-Hill, México, 1993, Cap. 14,15. [ Links ]
3. Benaim F. Quemaduras. En: Gutierrez F, Oria A (Edit.): Cirugía de Michans. Editorial El Ateneo, Buenos Aires, 1988. [ Links ]
4. Deitch E, Rutan R, Rutan T.: Burn management. In: Irwing R, Cerra F, Rippe J (Edit.): Intensive Care Medicine. Lippincott Raven, Philadelphia 1988. [ Links ]
5. Knighton D, Hunt T, Thakral K, Goodson W.: Role of platelets and fibrin in the healing sequence: an in vivo study of angiogenesis and collagen synthesis. Ann Surg. 1982; 196(4):379-388. [ Links ]
6. Informe/V1/23052013. Informe de la Agencia Española del Medicamento y Productos Sanitarios sobre el uso de plasma rico en plaquetas. 23 de mayo de 2103. [ Links ]
7. Pietrzak WS, Eppley BL.: Platelet rich plasma: biology and new technology. J Craniofac Surg. 2005; 16(6):1043-1054. [ Links ]
8. Anitua E, Alonso R, Girbau C, Aguirre JJ, Muruzabal F, Orive G. Antibacterial effect of plasma rich in growth factors (PRGF® -Endoret® ) against Staphylococcus aureus epidermidis strains. Clin Exp Dermatol. 2012; 37:652-657. [ Links ]
9. Anitua E, Sánchez M, Nurden AT, et al.: Plateletreleased growth factors enhance the secretion of hyaluronic acid and induce hepatocyte growth factor production by synovial fibroblasts from arthritic patients. Rheumatology (Oxford). 2007; 46(12):1769-1772. [ Links ]
10. Sánchez M, Anitua E, Orive G, Mujika I, Andia I. Platelet-rich therapies in the treatment of orthopaedic sport injuries. Sports Med. 2009; 39(5):345-354. [ Links ]
11. Andia I, Sanchez M, Maffulli N. Tendon healing and platelet-rich plasma therapies. Expert Opin Biol Ther. 2010; 10(10):1415-1426. [ Links ]
12. Knighton DR, Ciresi KF, Fiegel VD, Austin LL, Butler EL.: Successful treatment with autologous plateletderived wound healing factors (PDWHF). Ann Surg. 1986; 204(3):322-330. [ Links ]
13. Frykbert RG, Driver VR, Carman D, et al.: Chronic wounds treated with a physiologically relevant concentration of platelet-rich plasma gel: A prospective case series. Ostomy Wound Manage. 2010; 56(6):36-44. [ Links ]
14. Montón J, Pérez S, Gómez GJ. Experiencia clínica en el empleo de factores de crecimiento autólogos obtenidos de plasma rico en plaquetas. Cir plást iberolatinoam. 2007; 33(3):155-162. [ Links ]
15. Anitua E, Aguirre JJ, Algorta J, et al.: Effectiveness of autologous preparation rich in growth factors for the treatment of chronic cutaneous ulcers. J Biomed Mat Res B Appl Biomater. 2008; 84(2):415-421. [ Links ]
16. Driver VR, Hanft J, Fylling CP, Beriou JM.: Autogel Diabetic Foot Ulcer Study Group. A prospective, randomized, controlled trial of autologous platelet-rich plasma gel for the treatment of diabetic foot ulcers. Ostomy Wound Manage. 2006; 52(6):68-74. [ Links ]
17. Poon IK, Hulett MD, Parish CR.: Molecular mechanisms of late apoptotic/necrotic cell clearance. Cell Death Differ. 2010; 17(3):381-394. [ Links ]
18. Eppley BL, Woodell JE, Higgins J. Platelet quantification and growth factor analysis from platelet-rich plasma: implications for wound healing. Plast Reconstr Surg. 2004; 114(6):1502-1508. [ Links ]
19. Eppley BL, Pietrzak WS, Blanton M.: Platelet-rich plasma: a review of biology and applications in plastic surgery. Plast Reconstr Surg. 2006; 118(6):147e-59e. [ Links ]
20. Pallua N, Wolter T, Markowicz M.: Platelet-rich plasma in burns. Burns. 2010; 36(1):4-8. [ Links ]
21. Márquez-de-Aracena R, Montero-de-Espinosa I, Muñoz M, Pereira G.: Subconjunctival application of plasma platelet concentrate in the treatment of ocular burns. Preliminary results. (Article in Spanish). Arch Soc Esp Oftalmol. 2007; 82(8):475-481. [ Links ]
22. Kazakos K, Lyras DN, Verettas D, Tilkeridis K, Tryfonidis M. The use of autologous PRP gel as an aid in the management of acute trauma wounds. Injury. 2009; 40(8):801-805. [ Links ]
23. Henderson JL, Cupp CL, Ross EV, et al.: The effects of autologous platelet gel on wound healing. Ear Nose Throat J. 2003; 82(8):598-602. [ Links ]
24. Grayson LS, Hansbrough JF, Zapata-Sirvent RL, et al.: Quantitation of cytokine invols in skin graft donor site wound fluid. Burns. 1993; 19(5):401-405. [ Links ]
25. Hao T, Zhu J, Hu W, et al.: Autogenous platelet-rich plasma gel with acellular xenogeneic dermal matrix for treatment of deep II degree burns. Chinese Journal of Reparative and Reconstructive Surgery 2010; 24(6):647-649. [ Links ]
26. Chen Tm, Tsai JC, Burnouf T.:A novel technique combining platelet gel, skin graft, and fibrin glue for healing recalcitrant lower extremity ulcers. Dermatol Surg. 2010; 36(4):453-460. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Dr. Germán Rossani
Ca. José del Llano Zapata, 245 Miraflores
Lima, Perú
e-mail: grossani@ingecel.com