Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Cirugía Plástica Ibero-Latinoamericana
versão On-line ISSN 1989-2055versão impressa ISSN 0376-7892
Cir. plást. iberolatinoam. vol.42 no.3 Madrid Jul./Set. 2016
QUEMADOS
ORIGINAL / Series Clínicas
Experiencia con Nexobrid® para el desbridamiento enzimático de quemaduras faciales seguido de tratamiento conservador con Medihoney®
Experience with NexoBrid® in enzymatic debridement of facial burns followed by conservative treatment with Medihoney®
José-Manuel Sampietro-De-Luis*; Paloma López-Cabrera*; Álvaro-Jesús Bernal-Martínez*; Valentín Yuste-Benavente** y Alberto Agulló-Domingo***
* Médico Interno Residente.
** Médico Adjunto.
*** Jefe del Servicio.
Servicio de Cirugía Plástica, Hospital Universitario "Miguel Servet", Zaragoza, España.
Conflicto de intereses: los autores declaran no tener ningún interés financiero relacionado con el contenido de este artículo.
Trabajo galardonado con el primer premio en la 2a Convocatoria del Reconocimiento al Tratamiento Quirúrgico y No Quirúrgico del Paciente Quemado, organizada por la Revista Cirugía Plástica Ibero-Latinoamericana bajo el patrocinio de Mediwound® y con los auspicios de la Fundación Docente SECPRE, entregado en el 51o Congreso de la Sociedad Española de Cirugía Plástica, Reparadora y Estética (SECPRE) celebrado en Estoril (Portugal) del 2 al 4 de junio del 2016.
Dirección para correspondencia
RESUMEN
Introducción y Objetivos. El desbridamiento enzimático de las quemaduras ha sido objeto de estudio durante décadas; en este terreno, NexoBrid® (MediWound Ltd., Israel) se postula como una prometedora alternativa al desbridamiento quirúrgico clásico. Por otra parte, las propiedades antibacterianas y promotoras de la cicatrización de la miel también se han evaluado recientemente con buenos resultados clínicos.
Describimos nuestra experiencia preliminar con el empleo de NexoBrid® para el tratamiento de quemaduras faciales, seguido de curas tópicas con Medihoney® Wound Gel (Derma Sciences Ltd., EE.UU.).
Material y Método. Incluimos en el estudio todos los pacientes atendidos en nuestra Unidad de Quemados con quemaduras faciales dérmicas o subdérmicas que afectaban a 2 o más subunidades estéticas. Realizamos desbridamiento enzimático con NexoBrid® en las primeras 24 horas. Posteriormente, llevamos a cabo tratamiento conservador con curas tópicas con Medihoney® Wound Gel. Recogimos todos los datos de calidad del desbridamiento, necesidad de desbridamiento quirúrgico, tiempo hasta epitelización completa, presencia de infección y necesidad de cirugía correctora de secuelas.
Resultados. Tratamos 10 pacientes con quemaduras faciales de etiología diversa (llama, flash eléctrico, deflagración, escaldadura y química). El desbridamiento inicial fue completo en todos los pacientes. Se alcanzó la epitelización completa en una media de 13.88 días (10-20 días). Ningún paciente presentó infección clínicamente manifiesta ni precisó desbridamiento quirúrgico, cobertura mediante autoinjertos o cirugía de secuelas.
Conclusiones. Nuestra experiencia preliminar indica que parece factible la aplicación de NexoBrid® y su combinación con Medihoney® para el tratamiento conservador de las quemaduras faciales.
Palabras clave: Quemaduras, Cara, Facial, Desbridamiento enzimático, Bromelaína, Miel de manuka.
Nivel de evidencia científica: 4 Terapéutico.
ABSTRACT
Background and Objective. Enzymatic debridement of burns has been studied for decades. In this theme, NexoBrid® (MediWound Ltd., Israel) is postulated as a promising alternative to classic surgical debridement of burns. Moreover, the antibacterial and healing properties of honey have been recently evaluated with good clinical results.
This paper describes our preliminary experience with the use of NexoBrid® to treat burns in the facial area, followed by topical application of Medihoney® Wound Gel (Derma Sciences Ltd., USA).
Methods. All patients received in our Burns Unit with dermal or subdermal facial burns affecting 2 or more aesthetic subunits were included in the study. Enzymatic debridement was performed with NexoBrid® in the first 24 hours. Subsequently, conservative management was carried on by topical cures with Medihoney® Wound Gel. Data about quality of debridement, the need for surgical debridement, time to complete epithelialization, presence of infection, and the need for corrective surgery of sequelae were collected.
Results. Ten patients with facial burns of diverse etiology (flame, electric flash, deflagration, scald and chemical) were treated. The initial debridement was complete in all patients. Complete epithelialization was achived on an average of 13.88 days (10-20 days). No patient presented clinically apparent infection, and didn't require surgical debridement, coverage by autografts, nor surgery of sequelae.
Conclusions. Our preliminary results indicate that the application of NexoBrid® and its combination with Medihoney® for the conservative management of facial burns seems feasible.
Key words: Burns, Face, Facial, Enzimatic debridement, Bromelains, Manuka honey.
Level of evidence: 4 Therapeutic.
Introducción
El desbridamiento del tejido cutáneo necrótico en el paciente quemado supone un paso crítico en su tratamiento. A lo largo de la historia se han sucedido diversos cambios de paradigma en cuanto al método para llevar a cabo este procedimiento. Históricamente, esperar el desprendimiento espontáneo de la escara era un método extensamente aceptado. Sin embargo, a mediados del siglo XX se comenzó a hacer énfasis en la importancia del desbridamiento quirúrgico precoz y la cobertura mediante autoinjertos de las áreas de quemadura profunda (1), técnica traumática no exenta de complicaciones, como la pérdida hemática asociada, y que además precisa personal e instalaciones altamente especializados.
De forma paralela, una vez que se había llegado al convencimiento de que la eliminación precoz de la escara mejoraba el pronóstico del paciente quemado, se comenzaron a ensayar diferentes métodos no quirúrgicos que permitiesen la eliminación del tejido desvitalizado. Los principales intentos en este campo se pueden presentar en tres grandes grupos: las enzimas de origen bacteriano, las de origen vegetal y los ácidos (2).
Dentro del primer grupo encontramos sustancias como la proteasa derivada de Bacillus subtilis (Sutilains, Travase®, Boots Pharmaceuticals Inc., EE.UU.) cuya aplicación, si bien pareció prometedora durante el periodo de 1969 a 1975, finalmente no cumplió las expectativas al no ofrecer ventajas respecto al desbridamiento tangencial, presentar un mayor riesgo de infección, y dañar los elementos epiteliales sanos (3). La colagenasa derivada de Clostridium histolyticum (Santyl®, Healthpoint, Ltd., EE.UU.), sobre la que fueron publicados numerosos estudios en las décadas de 1960 y 1970, pero con la que una serie de inconvenientes en su aplicación clínica, así como la inconsistencia del desbridamiento obtenido, determinaron que su uso actual sea meramente anecdótico (2, 4).
El empleo de ácidos (ácido acético, ácido fosfórico, ácido pirúvico) como desbridantes se limitó a diferentes periodos de tiempo a lo largo del siglo XX. La complejidad de su aplicación para conseguir un desbridamiento eficaz y el desarrollo de acidosis sistémica dieron al traste con los intentos por generalizar su uso (5).
Respecto a las enzimas de origen vegetal, destacan las proteasas obtenidas de vegetales de la familia Bromeliaceae que reciben el nombre de Bromelaína. Su fuente principal es el fruto y el tallo de la piña. En la década de 1960, los primeros intentos de uso de Bromelaína a partir de preparaciones liofilizadas aportaron unos resultados poco consistentes (6). Sin embargo, con posterioridad se desarrolló un método de extracción de sustratos activos purificados que constituían una mezcla con alto poder desbridante y que recibió inicialmente el nombre de Debridase® (MediWound Ltd., Israel), más tarde de Debrase® (MediWound Ltd., Israel), y en la actualidad de NexoBrid® (MediWound Ltd., Israel) (7).
NexoBrid® se postula como una prometedora alternativa al desbridamiento quirúrgico clásico de las quemaduras (8). Hasta el momento está descrita en la bibliografía su aplicación en quemaduras de tronco y extremidades; pero no está descrito específicamente cómo se comporta este desbridante enzimático en un territorio anatómico de suma relevancia desde el punto de vista estético y social como es el facial (9).
Por otra parte, las propiedades antibacterianas y promotoras de la cicatrización de la miel, si bien son conocidas desde hace tiempo, se han evaluado recientemente en diversos ensayos clínicos con preparaciones médicas como Medihoney® (Derma Sciences Ltd., EE.UU.), con buenos resultados clínicos (10, 11).
En el presente trabajo describimos la experiencia preliminar de nuestra Unidad de Quemados con el empleo de NexoBrid® como desbridante enzimático en el territorio facial, seguido de curas tópicas con Medihoney® como agente favorecedor de la epitelización.
Material y método
Incluimos en el presente estudio todos los pacientes tratados en la Unidad de Quemados del Hospital Universitario "Miguel Servet" de Zaragoza (España) por presentar quemaduras faciales con zonas de afectación clínica sugerente de profundidad dérmica o mayor, que afectaran a 2 o más subunidades estéticas, durante el periodo comprendido entre septiembre de 2015 y abril de 2016. Quedaron excluidos aquellos pacientes que, cumpliendo los requisitos previos, llevaban más de 24 horas de evolución de las quemaduras en el momento de ser inicialmente atendidos en dicha Unidad.
Tratamos todas las quemaduras faciales mediante el protocolo de quemaduras faciales de nuestro hospital, según el cual, tras la valoración inicial por el equipo de Cirugía Plástica y Quemados, se realiza una cura húmeda con compresas embebidas en suero fisiológico (NaCl 0.9%) hasta la aplicación de NexoBrid® en un plazo máximo de 24 horas.
Para la aplicación del producto en el territorio facial empleamos anestesia general e intubación orotraqueal siempre que sea preciso tratar el área en torno a las vías aéreas y no exista traqueostomía. En caso de ser precisa la intubación orotraqueal, la mantenemos durante el periodo completo desde la aplicación del producto hasta su retirada. En caso de no presentar afectación en torno a la vía aérea, la aplicación se hace bajo anestesia general mientras que la posterior retirada del producto se realiza bajo sedación, siendo suficiente analgesia convencional (Dexketoprofeno, Metamizol y Tramadol) en el periodo intermedio.
Al inicio del procedimiento llevamos a cabo un lavado del área para eliminar esfacelos queratinizados, y delimitamos las zonas a tratar con vaselina. Estas zonas serán todas aquellas con signos de quemadura, salvo que exista alguna zona de afectación exclusivamente de grado I y homogénea, en cuyo caso no empleamos el producto sobre dicha región. Aplicamos también pomada oftálmica Oculos Epitelizante® (Laboratoires THEA, Francia) en ambas superficies corneales, vaselina sobre las hendiduras palpebrales cerradas y colocamos sobre ellas un apósito protector (Fig. 1). De forma simultánea preparamos el gel de NexoBrid® realizando la mezcla del sustrato liofilizado con el gel hasta conseguir un aspecto homogéneo. Extendemos esta mezcla sobre la zona a tratar, en una capa de 1.5 a 3 mm de espesor, que cubrimos después con una lámina transparente estéril durante las 4 horas que dura su aplicación (Fig. 2). Una vez superado el periodo de desbridamiento, retiramos cuidadosamente todos los restos del desbridante mediante arrastre con gasas embebidas en suero fisiológico. Tras retirar completamente el producto, el cirujano Jefe de la Unidad evalúa la eficacia del desbridamiento, y en cada caso si es precisa una nueva aplicación, que se realizaría transcurridas 24 horas.
Tras esta evaluación colocamos nuevamente cura húmeda durante 24 horas, tras la cual iniciamos la cura expositiva con Medihoney® Wound Gel (Derma Sciences Ltd., EE.UU.) que aplicamos cada 3 días hasta que se desprende sin dificultad la costra formada por el gel de cobertura (Fig. 3), lo que indica que se ha completado la epitelización. En caso de que a los 10 días no se hubiera desprendido, retiraríamos quirúrgicamente la costra y continuaríamos, de ser preciso, con el plan de curas. En caso de evolución desfavorable o epitelización retrasada, procederíamos al tratamiento quirúrgico de cobertura. En la realización de cada cura, un cirujano plástico de la Unidad evaluó la evolución de las lesiones atendiendo a la presencia o ausencia de complicaciones (especialmente de signos o síntomas de infección) y a la epitelización de las mismas.
En todos los casos llevamos a cabo la aplicación del tratamiento y la toma de fotografías documentales tras obtener la correspondiente firma del consentimiento informado por parte de los pacientes o de sus familiares/ tutor legal.
Resultados
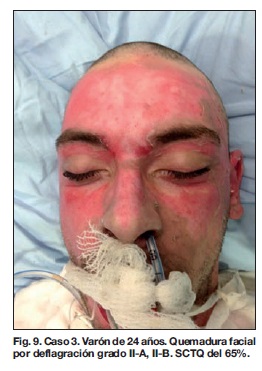
Recogimos 10 casos de quemaduras faciales de mecanismo heterogéneo (Tablas I y II): 5 quemaduras se produjeron por llama; 1 quemadura química por salpicadura de ácido sulfúrico concentrado al 97% (Fig. 4-7); 1 escaldadura por vapor de origen industrial; 1 quemadura por flash eléctrico; y 2 por deflagración de gasolina.
Los pacientes presentaban edades comprendidas entre los 24 y los 85 años (media de 47.3 años). Nueve fueron de sexo masculino y 1 femenino.
La superficie corporal total quemada media fue del 26%, con un intervalo entre el 1.5% y el 80%. Los pacientes presentaron quemaduras de grado II-A y II-B parcheadas, con excepción de 1 paciente que presentó zonas de grado III. La estancia hospitalaria estuvo comprendida entre los 9 y los 150 días (1 paciente falleció a los 5 días de ingreso), con una media de 36.1 días (Tabla II).
En todos los pacientes logramos un desbridamiento efectivo en la primera aplicación del gel desbridante, con aparición de un lecho dérmico sangrante bien vascularizado (Fig. 8) y en todos iniciamos el plan de curas con Medihoney® Wound Gel cada 72 horas.
Conseguimos la epitelización completa en todos los casos en un periodo de entre 10 y 20 días, con una media de 13.88 días (exceptuando 1 paciente que falleció a causa de insuficiencia hepática aguda con coagulopatía severa antes de completar la epitelización).
Ninguno de los pacientes precisó cobertura quirúrgica por retraso de la epitelización. Tampoco detectamos presencia de infección clínicamente manifiesta de las lesiones faciales en ninguno de los casos, y ningún paciente presentó complicaciones oculares derivadas de la aplicación del desbridante enzimático.
El periodo de seguimiento de los pacientes varió entre los 2 y los 8 meses, sin que hasta la fecha haya sido preciso realizar cirugía de secuelas (Fig. 4-17).
Discusión
Las quemaduras faciales son sumamente frecuentes. Según distintas series publicadas suponen entre un 30-50% del total de las quemaduras (12). Habitualmente se trata de quemaduras de segundo grado que epitelizan en un plazo de unos 10-14 días en los casos de espesor medio, y en unos 14-28 días en los casos de mayor profundidad, representando estos últimos en torno a un 15% (12). Son infrecuentes los casos de espesor completo (13). Pese a que se caracterizan por su tendencia a la cicatrización espontánea, con los enfoques clásicos de tratamiento se describe entre un 5-10% de necesidad de desbridamiento e injerto (14). Además, aquellos casos en los que se consigue una cicatrización espontánea más allá de los 21 días o en los que se realiza desbridamiento y cobertura pasados los 14 días de evolución, presentan resultados estéticos y funcionales significativamente inferiores (15).
La cara es un territorio anatómico con particularidades a tener en cuenta. En primer lugar, tiene una función estética y social de importancia capital en la vida de relación de los seres humanos; en general, el resultado estético obtenido mediante injertos cutáneos es mal tolerado por los pacientes. Y además, se trata de un territorio con una magnífica vascularización (16). Es por ello que a la hora de diseñar el protocolo de tratamiento de las quemaduras faciales nos planteamos maximizar las opciones de epitelización espontánea, evitando así la morbilidad y los malos resultados estéticos de la cobertura mediante autoinjertos. Para ello, propusimos la aplicación de Bromelaína como agente desbridante en base a los resultados descritos en la bibliografía y que comentamos a continuación, y a los resultados apreciados en su aplicación sobre otras localizaciones anatómicas en nuestra propia Unidad de Quemados.
Rosenberg y col. publicaron los resultados de la aplicación de Debridase® en 130 pacientes, sumando un total de 332 lesiones térmicas de segundo grado profundo y de tercer grado. Una única aplicación del producto durante un periodo de 4 horas fue suficiente en el 72.6% de las lesiones. En la primera aplicación se obtuvo un desbridamiento medio del 89% de la superficie inicial de la escara. En aquellos pacientes que tras el desbridamiento enzimático presentaron quemaduras de espesor parcial, se realizó cobertura de las mismas bien con aloinjertos, bien con apósitos favorecedores de la epitelización, o simplemente curas tópicas hasta su epitelización, sin precisar intervención quirúrgica para el desbridamiento ni para la cobertura de las lesiones. En aquellos sujetos que presentaron quemaduras de espesor total tras el desbridamiento enzimático, se realizó cobertura mediante autoinjertos sin precisar nuevo desbridamiento tangencial, evitando así mayor sangrado y dolor postoperatorio (17).
En las quemaduras, en torno a la zona de necrosis establecida, encontramos un área de estasis vascular potencialmente salvable (18). Singer y col. demostraron de manera experimental que la aplicación precoz de Debrase® conseguía disminuir el porcentaje de estas zonas de estasis que evolucionan hacia la necrosis de espesor completo. Además, reafirmaron mediante demostración histopatológica la eficacia en el desbridamiento de la Bromelaína purificada y su inocuidad para los tejidos sanos (19).
Estos mismos autores, mediante la aplicación de Debrase® en 40 quemaduras dérmicas de espesor medio en un modelo porcino, obtuvieron el desbridamiento completo de todas ellas. Además, comparándolas con otros 40 controles que no recibieron el desbridante enzimático, apreciaron que se produjo en las quemaduras tratadas una reepitelización significativamente más rápida (7.4 ± 0.8 días en el primer grupo frente a 9.1 ± 2.1 días en el segundo), poniendo de manifiesto por tanto los beneficios de la retirada precoz del tejido desvitalizado (20).
Las quemaduras en las manos son también sumamente frecuentes. Entre un 30-60% de los pacientes quemados presentan afectación de este territorio anatómico (21). Krieger y col. demostraron que la aplicación de Debrase® en las quemaduras profundas de las manos permite disminuir la necesidad de tratamiento quirúrgico. De un total de 69 quemaduras inicialmente clasificadas por su presentación clínica como subsidiarias de desbridamiento quirúrgico y cobertura mediante autoinjertos, comprobaron tras la realización de desbridamiento enzimático, que 44 de ellas (63.8%) presentaban remanente dérmico viable en su lecho y evolucionaron con curas tópicas hasta la epitelización completa. El tiempo medio hasta la epitelización fue de 23 días. Con un enfoque clásico, las quemaduras de este espesor serían tratadas mediante escisión quirúrgica e injerto. La presencia de menores remanentes viables con capacidad para iniciar la reepitelización es la responsable de este tiempo prolongado hasta el cierre de las lesiones. En este estudio, de las 25 quemaduras que precisaron autoinjertos, la superficie total injertada finalmente fue menor que la inicialmente prevista (22).
Un nuevo experimento en modelo porcino demostró histopatológicamente la inocuidad del gel desbridante derivado de la Bromelaína no solo para la piel indemne, como ya había sido demostrado (17), sino también para la dermis expuesta en zonas donantes y en los lechos de toma de biopsias, demostrando su selectividad por el colágeno que ha sufrido daño térmico (23).
Por su parte, un ensayo clínico multicéntrico y aleatorizado sobre 182 pacientes enfrentó un grupo de pacientes tratados con NexoBrid® frente a otro grupo de pacientes sometidos a desbridamiento quirúrgico. Como principales resultados obtuvo una reducción en el tiempo transcurrido desde la lesión hasta el desbridamiento completo (2.2 días frente a 8.7 días), menor necesidad de cirugía (24.5% frente a 70%), una menor área de escisión quirúrgica (13.1% frente a 57.6%) y una menor necesidad de autoinjertos (17.9% frente a 34.1%). La calidad de la cicatriz y la calidad de vida a largo plazo de los pacientes fueron comparables entre ambos grupos (9).
Por lo tanto, tras el análisis de la literatura científica existente podemos concluir que la aplicación de NexoBrid® permite un desbridamiento más selectivo que el desbridamiento tangencial, determinando de forma precisa la profundidad de las quemaduras y maximizando las probabilidades de epitelización a partir de remanentes epidérmicos, disminuyendo así las necesidades de cobertura mediante autoinjertos y la morbilidad que conllevan, hecho que motivó su inclusión en nuestro protocolo para el tratamiento conservador de las quemaduras faciales. No hemos encontrado referencias en la bibliografía sobre la aplicación de la Bromelaína en la cara (9). La serie presentada supone la primera experiencia con NexoBrid® en el área facial en nuestra Unidad.
Por otra parte, sabemos que la miel de manuka presenta propiedades antiinflamatorias y analgésicas y promueve el desbridamiento, la granulación y la epitelización, dando lugar a cicatrices de mejor calidad (10). Un estudio realizado sobre 105 pacientes con heridas que cicatrizaron por segunda intención, aleatorizó a los pacientes para recibir curas tópicas estándar frente a curas con Medihoney® . La mediana de tiempo de curación obtenida en ambos grupos fue de 140 días en el control y 100 en el que recibió miel de manuka (11).
Otro estudio sobre pacientes con úlceras neuropáticas en pie diabético incluyó 63 pacientes aleatorizados para recibir curas con apósitos impregnados en miel de manuka o apósitos convencionales. El tiempo medio hasta la curación fue de 31 ± 4 días en el primer grupo frente a 43 ± 3 días en el segundo (p < 0.05). En el primer grupo, el 78.13% de los casos negativizó sus cultivos durante la primera semana, frente al 35.5% en el segundo (24). En la cara, está descrito que el empleo de Medihoney® en quemaduras de segundo grado superficial aporta un tiempo medio de epitelización de 8.1 días. Ninguno de los pacientes presentó signos de infección ni cultivos patológicos (25).
A la vista de todos estos datos, una vez realizado el desbridamiento enzimático de las quemaduras faciales, estimamos oportuna la aplicación de Medihoney® Wound Gel como agente tópico esperando obtener unos resultados favorables en términos de epitelización y ausencia de infección análogos a los descritos en la literatura. Ésta fue la primera experiencia con la aplicación de este producto en nuestra Unidad de Quemados. Analizando los resultados presentados en nuestra serie de pacientes, podemos objetivar que la aplicación de NexoBrid® en el territorio facial parece comportarse de manera análoga a como lo hace en el resto de la superficie cutánea corporal, consiguiendo un desbridamiento selectivo y completo. Con las adecuadas precauciones, no se produjo en nuestra serie ningún caso de daño ocular, lo que podría suponer a priori una de las principales preocupaciones a tener con la aplicación de este producto en el territorio facial. Además, el desbridamiento enzimático fue eficaz en todos los pacientes de nuestra serie en la primera aplicación del producto, independientemente de la etiología de la quemadura. A esto seguramente contribuyó el hecho de que practicamos la aplicación del desbridante en todos los pacientes dentro de las primeras 24 horas posteriores a la quemadura, siendo este periodo el de mayor eficacia en el desbridamiento. Evitamos así la necesidad de un desbridamiento tangencial quirúrgico, que presenta una selectividad mucho menor y elimina tejido viable con capacidad de reepitelización. Posteriormente, conseguimos la epitelización completa mediante curas sucesivas sin que se presentaran signos de infección en ninguno de los casos recogidos. Logramos la epitelización completa en una media de 13.88 días. Teniendo en cuenta que todos los pacientes presentaban zonas de quemadura dérmica profunda, este resultado parece ser igual o superior al observado con terapias convencionales (14-28 días) (13).
Señalamos también que la aplicación de NexoBrid® está indicada para lesiones térmicas; sin embargo, en nuestra serie incluimos 1 caso de aplicación en una quemadura facial de causa química (caso 2), resultando un desbridamiento eficaz de la misma, con lo que pudo ser manejada de forma conservadora. Hasta donde hemos podido consultar, no hemos encontrado en la bibliografía ningún otro caso similar.
A la vista de los resultados obtenidos en esta serie inicial de pacientes, que parecen indicar una velocidad de epitelización igual o superior al tratamiento habitual en ausencia de complicaciones sin necesidad de cirugía correctora de secuelas, estimamos oportuno proseguir con la aplicación del protocolo descrito en nuestra Unidad de Quemados. El volumen de pacientes que habitualmente trabamos en esta Unidad está en torno a los 100 pacientes al año. En base a estas cifras, creemos que tras esta serie preliminar, y cuando consigamos una casuística suficiente, será necesario realizar un estudio comparativo frente a los casos manejados de forma clásica, teniendo en cuenta también los resultados estéticos y funcionales, así como los costes.
Conclusiones
Los resultados preliminares de la aplicación de nuestro protocolo de tratamiento de quemaduras faciales indican que parece factible la aplicación de NexoBrid® en el territorio facial. Por otra parte, parece también adecuada su combinación con Medihoney® . En nuestra opinión, lo positivo de estos resultados preliminares justifica que se prosiga con su aplicación en nuestra Unidad de Quemados.
Somos conscientes también de que es preciso realizar estudios comparativos con una mayor casuística para demostrar que este enfoque resulta superior a la terapia clásica en el manejo de las quemaduras faciales.
Agradecimiento
A todo el personal que trabaja o colabora en la Unidad de Quemados del Hospital Miguel Servet y en especial a su coordinador, el Dr. Enrique Monclús, por haber hecho posible la realización de este artículo.
Bibliografía
1. Janzekovic Z. A new concept in the early excision and immediate grafting of burns. J Trauma. 1970;10(12):1103-1108. [ Links ]
2. Klasen HJ. A review on the nonoperative removal of necrotic tissue from burn wounds. Burns. 2000;26(3):207-222. [ Links ]
3. Zawacki BE. The effect of Travase on heat-injured skin. Surgery. 1975;77(1):132-136. [ Links ]
4. Hummel RP, Kantz DP, MacMillan BG, Altemeier WA. The continuing problem of sepsis following enzymatic debridement of burns. J Trauma 1974;14:572-579. [ Links ]
5. Gimbel NS, Weissman F, Schirle J, Orten AU. Acid debridement of burned rats and men. Am J Surg. 1960;99:676-678. [ Links ]
6. Klein GK. Enzymatic débridement of third degree burns in animals with bromelains-a preliminary report. J Maine Med Assoc 1964;55:169-171. [ Links ]
7. Houck JC, Chang CM, Klein G. Isolation of an effective debriding agent from the stems of pineapple plants. Int J Tissue React 1983;5:125-134. [ Links ]
8. Cordts T, Horter J, Vogelpohl J, Kremer T, Kneser U, Hernekamp JF. Enzymatic debridement for the treatment of severely burned upper extremities-early single center experiences. BMC Dermatol. 2016;16(1):8-15. [ Links ]
9. Rosenberg L, Krieger Y, Bogdanov-Berezovski A, et al. A novel rapid and selective enzymatic debridement agent for burn wound management: a multi-center RCT. Burns. 2014; 40(3): 466-474. [ Links ]
10. Cooper RA, Molan PC, Krishnamoorthy L, et al. Manuka honey used to heal a recalcitrant surgical wound. Eur J Clin Microbiol Infect Dis. 2001;20(10):758-759. [ Links ]
11. Robson V, Dodd S, Thomas S. Standardized honey (Medihoney) with standard therapy in wound care: randomized clinical trial. J Adv Nurs. 2009;65(3):565-575. [ Links ]
12. Zatriqi V, Arifi H, Zatriqi S, Duci S, Rrecaj S, Martinaj M. Facial Burns-Our Experience. Mat Soc Med. 2013; 25(1): 26-27. [ Links ]
13. Choi M, Panthaki ZJ. Tangential excision of burn wounds. J Craniofac Surg. 2008;19(4):1056-1060. [ Links ]
14. Cole JK, Engrav LH, Heimbach DM, Gibran NS, Costa BA, Nakamura DY, et Al. Early excision and grafting of face and neck burns in patients over 20 years. Plast Reconstr Surg. 2002;109(4):1266-1273. [ Links ]
15. Fraulin FO, Illmayer SJ, Tredget EE. Assessment of cosmetic and functional results of conservative versus surgical management of facial burns. J Burn Care Rehabil. 1996;17(1):19-29. [ Links ]
16. Bichakjian CK, Johnson TM.Anatomy of the skin. Baker SR (ed). Local flaps in facial reconstruction, 2nd ed. London: Elsevier; 2007. pp. 3-13. [ Links ]
17. Rosenberg L, Lapid O, Bogdanov-Berezovsky A, et al. Safety and efficacy of a proteolytic enzyme for enzymatic burn debridement: a preliminary report. Burns. 2004;30(8):843-850. [ Links ]
18. Lewis GM, Heimbach DM, Gibran NS. Evaluation of the burn wound: management decisions. Herndon DN (ed). Total burn care, 4th ed. London: Elsevier; 2012. pp. 125-130. [ Links ]
19. Singer AJ, McClain SA, Taira BR, et al. Rapid and selective enzymatic debridement of porcine comb burns with bromelainderived Debrase: acute-phase preservation of noninjured tissue and zone of stasis. J Burn Care Res. 2010;31(2):304-309. [ Links ]
20. Singer AJ, Taira BR, Anderson R, et al. Reepithelialization of mid-dermal porcine burns after rapid enzymatic debridement with Debrase® . J Burn Care Res. 2011;32(6):647-653. [ Links ]
21. Ryssel H, Germann G, Kloeters O, et al. Dermal substitution with Matriderm® in burns on the dorsum of the hand. Burns. 2010;36(8):1248-1253. [ Links ]
22. Krieger Y, Bogdanov-Berezovsky A, Gurfinkel R, et al. Efficacy of enzymatic debridement of deeply burned hands. Burns. 2012;38(1):108-112. [ Links ]
23. Rosenberg L, Krieger Y, Silberstein E, et al. Selectivity of a bromelain based enzymatic debridement agent: a porcine study. Burns. 2012;38(7):1035-1040. [ Links ]
24. Kamaratos AV, Tzirogiannis KN, Iraklianou SA, Panoutsopoulos GI, Kanellos IE, Melidonis AI. Manuka honey-impregnated dressings in the treatment of neuropathic diabetic foot ulcers. Int Wound J. 2012;9:1-7. [ Links ]
25. Duncan CL, Enlow PT, Szabo MM, Tolchin E, Kelly RW, Castanon L, et al. A Pilot Study of the Efficacy of Active Leptospermum Honey for the Treatment of Partial-Thickness Facial Burns. Adv Skin Wound Care. 2016;29(8):349-355. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Dr. José Manuel Sampietro de Luis
Servicio de Cirugía Plástica
Hospital Universitario Miguel Servet
Po Isabel la Católica 1-3
50009, Zaragoza, España
jmsampi@gmail.com
Recibido (esta versión): 24 abril/2016
Aceptado: 27 mayo/2016