Introducción
Las quemaduras han sido desde siempre causa de morbilidad y mortalidad significativa. A principios de la década de 1940 se demostró que una de las medidas más efectivas para reducir la mortalidad en pacientes quemados es la escisión temprana de la escara,(1) de forma que el desbridamiento precoz se incorporó al tratamiento estándar de las quemaduras. Sin embargo, este tratamiento también incluye la cobertura precoz con autoinjertos cuando es posible. La asociación de desbridamiento y cobertura con autoinjerto ha demostrado disminuir las complicaciones precoces como la infección, y las tardías como la cicatrización patológica, pero no está exenta de complicaciones, siendo la agresividad quirúrgica y la pérdida hemática dos de las principales.(2 3)
El desbridamiento tangencial, que supone la extirpación de capas sucesivas de tejido, tiene una escasa capacidad para resecar de forma selectiva la escara necrótica, como ya han demostrado otros autores,(4) sacrificando dermis viable en muchos casos, o bien siendo insuficiente. Al eliminar tejido viable perdemos parte del potencial para la epitelización espontánea por un lado, así como parte de la dermis sana que podría llevar a un mejor resultado estético.(4)
Se han probado diferentes agentes para desbridar las quemaduras como alternativa a la cirugía; sin embargo, los resultados o bien han sido erráticos o bien su acción ha sido demasiado lenta, por lo que no se han llegado a incorporar al armamento para el tratamiento del paciente quemado agudo.(5) En los últimos años se han publicado resultados que demuestran un desbridamiento eficaz, específico y rápido de los tejidos quemados con el uso de Nexobrid® (Mediwound, Alemania), un producto formado por un concentrado de enzimas proteolíticas enriquecidas con bromelaína.(6,7) Su especificidad ha sido probada tanto en modelos experimentales como en pacientes quemados bajo ensayo clínico controlado y randomizado.(3,6,7) Ha demostrado la capacidad de preservar dermis viable tras el desbridamiento de quemaduras dérmico intermedias y profundas, reduciendo la tasa de quemaduras injertadas y la superficie total injertada, así como la morbilidad de la zona donante, aunque alargando el tiempo de cicatrización debido a que permite la reepitelización espontánea a partir de la dermis viable.(3,4,7,8)
Una de las principales complicaciones del tratamiento de las quemaduras es la colonización y posterior infección del lecho de la herida.(9) Este fenómeno ocurre por la asociación de grandes superficies cruentas con tiempos prolongados hasta la epitelización, sumado esto a la inmunosupresión inherente a la fisiopatología del paciente quemado. Los gérmenes responsables son muy variados, siendo los más frecuentes las enterobacterias y los microorganismos colonizadores de la piel sana del paciente.(10,11) La colonización y la infección constituyen causa de morbilidad y en ocasiones de mortalidad, y entre otras circunstancias alargan la estancia hospitalaria del paciente y aumentan su necesidad de cirugías. Por esta razón, surge el interés por conocer si el desbridamiento enzimático puede suponer un mayor riesgo de colonización de las heridas en los pacientes quemados al prolongar el tiempo de reepitelización de grandes áreas cruentas sobre dermis viable conservada tras el tratamiento, que no hemos encontrado recogido por otros autores en publicaciones previas.(3,7) Este problema cobra especial relevancia en pacientes con superficie corporal quemada (SCQ) mayores del 15%. En ellos, debido a las ventajas en cuanto a reducción del número de cirugías y de pérdida hemática entre otras, se aplica el producto en sesiones sucesivas de 15-20% de superficie en distintas zonas cada vez, para conseguir el desbridamiento de toda la extensión quemada.
En aquellos casos en los que las quemaduras son circulares, se puede producir la contracción de la piel quemada, siendo este hecho especialmente relevante en los miembros; al reducirse el continente sobre el contenido del compartimento del miembro existe riesgo de desarrollar un síndrome compartimental de origen extrínseco. Cuando esto se produce, el protocolo de tratamiento consiste en realizar una escarotomía para reducir la presión intracompartimental y evitar las complicaciones de este cuadro. Además, la escarotomía en sí no está exenta de morbilidad asociada, puesto que supone la apertura de espesor completo de la escara, asociándose en ocasiones retraso en la cicatrización, colonización, y resultados inestéticos de la misma. Se han publicado resultados que demuestran la eficacia de Nexobrid® en la reducción de la presión intracompartimental en el contexto de un síndrome compartimental inducido por quemadura en una serie experimental.(12) Esta circunstancia se explica de forma teórica porque la escarectomía precoz enzimática elimina el factor extrínseco que contribuye a aumentar la presión intacompartimental. Sin embargo no se conoce si la aplicación precoz del desbridamiento enzimático reduce realmente la incidencia de síndrome compartimental en humanos, y tampoco se ha evaluado la eficacia en el tratamiento del cuadro compartimental establecido.
Por último, el desbridamiento tangencial está asociado a pérdida hemática importante, tanto durante la intervención como en el postoperatorio del paciente. Para algunos autores, como Herndon, se pierde 1 ml por cada cm2 desbridado.(13) Existen otros factores relacionados con la pérdida hemática propios del paciente como la edad, el sexo y la SCQ, así como factores relacionados con el tratamiento como la precocidad del mismo, el uso de vasoconstrictores, procoagulantes tópicos, isquemia, etc. Algunos autores han mostrado que el uso del desbridamiento enzimático reduce significativamente la pérdida hemática respecto al tratamiento estándar medida como un menor descenso en los niveles de hemoglobina antes y después del desbridamiento enzimático.(3,6) Sin embargo, no analizan si el beneficio de este ahorro hemático es el mismo en función de la superficie corporal desbridada, puesto que actualmente la indicación de uso de este tratamiento se limita a adultos y además con una SCQ <15%. Se desconoce si estos beneficios expuestos en la literatura se mantienen en pacientes con quemaduras más extensas, en los que se realizan aplicaciones sucesivas del desbridante enzimático para alcanzar el desbridamiento completo de las quemaduras.
En este estudio hemos comparado el uso de Nexobrid® como desbridante enzimàtico frente a un Grupo Control con tratamiento estándar con el objetivo de evaluar la cantidad de intervenciones quirúrgicas, la colonización del lecho quirúrgico, la realización de escarotomías, así como los requerimientos transfusionales de los pacientes quemados tratados, en función de su SCQ.
Material y método
Llevamos a cabo un estudio de cohortes retrospectivo que incluye todos aquellos pacientes cuyo mecanismo lesional sea llama, escaldadura o contacto, tratados inicialmente con Nexobrid® en la Unidad de Quemados de nuestro centro (Unidad de Quemados del Hospital Universitario La Paz, Madrid, España) entre septiembre de 2015 y diciembre de 2016. Comparamos esta muestra con un Grupo Control formado por los pacientes intervenidos en la Unidad mediante desbridamiento tangencial y cobertura con injerto desde enero a diciembre de 2014, etapa en la que aún no existía aprobación para el uso de Nexobrid® en nuestro hospital. Ambos grupos presentan unas características demográficas, clínicas, índices de comorbilidad y gravedad homogéneas.
Estratificamos los grupos en función de su SCQ mayor o menor del 15%. Escogimos como punto de corte una SCQ del 15% debido a que la aplicación del producto Nexobrid® en superficies >15% se encuentra fuera de ficha técnica. La aplicación en pacientes mayores de 15% se realizó en tratamiento sucesivos, tratando 15-20% de la superficie cada vez que se aplicaba Nexobrid®, y nunca repitiendo sobre la misma zona tratada previamente para así realizar el desbridamiento de toda la extensión quemada.
El estudio fue aprobado por el Comité de Ética de Investigación Clínica de nuestro hospital. Todos los pacientes firmaron el consentimiento informado antes de cada intervención.
El protocolo de aplicación de Nexobrid® empleado se basa en la modificación del publicado por Rosenberg,(3) alargando el tiempo de cura húmeda pre y post-desbridamiento, siendo ambos superiores a las 8 horas. La cobertura tras las primeras 24 horas se realizó mediante hidrocoloides, apósitos biosintéticos o injertos en función de la profundidad del lecho quirúrgico.
El grupo control fue tratado mediante desbridamiento tangencial y cobertura con apósitos biosintéticos y/o injertos de acuerdo a su profundidad, y basándonos en los protocolos estándar de tratamiento del paciente quemado.
Recogimos los datos mediante revisión retrospectiva de las historias clínicas de nuestro hospital. Registramoslas variables demográficas de los pacientes como edad, sexo e índices de comorbilidad; las fechas de ingreso, cirugías y alta; las variables relacionadas con la quemadura: SCQ, mecanismo de lesión, profundidad, índices de gravedad (ABSI, BAUX revisado). Incluimos las variables relacionadas con la evolución del paciente: cantidad de cirugías (solo intervenciones en quirófano para desbridamiento o para cobertura), días desde la quemadura a la primera cirugía, días desde el ingreso a la primera cirugía, duración del ingreso, necesidad transfusional, y colonización y sepsis durante la estancia. La definición de sepsis en nuestro estudio se basó en los criterios publicados por la American Burn Association. Evaluamos la colonización de la quemadura mediante cultivo de una muestra de superficie obtenida de manera estéril a través de una torunda, repitiéndo semanalmente durante el ingreso.
Análisis estadístico
Procesamos los datos informáticamente mediante una base de datos en formato Microsoft® Excel, que más tarde fue importada para su tratamiento estadístico en el programa SPSS versión 20.0 (IBM SPSS Statistics®). Consideramos diferencias estadísticamente significativas aquellas que presentan una probabilidad de error menor del 5% (p <0.05).
Para la descripción de variables cuantitativas continuas utilizamos la media junto con la desviación estándar. Describimos las variables cualitativas mediante frecuencias absolutas y frecuencias relativas expresadas en porcentaje.
Realizamos las comparaciones entre variables cuantitativas continuas principalmente mediante pruebas no paramétricas, utilizando la U de Mann-Whitney. El análisis de frecuencias entre variables cualitativas, lo llevamos a cabo mediante la prueba de la χ2 o el test exacto de Fisher (si n <20, o si algún valor en la tabla de valores esperados era menor de 5).
RESULTADOS
El estudio incluyó un total de 242 pacientes, 159 hombres y 83 mujeres, con una media de edad de 47.87 años (mínimo 14 y máximo 92 años), con una desviación estándar (DS) 18.77. El mecanismo más frecuente de quemadura fue la llama que se produjo en 146 pacientes (60.5%), seguido por la escaldadura en 68 pacientes (28%) y por contacto en 28 pacientes (11.5%) (Gráfico 1). El 79.8% de la población presentó una puntuación de ABSI entre 3 y 6.

Gráfico 1 Representación de la frecuencia de los mecanismos de producción de las quemaduras en los pacientes del grupo de estudio
El Grupo Control está formado por 177 pacientes, siendo 112 hombres y 65 mujeres. De esta población, 7 pacientes presentaron quemaduras dérmico superficiales, 141 quemaduras de segundo grado dérmico profundas, y 29 de tercer grado (subdérmicas). La SCQ media en el grupo control fue de 8.46% (1% 84%; DS 13.86%). En cuanto a la estratificación en función de la SCQ, 156 pacientes presentaron quemaduras <15% y 21 pacientes >15%.
El Grupo Nexobrid® lo formaron 65 pacientes, de los cuales 47 fueron hombres y 18 mujeres. Incluyó 3 pacientes con quemaduras dérmico superficiales, 50 con quemaduras de segundo grado dérmico profundas, y 12 con quemaduras subdérmicas. La SCQ media en el grupo tratado con Nexobrid® fue de 10.65% (1% 51%; DS 11.14%). En este grupo 49 pacientes presentaron SCQ <15% y 16 quemaduras con SCQ >15%.
La media del Índice de BAUX revisado en el Grupo Control fue de 58.34 (16 - 145; DS 24.16), siendo de 58.04 (18 - 142; DS 27.23) en el Grupo Nexobrid®. No encontramos diferencias estadísticamente significativas entre ambos grupos (p >0.05). Además analizamos el Índice de Comorbilidad de Charlson, presentando una media de 0.69 (0 - 8; DS 1,33) en el Grupo Control y de 1.09 (0 - 8; DS 1.86) en el Grupo Nexobrid®, sin encontrar diferencias estadísticamente significativas entre ambos grupos (p >0.05). Presentamos las características generales de ambos grupos en la Tabla 1.
Tabla I Características generales de los grupos de estudio
| Grupo Control | Grupo Nexobrid® | |
|---|---|---|
| Edad (años) | 48.24 ± 19.92 | 46.87 ± 21.07 |
| Sexo | 112 Hombres / 65 Mujeres | 47 Hombres / 18 Mujeres |
| SCQ (%) | 8.46 ± 13.86 | 10.65 ± 11.14 |
| Índice ABSI | 4.99 ± 1.94 | 4.90 ± 1.98 |
| Índice BAUX revisado | 58.34 ± 24.16 | 58.04 ± 27.23 |
| Índice de comorbilidad de Charlson | 0.69 ± 1.33 | 1.09 ± 1.86 |
Datos expresados como media ± desviación estándar
Al estratificar ambos grupos en función de la SCQ obtuvimos una población de 205 pacientes con SCQ <15%, procedentes 156 del Grupo Control y 49 del Grupo Nexobrid®; y de 37 pacientes con SCQ >15%, procedentes 21 del Grupo Control y 16 del Grupo Nexobrid®. En la Tabla II resumimos los datos del análisis por subgrupos estratificados en función de la SCQ mayor o menor del 15%.
Tabla II Datos demográficos y clínicos de los pacientes en los grupos de estudio
| SCQ < 15% | SCQ ≥ 15% | |||
|---|---|---|---|---|
| Grupo Control | Grupo Nexobrid® | Grupo Control | Grupo Nexobrid® | |
| N° pacientes | 156 | 49 | 21 | 16 |
| Edad | 48.04 ± 18.65 | 44.30 ± 20.55 | 49.71 ± 11.38 | 54.75 ± 21.33 |
| SCQ % | 4.23 ±3.22 | 5.37 ± 3.58 | 39.95 ± 20.73 | 26.81 ± 10.94 |
| Índice BAUX revisado | 53.58 ± 19.59 | 49.68 ± 20.73 | 93.71± 25.92 | 83.68 ± 29.29 |
| Índice de Comorbilidad de Charlson | 0.69 ± 1.32 | 0.93 ± 1.65 | 0.68 ± 1.45 | 1.56 ± 2.39 |
| Cantidad de cirugías | 0.97 ± 0.54 | 0.30 ± 0.61 | 3.40 ± 2.52 | 2.00 ± 1.79 |
| Días desde la quemadura a 1a cirugía | 5.38 ± 5.22 | 1.32 ± 1.29 | 4.76 ± 3.96 | 0.93 ± 1.38 |
| Días ingreso a 1a cirugía | 3.32 ± 2.71 | 1.18 ± 1.03 | 4.33 ± 3.16 | 0.81 ± 1.37 |
| N° pacientes con quemadura circular en miembros | 8 | 5 | 12 | 8 |
| N° de pacientes con escarotomías | 1 | 1 | 10 | 0 |
| N° pacientes colonizados | 2 | 1 | 6 | 3 |
| N° pacientes con sepsis | 2 | 0 | 10 | 2 |
| N° de concentrados de hematíes | 0.29 ± 1.57 | 0.06 ± 0.31 | 23.23 ± 26.33 | 6.50 ± 10.96 |
| N° de pacientes que recibieron transfusiones | 8 | 2 | 17 | 8 |
| Días de ingreso | 10.56 ± 8.85 | 10.16 ± 8.42 | 41.00 ± 28.44 | 33.25 ± 16.20 |
Expresado como media ± desviación estándar
No encontramos diferencias estadísticamente significativas entre los grupos (p >0.05) para los índices de gravedad ni de comorbilidad.
La media de días transcurridos desde la quemadura hasta la primera cirugía en SCQ <15% para el Grupo Control fue de 5.38 (0 - 30; DS 5,22) mientras que en el Grupo Nexobrid® fue de 1.32 (0 - 6; DS 1.29). Obtuvimos diferencias estadísticamente significativas (p <0.01), presentando el Grupo Nexobrid® menos días hasta el primer desbridamiento. En el caso de la población con SCQ >15% la media de días transcurridos fue de 4.76 (0 - 16; DS 3.96) en el Grupo Control y 0.93 (0 - 5; DS 1.38) en el Grupo Nexobrid®. Otuvimos también diferencias estadísticamente significativas (p <0.01), con un menor número de días en el Grupo Nexobrid®.
Señalar también que no todos los pacientes acudieron a nuestro hospital tras sufrir la quemadura; en ocasionesdifirieron la consulta o bien fueron evaluados en otros centros. Por esta razón evaluamos el tiempo desde el ingreso hospitalario en nuestro centro hasta el primer tratamiento quirúrgico. En la población con SCQ <15% la media para el Grupo Control fue de 3.32 (0 - 11 ; DS 2.71) y en el Grupo Nexobrid® 1.18 (0 - 5; DS 1.03). Realizamos análisis estadístico y obtuvimos diferencias estadísticamente significativas, con menor días de ingreso hasta la primera cirugía en el Grupo Nexobrid® (p <0.01). Para la población con SCQ >15% la media para el Grupo Control fue de 4.33 (0 - 13; DS 3.16) y en el Grupo Nexobrid® 0.81 (0 - 5; DS 1.37). En el análisis estadístico observamos diferencias estadísticamente significativas, con menos días de ingreso hasta la primera cirugía en el Grupo Nexobrid® (p <0.01). No hubo diferencias significativas en cuanto a los días de estancia hospitalaria (desde el ingreso hasta el alta a domicilio) en los diferentes grupos.
En cuanto a la cantidad de cirugías, la media de intervenciones en los pacientes con SCQ <15% fue de 0.97 (0 - 3; DS 0.54) en el caso del Grupo Control y de 0.30 (0 - 2; DS 0.61) en el Grupo Nexobrid®. En el caso del grupo SCQ >15% la media de intervenciones fue de 3.40 (1 - 9; DS 2.52) en los controles y de 2.00 (0 - 8; DS 1.79) en el grupo Nexobrid®. Llevamos a cabo el análisis estadístico correspondiente y obtuvimos diferencias estadísticamente significativas para el grupo menor del 15% con p <0.05, no alcanzando significación en el grupo de más del 15% de SCQ, aunque existió una tendencia a un menor número de cirugías en el grupo experimental (Gráficos 2 y 3).

Gráfico 2 Representación de la distribución de la cantidad de cirugías en los grupos Nexobrid® y Control para SCQ <15%

Gráfico 3 Representación de la distribución de la cantidad de cirugías en los grupos Nexobrid® y Control para SCQ >15%
Al analizar la colonización obtuvimos cultivos positivos en un total de 12 pacientes. En la población con SCQ <15%, 2 pacientes tuvieron cultivos positivos en el Grupo Control, mientras que 1 paciente tuvo cultivos positivos en el Grupo Nexobrid®. Para la población con SCQ >15% hubo 6 pacientes con cultivos positivos en el grupo Control y 3 en el grupo Nexobrid®. No encontramos diferencias estadísticamente significativas al comparar ambos grupos (p >0.05).
Las escarotomías se llevaron a cabo en 11 pacientes del Grupo Control, siendo 1 de ellos del subgrupo SCQ <15% y 10 del subgrupo SCQ >15%. En el Grupo Nexobrid® hubo 1 único caso que pertenecía al subgrupo de SCQ <15%. Dentro del estrato de pacientes >15% SCQ, al revisar las características de las quemaduras encontramos que 11 pacientes del grupo control presentaban quemaduras dérmico profundas o subdérmicas circulares en miembros (superior o inferior), y por tanto con riesgo de precisar escarotomias; frente a 8 en el grupo Nexobrid®. Encontramos diferencias estadísticamente significativas al comparar ambos subgrupos de SCQ >15% para Nexobrid® y Control (p <0.05). No observamos diferencias estadísticamente significativas entre las poblaciones con SCQ <15% (Gráfico 4).
Las transfusiones que requirieron los pacientes se cuantificaron como el número de bolsas de concentrados de hematíes que recibió cada uno (260 cc/concentrado). Para la población con SCQ <15% recibieron transfusión 10 pacientes, 8 de ellos pertenecientes al Grupo Control y 2 al Grupo Nexobrid®. En la población SCQ >15% recibieron concentrados 25 pacientes, 17 del Grupo Control y 8 del Grupo Nexobrid®. En el grupo de pacientes con SCQ <15% se transfundieron una media de 0.29 concentrados (0 - 14; DS 1.57) en los controles y 0.06 (0 - 2; DS 0.31) en el Grupo Nexobrid®. En el caso de los pacientes con >15% la media de concentrados que recibió el Grupo Control fue de 23.23 (0 - 79; DS 26.33) y 6.50 (0 - 36; DS 10.96) en el Grupo Nexobrid® (Gráficos 5 y 6). En el análisis estadístico encontramos diferencias estadísticamente significativas (p <0.05) para el grupo con SCQ >15%, requiriendo menor cantidad de transfusiones el Grupo Nexobrid®. No hubo diferencias estadísticamente significativas en la población con SCQ <15%.

Gráfico 5 Representación de la distribución de los requerimientos transfusionales en los grupos Nexobrid® y Control para SCQ <15%.
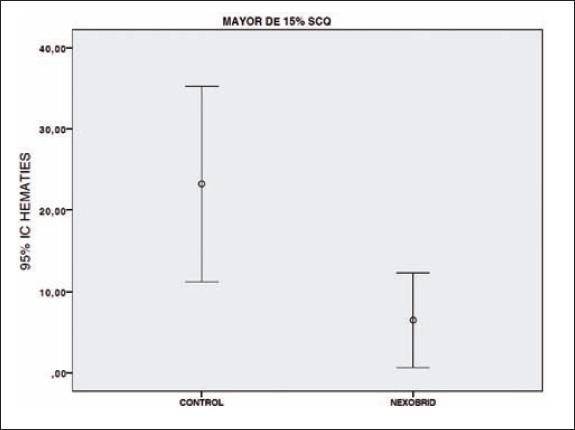
Gráfico 6 Representación de la distribución de los requerimientos transfusionales en los grupos Nexobrid® y Control para SCQ >15%
Analizamos el número de pacientes que desarrollaron sepsis durante el ingreso. El diagnóstico de sepsis se realizó de acuerdo a los criterios de la American Burn Association. En los subgrupos SCQ <15%, 2 pacientes desarrollaron sepsis en el Grupo Control y ninguno en el Grupo Nexobrid®. Para los subgrupos de SCQ% >15% hubo 10 pacientes con sepsis en el Grupo Control y 2 en el Grupo Nexobrid®. En el análisis estadístico obtuvimos diferencias estadísticamente significativas sólo para la población con SCQ >15% (p <0.05).
Discusión
En este estudio hemos comparado el uso de Nexobrid® como desbridante enzimático en pacientes quemados frente a un Grupo Control con tratamiento estándar con el objetivo de evaluar diferencias en la cantidad de intervenciones quirúrgicas realizadas, la colonización del lecho quirúrgico, la necesidad de escarotomías, así como los requerimientos transfusionales de estos pacientes. Para ello, estratificamos cada grupo en función de si la SCQ era mayor o menor del 15%, puesto que los pacientes de estos estratos son completamente diferentes desde el punto de vista clínico.
Encontramos diferencias estadísticamente significativas en algunas de las variables, como en cantidad de cirugías (en <15% con p <0.01), necesidad de escarotomías (en >15% con p <0.05) y necesidad de reemplazo sanguíneo (en >15% con p <0.05), sin embargo no fue así en la colonización de las heridas.
El tratamiento quirúrgico de las quemaduras ha ido evolucionando en las últimas décadas. Actualmente el tratamiento estándar incluye el desbridamiento precoz de las mismas, entendiendo este como el realizado en las primeras 48-72 horas tras la lesión,(15) e iniciar la cobertura estable mediante autoinjertos. Este protocolo ha demostrado eficacia en la reducción de infecciones del paciente, estancia media, mortalidad y menor tasa de cicatrización hipertrófica. Sin embargo, la cirugía no siempre es posible, bien por la inestabilidad clínica del paciente o bien por dificultades organizativas en los centros hospitalarios. El empleo del desbridamiento enzimático ha demostrado ser eficaz, rápido y selectivo.(3,6,7) Ha permitido eliminar la escara creada por desnaturalización térmica del colágeno en 4 horas, pudiendo ser aplicado en los primeros días de ingreso.
Al analizar los días desde la quemadura hasta la primera cirugía y desde el ingreso a primera cirugía en los pacientes de nuestro estudio, hemos obtenido diferencias estadísticamente significativas para ambas variables independientemente de la SCQ, de manera que transcurren menos días desde la lesión y el ingreso hasta la primera cirugía en el Grupo Nexobrid®. Este hallazgo ya lo presentó Rosenberg en uno de sus trabajos(6) y podría explicarse por el hecho de que en muchos pacientes no es necesario utilizar el quirófano para el empleo de Nexobrid® dado que la anestesia regional o sedoanalgesia se realiza en la cama de la Unidad de Quemados, donde el paciente permanece monitorizado hasta que se completa el desbridamiento. Esto facilita la aplicación de forma más temprana que en el tratamiento estándar, que necesita quirófano.
El desbridamiento tangencial precisa de cobertura precoz con injertos o apósitos para facilitar la epitelización del lecho. Este tratamiento estratificado requiere diferentes tiempos quirúrgicos para poder alcanzar la cobertura completa. El empleo de Nexobrid® ha demostrado eficacia en la conservación de dermis sana al retirar sólo la parte desnaturalizada por calor. La precisión en el desbridamiento ha permitido la conservación de tejido viable y también de su potencial de reepitelización en el lecho quirúrgico, reduciendo la cantidad de pacientes que precisan injerto de piel parcial, así como de la superficie total injertada respecto a la prevista.(3) Este hecho podría tener como resultado una menor necesidad de tiempos quirúrgicos para la cobertura.(14) Si analizamos nuestros pacientes encontramos que el grupo Nexobrid® presenta menor cantidad de cirugías durante su ingreso. Las diferencias son estadísticamente significativas en los pacientes de menos de un 15% de SCQ, donde al conservar dermis sana y ser pacientes con gran estabilidad clínica, se produce la epitelización sin necesidad de injertarlos, no necesitando pasar por quirófano. De hecho en este grupo poblacional se redujo un 69% la cantidad de cirugías (p <0.05). Sin embargo, cuando evaluamos el grupo con más de un 15% de SCQ, estas diferencias no son estadísticamente significativas; aunque observamos la misma tendencia de sus medias (3.40 ± 2,52 frente a 2.00 ± 1.79; p >0.05). Este resultado se explica porque los grandes quemados presentan mayores superficies por epitelizar, en situaciones de inestabilidad clínica, y con necesidad en muchas ocasiones de drogas vasoactivas. Todos estos factores influyen en la capacidad de epitelización de manera que se aumentan los tiempos para alcanzarla, siendo necesarios más procedimientos quirúrgicos para la cobertura, y equilibrando así las diferencias con el Grupo Control.
El tiempo hasta epitelización completa en los pacientes tratados con Nexobrid® ha mostrado ser más largo en los estudios publicados hasta la fecha debido a que se produce una epitelización espontánea a expensas de la dermis viable tras la aplicación del desbridante(3, 7) y no mediante el uso de injertos autólogos como es el tratamiento estandar.. Este aumento en el período de epitelización podría estar relacionada con un aumento en las tasas de colonización de las heridas, como se había observado con otros desbridantes.(5) De hecho, en 2003 Barret y Herdon(15) demostraron que el desbridamiento tangencial precoz es eficaz en la reducción de la colonización. Sin embargo no se ha publicado que el desbridamiento con Nexobrid® aumente la tasa de infección local.(3, 7) En nuestro estudio no hemos observado mayor tasa de colonización en el grupo Nexobrid®, sin diferencias estadísticas entre los grupos. No obstante, si evaluamos la tasa de sepsis encontramos una diferencia estadísticamente significativa en el grupo control de más del 15% de SCQ. Este aumento de incidencia en el grupo control lo atribuimos a un mayor número de cirugías y a la mayor necesidad de transfusión hemática, sugiriendo una evolución clínica más tórpida.
Durante los primeros días de ingreso las quemaduras profundas pueden sufrir una contracción de la escara, generando una discrepancia entre continente y contenido y aumentando así la presión de los compartimentos. Estacircunstancia es de especial importancia en los casos de quemaduras circulares en los miembros. Cuando existe sospecha o se instaura el aumento de la presión intracompartimental el protocolo incluye la escarotomía como tratamiento, que implica a su vez la apertura de la escara de espesor completo. Este procedimiento, aunque es de primera elección y se realiza para evitar las complicaciones devastadoras del síndrome compartimental, no está exento de morbilidad asociada, como el retraso en la cicatrización, la colonización e infección, la pérdida de injertos y la formación de cicatrices hipertróficas.
El uso de Nexobrid® se ha demostrado eficaz en animales de experimentación en la reducción de la presión compartimental ,(12) aunque no se ha publicado su eficacia en humanos. En nuestro grupo poblacional encontramos de forma observacional que la necesidad de escarotomía es menor en el grupo Nexobrid® frente al grupo control. La población de riesgo por quemadura circular dérmico profunda-subdérmica en miembro superior o inferior en el grupo control fue de 12 sobre 21 pacientes, y en el grupo Nexobrid® de 8 sobre 16. Estas diferencias sólo fueron significativas en el grupo de quemados de más del 15% de SCQ, donde la incidencia de quemaduras circulares en miembros es alta. En quemados de menor superficie la incidencia de escaras circulares es baja, y el requerimiento de líquidos en la resucitación también lo es, disminuyendo por tanto el riesgo de precisar una escarotomía. De hecho en nuestra muestra sólo se realizó 1 escarotomía en pacientes <15% de SCQ. Creemos por los resultados obtenidos que la escarectomía enzimática precoz podría evitar la contracción secundaria de la escara y por tanto el desarrollo de síndrome compartimental, aumentando el beneficio clínico del uso temprano de Nexobrid®. Sin embargo habría que diseñar un estudio prospectivo para evaluar la eficacia de Nexobrid® en la prevención del desarrollo de escarotomías, y así confirmar nuestros datos observacionales.
Diferentes estudios han demostrado el mayor sangrado de esta técnica, siendo para algunos autores la pérdida sanguínea de hasta 1 ml por cada cm2 desbridado.(13) A pesar de los esfuerzos técnicos para disminuir el sangrado, sigue siendo una de las principales complicaciones en el intra y postoperatorio inmediato de los pacientes. El uso de Nexobrid® ha demostrado disminuir la tasa de sangrado de los pacientes.(3,6,7) evaluado mediante la medición de la hemoglobina pre y postoperatoria; sin embargo no se valoraba en función de la superficie corporal desbridada. Si analizamos nuestros resultados observamos como la necesidad de transfusión es mayor en el Grupo Control, pero las diferencias no son estadísticamente significativas en los pacientes con menos de un 15% de SCQ. Esto se debe a que en estos pacientes el sangrado es más fácilmente controlable mediante técnicas convencionales como el uso de adrenalina tópica, infiltrada, trombina e isquemia. Cuando analizamos los pacientes con más de un 15% de SCQ observamos que la diferencia de la media de transfusión entre ambos grupos es estadísticamente significativa (23.23 ± 26.33 frente a 6.50 ± 10.96; p <0.05). En este tipo de pacientes el sangrado es mucho más importante durante los desbridamientos, por lo que el uso de Nexobrid® facilita el ahorro de un 73% de concentrados de hematíes.
Conclusiones
El empleo de Nexobrid® como técnica de desbridamiento posibilita, en nuestro medio, reducir el número de cirugías que requieren los pacientes quemados y acortar el tiempo transcurrido desde la quemadura o ingreso hasta el primer desbridamiento, tanto en grandes quemados como en pacientes con menos del 15% de SCQ.
Permite también llevar a más pacientes a epitelización espontánea prolongando el tiempo de curación; sin embargo en nuestra muestra no aumenta la tasa de colonización secundaria de las heridas, ni en grandes quemados ni en quemados por debajo del 15% de SCQ.
El desbridamiento enzimático precoz disminuye la necesidad de escarotomías en la población con quemaduras de riesgo (quemaduras circulares profundas en miembros). Finalmente permite reducir la pérdida hemática en los pacientes quemados, disminuyendo la tasa de transfusión y la cantidad de sangre transfundida en los grandes quemados.
















