Introducción
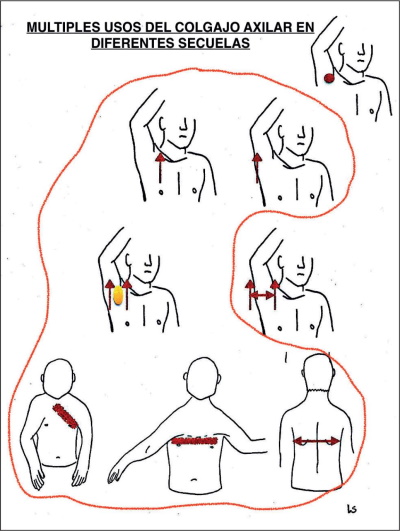
El colgajo de perforante axilar (CPA), descrito por Hyakusoku y col., es de gran utilidad en la mayoría de las contracturas cicatriciales de tórax y miembro superior que se producen en pacientes quemados, ya sean adultos o niños.(1)
Haciendo una reseña de la irrigación del tegumento axilar, sabemos que se basa principalmente en su arteria homónima. Si consideramos la realización de colgajos, vemos que las regiones anterior y lateral del hombro son las más útiles, no así la región posterior que se utiliza menos por presentar vasos poco accesibles. Las ramas más comunes en la elevación y realización de colgajos locales en esta zona incluyen las arterias: toracoacromial, torácica lateral y toracodorsal. A nivel posterior predomina la arteria circunfleja escapular. La arteria toracodorsal es la más versátil en lo que respecta al grupo; descrita por numerosos autores, entre ellos Angrigiani, Heitmann y col. describen 64 perforantes musculocutáneas de más de 0.5 mm. La arteria torácica lateral es la más anterior y yace en la superficie del serrato anterior, en el borde lateral de la fosa axilar, dando colaterales de menor calibre a la piel de dicha región.(2) La arteria toracoacromial está disponible para defectos más anteriores y laterales. Su calibre es generalmente similar a las anteriores y se acompaña de sus venas concomitantes; se accede a ella fácilmente al separar y rebatir el pectoral mayor. La longitud del pedículo y la posibilidad de reorientarlo son los aspectos más limitados debido a su recorrido cercano a la clavícula y su curso entre ambos pectorales, lo que la hacen moderadamente útil.
El presente trabajo se basa en el estudio de la anatomía vascular axilar (AVA) a fin de determinar la procedencia de la irrigación de la pastilla de piel correspondiente al colgajo de axila. El objetivo es demostrar el origen preciso de los vasos perforantes axilares para facilitar la disección y elevación del CPA, que utiliza la piel del hueco axilar en cirugía reparadora en pacientes con secuelas graves en tórax y miembro superior.
Material y metodo
Estudio transversal descriptivo que abarca el estudio anatómico de los vasos perforantes que nutren el tegumento axilar en base a 4 puntos fundamentales: 1) revisión bibliográfica de la técnica quirúrgica; 2) disección en cadáver; 3) mapeo de perforantes con sistema doppler en pacientes vivos no intervenidos; y 4) disección de colgajos en pacientes intervenidos por cicatrices retráctiles.1.- Revisión bibliográfica.
Realizamos búsqueda científica en PubMed basada en los términos: cicatriz de tórax, quemadura de tórax, colgajo perforante, irrigación de axila, colgajo en hélice, localizando aproximadamente 1.500 artículos relacionados con la terminología de los que seleccionamos aquellos que consideraban únicamente abordajes quirúrgicos y técnicas reparadoras mediante colgajos de perforantes de axila. Centramos nuestra atención en los artículos de los autores mencionados anteriormente, quienes detallan la técnica del colgajo de perforante axilar, así como el consenso de Tokyo de 2011. La bibliografía anatómica consultada se dirigió a los autores clásicos: Testut, Rouviere, Netter, entre otros, todos con sus descripciones arteriales anatómicas típicas de origen y ramas colaterales. Fu Chan Wei, Taylor, Koshima y Angrigiani, entre otros, describen la anatomía del árbol arterial en detalle con aplicación quirúrgica y numerosas aplicaciones de colgajos locorregionales, como el colgajo de perforante toracodorsal (TDap) en cirugía reparadora.(4,5) Además nos basamos en los principios descritos por Saint Cyr y su concepto de angiosoma-perforasoma (Fig. 1-3).
2. Disección en cadáver.
Realizamos 6 disecciones axilares en 3 cadáveres humanos formolizados al 40% pertenecientes a la Cátedra A de Anatomía de la Facultad de Ciencias Médicas de la Universidad Nacional de La Plata (Buenos Aires, Argentina). Los especimenes fueron 2 masculinos y 1 femenino, a los cuales se les realizó inyección previa de látex por vía arterial para la correcta identificación del árbol arterial.
Los criterios de exclusión abarcaron preparados cadavéricos de menos de 10 años de edad, cadáveres con deterioro del miembro superior y cicatrices en dicha región. Los criterios de inclusión abarcaron: preparados adultos con axila indemne, independientemente de su sexo, y contemplamos las colaterales arteriales y venosas de 1-1.5 mm de diámetro.
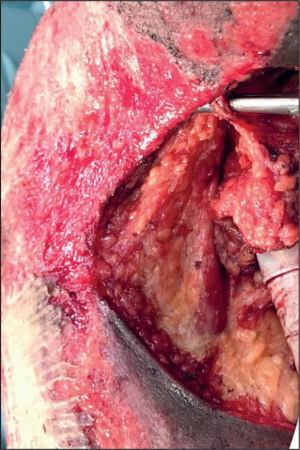
Para la inyección empleamos catéter rígido calibre 14G por vía arterial radial, con látex teñido color rojo. Realizamos la disección axilar bajo campo de aumento 2.5 X con lupas tipo Galileanas, de manera topográfica, identificando vasos perforantes (Fig. 4).
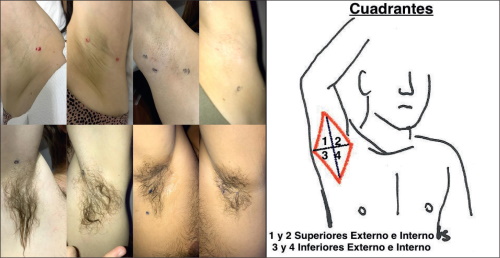
Basamos los límites a considerar en la disección en reparos musculares regionales evaluando la axila en decúbito dorsal y miembro superior elevado a un lado de la cabeza, en abducción y con el codo flexionado. Fueron súpero-interno: músculo deltoides hacia proximal y músculo bíceps (porción larga) hacia distal; súpero-externo: músculo tríceps (porción vasto interno); ínfero-externo: músculo dorsal ancho; e ínfero-interno: músculo pectoral mayor (Fig. 5). Posteriormente utilizamos dichos en la identificación vascular en pacientes sanos y también en la realización de los colgajos de los pacientes intervenidos quirúrgicamente (Fig. 6 A y B).
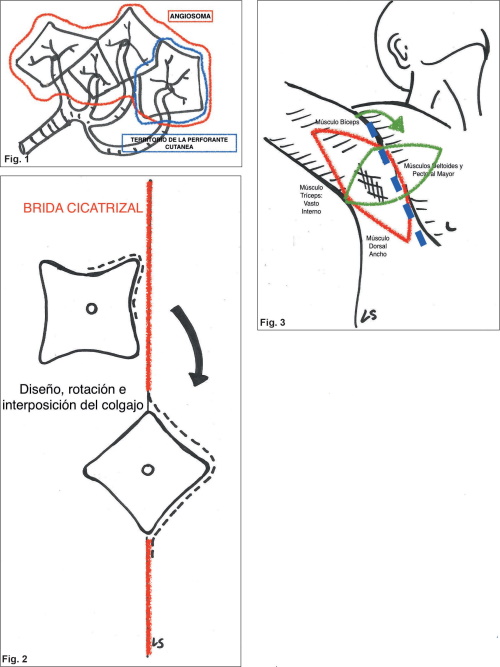
Figuras 1-3. Descripciones clásicas de la anatomía. Árbol arterial en detalle con aplicación quirúrgica, numerosas opciones de colgajos locorregionales como el colgajo perforante toracodorsal (TDap) en cirugía reparadora, y concepto de angiosoma-perforasoma.

Figura 4. Preparación de los especímenes anatómicos para disección en cadáver. Inyección con catéter rígido calibre 14G por vía arterial radial con látex teñido color rojo.
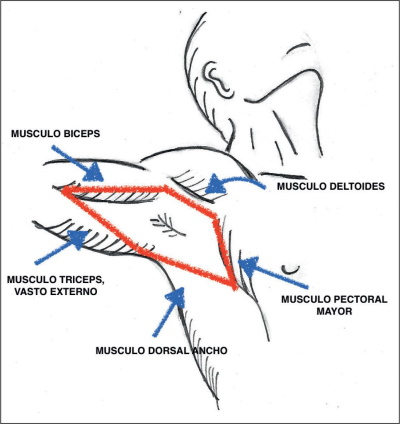
Figura 5. Límites para la disección axilar. Súpero-interno: músculo deltoides hacia proximal y músculo bíceps (porción larga) hacia distal. Súpero-externo: músculo tríceps (porción vasto interno). Ínfero-externo: músculo dorsal ancho. Ínfero-interno: músculo pectoral mayor.
Finalmente, identificamos los vasos perforantes teñidos con látex rojo ubicados en dichos cuadrantes de las 6 axilas (3 derechas y 3 izquierdas), favoreciendo así la visualización de las arteriolas de menor calibre (de hasta 1 mm) (Fig.7-9).
3. Mapeo doppler en pacientes vivos voluntarios no intervenidos.
Hicimos la demarcación de los límites de igual forma en pacientes vivos: 15 pacientes de forma bilateral (30 axilas), respetando las referencias anatómicas. Los criterios de inclusión abarcaron: rango de edad de 20 a 70 años, axilas sanas sin intervenciones quirúrgicas previas. Los criterios de exclusión fueron: cirugías previas regionales, pacientes diabéticos e índice de masa corporal superior a 28.
Empleamos doppler sonoro de 8 mgHz, marca Sonotrax®, el mismo utilizado para la marcación prequirúrgica.
4. Pacientes intervenidos.
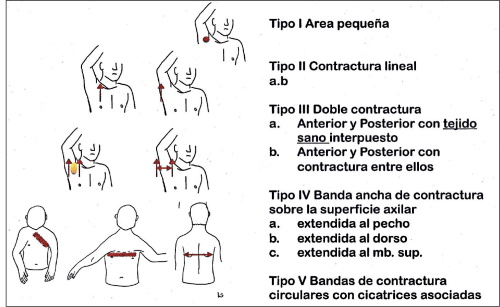
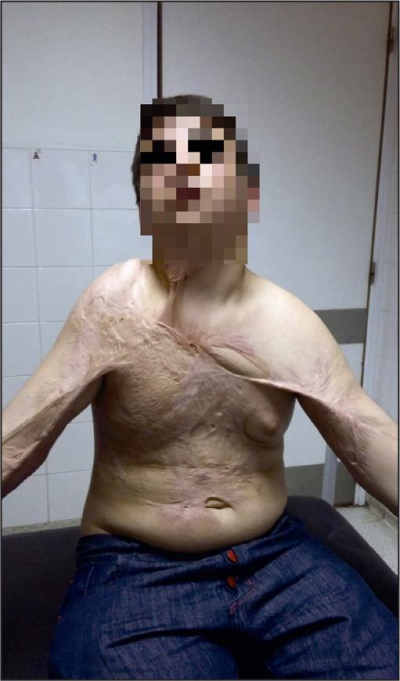
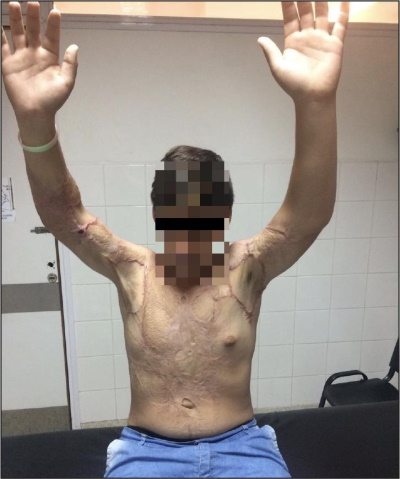
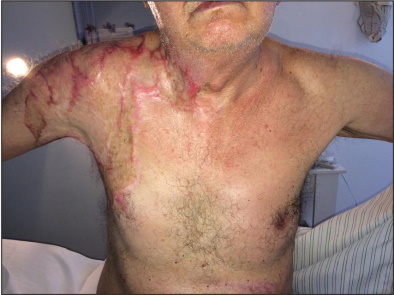
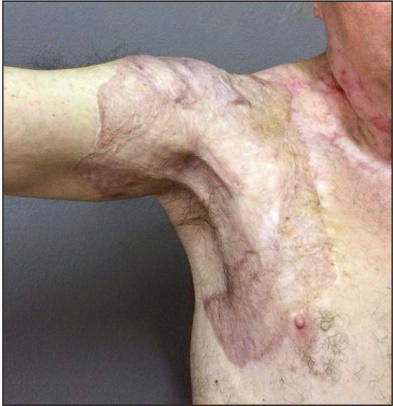
Entre febrero de 2015 y febrero de 2018, intervinimos quirúrgicamente a 7 pacientes: con secuelas graves de quemaduras por diferentes causas: 5 masculinos y 2 femeninos, con una edad promedio de 46 años. Los criterios de inclusión abarcaron: pacientes en un rango de edad de entre 13 y 80 años, secuelas de quemaduras con compromiso del tipo IIa y b, IIIa y IV. Excluimos: pacientes con secuelas tipo I a los cuales se les realizó injerto de piel simple o tratamiento kinésico local y corticoterapia, y los tipo V en los que hubo que realizar colgajos microquirúrgicos libres (Fig. 10 y 11).
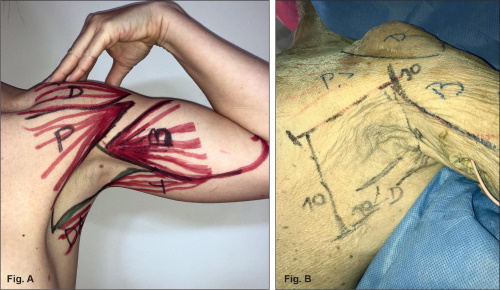
Figuras 6 A y B. Marcación de los mismos límites de disección axilar en pacientes sanos y en espécimen para disección en cadáver.
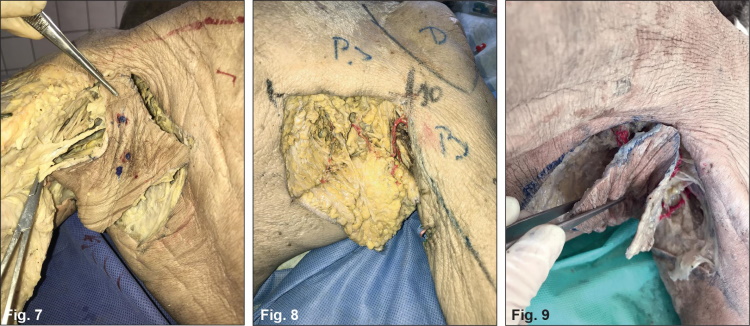
Figuras 7-9. Identificación de vasos perforantes teñidos con látex rojo en los cuadrantes axilares en la disección en cadáver, favoreciendo la visualización de arteriolas de menor calibre (hasta 1 mm).
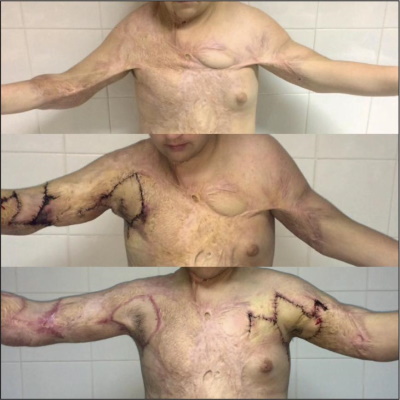
Figura 13. Secuencia de tratamiento (de superior a inferior): colgajo de perforante axilar (CPA), primero axila derecha y en un segundo tiempo axila izquierda.
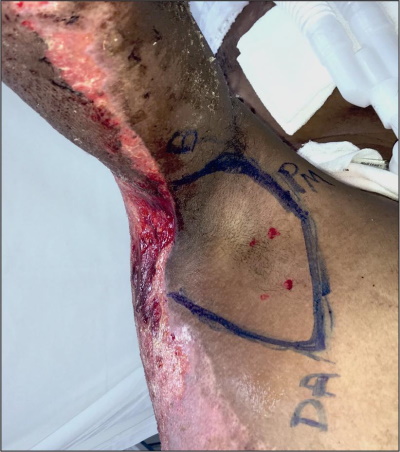
Figura 15. Caso 2. Paciente de 24 años de edad, tratamiento en agudo de quemadura del 30% tipo B para evitar secuela IIb. Preoperatorio: marcaje de colgajo y perforantes.
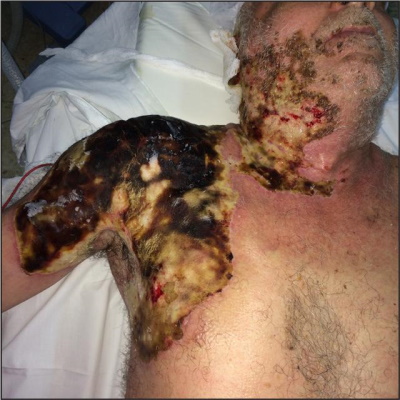
Figura 18. Caso 3. Paciente de 80 años de edad con secuela de quemadura del 18% B, IIa de la clasificación, con hueco axilar respetado.
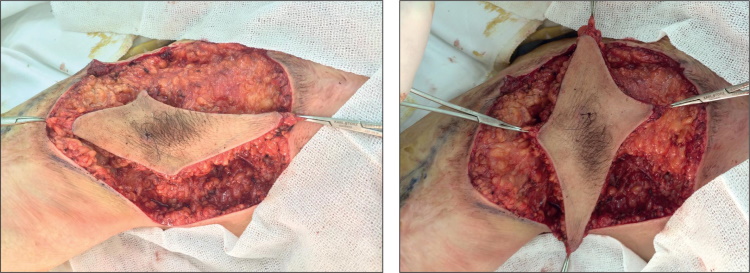
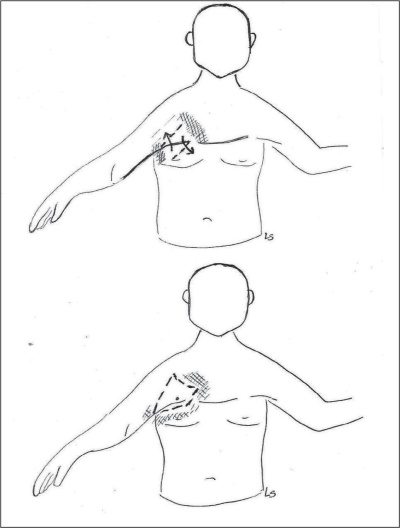
Figuras 21 y 22. Rotación a 90º intraoperatoria de los colgajos romboidales utilizados y como el eje mayor queda perpendicular a la brida.
En todos los casos empleamos dispositivo doppler sonoro portátil de 8 mHz, identificamos el pedículo del colgajo pre e intraoperatoriamente, llevamos a cabo disección completa del mismo y lo esqueletizamos en caso de necesitar rotar el colgajo 180º. Los pacientes permanecieron internados 2 a 4 días con reposo de la extremidad, movilización precoz y evitando la compresión del área. En todos colocamos drenaje laminar durante 48 horas (Fig. 12-22).
Resultados
1.- Revisión bibliográfica.
El alma del presente trabajo se basó en la publicación del año 1991 de Hyakusoku y col., quienes proponen el uso del CPA utilizando la piel sana del hueco axilar y diseñando el colgajo en el centro de la fosa. Describen el colgajo sin hacer referencia exacta de su vascularización: suponen que los vasos perforantes del centro de la axila son constantes y plantean la resolución de bridas que imposibilitan la movilidad del miembro superior, ya sea en la axila o en la fosa cubital. Se deja de esta forma de lado el concepto de pedículo randomizado (aleatorio) y se introduce la noción de la vascularización mediante vasos perforantes(6,7) (Fig. 3).
2.- Disección en cadáver.
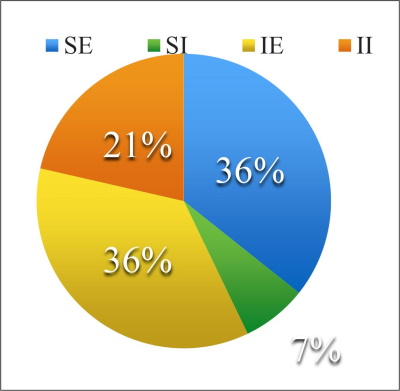
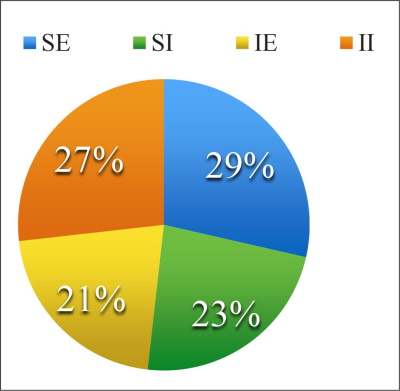
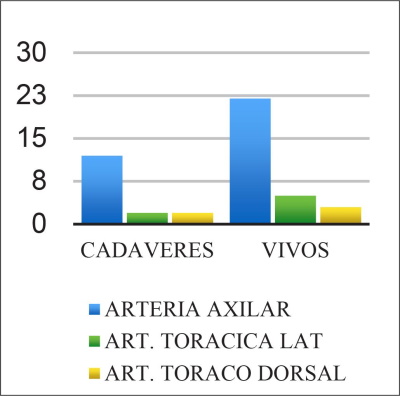
De las 6 axilas disecadas, hallamos en total 18 arteriolas perforantes de 1-3 mm: 12 de ellas se originan en la arteria axilar como ramas directas, 4 se originan en las arterias colaterales: torácica lateral (n=2) y toracodorsal (n=2). Por lo tanto, el 66.66% de las perforantes de los cuadrantes súpero e ínfero-externo y el centro de la axila provienen de la arteria axilar como ramas directas. Los cuadrantes internos comparten su origen en la arteria toracodorsal (ínfero-externo) y torácica lateral (ínfero-interno) y emergen en el borde externo del músculo dorsal ancho y pectoral mayor respectivamente (Fig. 23 A-C) (Tabla I) (Gráfico1).
3. Mapeo doppler en pacientes vivos voluntarios no intervenidos.
La medición y hallazgo con doppler fue de una prevalencia similar en los 4 cuadrantes, con una leve orientación a cuadrantes superiores. En pacientes de corta edad (menores de 15 años), encontramos menor número de perforantes. La media fue de 1 vaso, en varones ascendió a 3 y en mujeres encontramos 1 a 2 vasos. En estas últimas prevalecieron en la región interna, cerca del borde externo del pectoral mayor, probablemente por la mayor vascularización del tejido mamario, y los pacientes masculinos presentaron perforantes de mayor calibre debido a la masa muscular.
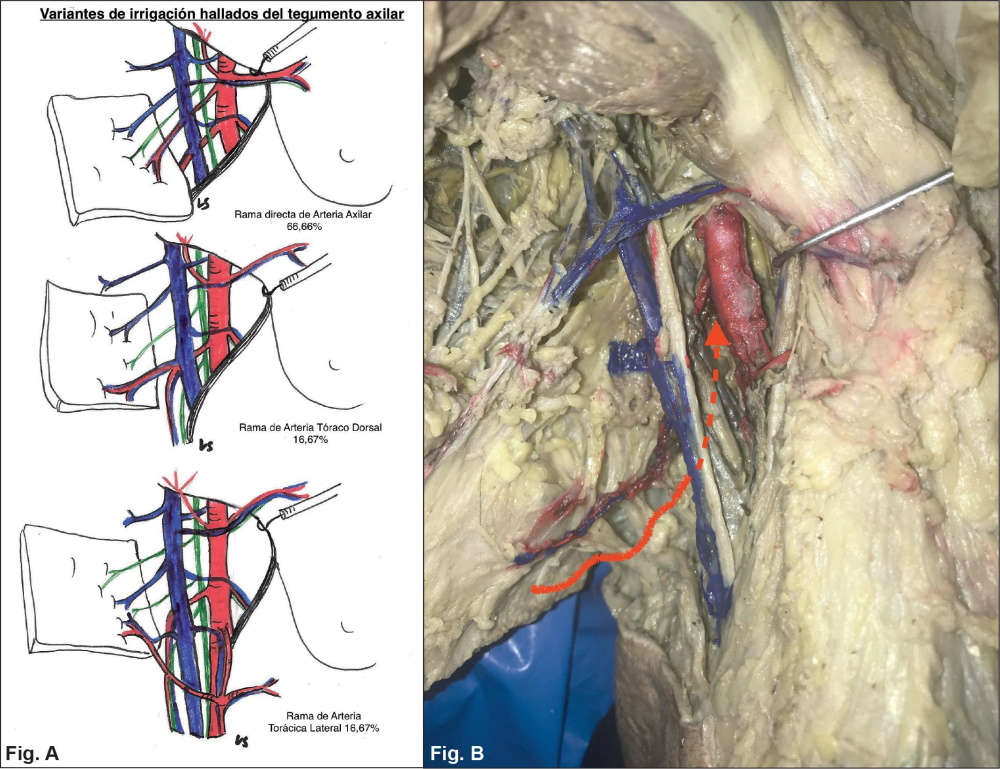
Figura 23 A. Porcentaje hallado en disecciones de vasos de origen de arterias perforantes. B. Rama directa de la arteria axilar. C. Rama de la torácica lateral.
Tabla I. Resultados de la disección vascular en cadáveres
| SEXO | AXILA | ARTERIA PERFORANTE CANTIDAD Y CUADRANTE | INYECCION POR VIA | ORIGEN DE LA ARTERIA PERFORANTE | |
|---|---|---|---|---|---|
| 1 | MASCULINO 60 años | Derecha Izquierda | 1: Sup-Int 2: Inf-Int 1: Sup-Ext 1: Inf-Ext | Radial | 2: Axilar 1: Toracica lateral 1:Axilar 1:Tóraco-dorsal |
| 2 | MASCULINO 70 años | Izquierda Derecha | 2: Sup-Ext 1: Inf-Ext 1: Inf -Ext 2: Sup-Ext | Humeral | 2: Axilar 1:Tóraco-dorsal 2: Axilar |
| 3 | MASCULINO 50 años | Derecha Izquierda | 2: Sup-Int 1: Sup-Ext 1: Inf-Int 2: Sup-Ext 1: Inf-Ext | Humeral Radial | 3: Axilar 2: Axilar 1: Torácica lateral |
Tabla II. Localización vascular con doppler por cuadrantes en voluntarios vivos
| CUADRANTE LOCALIZACION | AXILA DERECHA Perforantes halladas | AXILA IZQUIERDA Perforantes halladas | TOTAL PERFORANTES |
|---|---|---|---|
| SÚPERO-EXTERNO | 7 | 9 | 16 |
| SÚPERO-INTERNO | 6 | 7 | 13 |
| ÍNFERO-EXTERNO | 9 | 3 | 12 |
| ÍNFERO-INTERNO | 7 | 8 | 15 |
En la mayoría de los pacientes identificamos con facilidad el curso de las arterias y venas axilar y braquial, siendo la humeral la que arroja una rama perforante en el punto más apical del rombo trazado en el 90% de los pacientes (Fig. 24 y 25). En pacientes con índice de masa corporal de 26 a 28, hallamos los vasos con mayor dificultad, pero llegamos a un adecuado resultado (Tabla II) (Gráfico 2).
4. Pacientes intervenidos.
Los clasificamos según la tabla de retracciones (Fig.26). De los 7 pacientes intervenidos, las 2 mujeres presentaron quemaduras tipo IIa, y los 5 varones de tipo IIb (n=2), IIa (n=1), tipo IIIa (n=1) y tipo IV (n=1). En todos realizamos un CPA.
Identificamos las perforantes con sistema doppler de 8 mHz, evidenciando gran tracción del tegumento por la brida cicatricial en aquellos con secuelas tipo IIb y IIIa y b. Seleccionamos la arteria perforante de mayor calibre (por sonoridad y medición con doppler color) y cercanía a la brida. Una vez liberada la brida retráctil, evaluamos la nueva posición del vaso perforante. Esta última consideración debe tenerse en cuenta a la hora de disecar el vaso pivotante, ya que al liberar el tejido, este se moviliza involuntariamente. Avanzamos y disecamos el vaso hasta una profundidad de 3 cm, lo que permite al colgajo un mayor alcance y desplazamiento en distancia frente a lo que aportaría una técnica convencional como la Z-plastia (Fig. 27). Esqueletizamos el pedículo solo en aquellos casos en los que la superficie cutánea sana debía alcanzar mayor longitud para poder interponerse en la brida. Su diseño cuadrilobulado permitió el cierre directo de las zonas dadoras de todos los casos tratados. Medimos las longitudes iníciales y finales de las bridas y logramos tras la cirugía un alargamiento de la cicatriz de 6 +/- 1 cm respecto a la inicial.
En total realizamos 7 colgajos cuadrilobulados perforantes restaurando unidades funcionales. Recogimos 2 complicaciones menores: 1 paciente presentó dehiscencia menor de 2 cm2 y 1 sufrió epidermolisis menor de 1cm2 (Gráfico 3).
Evaluamos mediante kinesiología la movilidad de la región axilar (flexo-extensión) con escalas rúbricas al inicio, a los 6 meses de postoperatorio y al año, siendo deficiente (0-20%), regular (21-30%), buena (31-60%) y excelente (61-100%). En los resultados de los 7 pacientes la movilidad axilar fue etiquetada como excelente en 5 pacientes y buena en 2.
Discusión
La angiología humana ha sido muy evaluada por diferentes anatomistas y cirujanos reconstructivos a lo largo de los años, llegando a describir sus recorridos y relaciones con gran precisión. Hoy en día, la técnica quirúrgica se sustenta cada vez más en la anatomía. Su utilidad, estudio y modernas aplicaciones cobran relevancia a la luz de los avances científicos dotando a la Cirugía Reparadora de mayor precisión y sofisticación, por lo cual es imprescindible el conocimiento básico desde sus orígenes hasta sus más intrigantes variantes.
El crecimiento de los tejidos circundantes a la axila que sufren quemaduras y secuelas graves fue durante décadas motivo de interés para muchos autores. Es de gran importancia aportar conocimientos en el devenir de técnicas quirúrgicas que tratan esta zona anatómica y que favorezcan la elasticidad y pliabilidad cutánea sin alterar la movilidad de los miembros superiores ni el desarrollo de la glándula mamaria en las niñas, aportando piel similar a la original para respetar el concepto de “igual con igual” (like with like). Nos centramos así en el estudio de la piel de la axila, su irrigación y sus posibles usos, para intentar que, con nuestro aporte, sea posible mejorar la disección, ahorrar tiempo intraoperatorio y permitir resultados estables en el tiempo en un tejido que se halla en continua adaptación como lo es una zona funcional como la axila, con la importancia que todo ello reviste.
Según los grandes anatomistas, Testut, Netter, entre otros clásicos, la axila se nutre por ramas de la arteria homónima, la cual comienza en el punto medio de la clavícula como continuación de la arteria subclavia, desciende luego por el hueco axilar y termina en el borde inferior del músculo pectoral mayor, dando origen a la arteria braquial. Presenta en su recorrido 3 porciones: la primera, cubierta por la aponeurosis clavipectoral y el músculo pectoral menor, descansa sobre el serrato mayor, se relaciona hacia anterior con la vena homónima y hacia posterior con el plexo braquial. Su segunda porción se halla detrás del músculo pectoral menor cubierta por el pectoral mayor, entre las 2 raíces del nervio mediano. En su tercera porción descansa sobre los tendones de los músculos dorsal ancho y redondo mayor y tiene íntima relación con las ramas del plexo braquial.
Sus ramas colaterales comprenden la arteria toracoacromial, la torácica inferior, la lateral o mamaria externa, la subescapular (de la que se origina la rama toracodorsal) y las circunflejas anterior y posterior. De todas ellas, la mayoría destinadas a la irrigación de los músculos del hombro, cobra relevancia la mamaria externa dando ramas superficiales a los ganglios linfáticos axilares, a la piel de la fosa axilar así como a la glándula mamaria. La arteria axilar, termina con la braquial, quien la continúa para irrigar al miembro superior.(8)
Las descripciones anatómicas tradicionales no hacen hincapié precisamente en las perforantes cutáneas, ramas más superficiales o las que denominamos colaterales de menor calibre, refiriéndonos a vasos de 1 a 2 mm de diámetro. Sin embargo, sí se describen en la literatura quirúrgica asociadas a otros colgajos, por ejemplo en lo que respecta al colgajo miocutáneo de dorsal ancho. La arteria subescapular emite 2 ramas: la circunfleja escapular y la toracodorsal. Esta última emite ramas que irrigan al serrato anterior y al dorsal ancho y luego de irrigar a ambos, da numerosas y pequeñas perforantes en casi toda su extensión, lo que determina que sea posible utilizar islas cutáneas bien perfundidas dándole al colgajo una versatilidad óptima.(8) De acuerdo con dicha descripción, hemos hallado en nuestro estudio de disección cadavérica con inyección previa del árbol arterial numerosas perforantes que arriban al sector más superficial del tegumento axilar, teniendo como origen 3 vasos principales: la arteria axilar, la toracodorsal y la torácica lateral.
En el estudio de Taylor y col. de 1990, se utilizó un transductor doppler de 8 Mhz para identificar en pacientes las perforantes cutáneas dominantes de 1 mm, alcanzando una penetración de 2 a 3 cm. Los resultados fueron comparados con sus estudios previos en cadáveres humanos, hallando similares conclusiones. La publicación del año 1987 describe 276 perforantes cutáneas de 0.5 mm o mayores provenientes de vasos dominantes enteramente subcutáneas, las cuales se comunican en diferentes direcciones formando una red continua vascular. En muchos casos las uniones provenían de un sistema de arterias y arteriolas de choque de menor calibre.
Utilizando una figura del cuerpo humano de frente y perfil, se trazó un mapa localizando los vasos predominantes. En el esquema de perforantes se aprecian vasos cercanos a la fosa axilar, existiendo 1 predominante en el centro y a nivel del borde externo de los músculos pectoral mayor y bíceps. Coincidimos en nuestros 15 voluntarios (30 axilas) con el hallazgo de mayor número de arterias en dicha localización, con predominio en el sexo masculino por presencia de la masa muscular pectoral y en el femenino por el tejido glandular mamario. No hallamos en nuestras disecciones la perforante central de la fosa axilar mencionada por estos autores, ni tampoco en los pacientes intervenidos en los que evidenciamos que se sitúan hacia los cuadrantes internos.(9)
En lo que se refiere a la cirugía reparadora, el avance de la anatomía del árbol arterial fue variando a lo largo de las décadas. Los términos colgajo de perforante y colgajo en hélice fueron introducidos en 1991 por Teo y Hyakusoku para describir un colgajo cutáneo adiposo basado en un pedículo aleatorio (random) subcutáneo con una isla de piel de una longitud que superaba su anchura, consistente en 2 porciones, una a cada lado del pedículo. El colgajo rotaba 90º en el centro del pedículo, al igual que una hélice.(10)
Subsecuentemente, Hallock utilizó el término propeller (hélice) para definir un colgajo fasciocutaneo que elevó en la región posterior del muslo. El colgajo fue de diseño similar al descrito, pero se basó en la esqueletización del vaso perforante y la isla de piel rotó en 180º. Haciendo esto, parte del colgajo (la hoja larga) fue utilizada para cubrir el defecto y la otra parte del colgajo (la hoja corta) se posicionó sobre la zona dadora facilitando el cierre directo de la misma.(11)
Teo colaboró en la definición y aportó detalles de la técnica quirúrgica de los colgajos basados en perforantes. Gran número de autores reportaron la aplicación del concepto de los colgajos de perforantes en la reconstrucción de tejidos blandos en diferentes partes del cuerpo, sin embargo, no existía una clara definición en la literatura, lo que llevó a que se desarrollara en Tokio un consenso respecto a la misma. Como hemos mencionado anteriormente, se describe el CPA para reconstrucción de secuelas de quemaduras de tórax y miembros superiores. Se hace referencia a su uso en pacientes con grandes y extensas secuelas que, si bien son susceptibles de recibir tratamiento con injertos de piel, pueden también ser sometidos a este nuevo método compuesto por piel sana que rodea los sitios afectados.
Hyakusoku y col. presentaron un colgajo en hé lice romboidal sin utilizar el componente muscular, basado en la indemnidad de la piel de la fosa axilar o en la cara anterior del codo. El colgajo se diseñó en el ecuador de dichas regiones y se elevó como colgajo en isla. Los autores afirman en este punto la presencia de vasos perforantes constantes. En este apartado se demuestran mejoras en la técnica reportadas como colgajos multilobulados o en rueda desplegada, con resección e interposición de bandas retráctiles secuelares, orientados en un pedículo subcutáneo que se sitúa en el centro de cada colgajo.
El original método de colgajo propeller (en hélice) fue publicado además en Burns Journal en el año 2006 ampliando la casuística a pacientes considerados grandes quemados que presentaban piel de fosas axilares y de codos respetada, debido a que dichas zonas son protegidas por la misma flexión durante la injuria. En estos pacientes se tallaron colgajos en isla desde las fosas intactas, con un pedículo subcutáneo central y sin identificar el eje vascular utilizando sistema doppler, y se reemplazó la contractura cicatricial con la rotación e interposición de los colgajos. Estos colgajos fueron fácilmente rotados e incluso se pudo reemplazar simultáneamente 2 bandas retráctiles. Sin embargo, cubrir la zona dadora resultó dificultoso en ocasiones, siendo necesario emplear injertos de piel.(12)
Años después, en 2011, el Comité Consultor del Primer Encuentro de Colgajos de Perforantes en Hélice (propeller) en Tokio, logrando una terminología consensuada respecto a los colgajos en hélice y planteando la siguiente definición: un colgajo de perforante puede definirse como un colgajo en isla cuya disección alcanza su vaso dador que se sitúa en un eje axial de rotación; cada colgajo en isla puede transformarse en un colgajo en hélice. Sin embargo, los colgajos en isla que solo avanzan en su desplazamiento o son rotados pero en los que no se aísla completamente su pedículo, quedan excluidos de dicha definición.(13)
Hoy en día, es bien sabido que un colgajo es una parte de la piel y el tejido celular subcutáneo (tegumento) que se moviliza de un lugar a otro del organismo manteniendo su vascularización. El tegumento, como cualquier órgano del cuerpo humano, tiene una anatomía vascular intrínseca: se trata de una red vascular tridimensional, uniforme, elástica, con mayor densidad en la parte subdérmica y suprafascial. Esta red está irrigada por arterias cutáneas cuyo origen radica en troncos vasculares más profundos. En su trayecto, desde su origen hasta el tegumento, tienen relación con estructuras anatómicas tales como músculos, septos, fascias, tendones, etc. Este recorrido se denomina trayecto extrategumentario de las arterias cutáneas.
La comprobación de que los colgajos musculocutáneos tradicionales podían elevarse sin el músculo correspondiente, de que otros colgajos pueden movilizarse mejor disecando la arteria y vena que los nutren (colgajos en hélice), las enormes ventajas obtenidas en cuanto a la menor morbilidad de las zonas dadoras, y la mejor comprensión de las posibles áreas tegumentarias que pueden ser transferidas como colgajos, propiciaron que se aplicara el término perforante. En la actualidad se entiende por colgajo de perforante no sólo a aquel irrigado por una arteria cutánea que atraviesa un músculo, sino también a una forma de elevar colgajos mediante la localización y disección de la arteria cutánea que lo nutre. Es así que cualquier colgajo, sea irrigado o no por una arteria cutánea que perfora un músculo, por el solo hecho de conocer y ubicar la arteria al elevarlo, se denomina perforante.(14,15)
Debido a esta nueva definición, se evidencia la importancia de nombrar y definir a un colgajo de perforante por su irrigación y el conocimiento preciso de su vaso nutricio. Por esta razón, creemos conveniente y de gran relevancia conocer de manera exacta de dónde proviene el pedículo, cuál es su origen preciso o de dónde se origina la mayoría de las veces. Esta razón le daría sustento anatómico a su marcación, considerando que las grandes secuelas retráctiles modificarían por tracción la dirección y vitalidad del vaso perforante central, el cual puede no hallarse in situ, llevando a la incorrecta marcación preoperatoria así como al mal posicionamiento del colgajo. Resulta entonces fundamental el uso del método doppler e incluso el advenimiento de los métodos de imagen cada vez más precisos para su correcta detección, pre e intraoperatoria.
En la evolución tecnológica, los métodos de imagen fueron adquiriendo importancia y protagonismo. Se realizó en Tokio el siguiente estudio para la correcta detección preoperatoria de los vasos que irrigan los colgajos de perforantes. Analizaron de forma retrospectiva todos los casos entre abril de 2007 y abril de 2010 en la Escuela de Medicina Nippon (Tokio, Japón) empleando angiotomografía computarizada con multidetector en la planificación de los colgajos de perforantes para cirugías reconstructivas. Los parámetros examinados incluían: sexo y edad del paciente, causa y área del defecto a reconstruir, perforante utilizada, tipo de pedículo utilizado (si era perforante completa: el exceso de grasa alrededor del pedículo debía ser eliminado para rotar el colgajo 180º, o pedículo subcutáneo: sin disección completa), tamaño y forma del colgajo, tratamiento de la zona dadora, supervivencia del colgajo, y por último, tiempo de duración de la cirugía en relación al tiempo estimado.(16) En base a los resultados obtenidos, los autores creen que con la tomografía computarizada con multidetector es realmente útil en la planificación de múltiples colgajos en diferentes áreas del cuerpo, incluso en aquellos donde los diámetros de las perforantes son menores que en el colgajo de perforante de arteria epigástrica inferior. Específicamente, su hipótesis se basa en que el hallazgo de la perforante por imágenes previo al procedimiento aumenta la efectividad y localización exacta del vaso, lo cual es realmente útil en la planificación de los colgajos en hélice ya que permite una mejor resolución con cortes de menor intervalo y visualización tridimensional de los vasos de menor calibre con menor tiempo de ejecución.(17-19) Coincidimos con los autores en los resultados obtenidos utilizando esta técnica de imágenes y la hemos aplicado en 2 de nuestros pacientes intervenidos, corroborando la detección pre e intraoperatoria del pedículo del colgajo. Como conclusión final y de resumen en relación a lo planteado, observamos que el CPA ha sido aplicado según reparos regionales anatómicos y los límites exactos que propusimos, hemos ampliado sus indicaciones a pacientes pediátricos, aplicamos los conceptos desarrollados por autores de gran prestigio y experiencia, los cuales fueron sumamente útiles en nuestra curva de aprendizaje y nos permitieron arribar a nuevas conclusiones. Observamos que un estudio exhaustivo preoperatorio (doppler y angiotomografía) e intraoperatorio (doppler) permite disminuir sesgos en la elevación del tegumento afectado ante secuelas que distorsionan gravemente la anatomía normal. Sabemos ahora que conociendo la anatomía arterial regional con mayor precisión, determinando que las ramas superficiales provienen de 3 arterias regionales: axilar, torácica lateral y toracodorsal, podemos extender la disección, rotar los colgajos a 180º, diseñarlos a demanda partiendo de zonas irregulares, y lograr más alcance al mejorar la disección del pedículo. Además, pudimos solucionar el tratamiento de la zona dadora mediante el cierre por primera intención, y tratar pacientes en agudo evitando infecciones, disminuyendo la aparición de bridas, restando morbilidad al paciente que requirió menos días de hospitalización, así como el desarrollo de secuelas funcionales. Nos proporcionó resultados seguros, adecuados y estables en el tratamiento de secuelas graves de quemaduras en tórax y miembro superior. También nos aportó superficies de tejido más amplias y de mayor alcance que una Z-plastia convencional ya que otorga entre 60-75% de tejido nuevo, dando durabilidad y acompañando el crecimiento de la zona funcional con menor comorbilidad que otros colgajos, puesto que al identificar el vaso perforante no es necesario incluir músculo en la disección.
Conclusiones
Según el cuadrante axilar en el cual asienta el vaso perforante su identificación previa permite mejor aprovechamiento de la piel conservada, realizando diseños versátiles a demanda e incluso con redundancia del tegumento, lo que da estabilidad en el tiempo y ante el crecimiento y expansión de los tejidos en el caso de pacientes infantiles.
En secuelas de quemaduras graves en tórax y axila, en la mayoría de los tipos de retracción (IIa y IIb, IIIa IVa, IVb y IVc) se propone el uso del colgajo de perforante axilar ya que según su demostrado patrón vascular constante en la arteria axilar (66.66%) y realizando una correcta marcación se logra una gran seguridad en su ejecución. Requiere disección completa del pedículo con esqueletización de al menos 3 cm (incluso llegar hasta el origen en la arteria axilar) en casos donde se necesite rotación de 180º, siendo seguro rotarlo hasta 90º sin disección completa vascular.
El colgajo de perforante axilar presenta una curva de aprendizaje más rápida que un colgajo libre, acorta el tiempo intraoperatorio y la morbilidad de la zona dadora, es estable en el tiempo y factible de ser utilizado en el 90% de las secuelas de quemaduras de miembro superior y tórax.