Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO  Similares en Google
Similares en Google
Compartir
Oncología (Barcelona)
versión impresa ISSN 0378-4835
Oncología (Barc.) vol.27 no.4 abr. 2004
CARCINOMA DE ESÓFAGO
La ecografía endoscópica en la estadificación del carcinoma de esófago
M. Sobrino Faya
Servicio de Aparato Digestivo. Hospital Clínico Universitario. Santiago de Compostela
Los tumores malignos del esófago (adenocarcinoma y tumor de células escamosas) constituyen el grupo de neoplasias cuya incidencia ha experimentado un más rápido crecimiento en países occidentales1, 2. Sobre estos tumores se suelen plantear intervenciones terapéuticas consistentes en resección quirúrgica en bloque, quimio/radioterapia combinadas seguidas o no por resección o bien tratamiento endoscópico paliativo. Una nueva opción en algunos casos, es la posibilidad de curar estas lesiones cuando todavía se encuentran en una fase inicial, mediante procedimientos endoscópicos ablativos, incluyendo la resección mucosa3-7.
Para plantear la terapéutica idónea, así como para evaluar con la mayor precisión los resultados del tratamiento, resulta determinante conocer el grado de extensión de la enfermedad. La ultrasonografía endoscópica (USE) o ecoendoscopia, combina las posibilidades tecnológicas de los ultrasonidos y la endoscopia. Esta técnica aporta el mayor grado de precisión para efectuar la estadificación locorregional de los tumores esofágicos.
Mediante la ecoendoscopia se presenta la pared del tubo digestivo bajo el aspecto clásico de cinco capas (empleando una frecuencia de 7,5 MHz), cuya diferente ecogenicidad les confiere un aspecto alternante de capas claras y oscuras (o lo que es lo mismo, hiper e hipoecogénicas). Desde la luz del tracto gastrointestinal, la primera capa hiperecogénica corresponde a la interfaz entre la mucosa más superficial y el balón lleno de agua, del ecoendoscopio; la segunda capa, hipoecogénica, representa la mucosa profunda y la muscularis mucosae; la tercera capa hiperecogénica corresponde a la submucosa; la cuarta, hipoecogénica, a la muscular propia; la quinta, hiperecogénica, a la serosa o a la adventicia según el órgano explorado (Fig. 1).
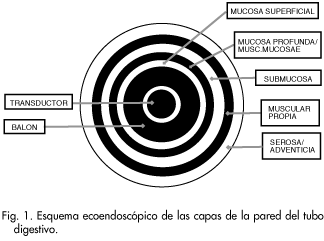
Sin embargo, la pared esofágica puede presentarse también bajo la apariencia de 3 capas, fundiéndose la capa hipoecogénica del epitelio con la muscular propia; pero si se aumenta la frecuencia ultrasónica a 12 e incluso a 20 MHz, aumenta el número de capas que se pueden apreciar (llegando hasta 9 capas) con lo que se distinguen, entre otras, la circular y la longitudinal de la muscular propia.
Sistema TNM
La extensión tumoral en el momento del diagnóstico se considera un factor determinante para el pronóstico de la enfermedad. Dos organizaciones, American Joint Committee of Cancer e International Union Against Cancer, completaron en 1987 la elaboración de un esquema unificado de clasificación de estadios tumorales, del que surgió el sistema de aceptación más amplia para registrar de una forma objetiva la extensión tumoral, el denominado sistema TNM en el que T describe la extensión en profundidad de la masa tumoral primitiva en la pared del tubo digestivo; N corresponde a la afectación linfática y M al grado de diseminación metastásica (Tablas I y II)8.

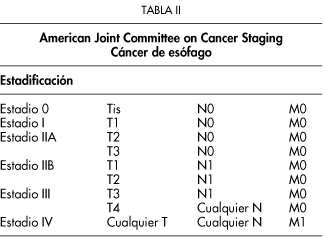
La existencia de adenopatías celíacas en pacientes con cáncer del esófago proximal, se considera diseminación metastásica (M1).
El pronóstico y el tipo de tratamiento del cáncer de esófago dependen principalmente de las estadificaciones T y N, es decir, de la profundidad de afectación tumoral en la pared y de la existencia, o no, de adenopatías9-11. La posibilidad de diferenciar las cinco capas posibilita una óptima apreciación del grado de invasión tumoral intraparietal, permitiendo una evaluación muy precisa del estadio T.
La ecoendoscopia supera a la ecografía, la tomografía computarizada (TC), la resonancia magnética (RM) y la tomografía por emisión de positrones (PET) en la estadificación locorregional del carcinoma esofágico antes y después del tratamiento, aunque el grado de estenosis puede limitar la técnica11-25. La precisión de la estadificación mediante USE ha quedado demostrada en estudios que han empleado muestras operatorias26.
En el cáncer de esófago, la ecoendoscopia debe considerarse una exploración de segunda intención. La detección de la enfermedad maligna debe realizarse previamente mediante endoscopia con toma de biopsias. La endoscopia convencional ha de servir también para optimizar la localización de la lesión, precisando (siempre que la estenosis tumoral no lo impida) las distancias a los incisivos de boca de Killian, extremos proximal y distal del tumor y región cardial.
En las neoplasias en fase evolutiva inicial (T1), el tumor se limita a mucosa, lámina propia o submucosa, permitiendo la USE descartar la invasión de la muscular propia y obteniendo unos niveles de precisión del 80%27, 28. No obstante, en estadios precoces suele requerirse el empleo de frecuencias iguales o mayores a 12 MHz, lo que permite obtener información útil para plantear mucosectomía. Las sondas de alta frecuencia, también conocidas como "minisondas", permiten detectar con precisión superior al 80% si existe invasión tumoral de la muscularis mucosae, lo que mejoraría la estadificación T de las neoplasias superficiales optimizando las posibilidades de la mucosectomía29. Sin embargo, las minisondas de alta frecuencia tienen el inconveniente de su limitada capacidad de penetración, que no supera los 3 cm, lo que en muchos casos limita las posibilidades de la estadificación N30.
En estadios más avanzados (T2, T3, T4) la neoplasia ofrece el aspecto de una masa, generalmente de predominio hipoecogénico, que infiltra y borra los límites entre capas de la pared esofágica. En el T2 afecta a la muscularis propia sin rebasarla. En la fase T3 se alcanza la adventicia y en la T4 la infiltración comprende a estructuras vecinas (aorta, ácigos, pericardio, bronquio, pleura). Cuando la estenosis impide completar la exploración pueden producirse subestadificaciones, entre otras razones, por no poder explorar los ganglios celíacos. En cualquier caso, la extensión locorregional también debe ser evaluada mediante TAC en las primeras fases del estudio de la enfermedad.
Adenopatías
Ciertas características endosonográficas se asocian a afectación neoplásica ganglionar. Los ganglios mayores de 10 mm, redondos, bien delimitados, heterogéneos, hipoecogénicos o con ecoestructura similar al tumor de origen, sugieren participación tumoral, aunque sólo la cuarta parte de los nódulos malignos reúnen todas estas características. Por el contrario, los nódulos menores de 10 mm, elongados, de contornos poco nítidos, homogéneos y más ecogénicos que el tumor, tienen más posibilidades de ser benignos.

Sin embargo, estos criterios deben restringirse (y con reservas) a frecuencias de 7,5 MHz. A 12 MHz pueden cambiar. Por ejemplo, pueden aparecer hipoecogenicidad y bordes definidos en un ganglio benigno.
Los nódulos menores de 5 mm no suelen ser malignos en general, pero el tamaño de los ganglios tampoco es un criterio definitivo de benignidad o malignidad, ya que ganglios mediastínicos benignos pueden medir varios centímetros, y nódulos de pocos milímetros pueden presentar invasión tumoral.
La ecoendoscopia puede detectar con precisión superior al 80%, adenopatías en las diferentes regiones y cadenas ganglionares -paraesofágicas cervicales y laterales, esofágicas superiores y laterales, recurrenciales izquierdas retroaórticas, ganglios del cayado de la vena ácigos, recurrenciales izquierdas (ventana aorto-pulmonar), infracarinales, mediastínicas posteroinferiores, pericardiales y celíacas-. En todo caso, no es objetivo de la USE detectar todas las adenopatías.
Punción con aguja fina guiada por ultrasonografía endoscópica (PAAF-USE)
Siempre que el tumor primario no se interponga en el trayecto de la aguja, la PAAF-USE puede incrementar la rentabilidad de la ecoendoscopia para la estadificación N, al permitir obtener material para estudio citológico de ganglios con invasión metastásica y muy especialmente para la valoración de afectación de los ganglios de la región celíaca31.
En un estudio prospectivo con 125 pacientes, para estadificación ganglionar de carcinoma esofágico mediante PAAF-USE, este procedimiento evidenció mayor sensibilidad y precisión que la TAC y la ecoendoscopia32.
Sumario
· El diagnóstico de cáncer de esófago se debe establecer mediante endoscopia y biopsias.
· La estadificación comienza con la realización de TAC para evaluar posible presencia de metástasis.
· La ecoendoscopia debe seguir a la endoscopia convencional y a la TAC, muy especialmente si se ha excluido la existencia de diseminación metastásica.
· La USE aporta la información más sensible y precisa sobre la afectación tumoral locorregional, lo que es esencial para optimizar la elección terapéutica.
Bibliografía
1. Powell J, McConkey CC. The rising trend in oesophageal adenocarcinoma and gastric cardia. Eur J Cancer Prev 1992; 1:265-9. [ Links ]
2. Blot WJ, Devesa SS, Kneller RW, Fraumeni JF Jr. Rising incidence of adenocarcinoma of the esophagus and gastric cardia. JAMA 1991; 265:1287-9. [ Links ]
3. Sibille A, Lambert R, Souquet J-C, Sabben G, Descos F. Long-term survival after photodynamic therapy for esophageal cancer. Gastroenterology 1995; 108:337-44. [ Links ]
4. Gossner L, Stolte M, Sroka R, Rick K, May A, Hahn EG, et al. Photodynamic ablation of high-grade dysplasia and early cancer in Barrett's esophagus by means of 5-aminolevulinic acid. Gastroenterology 1998; 114:448-55. [ Links ]
5. Soehendra N, Binmoeller KF, Bohnacker S, Seitz U, Brand B, Thonke F, et al. Endoscopic snare mucosectomy in the esophagus without any additional equipment: a simple technique for resection of flat early cancer. Endoscopy 1997; 29:380-3. [ Links ]
6. Giovannini M, Bernardini D, Moutardier V, Monges G, Houvenaeghel G, Seitz JF, et al. Endoscopic mucosal resection (EMR): results and prognostic factors in 21 patients. Endoscopy 1999; 31:698-701. [ Links ]
7. Hattori S, Muto M, Ohtsu A, Boku N, Manabe T, Doi T, Ishikura S, Yoshida S. EMR as salvage treatment for patients with locoregional failure of definitive chemoradiotherapy for esophageal cancer. Gastrointest Endosc 2003; 58(1):65-70. [ Links ]
8. Beahrs OH. Staging of cancer. CA Cancer J Clin 1991; 41(2):121-5. [ Links ]
9. Preston SR, Clark GW, Martin IG, Ling HM, Harris KM. Effect of endoscopic ultrasonography on the management of 100 consecutive patients with oesophageal and junctional carcinoma. Br J Surg 2003; 90(10):1220-4. [ Links ]
10. Chak A, Canto MI, Cooper GS, Isenberg G, Willis J, Levitan N, Clayman J, Forastiere A, Heath E, Sivak MV Jr. Endosonographic assessment of multimodality therapy predicts survival of esophageal carcinoma patients. Cancer 2000; 88(8):1788-95. [ Links ]
11. Botet JF, Lightdale CJ, Zauber AG, et al. Preoperative staging of esophageal cancer: comparison of endoscopic and dynamic CT. Radiology 1991; 181:419-25. [ Links ]
12. Souquet JC, Napoleon B, Pujol B, et al. Endosonography-guided treatment of esophageal carcinoma. Endoscopy 1992; 24(suppl 1):324-8. [ Links ]
13. Chak A, Canto M, Gerdes H, et al. Prognosis of esophageal cancers preoperatively staged to be locally invasive (T4) by endoscopic ultrasound (EUS): a multicenter retrospective cohort study. Gastrointest Endosc 1995; 42:501-6. [ Links ]
14. Binmoeller KF, Seifert H, Seitz U, et al. Ultrasonic esophagoprobe for TNM staging of highly stenosing esophageal carcinoma. Gastrointest Endosc 1995; 101:547-52. [ Links ]
15. Rice TW, Boyce GA, Sivak MV Jr. Esophageal ultrasound and the preoperative staging of carcinoma of the esophagus. J Thorac Cardiovasc Surg 1991; 101:536-43. [ Links ]
16. Fok M, Cheng SWK, Wong J. Endosonography in patient selection for surgical treatment of esophageal carcinoma. World J Surg 1992; 16:1098-103. [ Links ]
17. Hordijk ML, Zander H, van Blankenstein M, et al. Influence of tumor stenosis on the accuracy of endosonography in preoperative T staging of esophageal cancer. Endoscopy 1993; 25:171-5. [ Links ]
18. Kalantzis N, Kallimanis G, Laoudi F, et al. Endoscopic ultrasonography and computed tomography in preoperative (TNM) classification of oesophageal carcinoma (abstract). Endoscopy 1992; 24:653A. [ Links ]
19. Catalano MF, Sivak MV Jr, Rice TW, et al. Postoperative screening for anastomotic recurrence of esophageal carcinoma by endoscopic ultrasonography. Gastrointest Endosc 1995;42:540-44. [ Links ]
20. Tio TL, Coene PP, Schouwink MH, Tytgat GN. Esophagogastric carcinoma: preoperative TNM classification with endosonography. Radiology 1989; 173(2): 411-7. [ Links ]
21. Rasanen JV, Sihvo EI, Knuuti MJ, Minn HR, Luostarinen ME, Laippala P, Viljanen T, Salo JA. Prospective analysis of accuracy of positron emission tomography, computed tomography, and endoscopic ultrasonography in staging of adenocarcinoma of the esophagus and the esophagogastric junction. Ann Surg Oncol 2003;10(8):954-60. [ Links ]
22. Quint LE, Glazer GM, Orringer MB. Esophageal imaging by MR and CT: study of normal anatomy and neoplasms. Radiology 1985; 156(3):727-31. [ Links ]
23. Lehr L, Rupp N, Siewert JR. Assessment of resectability of esophageal cancer by computed tomography and magnetic resonance imaging. Surgery 1988; 103(3): 344-50. [ Links ]
24. Petrillo R, Balzarini L, Bidoli P, Ceglia E, D'Ippolito G, Tess JD, Musumeci R. Esophageal squamous cell carcinoma: MRI evaluation of mediastinum. Gastrointest Radiol. 1990 Fall; 15(4):275-8. [ Links ]
25. Takashima S, Takeuchi N, Shiozaki H, Kobayashi K, Morimoto S, Ikezoe J, Tomiyama N, Harada K, Shogen K, Kozuka T. Carcinoma of the esophagus: CT vs MR imaging in determining resectability. AJR Am J Roentgenol 1991;156(2):297-302. [ Links ]
26. McLoughlin RF, Cooperberg PL, Mathieson JR, Stordy SN, Halparin LS. High resolution endoluminal ultrasonography in the staging of esophageal carcinoma. J Ultrasound Med 1995; 14(10):725-30. [ Links ]
27. Rosch T. Endosonographic staging of esophageal cancer: a review of literature results. Gastrointest Endosc Clin N Am 1995; 5(3):537-47. [ Links ]
28. Hasegawa N, Niwa Y, Arisawa T, Hase S, Goto H, Hayakawa T. Preoperative staging of superficial esophageal carcinoma: comparison of an ultrasound probe and standard endoscopic ultrasonography. Gastrointest Endosc 1996; 44(4):388-93. [ Links ]
29. Murata Y, Suzuki S, Ohta M, Mitsunaga A, Hayashi K, Yoshida K, Ide H. Small ultrasonic probes for determination of the depth of superficial esophageal cancer. Gastrointest Endosc 1996; 44(1):23-8. [ Links ]
30. Nesje LB, Svanes K, Viste A, Laerum OD, Odegaard S. Comparison of a linear miniature ultrasound probe and a radial-scanning echoendoscope in TN staging of esophageal cancer. Scand J Gastroenterol 2000; 35(9):997-1002. [ Links ]
31. Reed CE, Mishra G, Sahai AV, Hoffman BJ, Hawes RH. Esophageal cancer staging: improved accuracy by endoscopic ultrasound of celiac lymph nodes. Ann Thorac Surg 1999; 67(2):319-21; discussion 322. [ Links ]














