My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Española de Enfermedades Digestivas
Print version ISSN 1130-0108
Rev. esp. enferm. dig. vol.105 n.3 Madrid Mar. 2013
https://dx.doi.org/10.4321/S1130-01082013000300003
Indicaciones inadecuadas en el consumo crónico de inhibidores de bomba de protones en un hospital de México. Estudio transversal
Inadequate prescription of chronic consumption of proton pump inhibitors in a hospital in Mexico. Cross-sectional study
Jaime Alberto Sánchez Cuén1, Ana Bertha Irineo Cabrales1, Gregorio Bernal Magaña1 y Felipe de Jesús Peraza Garay2
1Hospital Regional del Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado. Culiacán, Sinaloa. México.
2Universidad Autónoma de Sinaloa. Centro de Investigación y Docencia en Ciencias de la Salud. Culiacán, Sinaloa. México
Dirección para correspondencia
RESUMEN
Introducción: los IBP han sido un avance terapéutico enorme en las enfermedades relacionadas con el ácido. Sin embargo se ha detectado que hay mayoritariamente un abuso en su consumo. El objetivo del estudio fue determinar en nuestro medio la frecuencia de indicación inadecuada en el consumo crónico de IBP en pacientes ambulatorios en un hospital de especialidades.
Material y métodos: se realizó un estudio de revisión transversal descriptivo. La población estudiada fueron pacientes de un hospital de trabajadores del Estado, consumidores crónicos de IBP que acudieron a consulta externa. Se definió como consumidor crónico de IBP la toma diaria del medicamento durante más de un año e indicación inadecuada (no aprobada por guías clínicas). El muestreo fue aleatorio simple. Se investigaron los siguientes parámetros: diagnóstico e indicación de los IBP, tiempo de uso, en qué nivel de atención se prescribió (atención primaria o especializada), automedicación, con o sin endoscopia digestiva. Para el análisis estadístico se utilizó t de Student y Chi cuadrado, intervalos de confianza 95 % y significancia 0,05 %.
Resultados: se revisaron 153 pacientes, 40 (26,1 %) hombres y 113 (73,9 %) mujeres, edad promedio 58 (DE 11,4) años. La indicación de tratamiento crónico con IBP era adecuada en el 64,7 % de los pacientes e inadecuada en el 35,3 %. La indicación apropiada más frecuente (31,3 %) del consumo crónico de IBP fue la ERGE. La indicación inadecuada más frecuente fue la prescripción sin diagnóstico (22,2 %), polifarmacia sin AINE (16,6 %) y gastritis crónica (16,6 %. Antecedentes de endoscopia no tuvieron significación estadística (p > 0,05).
Conclusiones: la frecuencia de indicaciones inadecuadas en el consumo crónico de IBP fue alta y del 35,3%, similar a los publicados en hospitales de países desarrollados.
Palabras clave: Inhibidor de bomba de protones. Consumo crónico.
ABSTRACT
Introduction: PPIs have been an enormous therapeutic advance in acid-related diseases. However, it has been detected an abuse in its consumption. The aim of this study was to determine the frequency of inadequate prescription of chronic use of PPIs in outpatients in a speciality hospital.
Material and methods: we performed a cross-sectional descriptive study review. The study population were patients, chronic users of proton pump inhibitors (PPIs), attending outpatient consult in a hospital of government workers. We defined as chronic user of PPIs that patient that takes medication daily for over a year and inappropriate prescription, that one that has not been approved by the clinical guidelines. A simple random sampling was utilized. The following parameters were investigated: diagnosis and prescription of PPIs, time of use, at which level of care PPIs were prescribed (primary care or specialist), self-medication, with or without endoscopy. For the statistical analysis, we used Student's t-test and Chi-square, 95% confidence intervals and significance 0.05 %.
Results: we reviewed 153 patients, 40 (26.1 %) men and 113 (73.9 %) women, mean age 58 ± 11.4 years. The prescription of chronic treatment with PPIs was adequate in 64.7 % of patients and inadequate in 35.3 %. The most common appropriate prescription (31.3 %) of chronic use of PPIs was due to gastroesophageal reflux disease. The most common inadequate prescription was absence of diagnosis (22.2 %), polypharmacy without nonsteroidal antiinflammatory drugs (16.6 %) and chronic gastritis (16.6 %). History of endoscopy were not statistically significant.
Conclusions: the frequency of inappropriate prescriptions of chronic use of PPIs was high, around 35.3 %, similar to those reported in hospitals in developed countries.
Key words: Proton Pump Inhibitors. Chronic consumption.
Introducción
Los inhibidores de la bomba de protones (IBP) son uno de los fármacos prescritos con más frecuencia en el mundo ya que combinan una eficacia alta con una toxicidad baja. El omeprazol ocupa el 80 % de todas las prescripciones de IBP en el Reino Unido, su prescripción se ha duplicado sin razones suficientes que lo justifique. Aunque se asume que la prescripción ocurre principalmente en atención primaria, hay evidencia de su frecuente uso inadecuado también en la atención especializada. Los IBP han sido un avance terapéutico enorme, mejorando especialmente a largo plazo la calidad vida de los pacientes con síntomas de reflujo gastroesofágico y de sus complicaciones asociadas, así como en enfermedades gastroduodenales relacionadas con el ácido en tratamientos a corto plazo. Sin embargo, estos excelentes fármacos están claramente utilizados en exceso en tratamientos a largo plazo (1). Desde su introducción, a finales de la década de los años 80, los IBP (omeprazol, esomeprazol, lansoprazol, pantoprazol y rabeprazol) han mejorado sustancialmente el tratamiento de las enfermedades relacionadas con el ácido. Los IBP son los inhibidores de la producción de ácido más potentes y son más efectivos cuando la célula parietal es estimulada para producir ácido postprandial. Las diferencias en su eficacia clínica entre los distintos IBP es pequeña, al igual que no son claras sus diferencias cuando se comparan sus costes (2).
Existen guías de práctica clínica como la del Departamento Gubernamental Australiano de la Salud en 2011, con recomendaciones para el correcto uso de los IBP. Las indicaciones reconocidas ampliamente para la terapia con IBP son: la enfermedad por reflujo gastroesofágico (ERGE) con y sin esofagitis, en la confirmación endoscópica de enfermedad ulcerosa péptica, dispepsia no ulcerosa, esófago de Barrett, síndrome de Zollinger Ellison, estenosis esofágica péptica por esclerodermia, tratamiento corto de enfermedad ulcerosa como parte del régimen de tratamiento para erradicación del Helicobacter pylori (Hp) y profilaxis en el consumo de antiinflamatorios no esteroideos (AINE) sobre todo cuando se pueda deducir un mayor riesgo de dispepsia o ulceración, es decir cuando cumplan dos o más de los siguientes criterios: pacientes con más de 65 años, antecedentes de enfermedad ulcerosa péptica, previas complicaciones gastrointestinales serias, sobre todo hemorragia digestiva, uso concomitante de esteroides o anticoagulantes orales, uso prolongado de dosis altas de AINE, presencia de comorbilidad con enfermedad cardiovascular, renal o hepática, diabetes e hipertensión. Con respecto a la duración de la terapia con IBP debe de valorarse la respuesta satisfactoria en un curso inicial de 4-8 semanas con la dosis estándar. De 20-40 % de los pacientes con ERGE no requerirán otra prescripción en 6 a 12 meses. Se debe de considerar, aunque no está absolutamente demostrada, la estrategia de disminuir progresivamente la dosis del IBP. Como resumen se puede señalar que las indicaciones bien establecidas para el tratamiento crónico con IBP son: esofagitis severa (clasificación de Los Ángeles Grado C y D), esófago de Barrett, síndrome de Zollinger Ellison, esclerodermia y estenosis esofágica péptica y profilaxis en el tratamiento con AINE (3). Otras guías de práctica clínica agregan otras indicaciones de uso de IBP como la hemorragia por úlcera péptica, profilaxis en la úlcera por estrés en pacientes de alto riesgo (4-6), así como su uso crónico en la enfermedad por ERGE con endoscopia normal con o sin pH-metría patológica (7). Los tratamientos con IBP a demanda e intermitente aunque no son tan eficaces como el tratamiento continuado, sí son alternativas que se deben considerar en el tratamiento crónico de los pacientes con ERGE (8,9).
La seguridad y tolerabilidad de los IBP son factores a tener en cuenta en pacientes de edad avanzada que requieren su uso crónico de IBP, que por lo general tienen enfermedades crónicas concomitantes (10).
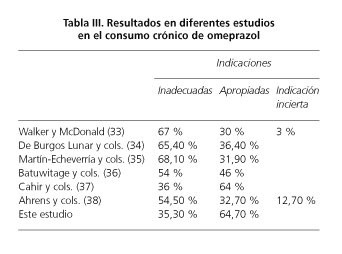
En términos generales los IBP son un grupo farmacológico muy seguro, con efectos secundarios poco importantes e infrecuentes, los que más se han descrito son: cefalea, estreñimiento, diarrea, erupciones cutáneas, no hay descritos casos de cáncer asociado al consumo prolongado con estos medicamentos (11). Los IBP pueden promover la aparición de gastritis predominantemente en el cuerpo gástrico en pacientes Hp positivos, acelerando así el desarrollo de la gastritis atrófica (12). Sin embargo, no hay evidencia de aumento en la proporción de metaplasia intestinal o displasia relacionado con el uso crónico de IBP con o sin infección por Hp. Es bien conocido que la hipergastrinemia generada por el uso a largo plazo de IBP estimula la hiperplasia de las células enterocromafines gástricas, pero a pesar de ello no se han detectado casos de progresión a tumor carcinoide (13). Se mencionan otros efectos adversos más discutibles como son: el síndrome de rebote de hipersecreción ácida (14,15), fracturas por fragilidad ósea (16), nefritis intersticial (17), neumonía (18,19), deficiencia de vitamina B12 (20,21), poliposis gástrica (22,23). Asimismo, la terapia de largo plazo de IBP puede causar anormalidades electrolíticas como hipocalcemia e hipomagnesemia severa, sintomática (24,25). Dosis altas de IBP pueden condicionar la aparición de sobrecrecimiento bacteriano intestinal (26,27). Algún estudio ha documentado un discreto mayor riesgo de fracturas óseas, riesgo que se incrementa en relación con la dosis y duración del tratamiento con los IBP (28). La pérdida de la acidez normal del estómago ha sido asociada a la colonización del aparato gastrointestinal superior, por lo tanto es plausible que el aumento del pH del estómago con terapia inhibidora ácida puede dar lugar a una carga creciente de microbios patógenos como de clostridium difficile, salmonela, campylobacter y shigella (29,30). Los IBP presentan interacción con otros fármacos a través de varios mecanismos, los más importantes incluyen la inhibición competitiva del citocromo P 450 implicado en el metabolismo del fármaco, y la alteración de la absorción de otros fármacos por cambios en niveles gástricos del pH (31,32). Se han realizado y publicado estudios para determinar el porcentaje de indicaciones inapropiadas en la prescripción de IBP, en Reino Unido, Walker y McDonald (33) y en 2001, en España De Burgos y cols. (34) y Martín-Echevarría y cols. (35) y en 2003, 67, 65,4 y 68,1 % respectivamente. En Swansea del Reino Unido, Batuwitage y cols. (36) y en 2006 encontraron que el 54 % de los pacientes se les habían prescrito los IBP inadecuadamente. En Irlanda, Cahir y cols. en 2007 observaron que tan solo en el 36 % de los pacientes estaba correctamente indicado el tratamiento crónico con IBP (37). En Alemania, Ahrens y cols. (38) en 2010 demostraron que el 54,5 % de las prescripciones de IBP no cumplían con las recomendaciones para la indicación de tratamiento crónico con IBP.
Nuestra hipótesis de trabajo fue determinar en nuestro medio la frecuencia de indicación inadecuada en el consumo crónico de IBP en pacientes ambulatorios de un hospital de especialidades, considerando que en la literatura médica la frecuencia de indicación inadecuada en el consumo crónico de IBP es superior al 60 %.
Material y métodos
Se realizó un diseño observacional, transversal, descriptivo, prospectivo, tipo encuesta descriptiva. El estudio fue aprobado por la Comisión de Investigación y Ética del Hospital Regional del Instituto de Seguridad y Servicios Sociales del los Trabajadores del Estado en Culiacán Sinaloa, ya que no viola los conceptos de autoría, plagio, conflicto de intereses y el consentimiento informado.
La población estudiada eran pacientes ambulatorios de un hospital de trabajadores del Estado, en una provincia al Noroeste de México, consumidores crónicos de IBP, que acudieron a consulta externa, en el periodo de febrero a mayo de 2012.
Los criterios de inclusión fueron: pacientes de ambos sexos, de 25 a 80 años de edad, consumo de IBP diario durante al menos un año. Se obtuvo consentimiento informado. Los criterios de exclusión fueron: falta de confianza en las respuestas a las preguntas formuladas y pacientes discapacitados y los criterios de eliminación, errores o pérdida de la recolección de los datos de las variables del estudio.
Definición de las variables. Se definió consumidor crónico de IBP como la persona que habían tomado el medicamento diariamente por un tiempo ≥ a un año. Indicación apropiada para el consumo crónico de IBP y apoyadas por guías clínicas como la del Departamento Gubernamental Australiano de la Salud (3), guías clínicas para el diagnóstico y tratamiento de la enfermedad por reflujo gastroesofágico y Guía de Práctica Clínica, actualización 2007, por la Asociación Española de Gastroenterología, Sociedad Española de Medicina de Familia y Comunitaria y Centro Cochrane Iberoamericano, y fueron: ERGE, esofagitis leve y severa (clasificación de Los Ángeles Grado A, B y C, D respectivamente), esófago de Barrett, síndrome de Zollinger Ellison, esclerodermia y estenosis esofágica y profilaxis en el consumo de AINE cuando se cumplen dos o más de los siguientes criterios: ≥ 65 años, antecedentes de enfermedad ulcerosa péptica, serias complicaciones gastrointestinales previas, uso concomitante de esteroides o anticoagulantes orales, uso prolongado de dosis altas de AINE, presencia de comorbilidad con enfermedad cardiovascular, renal o hepática, diabetes e hipertensión, ERGE con endoscopia negativa y pH-metría normal o patológica (Tabla I). Indicación inadecuada para el consumo crónico de IBP las que no cumplan con las guías clínicas antes señaladas.
El muestreo fue probabilístico aleatorio simple sistemático. El procedimiento fue el siguiente: se solicitó diariamente al área de consulta externa la lista de programación matutina y vespertina de pacientes citados en todas las especialidades del hospital a excepción de pediatría; se enumeraron los pacientes realizando un marco muestral, los datos numéricos se introdujeron a una página de Excel, se determinó realizar 20 entrevistas diarias, y a partir del número aleatorizado se inició la elección del paciente; identificándose el turno, el consultorio y la especialidad.
Los pacientes que reunieron los criterios de selección, se les realizó una entrevista, llenando el formulario, con la identificación del paciente y captura de variables como edad, género, y número de expediente; se realizaron preguntas cerradas estructuradas para la respuesta a las variables como tipo de medicamento IBP empleado, nivel de prescripción, especialidad o atención primaria, antecedente de endoscopia, posteriormente se verificó la información en los registros asistenciales en los archivos clínicos, así como el informe de los hallazgos de endoscopia si la hubiera. En caso de coincidir con las respuestas dadas se optaba por incluirlo al estudio, caso contrario o haber dado falsa la información no era incluido.
El tamaño de la muestra para una proporción fue de 153 pacientes, para detectar una diferencia entre las proporciones hipotética y la alternativa de 0,10 (Delta). La proporción de hipótesis nula se asumió ser de 0,50 y bajo la alternativa de 0,60. El estadístico de prueba usado fue la prueba unilateral (una cola) de Z. El nivel de significancia de la prueba fue en 0,05 y potencia de 0,80.
Análisis estadístico. Se utilizó el paquete estadístico SPSS v 16, (SPSS, inc., Chicago IL, EE.UU.). En el análisis de estadística descriptiva para variables cuantitativas con medidas de tendencia central y de dispersión; para variables categóricas se presentaron en porcentajes. Para estadística inferencial para variables cuantitativas se presentaron con estimadores puntuales e intervalos de confianza, se utilizó el test estadístico t de Student y para variables categóricas la Chi cuadrado. Para ambas variables se presentaron gráficos y tablas. Se consideró una significancia estadística de 0,05 con una confianza del 95 %.
Resultados
Se estudió un grupo de 153 pacientes, masculinos 40 (26,1 %) y femeninos 113 (73,9 %), la edad promedio fue de 58 (DE 11,4) años. La prescripción de los IBP se realizó en atención primaria en el 26,8 %, de especialidades en el 65,4 % y automedicación en el 7,8 %.
Los IBP utilizados crónicamente por el paciente fueron el omeprazol en 78,4 % y esomeprazol en 21,6 %.
En 99 pacientes (64,7 %) la indicación en el consumo crónico del IBP era correcta, mientras que en 54 pacientes (35,3%) fue inadecuada (Fig. 1).
Los porcentajes en las indicaciones apropiadas en el consumo crónico de IBP fueron: 31 (31,3 %) en pacientes por ERGE, 27 (27,3 %) por esofagitis erosiva con clasificación de Los Ángeles A y B, 25 (25,3 %) profilaxis ante el consumo continuado de AINE, 14 (14,1 %) por esofagitis erosiva con clasificación de Los Ángeles C y D, 1 paciente (1 %) por esófago de Barrett y 1 paciente (1 %) por ERGE con endoscopia normal y pH-metría patológica (Fig. 2).
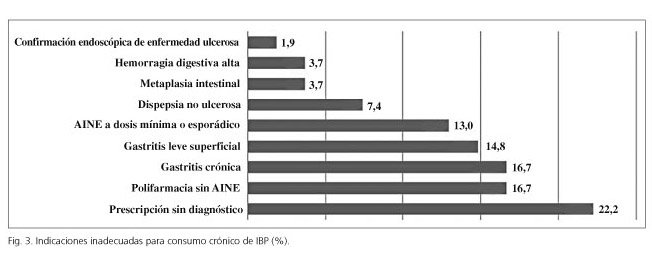
Las indicaciones inadecuadas para el consumo crónico de IBP fueron: 12 (22,2 %) prescripción sin diagnóstico, 9 (16,7 %) polifarmacia sin AINE, 9 (16,7 %) por gastritis crónica, 8 (14,8 %) por gastritis leve superficial, 7 (13 %) AINE a dosis mínima o esporádica, 4 (7,4 %) por dispepsia no ulcerosa, 2 (3,7 %) por metaplasia intestinal, 2 (3,7 %) por hemorragia digestiva alta y 1 (1,9 %) por confirmación endoscópica de enfermedad ulcerosa (Fig. 3).
En 76 (49,7 %) pacientes se les había practicado una endoscopia diagnóstica y en 77 pacientes (50,3 %) se indicó el IBP sin endoscopia previa. No hay diferencias en cuanto al género masculino y femenino. Tuvieron indicación correcta 10 hombres (25 %) y 31 mujeres (27,4 %) e incorrecta 30 hombres (75 %) y 82 mujeres (72,6 %) (p = 0,470). La edad promedio en los pacientes con indicaciones apropiadas e inadecuadas fue de 58 (DE 10,3) y 58,1 (DE 13,2) años respectivamente con una p = 0,963. Los médicos de atención primaria indicaron adecuadamente la prescripción de IBP en 30 pacientes (73,2 %) frente a 69 pacientes (69 %) en atención especializada. La prescripción inadecuada fue por tanto en 11 pacientes (26,8 %) en atención primaria frente al 31 pacientes (31 %) en atención especializada (p = 0,391). En 54 (71,1 %) y 45 (58,4 %) pacientes con y sin antecedente de endoscopia tenían indicación apropiada de IBP respectivamente, asimismo en 22 (28,9 %) y 32 (41,6 %) pacientes con y sin antecedente de endoscopia tenían indicación inadecuada de IBP respectivamente (p = 0,072) (Tabla II).
Discusión
Los IBP han mejorado sustancialmente el tratamiento de las enfermedades relacionadas con el ácido y tienen un perfil de seguridad excelente, son los IBP uno de los fármacos más comúnmente prescritos tanto en atención primaria como en atención especializada. Sin embargo, el consumo crónico ha evidenciado algunos efectos adversos infrecuentes como son deficiencia de vitamina B12, fragilidad ósea y fracturas, hipomagnesemia, hipopotasemia, poliposis fúndica gástrica, enteritis infecciosa, interacciones medicamentosas, síndrome de rebote de hipersecreción gástrica, susceptibilidad a neumonías. Aunque poco frecuentes, estos efectos adversos deben ser tenidos en cuenta sobre todo en aquellas indicaciones inapropiadas, que se dan en todo el mundo y que oscilan entre el 20 y el 75 %. Nuestro estudio detectó un 35,3 % de indicaciones inadecuadas en el consumo crónico de IBP, siendo su prescripción más frecuente en el género femenino (73,9 %). El IBP que más se prescribe es omeprazol (78,4 %). Las indicación apropiada más frecuente fue la ERGE (31,3 %), la esofagitis erosiva con clasificación de Los Ángeles A y B (27,3 %) así como la profilaxis con el consumo de AINE (25,3 %); la indicación inadecuada más frecuente fue la prescripción sin diagnóstico (22,2 %), la polifarmacia sin AINE (16,7 %) y la gastritis crónica (16,7 %). En estudios realizados en países desarrollados sobre la prescripción de IBP, Walker y McDonald (33) demostraron una indicación inadecuada del 67 % de los pacientes y Batuwitage y cols. (36) en el Reino Unido observaron una prescripción incorrecta de los IBP en un 56 % de los pacientes; asimismo de Burgos Lunar y cols. (34) encontraron que la prescripción de IBP se ajustó en solo el 36,4 % a los criterios apropiados y en España Martín-Echevarría y cols. (35) observaron un 68,1 % de indicaciones inadecuadas. En Alemania Ahrens y cols. (38) demostraron que en un 54,5 % de las prescripciones no cumplían con las recomendaciones para la indicación de IBP. Asimismo en Irlanda, Cahir y cols. (37) en 2007 observaron que tan solo en el 36 % de los pacientes estaba correctamente indicado el tratamiento crónico con IBP. Nuestro estudio es concordante con los resultados reseñados (Tabla III).
El consumo crónico de IBP sin una indicación apropiada podría evidenciar un desconocimiento de sus indicaciones y probable falta de coordinación entre los diferentes niveles de atención que podría corregirse con la elaboración de protocolos para la buena práctica en la atención de pacientes que requieren IBP, no solo en hospitales de países en vías de desarrollo sino también en los desarrollados, ya que no son ajenos a esta alta frecuencia de indicaciones inadecuadas. Las guías en la práctica clínica podrían mejorar la adherencia en la prescripción adecuada de IBP, pretendiendo que los beneficios se obtendrían con acciones de políticas sanitarias, concienciando su uso racional y evitar efectos adversos ya descritos en publicaciones científicas para fortalecer los programas de Hospital Seguro. Se concluye que la frecuencia de indicaciones inadecuadas en la prescripción del consumo crónico de IBP es del 35,3 % siendo alta y similar a otros hospitales de países desarrollados.
![]() Dirección para correspondencia:
Dirección para correspondencia:
Jaime Alberto Sánchez Cuén
Servicio de Gastroenterología
Hospital Regional ISSSTE de Culiacán. Calzada
Heroico Colegio Militar 875 Sur, colonia 5 de Mayo
80000 Culiacán, Sinaloa. México
e-mail:
sanchezcuen_jaime@hotmail.com
Recibido: 02-09-2012
Aceptado: 20-11-2012
Bibliografía
1. Forgacs I, Loganayagan A. Overprescribing proton pump inhibitors. BMJ 2008;336:2-3. [ Links ]
2. Cienfuegos Alfredo. Series: from physiology to the clinic: Gastric secretion and proton pump inhibitors. Rev Col Gastroenterol 2010;25:94-8. [ Links ]
3. National Prescribing Service. Proton pump inhibitors. Citado en http://www.nps.org.au/__data/assets/pdf_file/0012/111423/clinical_guidance_final_PPI.pdf [ Links ]
4. Nardino RJ, Vender RJ, Herbert PN. Overuse of acid-suppressive therapy in hospitalized patients. Am J Gastroenterol 2000;95:3118-22. [ Links ]
5. Noguerado Asensio A, Rodríguez Barrientos R, Zelaya Castro P, Sánchez Sempere A, Antuña Blanco F, Lutz García E, et al. Use of acid-suppressive medications in hospitalized patients. An Med Interna 2002;19: 557-60. [ Links ]
6. Ponce Romero M, Berenguer Lapuerta J. Indicaciones actuales de los inhibidores de la bomba de protones. Rev Clin Esp 2003;203:136-8. [ Links ]
7. Garrigues V, Bastida G, Bau I, Ponce J. Gastroesophageal reflux with normal endoscopy. What can be done? Rev Sdad Valenciana Patol Dig 2000;19:141-51. [ Links ]
8. DeVault KR, Castell DO; American College of Gastroenterology. Updated guidelines for the diagnosis and treatment of gastroesophageal reflux disease. Am J Gastroenterol 2005;100:190-200. [ Links ]
9. Elsevier Doyma, S.L. Grupo de trabajo de la guía de práctica clínica sobre ERGE. Manejo del paciente con enfermedad por reflujo gastroesofágico (ERGE). Guía de Práctica Clínica. Actualización 2007. Asociación Española de Gastroenterología, Sociedad Española de Medicina de Familia y Comunitaria y Centro Cochrane Iberoamericano; 2007. Programa de Elaboración de Guías de Práctica Clínica en Enfermedades Digestivas, desde la Atención Primaria a la Especializada: 1. Barcelona, marzo 2007. [ Links ]
10. Sobrino-Cossío S, López-Alvarenga JC, Remes-Troche JM, Galvis-García ES, Soto-Pérez JC, Teramoto-Matsubara O, et al. Proton pump inhibitors in gastroesophageal reflux disease: a custom-tailored therapeutic regimen. Rev Esp Enferm Dig 2012;104:367-78. [ Links ]
11. Martín de Argila de Prados C. Security of proton pump inhibitors. Rev Esp Enferm Dig 2011;103:98. [ Links ]
12. Martínez MJD, Henao RSC. Consumo crónico de medicamentos inhibidores de la bomba de protones (IBP) y el desarrollo de gastritis atrófica corporal. Rev Col Gastroenterol 2007;22(Pt 4):302-307. [ Links ]
13. Doweck J. Adverse effects of proton pump inhibitors. Acta Gastroenterol Latinoam 2009:39:219-22. [ Links ]
14. Reimer C, Søndergaard B, Hilsted L, Bytzer P. Proton-pump inhibitor therapy induces acid-related symptoms in healthy volunteers after withdrawal of therapy. Gastroenterology 2009;137:80-7. [ Links ]
15. Niklasson A, Lindström L, Simrén M, Lindberg G, Björnsson E. Dyspeptic symptom development after discontinuation of a proton pump inhibitor: A double-blind placebo-controlled trial. Am J Gastroenterol 2010;105:1531-7. [ Links ]
16. Insogna KL. The effect of proton pump-inhibiting drugs on mineral metabolism. Am J Gastroenterol 2009;104(Supl. 2):S2-4. [ Links ]
17. Simpson IJ, Marshall MR, Pilmore H, Manley P, Williams L, Thein H, et al. Proton pump inhibitors and acute interstitial nephritis: report and analysis of 15 cases. Nephrology (Carlton) 2006;11:381-5. [ Links ]
18. Gulmez SE, Holm A, Frederiksen H, Jensen TG, Pedersen C, Hallas J. Use of proton pump inhibitors and the risk of community-acquired pneumonia: a population-based case-control study. Arch Intern Med 2007;14;167:950-5. [ Links ]
19. de Jager CP, Wever PC, Gemen EF, van Oijen MG, van Gageldonk-Lafeber AB, Siersema PD, et al. Proton pump inhibitor therapy predisposes to community-acquired Streptococcus pneumoniae pneumonia. Aliment Pharmacol Ther 2012;36:941-9. [ Links ]
20. Sagar M, Janczewska I, Ljungdahl A, Bertilsson L, Seensalu R. Effect of CYP2C19 polymorphism on serum levels of vitamin B12 in patients on long-term omeprazole treatment. Aliment Pharmacol Ther 1999;13:453-8. [ Links ]
21. Hirschowitz BI, Worthington J, Mohnen J. Vitamin B12 deficiency in hypersecretors during long-term acid suppression with proton pump inhibitors. Aliment Pharmacol Ther 2008;27:1110-21. [ Links ]
22. Oh S. Proton pump inhibitors uncommon adverse effects. Aust Fam Physician 2011;40:705-8. [ Links ]
23. Jalving M, Koornstra JJ, Wesseling J, Boezen HM, DE Jong S, Kleibeuker JH. Increased risk of fundic gland polyps during long-term proton pump inhibitor therapy. Aliment Pharmacol Ther 2006;24: 1341-8. [ Links ]
24. Mackay JD, Bladon PT. Hypomagnesaemia due to proton-pump inhibitor therapy: A clinical case series. QJM 2010;103:387-95. [ Links ]
25. Hoorn EJ, van der Hoek J, de Man RA, Kuipers EJ, Bolwerk C, Zietse R. A case series of proton pump inhibitor-induced hypomagnesemia. Am J Kidney Dis 2010;56:112-6. [ Links ]
26. Raña Garibay R. Efectos adversos y falla a los inhibidores de la bomba de protones (IBP). Rev Gastroenterol Méx 2011;76(Supl.1):49-52. [ Links ]
27. Lombardo L, Foti M, Ruggia O, Chiecchio A. Increased incidence of small intestinal bacterial overgrowth during proton pump inhibitor therapy. Clin Gastroenterol Hepatol 2010;8:504-8. [ Links ]
28. Laine L. Proton pump inhibitors and bone fractures? Am J Gastroenterol 2009;104 (Supl.2):S21-6. [ Links ]
29. Leonard J, Marshall JK, Moayyedi P. Systematic review of the risk of enteric infection in patients taking acid suppression. Am J Gastroenterol 2007;102:2047-56. [ Links ]
30. Linney S, Fernandes T, Einarson T, Sengar A, Walker JH, Mills A. Association Between Use of Proton Pump Inhibitors and a Clostridium difficile-Associated Disease Outbreak: Case-Control Study. Can J Hosp Pharm 2010;63:31-7. [ Links ]
31. Gerson LB, Triadafilopoulos G. Proton pump inhibitors and their drug interactions: An evidence-based approach. Eur J Gastroenterol Hepatol 2001;13:611-6. [ Links ]
32. Labenz J, Petersen KU, Rösch W, Koelz HR. A summary of Food and Drug Administration-reported adverse events and drug interactions occurring during therapy with omeprazole, lansoprazole and pantoprazole. Aliment Pharmacol Ther 2003;17:1015-9. [ Links ]
33. Walker NM, McDonald J. An evaluation of the use of proton pump inhibitors. Pharm World Sci 2001;23:116-7. [ Links ]
34. de Burgos Lunar C, Novo del Castillo S, Llorente Díaz E, Salinero Fort MA. Study of prescription-indication of proton pump inhibitors. Rev Clin Esp 2006;206:266-70. [ Links ]
35. Martín-Echevarría E, Pereira Juliá A, Torralba M, Arriola Pereda G, Martín Dávila P, Mateos J, et al. Assessing the use of proton pump inhibitors in an internal medicine department. Rev Esp Enferm Dig 2008;100:76-81. [ Links ]
36. Batuwitage BT, Kingham JG, Morgan NE, Bartlett RL. Inappropriate prescribing of proton pump inhibitors in primary care. Postgrad Med J 2007;83:66-8. [ Links ]
37. Cahir C, Fahey T, Teeling M, Teljeur C, Feely J, Bennett K. Potentially inappropriate prescribing and cost outcomes for older people: a national population study. Br J Clin Pharmacol 2010;69:543-52. [ Links ]
38. Ahrens D, Chenot JF, Behrens G, Grimmsmann T, Kochen NM. Appropriateness of treatment recommendations for PPI in hospital discharge letters. Eur J Clin Pharmacol 2010;66:1265-127. [ Links ]











 text in
text in