Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Enfermedades Digestivas
versión impresa ISSN 1130-0108
Rev. esp. enferm. dig. vol.108 no.8 Madrid ago. 2016
https://dx.doi.org/10.17235/reed.2016.4103/2016
TRABAJOS ORIGINALES
Utilidad de la elastografía percutánea con la técnica de radiación acústica de la fuerza de impulso para el diagnóstico no invasivo de la pancreatitis crónica
Usefulness of percutaneous elastography by acoustic radiation force impulse for the non-invasive diagnosis of chronic pancreatitis
Camilo Julio Llamoza Torres1, María Fuentes Pardo2, Francisco Javier Álvarez Higueras3, Fernando Alberca de las Parras3,4 y Fernando Carballo Álvarez3,4
1Sección de Aparato Digestivo. Servicio de Medicina Interna. Hospital General Universitario Rafael Méndez. Lorca, Murcia.
2Medicina Familiar y Comunitaria. Área III de Salud de la Región de Murcia. Murcia.
3Servicio de Medicina de Aparato Digestivo. Unidad de Gestión Clínica de Digestivo. Hospital Clínico Universitario Virgen de la Arrixaca. Murcia.
4Instituto Murciano de Investigación Biosanitaria (IMIB-Arrixaca). Murcia.
Dirección para correspondencia
RESUMEN
Objetivo: determinar la precisión diagnóstica con la técnica de la radiación acústica de la fuerza de impulso (ARFI) para el diagnóstico de pancreatitis crónica (PC).
Material y métodos: estudio observacional, monocentro, de pacientes a quienes, por sospecha de pancreatitis crónica entre octubre de 2012 y septiembre de 2015, se les realizó un estudio por ultrasonografía endoscópica (USE) y se les clasificó según los criterios estándar y de Rosemont. Evaluamos los mismos pacientes mediante un equipo de ultrasonido ACUSON S2000™ equipado con el software Virtual Touch™ Quantification para obtener la velocidad de onda de corte (Vc) en la cabeza, cuerpo y cola del páncreas. Los datos fueron analizados mediante análisis de la varianza y técnicas de correlación no paramétricos; la precisión diagnóstica fue obtenida mediante el análisis de las curvas ROC.
Resultados: evaluamos 33 pacientes (45,5% mujeres) con media de edad de 58,3 ± 11,8 años. Diecisiete con PC y dieciséis clasificados como normal según los criterios estándar. Detectamos diferencias significativas en las medias de Vc en cuerpo de páncreas de pacientes sin (1,27 m/s) y con PC (1,57 m/s) (p = 0,037). El área bajo la curva ROC fue de 0,713 (IC 95% 0,532-0,895) y la precisión diagnóstica, de 69,7% para una Vc de 1,4 m/s en cuerpo pancreático. La media de la Vc en la cabeza (r = 0,421/p < 0,05) y cuerpo de páncreas (r = 0,455/p < 0,05) mostró correlación significativa con el número de criterios USE para PC.
Conclusión: la cuantificación percutánea de la rigidez pancreática mediante la técnica ARFI resulta de utilidad para el diagnóstico no invasivo de la pancreatitis crónica.
Palabras clave: Pancreatitis crónica. Elastografía. Radiación acústica de la fuerza de impulso.
ABSTRACT
Objective: To determine the accuracy of the acoustic radiation force impulse (ARFI) technique for the diagnosis of chronic pancreatitis.
Materials and methods: We present an observational, single-center study that included patients with suspected chronic pancreatitis in the period between October 2012 and September 2015 who underwent endoscopic ultrasound (EUS) and were classified according to the standard and Rosemont criteria. The same group of patients was assessed by the ARFI technology using ACUSON S2000™ equipment with Virtual Touch™ Quantification software for the assessment of pancreatic stiffness by obtaining the shear wave velocity (SWV) in the head, body and tail of the pancreas. Data were analyzed using ANOVA and nonparametric correlation methods. Diagnostic accuracy was obtained by analyzing receiver operating characteristic (ROC) curve.
Results: A total of thirty-three patients were studied (45.5% women); mean age was 58.3 ± 11.8 years. Seventeen with a diagnosis of chronic pancreatitis and sixteen classified as normal according to standard criteria. A significant difference was detected between the means of SWV in pancreatic body of patients without (SWV: 1.27 m/s) and with chronic pancreatitis (SWV 1.57 m/s), p = 0.037. The area under the ROC curve was 71.3% (95% CI 0.532-0.895) and the accuracy of ARFI for diagnosing chronic pancreatitis was 69.7% for a SWV of 1.4 m/s in the pancreatic body. The SWV means in head (r = 0.421, p < 0.05) and body (r = 0.455, p < 0.05) of the pancreas showed a significant correlation with the number of EUS criteria for chronic pancreatitis.
Conclusion: Quantification of pancreatic stiffness with ARFI elastography technique has proven to be useful for the non-invasive diagnosis of chronic pancreatitis.
Key words: Chronic pancreatitis. Elastography. Acoustic radiation force impulse.
Introducción
La pancreatitis crónica (PC) es un complejo proceso inflamatorio crónico del páncreas, caracterizado por la presencia de infiltrado inflamatorio crónico, activación de células estrelladas pancreáticas con producción de fibrosis parenquimatosa y pérdida progresiva de células acinares y, en menor medida, islotes de Langerhans (1-5). La ultrasonografía endoscópica (USE) se ha convertido en la técnica de elección para el diagnóstico de patología pancreática como la PC, sobre todo en estadios iniciales en los que otros procedimientos no alcanzan la misma precisión (1-6).
Se han establecido criterios morfológicos por USE que caracterizan la enfermedad, dividiéndolos en parenquimatosos y ductales, siendo más probable su diagnóstico ante la presencia de mayor número de los mismos. En la práctica clínica habitual, suele emplearse un punto de corte de 4 criterios diagnósticos (3). La clasificación estándar consiste en 9 criterios: focos hiperecogénicos, tractos fibrosos, lobularidad, quistes, calcificaciones, dilatación del Wirsung, dilatación de las ramas secundarias del Wirsung, irregularidad del conducto pancreático principal y paredes hiperecogénicas del Wirsung (3). Con la hipótesis de que no todos los criterios tienen la misma relevancia, se ha propuesto la clasificación de Rosemont (4), en la que se definen los criterios ecoendoscópicos de PC y su validez específica, estableciéndose grupos diferentes de pacientes en función de ellos. A pesar de ello, la variación interobservador de esta clasificación no mejora las previas (3-5).
Existe una correlación significativa entre el número de criterios por USE de PC y el grado de fibrosis pancreática evaluada histológicamente (7-11). Otra manera, pero indirecta, de evaluar el grado de rigidez tisular es mediante la elastografía, que es la representación mediante imágenes de una de las propiedades mecánicas de los objetos (elasticidad) al ser expuestos a una fuerza que tiende a deformarlos (12). La elastografía se puede clasificar en función de la medición física valorada en: a) strain o deformación; y b) velocidad de onda de distorsión o corte (Vc), o shear wave speed; o en función del método de excitación utilizado, en: a) por compresión manual: usando la fuerza directa con la mano o pulsaciones cardiovasculares; b) radiación acústica de la fuerza de impulso (ARFI: acoustic radiation force impulse); y c) por impulso mecánico (ejemplo: Fibroscan®) (12,13).
La literatura publicada sobre elastografía pancreática ha sido evaluada mediante tres diferentes abordajes: percutánea, endoscópica y por resonancia magnética (14). En 2005, Hirooka y cols. realizaron el primer reporte elastográfico del páncreas por USE (15) y Uchida y cols., mediante elastografía percutánea (16), ambos utilizando métodos cualitativos. La técnica ARFI, desarrollada por el grupo de Katty Nightingale (17), es un método dinámico que produce una excitación mecánica tisular por pulsos acústicos de corta duración (< 1 ms) en una región de interés (ROI), los cuales producen una distorsión tisular que produce ondas de corte transversales al ROI, que es un área definida de 10 x 6 mm. La Vc se expresa en metros por segundo (m/s) con un rango que va desde 0,5 hasta 5,5 m/s (18).
Los reportes de evaluación pancreática por la técnica ARFI se han ido incrementando en los últimos 3 años (12-22), debiendo señalar que actualmente solo se puede utilizar con un equipo ultrasonográfico percutáneo y no con USE. Yashima y cols. (19) presentaron el primer estudio de precisión diagnóstica con ARFI entre voluntarios sanos y pacientes con pancreatitis crónica, pero teniendo como prueba de referencia estándar imágenes por resonancia magnética nuclear (RMN) y/o colangiografía retrógrada endoscópica (CPRE), y describiendo para una Vc de 1,4 m/s una sensibilidad y especificidad del 75% y 72%, respectivamente. Göya y cols. (20) también evaluaron la precisión diagnóstica pero para el diagnóstico de pancreatitis aguda en el momento del ingreso hospitalario, describiendo para una Vc de 1,63 m/s una sensibilidad y especificidad del 100% y 98%, respectivamente. Por otro lado, Mateen y cols. (21), utilizando la misma técnica, evaluaron 166 individuos con diagnósticos de pancreatitis crónica aguda y controles normales, sin lograr diferenciar controles sanos de pancreatitis crónica, pero sí de los que tenían pancreatitis aguda.
En la actualidad, la elastografía pancreática asociada a USE se considera una herramienta complementaria y útil en el diagnóstico de la PC, pudiendo incluso clasificar a los pacientes en función de la gravedad de la misma (23,24). Sin embargo, está por determinar sistemáticamente si técnicas con menor capacidad invasiva, como es la elastografía percutánea basada en ARFI, pudieran resultar igualmente relevantes. En este sentido, el presente estudio pretende evaluar la precisión diagnóstica de esta técnica para el diagnóstico de PC.
Material y métodos
Estudio descriptivo, observacional, transversal, abierto, monocentro que evalúa pacientes mayores de 18 años con sospecha de pancreatitis crónica sometidos a estudio por USE en el periodo de octubre de 2012 a septiembre de 2015 en la Sección de Aparato Digestivo de un hospital general universitario. En los casos no concluyentes se evaluó con resonancia magnética pancreática estimulada con secretina y contrastada con gadolinio (s-CPRM). Se excluyó a los pacientes con una lesión ocupante de espacio pancreática, prótesis biliopancreática o procedimiento quirúrgico pancreático previo, así como a los que se negaron a participar.
La USE se realizó en su mayor parte bajo sedación profunda asistida por un especialista en anestesia y se utilizó una consola Aloka modelo Alpha7 y un ecoendoscopio radial Olympus GF-UE160-AL5 (aunque en el primer año se empleó un equipo radial Olympus GF-UM 160 y una miniconsola EU-M160 EXERA). Dichos equipos no tienen elastografía y para este estudio no se planteó el uso de contrastes.
Para el diagnóstico de PC en la USE se analizaron el tipo y el número de criterios de acuerdo a los criterios estándar descritos por Wiersema y cols. (3), definiendo como diagnóstico de PC la presencia de > 4 criterios y no diagnóstico si presentaba < 4 criterios; a excepción de los que cumplían criterios por s-CPRM utilizando los Criterios de Cambridge (6) o pico de captación de contraste pancreático en la fase venosa o portal o radio de captación de contraste pancreático con gadolinio (con contraste/sin contraste) menor de 1,7. También se evaluó la severidad de la pancreatitis crónica de acuerdo a los criterios de Rosemont (4).
Para la realización de la elastografía percutánea ARFI se utilizó un equipo de ultrasonidos ACUSON S2000™ equipado con el software Virtual Touch™ Quantification: VTQ (Siemens Medical Solutions USA, Inc.). Todos los pacientes estuvieron en ayuno de por lo menos 6 horas, siendo examinados en decúbito supino mediante un transductor convexo 6C1 HD 1.5-6 Mhz colocado en el epigastrio. Se pidió al paciente que se relajara y mantuviera la respiración en espiración para cada medición, realizando 10 mediciones de ARFI-VTQ en cabeza, cuerpo y cola del páncreas luego que se obtuvo una imagen definida en márgenes y ecotextura del mismo en modo B para minimizar la interposición de gas (principalmente de cámara gástrica) y secreciones entre la sonda y el ROI. La velocidad de la onda de corte se expresó en m/s con un rango teórico de 0,5 a 5,5 m/s. El ROI permite mediciones en profundidad de hasta un máximo de 6 cm. Si no se registraba adecuadamente una medición se obtenían resultados como X.XX m/s. El software VTQ cuenta con un reporte de función, por el cual los valores de una pluralidad de mediciones realizadas en un mismo lugar son automáticamente promediadas y presentadas como media, mediana, desviación estándar e intervalo intercuantílico. Se incluyeron en el análisis las mediciones con una tasa de éxito por área evaluada de > 60%. El tiempo empleado por paciente fue de entre 10 y 15 minutos.
Para el análisis estadístico las variables continuas se describen como medias y desviación estándar (DE); las variables discretas, como proporciones o tasas, y las variables categóricas, en proporciones. Para datos que no obtuvieron distribución normal se usaron pruebas no paramétricas. La precisión diagnóstica se calculó después de realizar el análisis de la correspondiente curva ROC (receiver operating characteristic - característica operativa del receptor). Para la asociación entre la Vc y el número total de los criterios parenquimatosos y ductales del estudio pancreático se obtuvo el coeficiente de correlación de Spearman por no cumplir con la normalidad. Los valores de elasticidad en los diferentes grupos de Rosemont se intentaron comparar por un análisis de varianza (ANOVA) de una sola cola después de la demostración de distribución normal de los datos por el test de Kolmogorov-Smirnov. Después que la heterogeneidad de las varianzas fue evaluada por el estadístico de Levene, el análisis post hoc fue realizado por el test de Games-Howell para evaluar la diferencia entre grupos. Los análisis estadísticos fueron realizados usando el paquete informático IBM® SPSS® Statistics versión 21.0 para Machintosh®.
El estudio fue aprobado por el comité de investigación local y fue llevado a cabo en conformidad con la Declaración de Helsinki. Todos los participantes cumplimentaron un consentimiento informado escrito.
Resultados
En el periodo comprendido entre el 1 de octubre de 2012 y el 31 de septiembre de 2015 fueron valorados 53 pacientes con sospecha de PC estudiados mediante USE. Se diagnosticó a 31 pacientes con PC; 30 pacientes mediante USE y un paciente con s-CPRM (Cambridge 3).
De los 31 pacientes con diagnóstico de PC se excluyeron 14 (un paciente se negó a la realización de la elastografía por motivos personales, 6 por cuestiones laborales no pudieron acudir al centro hospitalario, 4 presentaban prótesis biliopancreáticas y 3 habían sido intervenidos quirúrgicamente por complicaciones locales de la PC). De los 22 con diagnóstico de USE normal, un paciente fue excluido por fallecimiento debido a una hemorragia digestiva alta varicosa, 4 declinaron participar y una paciente con índice de masa corporal de 35 fue excluida ya que no se pudo alcanzar el páncreas con el ROI por estar ubicado a gran profundidad; por lo que se evaluó finalmente a 16 personas con USE normal.
Características basales de la población evaluada
De los 53 pacientes con sospecha de pancreatitis crónica, se evaluó a 33 pacientes. La media de edad de los 33 pacientes finalmente incluidos fue de 58,3 +/- 11,8 años, rango 32-84, siendo 15 hombres y 18 mujeres. Todos ellos referían historia de malestar epigástrico o en hemiabdomen superior postprandial y un 60,6% de ellos (20 personas) tenía como síntoma predominante dolor epigástrico. La diarrea crónica definida como alteración del ritmo defecatorio mayor de 2 semanas y esteatorrea solo se manifestó en el 6,06% (2 pacientes).
En el momento de la exploración 24 personas (72,7%) no bebían alcohol o tenían un consumo moderado previo menor de 20 g/alcohol al día, y el 57,6% no fumaba (19 pacientes). Ocho pacientes reportaron episodios previos de pancreatitis aguda (24,24%) y 7 (21,2%) presentaban diabetes mellitus tipo 2. Solo 3 pacientes (9,1%) presentaron una técnica de imagen previa con calcificaciones a nivel pancreático.
En el grupo con diagnóstico de pancreatitis crónica, la media en años fue de 58,76 (DE ± 13,58) y en el grupo control, de 57,81 (DE ± 10,08) sin diferencias significativas (p = 0,821). Se logró identificar un factor de riesgo relevante en 13 (76,5%) de los casos diagnosticados como pancreatitis crónica: 4 (23,5%) asociados al tabaco, 7 (41,2%) asociados a tabaco y alcohol, 2 (11,8%) a hiperlipidemia y pancreatitis recidivante. En 4 pacientes (23,5%) no fuimos capaces de determinar la causa.
Características ecoendoscópicas
De los 16 pacientes con PC evaluados por USE, 8 (50%) presentaron 4 criterios USE; 6 (37,5%) presentaron 5 criterios y 2 (12,5%) presentaron 7 criterios. Asimismo, utilizando la clasificación de Rosemont se pudo estratificar en consistente con pancreatitis crónica a 7 pacientes (43,8%); sugerente de pancreatitis crónica a 6 (37,5%), e indeterminado para pancreatitis crónica a 3 (18,8%). Estos últimos 3 pacientes presentaron 4 criterios USE estándar para pancreatitis crónica, 3 parenquimatosos menores y 1 criterio ductal menor.
En el grupo de pacientes en los que se descartó pancreatitis crónica mediante USE (16 pacientes) el 12,5% (2 pacientes) presentó solo 1 o 2 criterios parenquimatosos USE; el resto (14 pacientes: 87,5%) no presentó ninguna alteración por USE.
Elastografía pancreática por técnica de fuerza de impulso de radiación acústica ARFI
Se obtuvieron media, mediana, desviación estándar y rango en cada una de las 30 mediciones de velocidad de corte (Vc) por sujeto; 10 en cabeza, cuerpo y cola del páncreas, respectivamente.
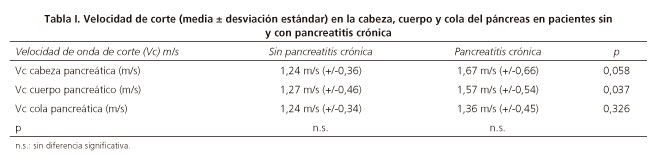
Se encontraron diferencias significativas entre las medias de Vc medidas en el cuerpo pancreático entre los pacientes con PC y exploración USE normal (p = 0,037), mas no así en las mediciones realizadas en cabeza (p = 0,058) y cola pancreática (p = 0,326), teniendo en cuenta el estadístico U de Mann-Withney para muestras con heterogeneidad de varianzas según la prueba de Levene (Tabla I).
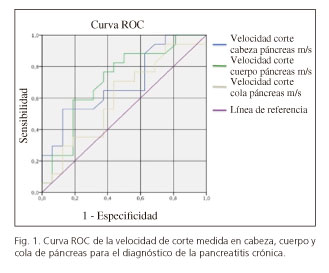
Se realizó un análisis de curva ROC de las velocidades de corte en cabeza, cuerpo y cola de páncreas, obteniendo un área bajo la curva (ABC) de 0,695 (IC 95% 0,514-0,876), 0,713 (IC 95% 0,532-0,895) y 0,601 (IC 95% 0,404-0,798), respectivamente (Fig. 1).
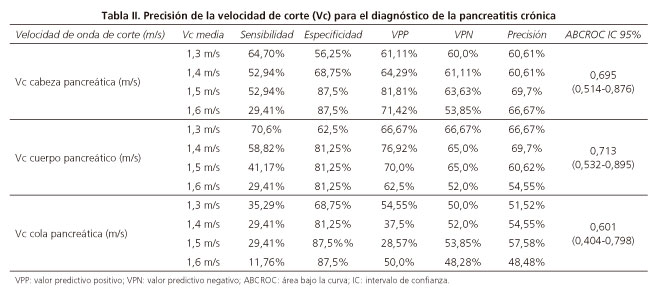
La precisión diagnóstica de la Vc para el diagnóstico de PC se muestra en la tabla II. Al evaluar las curvas ROC de las Vc, se concluye que una Vc > de 1,4 m/s medida en el cuerpo pancreático tiene una sensibilidad de 58,8% pero un valor predictivo positivo de 76,92% y 65,0% de valor predictivo negativo para el diagnóstico de PC, con un área bajo la curva (AUCROC IC 95%) de 0,713 (0,53-0,89).
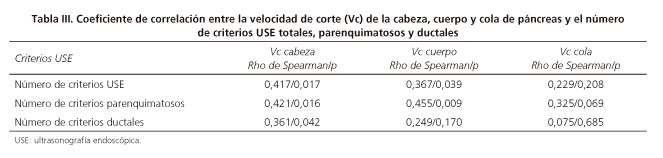
Se evaluó la correlación entre el número de criterios USE totales y la Vc en cabeza, cuerpo y cola, obteniendo un coeficiente de correlación de Spearman rs de 0,417, 0,367 y 0,229, respectivamente (Tabla III). Se excluyó en el análisis a la paciente diagnosticada con pancreatitis crónica mediante RMN estimulada con secretina y contrastada con gadolinio.
Se evaluó la diferencia de Vc en cabeza, cuerpo y cola de páncreas entre un paciente sin y con PC de acuerdo a la clasificación de Rosemont. Se detectó heterogeneidad de las varianzas por el estadístico de Levene; por lo que se realizó un análisis post ad hoc, utilizando las correcciones de Games-Howell (Tabla IV).
En el grupo de pacientes con PC no se detectaron diferencias en la Vc de cabeza, cuerpo y páncreas cuando se evaluó la etiología. La Vc en las diferentes partes del páncreas en los pacientes con consumo moderado/alto de alcohol fue similar a la de los pacientes sin consumo o con bajo consumo. Asimismo, no se encontraron diferencias en el número de criterios USE entre los que tenían un consumo mínimo o ausente de alcohol (< 20 g/día) y aquellos con un consumo moderado-severo (> 20 g/día).
La Vc en PC no dependía de la edad del paciente. Ni la Vc ni el número de criterios USE fueron significativamente diferentes al dividir a los pacientes en menores de 65 años y con edad > 65 años.
Discusión
Presentamos los resultados de la precisión diagnóstica de un método de diagnóstico no invasivo basado en elastografía percutánea para el diagnóstico de la PC. De los 31 casos de PC reclutados, 14 se excluyeron por diferentes motivos; en la mitad de ellos se debió a que tenían complicaciones locales propias de dicha patología, por lo que los casos más severos de PC no se pudieron evaluar mediante elastografía percutánea y podrían haber dado valores más altos en las mediciones elastográficas, lo que pudo haber mejorado la precisión diagnóstica.
La Vc se obtuvo de mediciones realizadas en las tres principales partes del páncreas (cabeza, cuerpo y cola) tanto en los pacientes normales como con PC. Entre las tres partes pancreáticas del grupo normal no hubo diferencias, pero en los pacientes con PC sí se observaron, aunque no se alcanzó diferencia significativa, probablemente por el limitado número de pacientes.
Al comparar las medidas de Vc de las diferentes partes del páncreas entre los pacientes sin y con pancreatitis crónica resultaron diferencias en todas ellas, pero solo se alcanzaron diferencias significativas en las mediciones realizadas en el cuerpo (1,27 m/s vs. 1,57 m/s; p = 0,037) (Tabla I). La sensibilidad descrita para la ultrasonografía convencional varía entre 52% y 86% (24), principalmente por la presencia de cambios morfológicos groseros como calcificaciones o dilatación marcada de los conductos pancreáticos, lo que refleja principalmente valoraciones realizadas en estadios avanzados. Hay que señalar que, en nuestra serie, la media de criterios USE fue de 4,6 criterios y se excluyeron los estadios más avanzados ya que desde el inicio no cumplían los criterios de inclusión de evaluación elastográfica. Se ha establecido el número óptimo de alteraciones parenquimatosas y ductulares para el diagnóstico de PC por USE, con una sensibilidad y especificidad elevadas (3,4), pero al evaluar a pacientes con enfermedad en estadios iniciales la sensibilidad se reducía hasta un 86% (24).
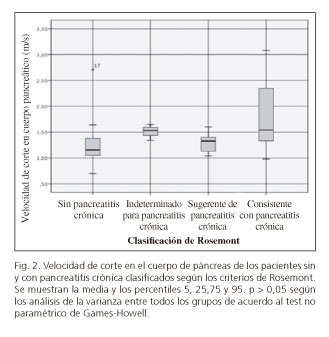
Utilizando la histología como referencia, se han evaluado los criterios USE para PC no calcificante reportando sensibilidades de entre el 75-91% y especificidades del 85-100% (7-11). Pero estos estudios tienen muchas limitaciones, como la de inclusión de pacientes con alta probabilidad pre-prueba de PC en la presencia de altos factores de riesgo (7), inclusión de pacientes con resecciones quirúrgicas por cáncer (8) y variabilidad en el número de criterios utilizados para definir PC por USE e histología (9). Nuestra serie encontró una correlación significativa entre el número de criterios USE, principalmente los parenquimatosos y las Vc a nivel de cabeza y cuerpo de páncreas (Tabla III). No obstante, cuando se evalúa la severidad de la PC, no encontramos diferencias significativas entre las Vc en los diferentes estadios (Tabla IV); a pesar de ello, se puede observar que existe una tendencia general a poder diferenciar los pacientes normales de los que tienen PC avanzada (Fig. 2). Esta diferenciación grosera recuerda al poder discriminativo de los estudios de elastografía de transición hepática, diferenciando claramente la ausencia de ella (F0) y estadios iniciales (F1) de los avanzados (F4), siendo difícil determinar los estadios intermedios (F2,F3).
La elastografía asociada a USE es una técnica que demuestra alta precisión para el diagnóstico diferencial de tumores sólidos pancreáticos y masas inflamatorias con una sensibilidad del 100% y especificidad del 88%-96% (23-28). Itokawa y cols. (27) introdujeron el concepto de strain ratio (razón de distorsión: SR) como un método semicuantitativo para evaluar objetivamente la dureza tisular, que no es más que la relación de las distorsiones producidas por una fuerza sobre dos áreas en estudio contiguas. En 2013 (23), Iglesias-García y cols., mediante elastografía-USE, utilizaron el SR y obtuvieron una precisión diagnóstica del 91,1% para PC con un punto de corte de SR de 2,25, describiendo una correlación directa entre el SR y los diferentes estadios de PC según la clasificación de Rosemont. La elastografía por USE, a pesar de obtener una alta precisión diagnóstica utilizando métodos indirectos de cuantificación, no deja de ser operador dependiente y con un grado de relativa invasividad.
En 2012, Yashima y cols. (19), utilizando la tecnología ARFI, presentaron un estudio en 52 voluntarios sanos y 46 con PC describiendo los valores de corte para diferenciar sanos de enfermos, con una sensibilidad, especificidad, valor predictivo positivo y valor predictivo negativo del 75%, 72%, 69% y 78%, respectivamente. Debemos señalar que la forma de diagnóstico que utilizaron para PC fue basada en técnicas de CPRE y/o de RMN, sin una descripción morfológica por USE, al tiempo que más del 70% de pacientes con PC presentaban un estadio avanzado. Siguiendo con el análisis de los criterios de inclusión, la falta de estudio morfológico por USE en los pacientes clasificados como normales en el estudio de Mateen y cols. (21), pero con historia de molestias abdominales, podría explicar la ausencia de diferencias en la Vc entre ellos y los clasificados como pancreatitis crónica, entendiendo una mala clasificación inicial no intencionada.
No pudimos evitar el sesgo de selección ya que se excluyó a los pacientes con complicaciones locales pancreáticas, que requirieron procedimientos endoscópicos o alguna técnica quirúrgica pancreática, los cuales podrían falsear los datos de rigidez pancreática. Otro sesgo de nuestro estudio fue haberlo realizado solo en un centro hospitalario y no ser ciego. Esto se debe principalmente al hecho de haber realizado el estudio en el escenario de práctica clínica real y tratarse de una patología con baja incidencia y prevalencia. Asimismo, debe tenerse en cuenta el desfase temporal entre la realización de la USE y la realización de la elastografía.
La fibrosis pancreática, que probablemente es la principal causa de rigidez pancreática en PC, no se considera sinónimo de enfermedad ya que existen otras causas de fibrosis pancreática, entre ellas la edad avanzada, el consumo de alcohol, de tabaco, etc. En nuestro grupo de pacientes con PC no se detectaron diferencias cuando se compararon la edad (mayor o menor de 65 años), el consumo de alcohol (menor o > 20 g/día), la etiología de la PC, y las medias de la Vc y el número de criterios USE, lo cual puede ser consecuencia del limitado número de pacientes evaluados.
En conclusión, a pesar de presentar un número reducido de pacientes, hemos conseguido correlacionar de manera significativa los hallazgos morfológicos obtenidos mediante USE en PC con los resultados elastográficos percutáneos no invasivos. Si se mejorara la precisión diagnóstica obtenida para esta última técnica para el diagnóstico de PC con un mayor número de pacientes evaluados, la ausencia de efectos adversos y la excelente tolerancia justificarían la generalización de su uso inmediatamente después de establecerse la sospecha diagnóstica, e incluso para seguimiento evolutivo de los mismos.
Agradecimientos
Agradecemos a todo el personal de la sección de Aparato Digestivo del Hospital General Universitario Rafael Méndez por facilitar la realización del presente estudio.
![]() Dirección para correspondencia:
Dirección para correspondencia:
Camilo Julio Llamoza-Torres.
Sección de Aparato Digestivo.
Hospital General Universitario Rafael Méndez.
Ctra. Nacional 340, km. 589. 30817 Lorca, Murcia.
e-mail: info@llamozatorres.com
Recibido: 17-11-2015.
Aceptado: 12-04-2016
Bibliografía
1. Luaces-Regueira M, Iglesias-García J, Lindkvist B, et al. Smoking as a risk factor for complications in chronic pancreatitis. Pancreas 2014;43:275-80. DOI: 10.1097/01.mpa.0000437324.52598.ee. [ Links ]
2. Domínguez-Muñoz E, Lucendo A, Carballo F, et al. Estudio español multicéntrico de estimación de la prevalencia e incidencia de la pancreatitis crónica y sus complicaciones. Rev Esp Enferm Dig 2014;106(4):239-45. [ Links ]
3. Wieserma MJ, Hawes RH, Lehman GA, et al. Prospective evaluation of endoscopic ultrasonography and endoscopy retrograde cholangiopancreatography in patients with chronic abdominal pain of suspected pancreatic origin. Endoscopy 1993;25:555-64. DOI: 10.1055/s-2007-1010405. [ Links ]
4. Catalano MF, Sahai A, Levy M, et al. EUS-based criteria for the diagnosis of chronic pancreatitis: The Rosemont classification. Gastrointest Endosc 2009;69:1251-61. DOI: 10.1016/j.gie.2008.07.043. [ Links ]
5. Stevens T, López R, Adler DG, et al. Multicenter comparison of the interobserver agreement of standard EUS scoring and Rosemont classification scoring for the diagnosis of chronic pancreatitis. Gastrointest Endosc 2010:71:519-26. DOI: 10.1016/j.gie.2009.10.043. [ Links ]
6. Balci C. MRI assessment of chronic pancreatitis. Diagn Interv Radiol 2011;17:249-54. [ Links ]
7. Albashir S, Bronner MP, Paris MA, et al. Endoscopic ultrasound, secretin endoscopic pancreatic function test, and histology: Correlation in chronic pancreatitis. Am J Gastroenterol 2010;105:2498-503. DOI: 10.1038/ajg.2010.274. [ Links ]
8. Varadarajulu S, Eltoum I, Tamhane A, et al. Histopathologic correlates of noncalcific chronic pancreatitis by EUS: A prospective tissue characterization study. Gastrointest Endosc 2007;66:501-9. DOI: 10.1016/j.gie.2006.12.043. [ Links ]
9. Chong AK, Hawes RH, Hoffman BJ, et al. Diagnostic performance of EUS for chronic pancreatitis: A comparison with histopathology. Gastrointest Endosc 2007;65:808-14. DOI: 10.1016/j.gie.2006.09.026. [ Links ]
10. Le Blanc LJ, Chen JH, Al Haddad M, et al. Endoscopy ultrasound and histology in chronic pancreatitis: How are they associated? Pancreas 2014;43(3):440-4. [ Links ]
11. Vega-Peralta J, Attam R, Arain MA, et al. Correlation of EUS with histopathology in 50 patients undergoing total pancreatectomy (TP) with islet autotransplantation (IAT) for minimal change chronic pancreatitis (MCCP). Gastrointest Endosc 2011;73Suppl:AB324. DOI: 10.1016/j.gie.2011.03.675. [ Links ]
12. Shiina T. JSUM ultrasound elastography practice guidelines: Basics and terminology. J Med Ultrasonics 2013:40:309-23. DOI: 10.1007/s10396-013-0490-z. [ Links ]
13. Itoh Y, Takehara Y, Kawase T, et al. Feasibility of magnetic resonance elastography for the pancreas at 3T. J Magn Reson Imaging 2015 Jul 7. DOI: 10.1002/jmri.24995. [ Links ]
14. Hirooka Y, Kuwahara T, Irisawa A, et al. JSUM ultrasound elastography practice guideline: Pancreas. J Med Ultrasonics 2015;42:151-74. DOI: 10.1007/s10396-014-0571-7. [ Links ]
15. Hirooka Y, Itoh A, Hashimoto S, et al. Utility of EUS:elastography in the diagnosis of pancreatic diseases. Gastrointest Endosc 2005;61:AB282. DOI: 10.1016/S0016-5107(05)01447-1. [ Links ]
16. Uchida H, Hirooka Y, Itoh A, et al. Utility of elastography in the diagnosis of pancreatic diseases using transabdominal ultrasonography. Gastroenterology 2005;128:A536. DOI: 10.1016/S0016-5107(05)01447-1. [ Links ]
17. Gennisson JL, Deffieux T, Fink M, et al. Ultrasound elastography: Principles and techniques. Diagnostic and Interventional Imaging 2013;94:487-95. DOI: 10.1016/j.diii.2013.01.022. [ Links ]
18. Friedrich-Rust M, Schlueter N, Smaczny C, et al. Non-invasive measurement of liver and pancreas fibrosis in patients with cystic fibrosis. J Cyst Fibros 2013;12(5):431-9. DOI: 10.1016/j.jcf.2012.12.013. [ Links ]
19. Yashima Y, Sasahira N, Isayama H, et al. Acoustic radiation force impulse elastography for noninvasive assessment of chronic pancreatitis. J Gastroenterol 2012:47:427-32. DOI: 10.1007/s00535-011-0491-x. [ Links ]
20. Göya C, Hamidi C, Hattapoğlu S, et al. Use of acoustic radiation force impulse elastography to diagnose acute pancreatitis at hospital admission. J Ultrasound Med 2014;33:1453-60. DOI: 10.7863/ultra.33.8.1453. [ Links ]
21. Mateen M, Muheet K, Mohan R, et al. Evaluation of ultrasound based acoustic radiation force impulse (ARFI) and eSie touch Sonoelastography for diagnosis of inflammatory pancreatic diseases. J Pancreas 2012;13(1):34-44. [ Links ]
22. Kawada N, Tanaka S, Uehara H, et al. Potencial use of point shear wave elastography for the pancreas: A single center prospective study. Eur J Radiol 2014;83:620-4. DOI: 10.1016/j.ejrad.2013.11.029. [ Links ]
23. Iglesias-García J, Domínguez-Muñoz E, Castiñeira-Alvariño M, et al. Quantitative elastography associated with endoscopic ultrasound for the diagnosis of chronic pancreatitis. Endoscopy 2013;45:781-8. DOI: 10.1055/s-0033-1344614. [ Links ]
24. Kelly KA, Hollingsworth MA, Brand RE, et al. Advances in biomedical imaging, bioengineering, and related technologies for the development of biomarkers of pancreatic diseases. Pancreas 2015;44(8):1185-94. DOI: 10.1097/MPA.0000000000000552. [ Links ]
25. Giovannini M, Hookey LC, Bories E, et al. Endoscopic ultrasound elastography: The first step towards virtual biopsy? Preliminary results in 49 patients. Endoscopy 2006;38:344-8. DOI: 10.1055/s-2006-925158. [ Links ]
26. Janssen J, Schlörer E, Greiner L. EUS elastography of the pancreas: Feasibility and pattern description of the normal pancreas, chronic pancreatitis, and focal pancreatic lesions. Gastrointest Endosc 2007;65:971-8. DOI: 10.1016/j.gie.2006.12.057. [ Links ]
27. Itokawa F, Itoi T, Sofuni A, et al. EUS elastography combined with the strain ratio of tissue elasticity for diagnosis of solid pancreatic masses. J Gastroenterol 2011;46:843-53. DOI: 10.1007/s00535-011-0399-5. [ Links ]
28. Mei M, Ni J, Liu D, et al. EUS elastography for diagnosis of solid pancreatic masses: A meta-analysis. Gastrointest Endosc 2013;77(4):578-89. DOI: 10.1016/j.gie.2012.09.035. [ Links ]











 texto en
texto en