INTRODUCCIÓN
Existen pocos trabajos controlados sobre calidad en relación a la colangiopancreatografía retrógrada endoscópica (CPRE). Y es paradójico, pues se trata del procedimiento endoscópico con mayor morbimortalidad, así como el que más demandas judiciales genera 1,2.
Conocer el nivel de calidad, en este aspecto o en cualquier otro, exige medir los aspectos más relevantes de la atención que ofrecemos, habitualmente en forma de indicadores. Los indicadores de calidad pueden dividirse en tres categorías: "estructura", "proceso" y "resultados" 3. "Estructura" engloba todo lo relativo a los atributos estables en los que se da la asistencia, tanto materiales como organizativos; "proceso" comprende todo lo que se hace por los pacientes y la habilidad con que se hace; "resultado" se refiere a lo que beneficia a los pacientes, cambio en la salud que pueda ser atribuido a la asistencia recibida.
En este contexto, la Sociedad Española de Patología Digestiva (SEPD) ha emprendido un proyecto para aportar indicadores de calidad y seguridad útiles sobre los procedimientos de endoscopia digestiva, adaptados a nuestro medio y referidos según niveles de evidencia 4,5. En este trabajo se proponen los procedimientos e indicadores de calidad para la CPRE.
METODOLOGÍA
El trabajo, siempre inmerso en el mencionado proyecto de la SEPD 4, se desarrolló de manera análoga a este. En primer lugar, se formó un grupo multidisciplinar que revisó la bibliografía y diseñó el procedimiento para CPRE. Su propuesta fue revisada por un panel de profesionales seleccionados desde la SEPD hasta alcanzar una versión definitiva. Posteriormente, se elaboraron cuadros de indicadores para estos procedimientos.
Estrategias de búsqueda y selección de estudios
La estrategia de búsqueda y selección fue global para todo el proyecto de la SEPD y se detalla en su producto inicial 4). Se han hecho dos búsquedas básicas: una de GPC y otra de artículos originales y revisiones. Además, de forma secundaria se revisaron las bibliografías de los estudios incluidos, de las revisiones más significativas y de las guías clínicas y metaanálisis publicados. Las referencias detectadas fueron revisadas por pares y seleccionadas si contenían recomendaciones para la correcta preparación, ejecución y seguimiento de la prueba, o incluían indicadores de calidad relacionados con estructura, proceso o resultado.
Diseño de los procedimientos de endoscopia
A partir de la bibliografía seleccionada y la experiencia de los autores se recopilaron y ordenaron las actividades necesarias para el procedimiento. No se incluyeron los procedimientos comunes a toda exploración endoscópica ni la descripción de técnicas específicas que pudieran aplicarse en algunas situaciones. El resultado se diagramó empleando diagramas de vías paralelas. Las propuestas del grupo fueron revisadas y criticadas por un panel de profesionales seleccionados desde la SEPD hasta alcanzar una versión definitiva.
Construcción de los indicadores
Para conseguir indicadores válidos se valoró la calidad del conocimiento disponible de las actividades incluidas en los procedimientos y los documentos seleccionados en la búsqueda. Para ello se utilizó la filosofía de graduación de la calidad del conocimiento disponible del modelo GRADE como alta, moderada, baja y muy baja 6,7.
Para asegurar la fiabilidad y facilitar el cálculo de los indicadores, cada uno de ellos se acompaña de una ficha que incluye: ámbito de aplicación (procedimientos en los que se aplica); denominación; fórmula de cálculo; tipo de indicador y relación temporal con la prueba (preprocedimiento, procedimiento, posprocedimiento); dimensión de la calidad con que se relaciona; justificación, exclusiones y aclaraciones; y nivel de evidencia que lo sustenta.
Quedan excluidos los indicadores comunes a las pruebas de endoscopia digestiva, que se desarrollan en otro trabajo 4, si bien hacemos alguna referencia complementaria en algunos de ellos por tener peculiaridades muy específicas de la CPRE.
RESULTADOS Y DISCUSIÓN
Procedimiento de CPRE
Su misión es maximizar la calidad y seguridad de la prueba para favorecer el diagnóstico y tratamiento de los pacientes, optimizando los resultados en salud que se derivan de ella (Fig. 1). Comprende las actividades siguientes:
1. Situar al paciente. Existen tres posiciones útiles: usualmente se sitúa en oblicuo lateral izquierdo prono, aunque es posible utilizar la estándar (decúbito lateral izquierdo) o el prono.
2. Empleo de sedación profunda o anestesia general.
3. Comprobar correcto funcionamiento del duodenoscopio. Debe ofrecer una visión adecuada y de calidad, y han de ser operativos la angulación del extremo, la uña elevadora y los mecanismos de aire y agua y de succión.
4. Preparar equipo de escopia y enfocar en hipocondrio derecho.
5. Lubricar duodenoscopio.
6. Insertar duodenoscopio:
Entrada a ciegas hasta visualizar imagen pilórica en "sol naciente".
Rotación izquierda para acometer bulbo.
Rotación derecha para acceder a segunda porción.
Enfocar papila.
Girar mando pequeño en sentido horario y grande en antihorario.
Rectificación del tubo en sentido horario.
Si no hay éxito, utilizar la vía larga: seguir introduciendo el tubo para aumentar la curvatura gástrica hasta enfrentar papila
7. Observar y describir anomalías en zona papilar: infiltraciones mucosas difusas, patología papilar, divertículos, pólipos y ampulomas. En este último caso hay que biopsiar para ayudar a la estadificación, si no está realizado.
8. Canulación biliopancreática:
Usar preferentemente canulotomo o esfinterotomo con guía para disminuir las complicaciones.
Direccionar la cánula al conducto deseado: vía biliar, entre las 11 y la 1; vía pancreática, entre la 1 y las 2.
Comprobar situación y avance mediante escopia (dirección de guía y contraste), intentando no utilizar contraste hasta tener seguridad de estar en el conducto deseado.
Si no es posible acceder al conducto deseado tras cinco intentos (canulación difícil), valorar precorte. Si se pretende y no se consigue entrar en vía biliar, valorar doble guía (dejar guía en páncreas, retirar y reintroducir esfinterotomo con nueva guía), colocación de prótesis de páncreas o suspensión de la prueba. En este último caso, se puede repetir más adelante o desistir de la prueba para usar ecoendoscopia con técnicas de rendez-vous o drenaje.
9. Actuar en función de los hallazgos:
En vía biliar, dejar guía para asegurar la vía y el recambio de dispositivos, y valorar esfinterotomía. Además:
-En caso de coledocolitiasis visualizada o de sospecha, se valorará el paso de balón o el uso decestas de Dormia. Si fracaso, valorar practicar esfinteroplastia con balón o colocación de prótesis. -Estenosis tumoral: toma de muestra y colocación de prótesis. -Estenosis no tumoral: dilatación con o sin prótesis. -Fístulas o fugas biliares: esfinterotomía con o sin prótesis.
En vía pancreática, si se encuentra estenosis se practicará dilatación con o sin prótesis. En caso de litiasis, proceder a su extracción con balón o cesta.
Ante dudas diagnósticas se puede acudir a la colangioscopia directa o indirecta.
10. Retirar el tubo. Maniobrar lentamente con la precaución de aspirar aire y contenido gástrico al extraer.
11. Finalizar exploración. Se retira completamente el tubo, que se pasa al personal auxiliar para su limpieza y nueva preparación. Valorar profilaxis antibiótica.
Indicadores
Se han incluido un total de 26 indicadores (Tabla 1), de los cuales siete son de estructura (son comunes a todos los procedimientos), 17 son de proceso y dos corresponden a resultado. La relación completa de indicadores se recoge en la Tabla 2, si bien solo vamos a desarrollar los siguientes por considerarlos distintivos de la técnica: de proceso-preprocedimiento (profilaxis antibiótica y valoración de dificultad del procedimiento [grado de Schutz]) y de proceso-procedimiento (canulación profunda del ductus en papila nativa, extracción de coledocolitiasis, resolución de estenosis y estimación de la radiación). También se han desarrollado dos indicadores de resultado de efectos adversos, la pancreatitis post-CPRE y la hemorragia post-CPRE, por considerarlos muy específicos y con carga asistencial.
Tabla 1 Indicadores de calidad en la colangiopancreatografía retrógrada endoscópica (en negrita, los que se desarrollan en el texto)

La numeración es consecutiva a la establecida para marcadores de la colonoscopia (5), pues se trata de un mismo proyecto.
No se ha incluido ningún indicador referido al volumen de CPRE por centro que suele recomendarse en algunas guías, ya que se trata más de un indicador de "cantidad" que de "calidad". Además, lo que se pretende medir con él es la experiencia o entrenamiento del endoscopista, aspecto que ya se tiene en cuenta y se incluye entre los indicadores comunes a toda endoscopia 4).
Lógicamente, no todos los indicadores tienen el mismo peso. De hecho, la Asociación Americana de Endoscopia Gastrointestinal (ASGE) define unos indicadores para CPRE como prioritarios, los cuales estiman como esenciales para obtener buenos resultados, que incluyen los siguientes: indicación adecuada, canulación del ductus, extracción de litiasis y pancreatitis post-CPRE 8.
Debemos recordar que en el sistema GRADE, empleado para valorar la evidencia que sustenta estos indicadores, el grado "alto" de evidencia se corresponde con estudios aleatorizados bien diseñados, que son escasos en este ámbito. Como consecuencia, el grado de evidencia en ellos se polariza en los extremos ("muy alta" o "baja") y se obtiene, en el primer caso, sobre todo a partir de guías clínicas. Por eso muchos de los indicadores seleccionados coinciden con las de estas. Los estudios aleatorizados de evidencia moderada u otros tipos de diseño son escasos.
Como aclaración a la numeración aportada de los indicadores (Tabla 1), es consecutiva a la ya iniciada en los dos artículos previos para indicadores generales 4 y de colonoscopia 5.
B.07. Profilaxis antibiótica
Existen guías clínicas que recomiendan profilaxis antibiótica en ciertos casos, como la obstrucción biliar conocida o probable, fístulas biliares o pancreáticas, pseudoquistes o necrosis pancreáticas, pacientes inmunodeprimidos portadores de trasplante hepático y colangitis bacteriana activa 8,9. En una revisión Cochrane de 2010 se concluye que los antibióticos profilácticos reducen la bacteriemia y parecen prevenir la colangitis, la pancreatitis y la septicemia en los pacientes sometidos a CPRE electiva, aunque en el subgrupo de pacientes con CPRE sin complicaciones el efecto de los antibióticos puede ser menos evidente 10. En una revisión reciente 11, la Asociación Americana de Endoscopia Gastrointestinal (ASGE) no recomienda profilaxis antibiótica cuando no hay sospecha de obstrucción del tracto biliar o se prevé un drenaje biliar completo, y sí en caso contrario y en pacientes con trasplante hepático. Los antibióticos a utilizar han de proporcionar cobertura frente a la flora biliar (como enterococos y gérmenes Gram negativos).
B.08. Valoración de dificultad del procedimiento (grado de Schutz)
Para poder conocer la efectividad de un procedimiento como la CPRE es esencial conocer la posibilidad de éxito esperado. En este sentido, Schutz publicó una escala que intenta aportar datos de éxito esperado según la dificultad esperada del procedimiento (Tabla 2) 12. Posteriormente, un registro holandés ha analizado la influencia que dicha clasificación, recogida durante un año según un sistema estandarizado (Rotterdam Assessment Form for ERCP [RAF-E]) 13 tiene en el éxito del procedimiento, y se ha establecido que se relaciona con los niveles de dificultad (75,2%, 84,3% y 88,1%, respectivamente, para grados 3, 2 y 1), si bien se mueve en rangos estrechos.
Aquellos endoscopistas con menor volumen de procedimientos probablemente deberían realizar solo procedimientos grado 1, dejando los grados 2 y 3 para centros con mayor volumen 14,15. En este sentido la ASGE ha propuesto, basándose en esta escala, una escala de cuatro grados con recomendaciones específicas (niveles 1 y 2 para endoscopistas básicos y 3 y 4 para expertos) (16) (Tabla 3).
C.11. Canulación profunda del ductus que se quiere canular en una papila nativa
Lograr la canulación del ductus de interés (biliar, pancreático o ambos, según el caso) es la base para conseguir el éxito diagnóstico y/o terapéutico que se persigue con la prueba (8,15), por lo que debe quedar registrado en todos los casos. Se considera canulación satisfactoria cuando la guía pasa la papila y se introduce en el conducto deseado, para luego profundizar y poder inyectar contraste, a fin de visualizar todo el sistema ductal de interés. Se incluye cualquier tipo de precorte cuando falla la técnica estándar, para evitar la necesidad de una segunda endoscopia o una colangiografía percutánea.
El indicador se limita a casos de anatomía papilar normal, excluyéndose, además:
Los casos fallidos a causa de sedación inadecuada, existencia de contenido gástrico, cirugía abdominal previa como la pancreatoduodenectomía, gastroyeyunostomía y hepatoyeyunostomía, así como la obstrucción del antro o del duodeno proximal, incluyendo deformidades duodenales por pancreatitis, edema, etc.
Pacientes con esfinterotomía anterior.
La referencia en cuanto a un posible estándar viene determinada por acuerdos de grupos de trabajo y por los resultados de un metaanálisis que incluye estudios prospectivos y que establece un porcentaje de canulación del conducto biliar del 89,3% (CI 95%, 0,866-0,919) y del 84% del pancreático, independientemente del tipo de centro 17. Por otro lado, se ha visto que la posibilidad de canular depende de la experiencia del endoscopista: si hace ≤ 50 CPRE/endoscopista/año, es del 84,2%; si > 50 CPRE/endoscopista/año, del 91% (media 89%) (p < 0,001) 18. Dado que la mayor parte de los pacientes incluidos en los estudios procede de centros de referencia, hemos decidido bajar discretamente los estándares establecidos por la ASGE (> 90%) 8 por encontrar que son excesivamente optimistas y no reflejan la realidad de nuestro medio.
Un punto interesante es la consideración de vía biliar de difícil canulación y para la ESGE 19 se considera que es aquella que no se puede conseguir tras cinco intentos, tras cinco minutos o tras más de una canulación pancreática 20. Sin embargo, está claro cómo podría incluirse esta definición en este indicador de canulación profunda del ductus.
C.12. Extracción de coledocolitiasis
En los casos en que la prueba se practica con el objetivo de extraer cálculos, siempre debe quedar registrado si esto se consigue o no y aportar información suficiente sobre su tamaño y localización, así como de la existencia de constricciones o alteraciones anatómicas, como las de índole posquirúrgica 21.
El indicador se limita a casos con cálculos pequeños y anatomía normal, aunque también puede ser útil seguir esta proporción en el resto de cálculos, más difíciles de extraer.
En lo que respecta a los casos a los que se limita, deberían extraerse más del 90% de ellos, recurriendo a la ayuda de esfinterotomía y de balón o cesta.
Como ocurre con la canulación, los datos del metaanálisis muestran un éxito en la extracción del 88,3% (CI 95%, 0,825-0,941) 17. Es por ello que, como ocurre con la canulación, decidimos poner unos estándares algo más realistas que los establecidos por la ASGE (> 90%) 8,15, si bien los resultados del metaanálisis 17 probablemente incluyen todas las litiasis, independientemente de su tamaño menor de 10 mm.
Existen situaciones que aumentan la complejidad y, además del tamaño de la litiasis, se encuentran las alteraciones anatómicas asociadas, la estenosis, la imposibilidad de ser capturadas por una cesta o de hacer litotricia y el síndrome de Mirizzi 22.
C.03. Resolución de estenosis
En los casos en que la prueba se practica con el objetivo de colocar un stent por obstrucción biliar siempre debe quedar registrado si se consigue o no, si se hace esfinterotomía 23 y si se ha hecho precorte para acceder a la vía biliar 8,15, y aportar información suficiente sobre la indicación, localización de la obstrucción, así como la existencia de constricciones o alteraciones anatómicas, como las de índole posquirúrgica.
El indicador se limita a los casos expuestos, aunque también puede ser útil seguir esta proporción en el resto. Se considera como relativamente fácil la colocación de un stent en una obstrucción biliar distal al hilio y es esencial en el caso de ictericia obstructiva, sobre todo si se asocia a colangitis.
En lo que respecta a los casos a los que se limita o indica, debería poder colocarse stent en más del 90% de ellos 8,15, encontrando en los metaanálisis cifras de un 97,5% (CI 95%, 0,967-0,984) 17. Solo la dilatación de una estenosis no sería un indicador apropiado por el alto índice de recidivas.
C.14. Estimación de la radiación
El uso de fluoroscopia es inherente a la ERCP, que por ello entraña un riesgo de exposición a la radiación (tanto del paciente como de los profesionales sanitarios presentes durante la prueba) no inferior al de otras pruebas radiológicas 24. Por eso, medir el tiempo de fluoroscopia e incluir esta medición como indicador de calidad ha sido propuesto desde hace más de diez años en diferentes guías 8,25. La posibilidad de optimizar la radiación empleada sin menoscabo de la efectividad de la prueba avala su uso 26.
No obstante, es sabido que la correlación entre el tiempo de fluoroscopia y la dosis de radiación recibida es pobre 27, por lo que, cuando sea posible, es preferible utilizar otras medidas para estimarla, como el producto dosis-área (DAP) 24. Diferentes estudios avalan la posibilidad de disminuir la radiación recibida empleando el mismo tiempo de fluoroscopia 24.
E.02. Efectos adversos
Se ha demostrado que se producen menos complicaciones cuando los endoscopistas realizan más de 50 exploraciones al año 18).
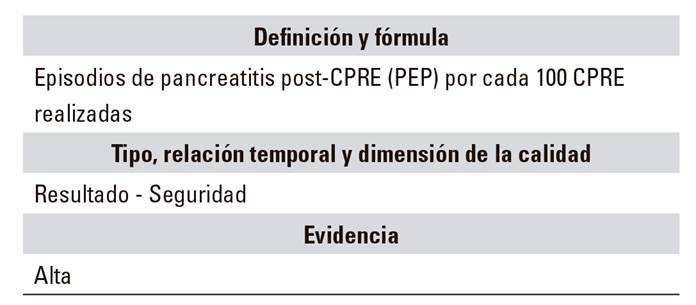
E.02.1. Efectos adversos: pancreatitis post-CPRE
Se considera por consenso una pancreatitis post-CPRE (PEP) 28 al cuadro de dolor abdominal de novo o al empeoramiento de uno prexistente, compatible con pancreatitis clínica, que tras las 24 horas siguientes a una CPRE, que cursa con elevación de la amilasa sérica (y/o lipasa) de tres veces los niveles normales y que precisa al menos dos días de hospitalización 29. Este concepto es muy importante pues se han descrito movilizaciones enzimáticas hasta en un 75% de los pacientes tras una CPRE 30. La incidencia está en un 3,5% (1,6 y un 15,7%) 31. Aunque estas cifras manejadas por metaanálisis son reales, habría que plantearse extraer las indicaciones con riesgo muy elevado (sospecha de disfunción de esfínter de Oddi) para establecer cifras más adecuadas. No existe acuerdo en las diferentes guías acerca de los estándares aceptables 8,15, si bien deberíamos movernos en cualquier caso por debajo del 7%. Existen varios factores que han demostrado un aumento del riesgo, tanto preprocedimiento como intraprocedimiento 29 (Tabla 4).
Se han definido varios métodos para reducir la incidencia 32: selección adecuada de enfermos e indicaciones, profilaxis con indometacina rectal 33,34, uso de stents pancreáticos si existe canulación pancreática inicial 35 y canulación con guía.
E.02.2. Efectos adversos: hemorragia post-CPRE
El riesgo de sangrado en la CPRE se sitúa entre el 0,5 y el 5% 36, estableciéndose el 1% como la cifra más aproximada 37 y casi siempre relacionada con la esfinterotomía endoscópica 38.
Se define como la presencia de síntomas clínicos o extravasación de sangre al tubo digestivo 39 y se debe esperar tras la esfinterotomía al menos 2-3 minutos para darle valor 40. Por otro lado, y además suele ser más grave, se ha definido también el sangrado diferido, que es la existencia de melenas o caída de hemoglobina o necesidades transfusionales en los diez días siguientes a una CPRE. Este tipo de sangrado se asocia con más facilidad al uso de antitrombóticos.
El empleo de esfinteroplastia con balón es seguro y se recomienda su uso sin esfinterotomía en pacientes con alteraciones de la coagulación o papila yuxtadiverticular 36.
La tabla 5 36 resume los factores de riesgo de sangrado en la CPRE. Se debe destacar como factor principal el uso de antitrombóticos, aunque el uso de aspirina no ha demostrado un aumento del sangrado, por lo que podría realizarse una esfinterotomía en pacientes que la usan 41,42,43.
En resumen, la CPRE es una técnica intervencionista y son indicadores de calidad asociados a la misma con una evidencia alta: el éxito en la canulación profunda del conducto deseado (biliar, pancreático o ambos), la extracción de las coledocolitiasis y la resolución de estenosis. Asimismo, tiene fuerza la medición de efectos adversos, principalmente la pancreatitis post-CPRE y la hemorragia asociada a esfinterotomía.











 texto en
texto en