INTRODUCCIÓN
Se sabe que la sedación en la endoscopia gastrointestinal disminuye el disconfort y la ansiedad del paciente, aumentando la tolerancia y aceptación de la misma, además de aumentar la satisfacción por parte del endoscopista ya que disminuye los movimientos del paciente, lo que se traduce en una mejora de la visualización de la mucosa y disminución de los riesgos en la terapéutica 1. Al no existir un protocolo de sedación específico, son numerosos los estudios realizados con los fármacos disponibles, además de guías publicadas al respecto 1,2.
Las benzodiazepinas solas o en combinación con opioides se han usado desde hace décadas constituyendo el régimen de sedación tradicional en la práctica clínica 3,4. Más recientemente el propofol ha ganado popularidad por sus características farmacocinéticas. A pesar del uso ampliamente extendido del propofol, existe cierta cautela en su administración por parte de personal no anestesista debido a que no tiene antagonista y tiene el potencial de inducir anestesia general, si bien su seguridad, en manos de endoscopistas entrenados, ha sido demostrada en numerosos estudios 5,6,7,8,9,10,11,12.
En nuestra experiencia, la realización de gastroscopias diagnósticas con bajas dosis de midazolam en combinación con propofol puede tener ventajas en cuanto a la disminución de la dosis de propofol requerida sin incrementar los efectos adversos, además de mantener altos niveles de satisfacción por el paciente. A partir de esta perspectiva, se desarrolló este estudio comparando dos estrategias de sedación intravenosa (IV) en la endoscopia digestiva alta (EDA) diagnóstica.
PACIENTES Y MÉTODOS
Se desarrolló un estudio prospectivo, randomizado y a doble ciego en el que se comparó el uso de propofol solo, con el de midazolam más propofol en la endoscopia digestiva alta (EDA) diagnóstica. Los objetivos primarios del mismo fueron la valoración de la seguridad y la eficiencia y los objetivos secundarios, la valoración de la calidad de la endoscopia y la satisfacción del paciente:
• Seguridad (frecuencia de las siguientes complicaciones: hipoxemia, bradicardia e hipotensión). Una presión sistólica menor de 80 o el descenso de 30% de su valor basal fue considerada hipotensión. Una caída mayor o igual al 20% de la frecuencia cardiaca de base se consideró bradicardia. La hipoxia fue definida como saturación de oxígeno por debajo del 90%.
• Eficiencia (tiempos transcurridos entre la administración inicial de cualquiera de los tipos de sedación IV a nuestros pacientes y su alta en el hospital). Para la evaluar el impacto de la sedación en la eficiencia en nuestra Unidad de Endoscopias, durante la prueba fueron medidos y recogidos los siguientes parámetros:
El tiempo de inducción, definido como el tiempo transcurrido desde el comienzo de la sedación hasta el comienzo de la exploración.
El tiempo de sedación, el tiempo que transcurre desde la administración de la primera dosis de sedación hasta la administración de la dosis final de la misma.
La duración del procedimiento, definida como el tiempo transcurrido entre el paso del endoscopio a través de la boca de Killian hasta su completa retirada.
La duración global de la EDA que abarca el espacio de tiempo comprendido desde que se empieza a administrar la sedación hasta la retirada del endoscopio.
El tiempo de recuperación, tiempo entre el fin de la endoscopia y el alta del paciente.
La duración global del procedimiento, definido como el tiempo transcurrido desde la administración de la primera dosis de la sedación hasta la recuperación y alta del paciente posprocedimiento.
• Calidad de la endoscopia (evaluación y puntuación de la exploración por dos endoscopistas según la adecuada visualización de la misma). Dos facultativos independientes, el endoscopista que desarrollaba la endoscopia y un segundo gastroenterólogo que estaba presente en la sala durante la misma, aunque no involucrado en el procedimiento endoscópico, evaluaban la exploración. Para ello se tomó como referencia una escala no validada pero ya utilizada para el mismo fin en el artículo publicado por Meining y cols. 13 en el 2007. La endoscopia se dividió en pasos (P1: paso del endoscopio a través de la garganta; P2: visualización del esófago; P3: valoración de los pliegues del cardias proximal; P4: paso a través del estómago hacia píloro por la curvatura inferior; P5: paso a través del anillo pilórico; P6: valoración completa del bulbo duodenal; P7: introducción y visualización de la segunda porción duodenal; P8: valoración completa de los pliegues duodenales; P9: visualización completa del antro; P10: visualización del pliegue angular; P11: realización de la maniobra de retrovisión; P12: visualización del fundus y cardias en retrovisión; P13: visualización del cuerpo gástrico y de la curvatura inferior; P14: retirada a través del esófago). Cada paso de la endoscopia fue evaluado de forma subjetiva por los endoscopistas utilizando una escala de calidad que variaba de 1 a 6 (siendo 6 excelente; 5 bueno; 4 moderado; 3 suficiente; 2 pobre; 1 inaceptable) con el propósito de ver si la calidad de la endoscopia estaba significativamente influenciada por el modo de sedación. Las puntuaciones globales para el examen completo y para los tres órganos diferentes (esófago, estómago y duodeno) también se incluyeron en la evaluación (P15: valoración general completa del tracto gastrointestinal superior; P16: valoración general del esófago; P17: valoración general del estómago; P18: valoración general del duodeno).
• Satisfacción del paciente (opinión de los pacientes expresada en un cuestionario pre-alta hospitalaria). Previo al alta, con el objetivo de medir la satisfacción de los pacientes tras la prueba, se les pasó un cuestionario acerca de la calidad de la sedación y su experiencia en general acerca de la prueba. Se usó una escala analógica visual que comprendía del cero (muy insatisfecho) al 10 (completamente satisfecho). Este cuestionario también evaluaba el grado de amnesia y la voluntad de someterse (si hubiera indicación) a este procedimiento en el futuro (Fig. 1).
Selección de pacientes
Durante un periodo de dos meses fueron incluidos en el estudio 83 pacientes con edades comprendidas entre 18 y 80 años con una clasificación de riesgo anestésico en niveles ASA I-II (American Society of Anesthesiologists), que se iban a someter a una EDA diagnóstica. Los criterios de exclusión fueron: embarazo, pacientes con abuso de alcohol y drogas, historia de enfermedad respiratoria significativa, síndrome de apnea del sueño, fallo cardiaco, pacientes que habían tomado alguna clase de medicamento con acción sedante 24 horas antes del procedimiento y aquellos que se negaron a firmar los consentimientos informados.
Protocolos de sedación
Los pacientes fueron asignados de forma aleatoria y prospectiva siguiendo una tabla de números aleatorios generada por ordenador a recibir propofol (grupo A) o midazolam más propofol (grupo B). La aleatorización se realizó con el programa Epidat 3.0. En ningún paciente fue aplicada anestesia tópica orofaríngea ni fármacos antagonistas como protocolo. Para garantizar el enmascaramiento de la secuencia de aleatorización, se trasladó la asignación de grupo a sobres numerados que permanecieron cerrados hasta el momento de la sedación. Se asignó un sobre al paciente una vez firmados los consentimientos (consentimiento de la gastroscopia, sedación y participación en el estudio), que abrió la enfermera encargada de la administración de la sedación. Esta enfermera, presente durante todo el procedimiento, preparó y se encargó de administrar la medicación. El grupo A recibió un bolo IV de placebo (suero salino); el grupo B recibió un bolo IV de 3 mg de midazolam. Tras este bolo inicial (enmascarado para paciente y endoscopistas), se administró en ambos grupos un bolo de 20 mg de propofol. A partir de aquí, bolos de 20 mg de propofol se administraron a demanda, a petición del endoscopista, durante todo el procedimiento tanto para alcanzar como para mantener la sedación adecuada. Se estableció la sedación deseada como nivel de sedación 2-3 de acuerdo a la escala de evaluación alerta/sedación [OAAS] 13.
Procedimiento endoscópico, monitorización del paciente y recogida de datos
Los procedimientos endoscópicos fueron desarrollados por 9 endoscopistas experimentados, facultativos del centro. En cada una de las endoscopias, un facultativo realizaba la endoscopia mientras otro evaluaba la misma. Todas las endoscopias fueron desarrolladas con endoscopio Olympus GIF 140(r) o GIF 160(r).
Los pacientes recibieron oxígeno en gafas nasales desde los 5 minutos anteriores al comienzo de la sedación hasta la retirada del endoscopio. La monitorización incluyó la medida no invasiva de la presión sanguínea (basal, tras la retirada del endoscopio y antes de abandonar la sala de recuperación), la frecuencia cardiaca y la saturación de oxígeno que fueron medidas con pulsioxímetro de forma continua.
Un gastroenterólogo que no realizaba la endoscopia, pero sí la evaluación del procedimiento, era además el responsable de recoger los datos relativos a la sedación administrada, los intervalos de tiempo descritos mencionados previamente y los parámetros fisiológicos del paciente.
Recuperación del paciente
Inmediatamente después del procedimiento los pacientes fueron trasladados a un área de recuperación. El tiempo de recuperación tras el procedimiento fue medido usando la escala de Aldrete (15), aplicando al paciente dicha escala a intervalos de 10 minutos tras el procedimiento. Los pacientes que alcanzaban una puntuación mayor o igual a 9 eran considerados aptos para el alta.
Aspectos éticos
El protocolo del estudio fue aprobado por el comité ético de nuestro hospital (código 201). El ensayo se realizó en condiciones de respeto a los derechos fundamentales de la persona y a los postulados éticos que afectan a la investigación biomédica con seres humanos, siguiéndose a estos efectos los contenidos en la declaración de Helsinki y sucesivas actualizaciones. Todos los pacientes firmaron un consentimiento informado para la realización de la gastroscopia, otro para la administración de la sedación y un tercero para la participación en el estudio.
Análisis estadístico
Hemos calculado que con errores alfa y beta de 0,05 y 0,20 se necesitan 40 sujetos por grupo para detectar diferencias de 5 minutos en el tiempo total de procedimiento (desviación típica de 8 minutos). Asimismo este tamaño muestral permite detectar diferencias en tiempo de inducción de 1 minuto (desviación típica esperada 1,5 minutos) 16,17.
Nuestros datos fueron analizados usando SPSS 11.5.1 y Epidat 3.0. Se desarrollaron estadísticos descriptivos de todas las variables. Se compararon las variables de calidad entre grupos con los test Chi-cuadrado de Pearson, t de Student y ANOVA para variables cualitativas y cuantitativas. Las variables con medidas repetidas en el tiempo fueron analizadas con el test de ANOVA. Las variables cuantitativas fueron evaluadas por el coeficiente de correlación de Pearson. Si la distribución de la variable no era normal, se empleaban test no paramétricos. Un valor de p menor de 0,05 fue considerado estadísticamente significativo.
RESULTADOS
Pacientes y medicación utilizada
Ochenta y tres pacientes fueron incluidos y aleatorizados. De ellos, 42 recibieron placebo más propofol (grupo A) y 41 pacientes recibieron midazolam más propofol (grupo B).
No hubo diferencias entre ambos grupos con respecto a la edad, peso, sexo y ASA (Tabla 1). Las indicaciones más comunes por las que se solicitó la EDA fueron dolor epigástrico y dispepsia sin existir diferencias en los grupos con respecto a las mismas. La dosis de propofol fue significativamente menor (p < 0,01) en los pacientes del grupo B (midazolam más propofol) en comparación con los pacientes del grupo A (propofol más placebo). La dosis media de propofol fue de 115,90 mg (SD 40,57) en grupo A y 83 mg (SD 40,34) en el grupo B (Tabla 1).
Perfil de seguridad
La interrupción del procedimiento endoscópico fue necesario solamente en cuatro casos, todos ellos pertenecientes al grupo B; dos de ellos por extravasación accidental de la vía y en los otros dos pacientes por intolerancia y agitación. Entonces se procedió a la retirada del endoscopio, se reveló el grupo al que pertenecía y se inyectó flumazenilo. Todos estos pacientes fueron incluidos en el análisis por intención de tratar, sin embargo, algunos de los datos no pudieron ser completados debido a la retirada prematura del endoscopio.
No hubo diferencias estadísticamente significativas en cuanto a la incidencia de complicaciones entre los dos grupos (Tabla 1). Las complicaciones entre ambos grupos fueron manejadas satisfactoriamente de forma conservadora. El 7,3% (3 pacientes) pertenecientes del grupo A y el 9,8% (4 pacientes) del grupo B presentaron desaturación de oxígeno transitoria menor o igual al 90%. La saturación de oxígeno más baja registrada fue del 79%. No hubo diferencias entre ambos grupos en la incidencia de desaturaciones transitorias (p = 0,15), siendo estas manejadas mediante la maniobra de tracción mandibular y el incremento del flujo de oxígeno administrado. La incidencia de bradicardia fue más alta en el grupo A (17,1%; 7 pacientes) que en el grupo B (7,5%; 3 pacientes) sin presentar diferencias significativas (p = 0,09). La hipotensión afectó al 7,3% y al 10% (3 y 4 pacientes) en el grupo A y B respectivamente, sin significación estadística (p = 0,18). Todos los episodios de hipotensión y bradicardia se autolimitaron sin requerir intervención terapéutica alguna.
Análisis de los tiempos en relación con el procedimiento
La media de tiempo de inducción (tiempo desde el comienzo de la sedación hasta el comienzo de la exploración) en el grupo placebo más propofol (grupo A) fue 4,07 minutos (SD 1,65) y en el grupo midazolam más propofol (grupo B) fue 3,00 minutos (SD 1,30), siendo la diferencia estadísticamente significativa (p = 0,001). Sin embargo, las diferencias en lo que respecta a la duración del procedimiento, el tiempo de recuperación y la duración global de la EDA no resultaron significativas (Fig. 2).

Fig. 2 Duración media expresada en minutos de: tiempo de inducción, definido como el tiempo transcurrido desde el comienzo de la sedación hasta el comienzo de la exploración; tiempo de sedación, el tiempo que transcurre desde la administración de la primera dosis de sedación hasta la administración de la última dosis; duración del procedimiento, definida como el tiempo transcurrido entre el paso del endoscopio a través de la boca de Killian hasta su completa retirada; duración global del procedimiento: el tiempo transcurrido desde la administración de la primera dosis de la sedación hasta la recuperación y alta del paciente posprocedimiento (m: minutos; ns: no significativa).
Evaluación posprocedimiento: calidad de la prueba y satisfacción del paciente
La calidad de la exploración según la puntuación dada a la evaluación endoscópica por los facultativos fue similar, sin diferencias significativas en ambos grupos independientemente de la sedación administrada (Tabla 2).
Tabla 2 Puntuación dada por cada facultativo en cada paso del desarrollo de la endoscopia
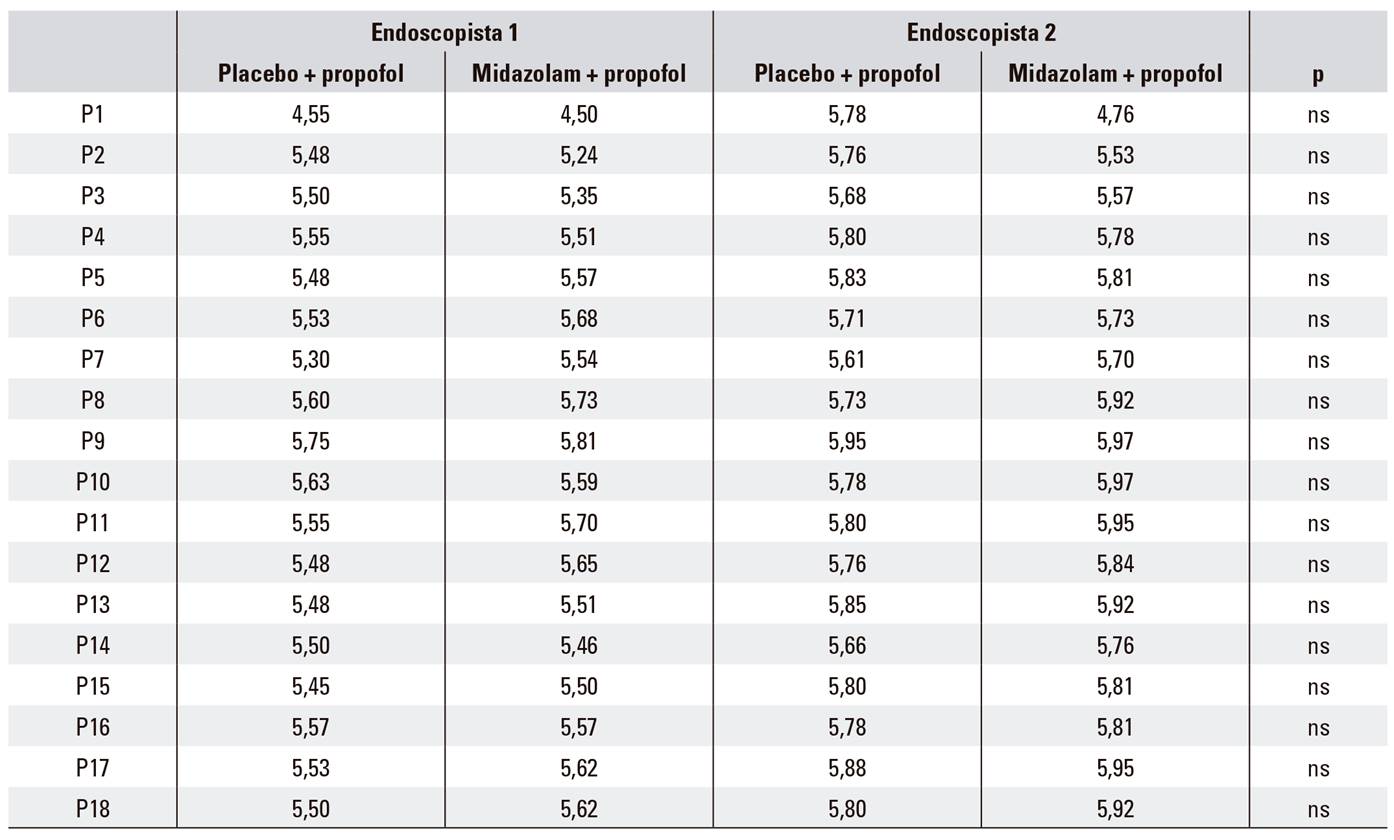
P1: paso del endoscopio a través de la garganta; P2: visualización del esófago; P3: valoración de los pliegues del cardias proximal; P4: paso a través del estómago hacia píloro por la curvatura inferior; P5: paso a través del anillo pilórico; P6: valoración completa del bulbo duodenal; P7: introducción y visualización de la 2.ª porción duodenal; P8: valoración completa de los pliegues duodenales; P9: visualización completa del antro; P10: visualización del pliegue angular; P11: realización de la maniobra de retrovisión; P12: visualización del fundus y cardias en retrovisión; P13: visualización del cuerpo gástrico y de la curvatura inferior; P14: retirada a través del esófago; P15: valoración general completa del tracto gastrointestinal superior; P16: valoración general del esófago; P17: valoración general del estómago; P18: valoración general del duodeno). Rango de puntuación: 1-6 (1 inaceptable- 6 excelente). ns: no significativa.
Los pacientes aceptaron por igual ambos métodos de sedación. El grado medio de satisfacción fue de 9,85 y 9,92 (SD 0,52 y 0,35) sobre 10 en los grupos A y B respectivamente. En el grupo A, el 7,3% (3 pacientes) mostraba algún recuerdo de la prueba; uno de ellos recordaba la entrada y dos de ellos la salida. En el grupo B, ninguno de los pacientes recordaba la prueba. Aunque no era a priori un objetivo del estudio, ambos grupos, mostraron similares propiedades amnésicas.
El 97,6% (40 pacientes) en el grupo A y el 100% (39 pacientes) en el grupo B, expresó su voluntad de repetir la exploración en un futuro si ello fuera necesario, mostrando además su conformidad con el método de sedación administrado.
DISCUSIÓN
En los últimos años, muchos estudios y metanálisis han sido publicados comparando la sedación tradicional con la sedación basada en la administración de propofol 18,19,20. Por otro lado, algunas desventajas del propofol como la sobresedación, la mayor depresión cardiorrespiratoria y el dolor en la zona de inyección, especialmente si se usa una vena de pequeño calibre 21,22,23,24, han dado lugar al desarrollo de estudios con propofol en asociación con pequeñas dosis de opioides o benzodiacepinas sugiriendo una acción sinérgica sin incremento de los efectos adversos y reduciendo la dosis total de propofol necesitada 25,26. Este protocolo, que tiene por objetivo el conseguir un nivel de sedación moderado-profundo, ha sido descrito en la literatura como sedación balanceada (SB) 27,28,29 y comparado con la administración de propofol como único fármaco sedante 29,30,31,32,33.
En nuestro estudio, la combinación de ambos fármacos, midazolam y propofol, disminuyó la dosis de propofol requerida de forma significativa, 115 mg fueron administrados en el grupo A, frente 83 mg en grupo B. Sin embargo, la dosis media de propofol en el grupo A (115 mg) parece ser menor que las descritas en otras series en las que el propofol era el único agente sedante 13,29,34,35, advirtiéndose que en estos estudios se alcanzó, en mayor medida, la sedación profunda. Respecto al midazolam, en la mayor parte de las series revisadas observamos una tendencia usar dosis más bajas que las utilizadas en este estudio en combinación con el propofol 12,29,30. La dosis de midazolam en el presente estudio fue establecida en base a la experiencia general en ese momento en nuestra Unidad. Lo mismo podemos decir respecto a la dosis de propofol.
Cuando comparamos ambos protocolos de sedación encontramos que los efectos adversos fueron escasos, poco relevantes y comparables entre ambos grupos. La depresión respiratoria y los efectos adversos cardiovasculares como hipotensión o bradicardia han sido asociados principalmente al propofol. La bradicardia constituyó el efecto adverso más frecuente en nuestra serie, sobre todo en el grupo del propofol, ocurriendo en 7 (17,1%) y 3 (7,5%) pacientes en los grupos A y B respectivamente. Estos datos demuestran la seguridad entre ambos regímenes ya descrita en otros estudios que comparaban la administración de propofol con la SB 12,29,30,31,32,33.
Nuestros datos mostraron que el protocolo SB que combinó bajas dosis de midazolam con propofol (grupo B) consiguió una sedación más rápida que el propofol administrado en monoterapia (grupo A). Esta diferencia en el tiempo de inducción, aunque estadísticamente significativa, no deja de ser algo aislado ya que no se encontró ninguna otra significación estadística en la duración del procedimiento, el tiempo de recuperación y la duración global de la EDA. El tiempo de inducción con propofol y midazolam (SB) en el grupo B, 3 minutos, se muestra similar 27,28 o menor 29,30,33 al descrito en otros estudios que emplean también SB. Cohen y cols. 36, sin embargo, encontraron que la adición de narcótico y benzodiazepina al propofol no alteraba de forma apreciable el tiempo de inducción si se comparaba con otros estudios donde se usó propofol en monoterapia. En el grupo A (propofol más placebo) el tiempo de inducción de la sedación (4,07 minutos) fue muy similar al descrito en otros estudios 30,33,18 pero en general, se han recogido tiempos de inducción menores (2-3 minutos) con propofol en monoterapia 29,34. Actualmente la tendencia es comenzar con un bolo inicial de 0,5-1 mg/kg y probablemente, de esta forma, el tiempo de inducción hubiera sido menor en el grupo A. En este sentido también se puede argumentar que al poner el midazolam se debería haber esperado 2-3 minutos para que comenzara su efecto, lo cual provocaría un tiempo de inducción más prolongado en el grupo B, pero si tras el bolo inicial de placebo en un grupo y 3 mg de midazolam en el otro se hubiera esperado 2-3 minutos, el enmascaramiento se pondría en peligro ya que el endoscopista podría intuir el efecto del midazolam mediante un mayor nivel de sedación del paciente. De cualquier forma, el tiempo que transcurre desde el comienzo de la sedación hasta la introducción del endoscopio, de 3 y 4 minutos en cada grupo respectivamente, para ese tiempo, el efecto del midazolam ya ha comenzado.
Aunque el tiempo recuperación total del paciente fue más corto al utilizar solamente propofol, las diferencias no fueron significativas. En otras series si se ha descrito la acción sinérgica al combinar propofol con midazolam prolongándose la recuperación del paciente de forma significativa 30,31,32,33. En este sentido, en el estudio desarrollado por Levitzky y cols., la SB ha mostrado ventaja de forma significativa sobre los sedantes tradicionales 27.
Una evaluación endoscópica de calidad es imprescindible para realizar un diagnóstico preciso. De esta forma hemos querido ver si la adecuada visualización endoscópica, asociada a la tolerancia a la insuflación, pudiera verse influenciada por el modo de sedación, concluyendo que no hubo diferencias entre ambos protocolos. Meining y cols. 13, usando idéntica escala, al comparar la administración de propofol en uno de los brazos con midazolam en otro, encontró que la sedación con propofol mejoraba de forma significativa la calidad de la endoscopia, produciendo el midazolam, más eructos, náuseas y menor tolerancia a la insuflación gástrica.
La satisfacción del paciente constituye una importante ventaja de la medicación. No hay validado ningún cuestionario relacionado con la satisfacción del paciente posendoscopia. El mGHAA-9 se ha usado para evaluar la satisfacción de aspectos subjetivos de los centros de endoscopias y sistemas hospitalarios pero se ha considerado insuficiente para evaluar la satisfacción de los pacientes con la sedación 37,38. La satisfacción del paciente con la sedación administrada fue similar en ambos grupos. Por lo que podemos concluir que el uso combinado del propofol con midazolam no reduce la satisfacción entre los pacientes. Algunos estudios muestran significativamente un nivel mayor de satisfacción en los regímenes de sedación que incluyen propofol 27,30,34.
La amnesia es un efecto altamente deseable por los endoscopistas. Ambos fármacos midazolam y propofol poseen efecto amnésico, aunque este último en menor grado 36. Aun sin ser significativo, el recuerdo del procedimiento fue menor en el grupo de SB, viéndose estos mismos resultados en la serie de Molina-Infante y cols. 30 en la que también se comparó la sedación con propofol en monoterapia vs. propofol y midazolam.
Nuestro estudio tiene algunas limitaciones. Una de ellas es que solamente se incluyó a pacientes con ASA I y II y la edad fue limitada a los 80 años. Otras series, sin embargo, han incluido a pacientes de más alto riesgo y mayor edad con similares resultados en cuanto a la seguridad 6,12,30,31.
Otra limitación observada es que, aunque este ensayo tenía por objetivo el mantener una sedación moderada, el nivel de sedación no fue debidamente comprobado mediante la escala de evaluación alerta/sedación [OAAS] 14 de forma reglada a intervalos de tiempo, por lo que no podemos descartar la sedación profunda en algún momento del procedimiento, sobre todo en el grupo A, ya que la SB permite más la sedación moderada que el propofol en monoterapia 18,29.
Por otra parte, la utilización de cuestionarios de satisfacción inmediatamente al finalizar los procedimientos ha demostrado que, a pesar de ser un método más simple, con más alta tasa de respuesta y probablemente más barato, sobreestima la satisfacción percibida por los pacientes ya que el grado de satisfacción decrece cuando los cuestionarios son rellenados días después de la prueba endoscópica. En este sentido, el estudio de Lin y cols. 39, que comparaba ambos escenarios concluyó que, a pesar de la debilidad mostrada en las encuestas pre-alta hospitalaria, la magnitud de las diferencias entre ambos era pequeña, resultando valores significativos en 4 de las 11 preguntas del cuestionario. En nuestro caso, el cuestionario pasado a nuestros pacientes era anónimo (el desenmascaramiento puede llevar a los pacientes a sobreestimar la sedación), pudiendo acortar las diferencias encontradas en el estudio anterior. Además el escenario para la evaluación de la satisfacción al comparar los dos protocolos de sedación ha sido el mismo (pre-alta hospitalaria), por lo que aunque exista cierta sobrestimación en los resultados no habría sesgo al comparar ambos grupos.
Otra cuestión diferente sería el posible estado de euforia causado por las benzodiazepinas pudiendo dar lugar a una puntuación mayor en cuanto al grado de satisfacción en el grupo B.
En resumen, y a pesar de las limitaciones, el protocolo de sedación utilizado en nuestro estudio de midazolam combinado con propofol proporciona los beneficios logrados de la monoterapia con propofol sin aumentar los efectos adversos, proporcionando una rápida sedación y recuperación, con similar calidad de la exploración e igual satisfacción de los pacientes, ampliando así el cuerpo existente en la literatura que muestra la seguridad en la sedación endoscópica dirigida por endoscopistas.











 texto en
texto en 




