My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Española de Cirugía Oral y Maxilofacial
On-line version ISSN 2173-9161Print version ISSN 1130-0558
Rev Esp Cirug Oral y Maxilofac vol.28 n.3 Madrid May./Jun. 2006
ARTÍCULO ESPECIAL
Documento de consenso sobre la utilización de profilaxis antibiótica en cirugía y procedimientos dentales
Consensus document on the use of antibiotic prophylaxis in dental surgery and procedures
J.L.Gutiérrez1, J. Vicente Bagán2, A.Bascones3, R.Llamas4, J.Llena5, A.Morales6, B. Noguerol7, ,
P. Planells8, J. Prieto9, J.I. Salmerón10
1 Sociedad Española de Cirugía Bucal
2 Director de la Revista Medicina Oral, Patología Oral, Cirugía Bucal
3 Sociedad Española de Medicina Oral
4 Sociedad Española de Odontología Conservadora
5 Sociedad Española de Prótesis Estomatológica
6 Sociedad Española de Implantología
7 Sociedad Española de Periodoncia
8 Sociedad Española de Odontopediatría
9 Sociedad Española de Quimioterapia
10 Sociedad Española de Cirugía Oral y Maxilofacial
Dirección para correspondencia
RESUMEN
La profilaxis antibiótica en Odontología tiene como objetivo prevenir la aparición de infección a partir de la puerta de entrada que produce la actuación terapéutica, por lo que se encuentra indicada siempre que exista un riesgo importante de infección, ya sea por las características mismas de la operación o por las condiciones locales o generales del paciente. Sin embargo, los ensayos clínicos con antibióticos en patologías dentarias responden poco a los criterios metodológicos requeridos, y además no son lo suficientemente numerosos.
Se presentan los resultados de una conferencia de expertos integrada por los Presidentes de Sociedades Científicas Españolas más representativas que han analizado la bibliografía existente y han aportado sus valiosas experiencias profesionales. Se describen las circunstancias técnicas, se analizan los fundamentos biológicos y farmacológicos y se aplican a las situaciones médicas más representativas. Se concluye que la profilaxis antibiótica en Odontología cuenta con indicaciones bien fundamentadas y precisas, ofreciendo a la comunidad científica internacional un protocolo práctico de actuación.
Palabras clave:
Profilaxis; Antibióticos; Odontología.ABSTRACT
The goal of antibiotic prophylaxis in Odontology is to prevent the onset of infections through the entranceway provided by the therapeutic action, therefore it is indicated providing there is a considerable risk of infection, either because of the characteristics of the operation itself or the patients local or general condition. Nonetheless, clinical trials with antibiotics in dental pathologies have had scant regard for the required methodological criteria and, in addition, are not sufficiently numerous. This text presents the results of an expert conference comprising the Presidents of the most representative Scientific Societies in Spain who have analyzed the existing literature and have drawn on their valuable professional experience. It describes the technical circumstances, analyzes the biological and pharmacological foundations and their application to the most representative medical situations. It is concluded that antibiotic prophylaxis in Odontology has certain well-founded, precise indications and offers the international scientific community a practical protocol for action.
Key words: Prophylaxis; Antibiotics; Dentistry.
Introducción
Clásicamente se ha considerado la profilaxis como la administración pre- o peri-operatoria de un antibiótico para la prevención de una complicación infecciosa local y/o sistémica y sus correspondientes consecuencias clínicas.
La finalidad de la profilaxis antibiótica en cirugía es prevenir la posible aparición de infección a nivel de la herida quirúrgica, creando un estado de resistencia a los microorganismos mediante concentraciones antibióticas en sangre que eviten la proliferación y diseminación bacteriana a partir de la puerta de entrada que representa la herida quirúrgica.
El 10% de las prescripciones antibióticas realizadas en nuestro país se utiliza para infecciones odontogénicas, y una parte significativa de ellas para profilaxis en cirugía y procedimientos dentales.1 Al igual que las recomendaciones acerca de la utilización de los antibióticos en el tratamiento de infecciones odontogénas, las recomendaciones de la profilaxis antibiótica no pueden basarse en ensayos clínicos (ni por ende, en la Medicina Basada en la Evidencia), ya que los ensayos clínicos con antibióticos en patologías dentarias responden poco a los criterios metodológicos requeridos, y además no son lo suficientemente numerosos para establecer una conducta. Por ello la estrategia general de prescripción antibiótica terapéutica o profiláctica se basa en acuerdos profesionales y documentos de consenso.
Las recomendaciones propuestas en este documento están basadas en el consenso de los profesionales que han participado en el desarrollo del mismo.
Fundamentos teóricos
Complicaciones a evitar
Las infecciones locales polimicrobianas son infecciones cutáneo- mucosas, dentales u óseas que se favorecen como consecuencia de procedimientos dentales invasivos,2 y que se traducen clínicamente en flemones, abscesos, pérdida de dientes, pérdida implantaria o de la estructura protésica. En un estudio llevado a cabo en nuestro país se demostró que las complicaciones subsiguientes a la extracción del tercer molar son una enfermedad infecciosa y no exclusivamente inflamatoria, ya que se encontraron diferencias estadísticamente significativas en la frecuencia de complicaciones infecciosas entre los grupos que recibieron tratamiento preventivo (5 días) o profilaxis preoperatoria (dosis única) con amoxicilina/ ácido clavulánico 2000/125 mg, y el grupo que recibió placebo (2,7; 5,3 y 16% respectivamente).3 Las tasas de complicación infecciosa eran mayores en caso de osteotomía o mayor duración del acto quirúrgico, siendo en estos casos claramente mejor el tratamiento que la profilaxis o el placebo. El inóculo infectante aumenta conforme se prolonga el tiempo del acto quirúrgico. Así la probabilidad de infección alrededor de los implantes dentales depende fundamentalmente de lo traumática o prolongada que sea la cirugía,4 considerándose que las poco frecuentes pérdidas precoces del implante,5 se deben a la contaminación durante la fase de inserción del mismo.6
Las infecciones sistémicas monomicrobianas son las infecciones que asientan en pacientes con focalidad susceptible de infectarse (alteraciones endocárdicas, prótesis óseas o articulares), en pacientes con mayor susceptibilidad para la infección sistémica por determinados microorganismos (pacientes esplenectomizados e infección por bacterias capsuladas del género Streptococcus o Haemophilus), o en pacientes con alteraciones generalizadas del sistema inmune que faciliten una septicemia (inmunodeprimidos, inmunocomprometidos y desnutridos). Generalmente, el primer paso suele ser la bacteriemia, que se produce tras un procedimiento invasivo. Esta bacteriemia se encuentra bien estudiada en la muy prevalente enfermedad periodontal (periodontitis), debido a la permeabilidad del epitelio que rodea la interfase diente-tejido, y a los niveles de prostaglandinas en la circulación local que incrementan el número de leucocitos y niveles de fibrinógeno, enlentenciendo la circulación en estos casos, lo que favorece el paso de bacterias a sangre.7 Así en modelos animales, la endocarditis subsiguiente a bacteriemia es del 48% en ratas con enfermedad periodontal versus un 6% en ratas sanas.8 En humanos, la bacteriemia subsiguiente a procedimientos invasivos se sitúa en un 51-55%.9
Balance Coste-Beneficio
El criterio del facultativo para la elección o no de profilaxis antibiótica debe basarse en el concepto de coste riesgo-beneficio. El coste económico de las maniobras profilácticas (que son usualmente de curso corto) es satisfactorio cuando se compara con el coste total del tratamiento odontológico. Evidentemente el beneficio es la prevención por parte del antibiótico de las complicaciones infecciosas subsiguientes a la cirugía y/o procedimientos. Finalmente, el riesgo de la maniobra profiláctica antibiótica es la aparición de reacciones adversas (fundamentalmente alérgicas) y la selección de resistencias.
Población bacteriana diana
La población bacteriana diana depende de la localización de la complicación infecciosa a cubrir. Así las infecciones locales tras procedimientos odontogénicos son habitualmente polimicrobianas, ya que muchas de las especies aisladas suelen ir en parejas (Bacteroides sp. y Fusobacterium; Peptostreptococcus sp. y Prevotella sp.; Prevotella sp. y Eubacterium sp.),10,11 con un fuerte componente aerobio/ anaerobio,12-14 y en mucho menor grado, microaerófilo, como corresponde a la posible contaminación/infección en el acto quirúrgico por microbiota normal de la boca y saliva, así como por odontopatógenos de enfermedad periodontal, que presenta una prevalencia muy elevada (el 50% de la población adulta presenta gingivitis y el 30% periodontitis).15
Las infecciones sistémicas a prevenir en pacientes con enfermedad de base son las subsiguientes a la bacteriemia post-manipulación dental, que se produce generalmente tras procedimientos invasivos. Esta bacteriemia es en general monomicrobiana, y se origina por la contaminación/infección por microbiota normal u odontopatógenos en el acto quirúrgico. Se sabe desde los años 30 que, tras manipulaciones dentales, el número de hemocultivos positivos a bacterias del género Streptococcus es del 75% en individuos con caries, gingivitis y periodontitis versus un 30% en sujetos sanos.16,17
Los microorganismos más frecuentemente involucrados son Streptococcus del grupo viridans, seguidos de especies coagulasa negativo (epidermidis) y coagulasa positivo (aureus, y quizá lugdunensis) del género Staphylococcus de origen oral, y por último en un 4-7% de casos, bacilos gram negativos grupo HACEK (Haemophilus, Actinobacillus, Cardiobacterium, Eikenella, Kingella), varios de ellos considerados como odontopatógenos. 19 No debe olvidarse la detección de bacteriemias por anaerobios (Eubacterium, Peptostreptococcus, Propionibacterium, Lactobacillus) en un porcentaje alto cuando se utilizan los métodos adecuados (hemocultivos para anaerobios).20,21 En la
tabla 1 se muestran los patógenos odontógenos más frecuentes.
Régimen de administración del antibiótico
El principal objetivo de la profilaxis antibiótica es alcanzar niveles elevados de antibiótico en el suero durante el proceso quirúrgico, y durante unas horas más tras el cierre de la incisión. En este sentido la dosis empleada debe ser alta, nunca inferior a la usada como tratamiento. La administración previa a la intervención quirúrgica o procedimiento puede ser suficiente en la mayoría de las intervenciones. Sólo en aquellos casos en los que la vida media del antibiótico es inferior a una hora y la duración de la intervención de 2-3 horas, o más de dos veces la vida media del antibiótico, sería necesario repetir dosis. De forma similar si se produjese una pérdida sanguinea superior a 1-2 l durante el procedimiento, debería considerarse la administración de una dosis adicional de antibiótico.22-25
Estado de salud del paciente
Los procedimientos buco-dentales invasivos (anestesias locales intraligamentarias, procedimientos endodóncicos, curetajes, sondajes, extracción dentaria simple y compleja, trasplantes/reimplantes y cirugía periapical, periodontal, ósea, implantológica, de las mucosas así como biopsia de glándulas salivales, etc.) son aquellos que conllevan riesgo de infección en sujetos sanos en algunos casos y siempre en individuos con riesgo de infección local y/o general (sujetos transplantados, con injertos, inmunodeprimidos, desnutridos, con patología asociada no controlada, etc).2,26
Los procedimientos buco-dentales no invasivos (aplicación de fluor o sellado de fisuras, cuidados protésicos no sangrantes, retirada post-quirúrgica de suturas, ortodoncia, radiología y anestesia no intraligamentaria), no presentan riesgo de infección ni en sujetos sanos ni en sujetos con riesgo y por tanto nunca son candidatos a profilaxis antibiótica.2,26
En el caso de sujetos con riesgo de infección sistémica (sujetos con riesgo de endocarditis y portadores de prótesis articulares) estará indicada la profilaxis para procedimientos invasivos, siendo verdadera profilaxis preoperatoria (no cabiendo en este caso el concepto de tratamiento preventivo),2,26 y generalmente en monodosis. En estos últimos casos es donde más se discute sobre implicaciones médico-legales, habiéndose producido litigios por ausencia de profilaxis o por la administración de antibióticos incorrectos o a tiempos incorrectos en la prevención de la endocarditis bacteriana. 27
Efectos no deseables (económicos, biológicos-resistencias, médicos-alérgicos)
Por la acción exclusiva de los antibióticos sobre estructuras bacterianas los efectos adversos no son frecuentes cuando se comparan con otro tipo de fármacos.
En general la incidencia de efectos adversos de los antibióticos o las reacciones idiosincrásicas a los mismos son poco frecuentes. Esto permite que por en ejemplo en situaciones como la profilaxis de endocarditis bacteriana en pacientes sin historia de alergia a la penicilina se puedan utilizar dosis única de amoxicilina 2 g sin temor a encontrar reacciones anafilácticas.28
La selección de resistencias en flora normal (faríngea o intestinal) depende del tipo de antibiótico utilizado, ya que la capacidad de selección de resistencias en la misma es distinta para cada compuesto,29,30 y menor con pautas cortas a dosis altas de profilaxis o tratamiento.31
Toma de decisiones (empirismo ecuacional)
En última instancia la decisión de profilaxis es potestativa del facultativo que atenderá a la ecuación: riesgo = daño x probabilidad de sufrirlo. Este enfoque es subjetivo, Ante la probabilidad, aunque sea remota, de daños irreparables, la prevención de complicaciones infecciosas sistémicas (p. ej. endocarditis infecciosa, infección tardía de prótesis articular) debe percibirse como importante por parte de los especialistas que las tratan (cardiólogos, traumatólogos, infectólogos, etc.). La prevención de complicaciones locales (p. ej. periimplantitis) como resultado de maniobras odontológicas quedará a criterio del especialista que la realiza, dada la escasez de ensayos clínicos adecuados.
Fundamentos clínicos
La aparición de una solución de continuidad en la piel, mucosa o tejidos duros de la boca como consecuencia del trauma quirúrgico o procedimental, conlleva la alteración de la principal barrera que frena la invasión de microorganismos. De esta manera los patógenos entran y pueden colonizar e infectar los tejidos profundos. Esto hace que, dependiendo del inóculo bacteriano, aumente la posibilidad de infección según sea un procedimiento o cirugía limpia, limpia-contaminada, contaminada o sucia. A mayor contaminación, mayor es el riesgo de infección postquirúrgica.
El riesgo de contaminación del campo quirúrgico se incrementa con el tiempo de exposición y la complejidad de la solución de continuidad producida, y se minimiza con una adecuada técnica quirúrgica y con el buen estado del paciente. Pero el que se ha demostrado como factor más crítico y sujeto a debate es la profilaxis antibiótica.
Las medidas de control en la técnica quirúrgica para minimizar el riesgo de infección son: incisiones limpias; levantamientos mucoperiósticos libres de desgarros; irrigaciones como método de enfriamiento y arrastre de partículas de los fresados del hueso alveolar; aspiración constante y hemostasia cuidadosa. En caso de utilizar anestesia local, hay que evitar posibles desgarros tisulares con la aguja y asegurarse de la administración lenta del anestésico. Asimismo se debe tener precaución esmerada con separadores, retractores y depresor lingual en labios, colgajos y tejidos. Si fuera preciso la colocación de drenajes y apósitos compresivos se realizará en la posición adecuada. Finalmente, debemos recordar que algunas de las suturas efectuadas son puntos de aproximación, por lo que existe un tránsito tanto del ambiente húmedo propio de la cavidad bucal, como de residuos alimenticios, por lo que se recomienda hacer enjuagues con antisépticos o suero fisiológico a partir de las 24 horas siguientes a la intervención quirúrgica.
Como norma general, la profilaxis está indicada siempre que exista un riesgo importante de infección, ya sea por las características mismas de la operación o por las condiciones locales o generales del paciente. Entre los factores que van a determinar la posibilidad de aparición de infección destacan el tipo y tiempo de cirugía así como el riesgo quirúrgico del paciente por su comorbilidad (valorable en términos de riesgo anestésico o clase ASA): diabetes, nefropatías, hepatopatías (cirrosis), cardiopatías y terapéuticas inmunosupresoras (corticoides, radioterapia, quimioterapia, infecciones previas con antibioticoterapia no bien conocida o racionalizada). Las intervenciones menores en pacientes sanos en general no requieren profilaxis.
¿Qué tipo de pacientes requieren profilaxis antibiótica?
La utilización o no de profilaxis antibiótica en los procedimientos y técnicas quirúrgicas odontológicas dependerá del tipo de paciente y del tipo de procedimiento que se lleve a cabo. Determinados pacientes son candidatos a profilaxis en procedimientos invasivos. Por el contrario, los procedimientos no invasivos no requieren profilaxis en ningún caso.
A tal fín, los pacientes podrían clasificarse en: a) pacientes sanos, b) pacientes con factores de riesgo de infección local o sistémica y c) pacientes con factores de riesgo de infección focal tras bacteriemia.
En el sujeto sano la profilaxis se basa exclusivamente en el riesgo del procedimiento,26 presentando alto riesgo los trasplantes, reimplantes, injertos, cirugía tumoral y ósea (al igual que en cirugía ortopédica y traumatológica), así como la cirugía periapical y las inclusiones dentarias donde, además, es frecuente que coexista una infección previa.2,26
Los pacientes con factores de riesgo de infección local o sistémica son aquellos que presentan un aumento de susceptibilidad general a las infecciones. Son pacientes oncológicos, pacientes con inmunodepresión congénita o inmunológica (por ejemplo, lupus eritematoso), pacientes con inmunodepresión medicamentosa (corticoterapia, quimioterapia) tras trasplante, injerto o cualquier otra causa, pacientes con inmunodepresión infecciosa (síndrome de inmunodeficiencia adquirida), pacientes con trastornos metabólicos (diabetes) y pacientes con insuficiencia renal o hepática.26 Además, están los pacientes esplenectomizados donde existe un mayor riesgo de infecciones por los géneros Streptococcus y Haemophilus.32,33
Los pacientes con factores de riesgo de infección focal tras bacteriemia son aquellos que presentan riesgo de endocarditis infecciosa o de infección de prótesis osteoarticulares. Con respecto a la endocarditis infecciosa, el 14-20% de las mismas tienen un origen oral.9,34 Los antibióticos, aparte de reducir la prevalencia y magnitud de la bacteriemia, 9,35 (nunca llegan a eliminarla por completo), impiden la adherencia bacteriana al endocardio, 36 lo que pudiera ser el mecanismo último de eficacia profiláctica. Las condiciones patológicas asociadas a riesgo de endocarditis infecciosa han sido definidas por la American Heart Association (AHA) en Estados Unidos, la British Society of Antimicrobial Chemotherapy (BSAC) en el Reino Unido y la Agence Française de Sécurité Sanitaire des Produits de Santé (Afssaps),2,37,38 entre otros. Con respecto a las infecciones de prótesis osteoarticulares, la elección de la profilaxis antibiótica del procedimiento dental se basaría en su morbilidad39 devastadora y alta mortalidad, y no en la baja prevalencia de la asociación de estas infecciones con procedimientos dentales.32 A pesar de esta baja prevalencia, la profilaxis está indicada en prótesis implantadas hace menos de 2 años o cuando haya existido una infección de prótesis previa.2
En la
tabla 2 se señalan los pacientes considerados de riesgo.
¿Qué procedimientos odontológicos requieren
profilaxis antibiótica?Ante estos hechos es necesario diferenciar entre procedimientos buco-dentales invasivos, aquellos susceptibles de producir un sangrado significativo (
Tabla 3), y los no invasivos, aquellos que no son susceptibles de producir un sangrado significativo. Generalmente, los procedimientos invasivos pueden ser considerados de alto riesgo en pacientes frágiles.
Las heridas quirúrgicas fueron clasificadas por Altemeier de acuerdo con su riesgo potencial de contaminación e infección, en una clasificación,40 que el tiempo ha consagrado por su utilidad práctica:
Tipo I. Heridas limpias (no apertura de mucosas como la cavidad oral): Tasa verificada de infección de 1 a 4%. No precisan profilaxis antibiótica.
Tipo II. Heridas limpias-contaminadas (apertura de mucosas como la cavidad oral, inserción de implantes dentales o intervención por patología inflamatoria): Tasa verificada de infección de 5 a 15%. Requieren profilaxis antibiótica con fármacos que cubran microorganimos grampositivos y anaerobios.
Tipo III. Heridas contaminadas (patología oncológica en la que se actúa simultáneamente sobre la cavidad oral y el cuello): Tasa verificada de infección de 16 a 25%. Debe efectuarse profilaxis antibiótica cubriendo gramnegativos, cuya cobertura es controvertida en cirugías limpias y limpias contaminadas.
Tipo IV. Heridas sucias e infectadas: Tasa verificada de infección superior al 26%. Precisan de un tratamiento antibiótico adecuado siempre.
Son candidatos a profilaxis en pacientes con factores de riesgo para infección local o sistémica (pacientes con factores de inmunodepresión), todos los procedimientos invasivos citados en la
tabla 3.En los pacientes con factores de riesgo de infección focal tras bacteriemia (endocarditis, infección de prótesis) está siempre indicada la profilaxis de los procedimientos invasivos que puedan realizarse en este tipo de pacientes.
En el sujeto sano la profilaxis sólo está recomendada en caso de exodoncia de diente incluido, cirugía periapical, cirugía ósea, cirugía implantaria, injertos óseos y cirugía de tumores benignos.
Criterios de selección: diana bacteriana, flora normal, aspectos farmacocinéticos y farmacodinámicos y selección del antibiótico adecuado
El antibiótico y la diana bacteriana de la profilaxis
Las bacterias que causan las infecciones odontogénicas son generalmente saprofitas. Durante la evolución de la caries dental, las bacterias que penetran en los túbulos dentinarios son fundamentalmente anaerobios facultativos como Streptococcus spp, Staphylococcus spp y lactobacilos. Cuando la pulpa se necrosa, las bacterias avanzan por el conducto radicular y el proceso evoluciona hacia una inflamación periapical. En esta fase predominan Prevotella spp, Porphyromonas spp, Fusobacterium spp y Peptostreptococos spp. La microbiología de las complicaciones infecciosas es variada, existen múltiples combinaciones de todos estos organismos, con diferentes características, pero tanto las bacterias anaerobias como las aerobias están presentes habitualmente.
Frente a los bacilos gram positivos aerobios o facultativos implicados (Eubacterium, Actinomyces y Propionibacterium) y espiroquetas, todos los grupos de antibióticos habitualmente utilizados (aminopenicilinas, amoxicilina + ac. clavulánico, macrólidos, lincosamidas y metronidazol) son activos excepto el metronidazol. Frente a cocos gram positivos implicados (Streptococcus, Staphylococcus y Peptostreptococcus) sólo la amoxicilina + ac. clavulánico presenta una cobertura adecuada.2 Frente a Veillonella, todos son activos excepto los macrólidos (eritromicina, claritromicina y azitromicina). Frente a los bacilos gram negativos implicados (Prevotella, Porphyromonas, Fusobacterium, Selenomonas, Eikenella, Capnocytophaga, Actinobacillus, Campylobacter rectus y Tanerella forsytensis), amoxicilina + ac. clavulánico y clindamicina presentan una cobertura adecuada (excepto para Eikenella corrodens en el caso de la lincosamida). La alta prevalencia de producción de b-lactamasa en la flora anaerobia oral normal o patológica hace que la amoxicilina sin inhibidor de b-lactamasa (ác. clavulánico) no sea un antibiótico adecuado desde el punto de vista fisiopatológico. En la tabla 4 se resume la actividad de los principales antibióticos frente a los patógenos odontógenos más frecuentes.
El antibiótico y la flora normal
El régimen antibiótico adecuado será aquel que más selectivamente actúe sobre las bacterias que pueden producir complicaciones, respetando al máximo la flora saprofita habitual.
Es importante considerar el aspecto ecológico a la hora de elegir el régimen antibiótico a utilizar. Se debe elegir el antibiótico y el régimen posológico (este factor con menos importancia si el curso profiláctico es corto o de dosis única) que menos altere la flora saprófita normal. Tomando Escherichia coli como índice de flora intestinal, los macrólidos y cetólidos son respetuosos ya que este microorganismo es resistente a estos compuestos. Las quinolonas, sin embargo, han seleccionado un alto grado de resistencias,42 pero estos compuestos no están indicados en odontología. Mientras la amoxicilina ha seleccionado altas tasas de resistencias a E. coli por producción de b-lactamasa, la sensibilidad de la amoxicilina unida al ác. clavulánico es muy alta. Donde se ha estudiado más extensivamente la flora normal es en nasofaringe tomando como bacteria índice Streptococcus pneumoniae, microorganismo del mismo género que otras especies que son aislamientos prevalentes en infecciones odontogénicas (grupo viridans).43
Con respecto a los estreptococos se ha relacionado el consumo de antibióticos como única causa con las resistencias en las especies S. pyogenes y S. pneumoniae, tanto desde un punto de vista temporal,44,45 como geográfico,46,47 estando las resistencias a macrólidos en estas dos especies ligadas a nivel local.48 Mientras que la responsabilidad de las aminopenicilinas en la selección de resistencias en S. pneumoniae es baja, los fármacos que más resistencias a penicilina y macrólidos seleccionan en S. pneumoniae son las cefalosporinas orales de administración dos veces al día, pero no son fármacos de elección en odontología y sobre todo, los macrólidos de administración una o dos veces al día en S. pneumoniae y S. pyogenes. Estos hechos tienen traducción en las especies del grupo viridans del género Streptococcus donde la alta resistencia a macrólidos (eritromicina, claritromicina) 49 se asocia frecuentemente a alta resistencia a tetraciclinas,50 y a clindamicina y azálidos (azitromicina).51 Considerando que el consumo de antibióticos en odontología supone el 10% del total del consumo de antibióticos en la comunidad, como se ha comentado, es posible sospechar un grado de responsabilidad no despreciable en la selección de resistencias por tratamientos antimicrobianos en odontología. Así en nuestro país se ha descrito una alta prevalencia de bacteriemias iatrogénicas orales causadas por estreptococos resistentes a eritromicina (40,8%) y clindamicina (21%), siendo la mayoría de los aislados sensibles a aminopenicilinas. 52
Aspectos farmacocinéticos farmacodinámicos
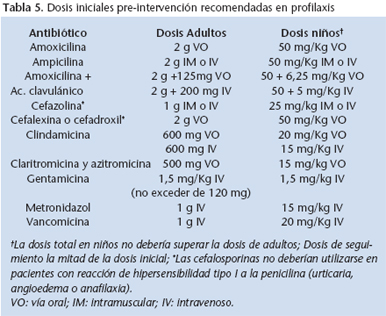
Para algunos antibióticos, las concentraciones antibióticas en el fluido gingival son similares o superiores a las séricas, como se ha visto en el caso de amoxicilina + ác. clavulánico, 53,54 espiramicina, metronidazol, 55 y quinolonas (fármacos no indicados en el campo odontológico en la actualidad). La cobertura farmacodinámica se entiende como el valor de la "relación entre los parámetros farmacocinéticos séricos y susceptibilidad in vitro" que predice eficacia: a) porcentaje del intervalo de dosificación en que los niveles de antibiótico superan la CMI (mínima concentración antibiótica que produce inhibición del crecimiento bacteriano in vitro) que debe ser superior al 40-50% para b-lactámicos, macrólidos y lincosamidas, y b) relación del área bajo la curva de los niveles séricos/CMI que debe ser superior a 25 para azálidos (azitromicina). Se han publicado trabajos que aplican estos conceptos en odontología, analizando distintos antibióticos frente a los cinco aislados más prevalentes (pero no frente a todas las bacterias implicadas) en infecciones odontogénicas (Streptococcus grupo viridans, Peptostreptococcus sp., Prevotella intermedia, Porphyromonas gingivalis y Fusobacterium nucleatum).43 Sólo amoxicilina + ac. clavulánico a dosis de 875/125 mg cada 8 h o la nueva formulación de 2000/125 mg cada 12h así como la clindamicina 300 mg cada 6-8h cumplen los requisitos farmacodinámicos.56,57 Sin embargo, la clindamicina ofrece una peor cobertura frente a estreptococos orales y Peptostreptococcus adecuadamente, presentando un nivel no despreciable de resistencias. El metronidazol no tiene actividad frente a bacterias aerobias y los macrólidos, incluyendo la espiramicina, tienen un elevado porcentaje de resistencias a los estreptococos orales y ofrecen una actividad muy limitada frente a Peptostreptococcus spp y Fusobacterium nucleatum.
En la
tabla 5 se reflejan las posologías recomendadas para profilaxis de diferentes antibióticos.
Selección del Antibiótico adecuado
El antibiótico a elegir (en caso de considerar necesaria la profilaxis por el tipo de procedimiento y tipo de paciente) debe cumplir las siguientes características:
1. Espectro bacteriano adecuado, cubriendo todas las especies involucradas en las infecciones polimicrobianas locales o monomicrobianas focales distales, incluyendo microorganismos aerobios, microaerófilos, sin olvidar los anaerobios que debido a la dificultad en su aislamiento en ocasiones no son considerados prevalentes en bacteriemias de origen oral.
2. Espectro clínico amplio, para cubrir el mayor número de procedimientos odontológicos
3. Espectro ecológico restringido para limitar al máximo los efectos sobre la flora saprófita habitual.
4. Farmacocinética y farmacodinamia adecuadas, para permitir su utilización en monodosis pre-operatoria en el caso de la profilaxis, o intervalos de dosificación amplios en el tratamiento preventivo de corta duración, con vidas medias o formulaciones de liberación prolongada que mantengan concentraciones adecuadas a nivel local (fluido gingival) o sistémico (suero) durante todo el tiempo que dure el procedimiento odontológico (profilaxis).
5. Perfil de seguridad adecuado, incluso en población infantil y tercera edad.
Los antibióticos administrados oralmente que son efectivos ante infecciones odontogénicas incluyen penicilina, clindamicina, eritromicina, cefadroxilo, metronidazol y las tetraciclinas. Penicilina V fue la penicilina de elección ante infecciones odontogénicas. Es bactericida, y aunque su espectro de acción, es relativamente estrecho, era el apropiado para los tratamientos de infecciones odontogénicas. Para la profilaxis de endocarditis asociada con tratamientos dentales, la amoxicilina es el antibiótico de primera elección.37 La amoxicilina más el ácido clavulánico es en la actualidad el fármaco de elección de este grupo al presentar la gran ventaja de conservar su actividad contra las b-lactamasas producidas comúnmente por microorganismos que se asocian con infecciones odontogénicas.
Una alternativa, en casos de pacientes alérgicos a las penicilinas, es la clindamicina. Es bacteriostático, pero su actividad bactericida se consigue clínicamente con la dosis generalmente recomendada. Los últimos macrólidos, claritromicina y azitromicina pueden ser usados también, si el paciente es alérgico a la penicilina. Metronidazol se suele usar sólo contra anaerobios y se suele reservar para situaciones en las que sólo se sospeche de bacterias anaerobias. Las tetraciclinas tienen un uso muy limitado en la odontología. Como las tetraciclinas pueden causar alteraciones en el color de los dientes, no se deben prescribir en niños menores de 8 años, mujeres embarazadas o madres lactantes.
Valor de los antisépticos e higiene bucodental.
El uso de antisépticos tópicos en la cavidad oral reduce el inóculo bacteriano, pero no ha demostrado ser eficaz en la profilaxis de la colonización bacteriana. No obstante, el uso de antisépticos preoperatorios en la cavidad oral puede reducir las complicaciones derivadas del trauma en la mucosa, especialmente en pacientes con valvulopatías, implantes de material aloplástico, injertos óseos, inmunodeprimidos, ancianos y en pacientes con mala higiene oral.
Análisis de la patología dentaria
La caries es una enfermedad multifactorial, en la que interviene, entre otros factores, una microbiota muy variada, las bacterias mas frecuentes son los estreptococos del grupo mutans, seguidas del género de Lactobacillus. Estas bacterias intervienen en la formación de la placa bacteriana, pero con una composición diferente según la localización.58,59
La penetración bacteriana del diente se produce sin necesidad de una solución de continuidad en la superficie externa, produciéndose fundamentalmente a través de las laminillas o craks, los pits y las áreas intervarillas del esmalte, incluso en dientes normales sin caries. En casos de caries de esmalte incipiente no cavitada, se puede observar la invasión bacteriana en las capas mas profundas del esmalte, alcanzando el límite amelo dentinario e incluso en las capas profundas de la dentina,60,61 donde se detectan, en los estadios iniciales de la caries dentinaria, fundamentalmente Lactobacillus, siendo colonizado posteriormente por Streptococcus y Actinomyces spp.
Los estreptococos del grupo mutans (S. mutans, S. sobrinus, S. cricetus, S. ratius, S. ferus, S. downwi y S. macacae),62 son los mas importantes en la etiopatogenia de la caries, por lo que la prescripción de una tratamiento antibacteriano, en pacientes de alto riesgo que aún no tengan lesión evidente, es aconsejable de modo profiláctico.63 Se utiliza clorhexidina, fluoruros tópicos y antibióticos del tipo de la vancomicina (bloquea la síntesis de la pared bacteriana), la kanamicina y actinomicina (bloque la síntesis proteica) así como soluciones halogenadas a base de yodo y flúor.63
El número de bacterias que invaden la pulpa o los tejidos periapicales es directamente proporcional al grado de extensión de las vías de penetración. La invasión bacteriana de la pulpa condiciona siempre una respuesta inflamatoria pulpar y la gravedad del proceso que se desarrolla va a depender de una serie de factores como son : el carácter de la invasión, la microbiota, el número de microorganismos, las endotoxinas, las exoenzimas, los metabolitos, las exotoxinas, el tiempo de actuación y la capacidad defensiva del hospedador.64
Las bacterias que contaminan el tejido pulpar, pueden invadir asimismo los tejidos periapicales, pero el grado de invasión bacteriana depende no sólo de la capacidad de multiplicarse, sino también, de la motilidad de las bacterias.64
La mayoría de las bacterias que originan patología periapical son sensibles, en orden de efectividad, al tratamiento con amoxicilina/ ácido clavulánico, ampicilina/sulbactam, Clindamicina, metronidazol, macrólidos, penicilinas (ampicilinas, amoxicilinas).
Uno de los grandes problemas del fracaso endodontico es debido a la persistencia de la invasión bacteriana a nivel del conducto o del periápice, por causas muy diversas, habiéndose aislado preferentemente dos especies bacterianas: Actinomyces israelii,65 y Enterococcus faecalis.66 Se ha observado resistencia de Actinomyces israelli, 67 a metronidazol y de Enterococcus faecalis a clindamicina.6
Análisis de la patología quirúrgica bucal y maxilofacial
Los datos de la literatura son contradictorios, si bien las series parecen indicar que la reducción de las complicaciones postoperatorias se debe tanto a la mejora en la técnica quirúrgica como a un uso racional de la profilaxis antibiótica. En términos generales, se recomienda la antibioterapia per y postoperatoria en aquellos casos en que haya alto riesgo de infección o signos clínicos evidentes de infección.
Las intervenciones quirúrgicas pueden ser clasificadas en dos grandes grupos, atendiendo a la presencia de gérmenes o no en la zona de la intervención. Enumeramos a continuación una serie de operaciones tipo de la especialidad:
1. Intervenciones quirúrgicas sin presencia de gérmenes: dientes retenidos; exostosis, torus; tumores odontogénicos, quistes (no infectados); épulis, cirugía preprotésica y preortodóntica; fracturas maxilares (cerradas); afección glandular; osteotomías; injertos, colgajos y otros.
2. Intervenciones quirúrgicas con presencia de gérmenes: pericoronaritis del tercer molar, quistes inflamatorios, restos radiculares, granulomas, etcétera; sialolitiasis, fracturas abiertas, traumatismos, heridas contusas; sobreinfección añadida a la lesión tumoral, radionecrosis y otros.
Cirugía oral
La tasa de infección es baja, por lo que en pacientes sanos la mayoría de procedimientos en cirugía oral no requieren antibioterapia. Se empleará tratamiento antibiótico profiláctico en casos de infección activa, pacientes con comorbilidad o inmunocomprometidos.
Exodoncia de cordales. Algunas series parecen demostrar que el uso de antibioterapia postoperatoria no mejora el pronóstico frente a la posibilidad de infección postoperatoria.69,70 Sin embargo, una parte de autores recomiendan el uso de la profilaxis basándose en el descenso significativo de complicaciones posquirúrgicas como el dolor, el trismus, el retraso en la cicatrización de la herida y la tumefacción.71-74 En un reciente ensayo clínico aleatorizado, doble ciego, de grupos paralelos se comparó la eficacia de la antibioterapia pre y postoperatoria con placebo. En el estudio se aleatorizó a los pacientes en tres grupos: Grupo placebo, grupo de profilaxis preoperatorio (amoxicilina/ácido clavulánico 2000/125 mg en una sola dosis antes de la cirugía) y grupo de profilaxis postoperatoria o tratamiento preventivo (amoxicilina/ácido clavulánico 2000/125 mg cada 12h durante 5 días comenzando dentro de las 3 horas después de la cirugía). La prevalencia de infección postquirúrgica fue significativamente mayor (P=0,006) en el grupo de pacientes tratado con placebo (16%) que en el grupo de pacientes que recibió amoxicilina/ácido clavulánico 2000/125 mg, bien como profilaxis preoperatoria (5,3%), bien como profilaxis postoperatoria (2,7%). En las intervenciones que precisaron osteotomía, el tratamiento preventivo fue mejor que la profilaxis preoperatorio y el placebo (24, 9 y 4%, respectivamente).3
Implantología. Conceptualmente encuadradada dentro de las heridas tipo II, una reciente revisión de la literatura sobre la eficacia de los antibióticos en la prevención de complicaciones y fracasos tras la realización de implantes dentales concluyó que no hay evidencia ni para recomendar ni para desaconsejar el uso de antibióticos para la prevención de complicaciones y fracasos de implantes dentales, debido a la ausencia de ensayos clínicos aleatorizados y controlados.75
Gynther y cols., compararon la eficacia de penicilina V administrada antes y después de la intervención frente a placebo 279 pacientes, no encontrando diferencias en lo referido a tasa de infección postoperatoria o supervivencia del implante entre los dos grupos. 76 Dent y cols., en un estudio multicéntrico en 2641 implantes dentales encontraron una significativa menor tasa de fracasos en aquellos que habían recibido antibióticos preoperatorios en comparación con aquéllos que no habían recibido. Finalmente, en un estudio reciente no se observó mayor eficacia con el uso de antibioterapia postoperatoria durante 7 días frente a dosis única intraoperatoria. 77 En pacientes con radioterapia previa se emplean regímenes prolongados de antibioterapia para evitar la presencia de osteomielitis o pérdida de los dispositivos de implantes osteointegrados. Igualmente, basándonos en la experiencia clínica, en pacientes con inmunodeficiencias, enfermedades metabólicas (como diabetes), pacientes con factores de riesgo de endocarditis, la utilización de antibióticos estaría recomendada.
Traumatología
Está ampliamente aceptado el uso de antibioterapia profiláctica en fracturas complejas o múltiples.
Fracturas de mandíbula y dentoalveolares. Los esquemas de tratamiento antibiótico son los clásicos del resto de la patología cervicofacial (penicilina y derivados y cefalosporinas de tercera generación). El tratamiento profiláctico antibiótico en las fracturas no complicadas no parece aportar beneficios si bien muchos profesionales tratan estas fracturas para cubrir las posibles infecciones para reducir su incidencia. El tratamiento antibiótico en las primeras 72 horas no resulta necesario. El tratamiento antibiótico de las complicaciones infecciosas (abscesos, pseudoartrosis, osteomielitis, etc.) es donde mayor consenso existe, si bien en este caso ya deja de ser antibioterapia profiláctica para convertirse en terapéutica.
Fracturas orbitarias. No hay consenso en la literatura (algunos autores abogan por el tratamiento antibiótico mientras que otros no).
Fracturas de tercio medio y superior. Se emplean cefalosporinas de tercera generación, en aquellos casos en que se presente licuorrea.
Cirugía ortognática y cirugía preprotésica
Se consideran cirugías limpias-contaminadas, en las cuales algunas series han demostrado la efectividad de la profilaxis antibiótica postoperatoria (penicilina, cefalosporinas que no mejoran el pronóstico y suponen un mayor coste), si bien otros autores parecen demostrar que no hay evidencias de mejor pronóstico frente a infección por el uso de antibioterapia postoperatoria, especialmente si se administra vía oral.
Se ha descrito una mayor incidencia de infecciones en cirugía bimaxilar sin tratamiento antibiótico.
Algunos estudios han utilizado levofloxacino oral o cefazolina iv en osteotomías mandibulares, pero en el caso de ésta última, es mejor utilizar amoxicilina-clavulánico por cepas resistentes a cefazolina.
El tiempo de tratamiento se había establecido en publicaciones previas en 5 días para cobertura antibiótica profiláctica, pero la incidencia de infección postoperatoria es igual en regímenes de 1 ó 5 días, si bien hay cierta mejoría en la morbilidad postoperatoria prolongando el tratamiento durante 5 días.
Glándulas salivales
En cirugías como parotidectomía o submaxilectomía se ha demostrado la ausencia de efectividad del uso de profilaxis antibiótica.
Cirugía oncológica, reconstructiva y cervical
Se ha demostrado que el uso de antibióticos perioperatorios reduce significativamente la incidencia de infecciones postoperatorias. Como en los casos anteriores, en patología cervical y, fundamentalmente, en cirugía oncológica, se pueden utilizar regímenes de antibioterapia profiláctica combinando clindamicina y cefazolina, cefalosporinas, aminoglucósidos, quinolonas o derivados de la penicilina con inhibidores de betalactamasas.
El riesgo de infección surge ante la posibilidad de poner en contacto áreas limpias con la mucosa oral, puesto que la principal fuente de contaminación en estos pacientes es la saliva que transporta una cantidad importante de bacterias. Otros factores contribuyentes son el mal estado general, los estados de inmunosupresión, radioterapia o quimioterapia preoperatoria, colgajos de reconstrucción o aquellos procedimientos que expongan a los tejidos a isquemia o necrosis tisular. Las fuentes de microorganismos en estas patologías son la saliva, la piel, dientes y el propio tumor, por lo que el antibiótico a elegir debe cubrir no sólamente a los microorganismos comunes de la saliva, como cocos grampositivos y anaerobios, sino también a gramnegativos que se aíslan comúnmente en los tumores. Gran parte de las referencias en la literatura no consideran que haya que cubrir los microorganismos gramnegativos en cirugía oncológica de cabeza y cuello, pero recientes publicaciones si parecen asociar un mejor pronóstico con cobertura de gramnegativos.
Una pauta de antibioterapia puede ser gentamicina + clindamicina, que cubren bien grampositivos, gramnegativos y anaerobios (no así la cefazolina que no cubre anaerobios). También amoxicilina- clavulánico y ampicilina-sulbactam tienen el mismo espectro, frente a la clindamicina que no cubre suficientemente a los anaerobios.
La duración del tratamiento no está estandarizada quedando en muchos casos a criterio del cirujano. La antibioterapia postoperatoria suele mantenerse hasta la retirada de los drenajes, si bien se prolonga en casos de infección de herida quirúrgica, dehiscencia o fístula.
Análisis de la patología periodontal
Aunque la mayor parte de los principios de la profilaxis antibiótica en periodoncia se basan en conceptos generalizables a la profilaxis por procedimientos bucales quirúrgicos, las infecciones periodontales presentan particularidades que es conveniente tratar de forma separada.
¿Qué procedimientos en Periodoncia requieren tratamiento profiláctico con antibioterapia?
Esta pregunta podría formularse de otra manera: ¿qué procedimientos en periodoncia producen bacteriemias?
Todos los procedimientos dentales que inducen sangrado desarrollaran una bacteriemia que rara vez persistirá más de 15 minutos.78 Podrían considerarse que cumplen en Periodoncia estos criterios los siguientes procedimientos o técnicas:
Se ha observado que el sondaje periodontal en humanos causa una bacteriemia transitoria, confirmada mediante hemocultivos.79,80 Asimismo estudios en animales han puesto de manifiesto que las técnicas de raspado y alisado radicular pueden causarla.81 En humanos se ha observado que las técnicas de raspado y alisado radicular causan un bacteriemia transitoria, independientemente de que éstas se realicen mediante instrumentación con curetas o que se utilice instrumentación ultrasónica.82,83 La aplicación de clorhexidina al 0,12% mediante irrigación subgingival, inmediatamente o durante la instrumentación con aparatología ultrasónica o curetas, reduce pero no elimina la bacteriemia transitoria.82,83 La utilización de otros antisépticos como povidona yodada tras la instrumentación periodontal, no ha demostrado eficacia para reducir o eliminar la bacteriemia transitoria.
La cirugía periodontal causa una bacteriemia transitoria que se reduce de forma significativa con la utilización de profilaxis antibiótica. 85 Aunque la utilización de antibioterapia en los procedimientos de cirugía periodontal es muy discutida, las infecciones postoperatorias se producen a pesar de que la prevalencia de éstas infecciones sea baja.86 Al retirar las suturas se produce también una bacteriemia transitoria.87
La controversia podría producirse cuando se analiza la evidencia sobre bacteriemias producidas por maniobras no invasivas como el cepillado de dientes o mascar un chicle.88,89 En la
tabla 6 se muestra la incidencia de bacteriemias comparando actuaciones de tratamiento dental y las maniobras de higiene bucal.92,90
La cuestión que surge entonces es, si estímulos productores de bacteriemias se producen de forma espontánea varias veces al día sin ningún tipo de cobertura antibiótica, ¿otros procedimientos invasivos relacionados con manipulaciones quirúrgicas deberán realizarse bajo cobertura antibiótica?
Aunque se invoca que la extensión de la inflamación y la gravedad de la misma estarían relacionadas con la magnitud de la bacteriemia y es lógico pensar así, no se ha relacionado de forma experimental con el grado clínico-anatomopatológico de la inflamación.
Estudios histológicos han demostrado que, incluso en condiciones de normalidad clínica, está siempre presente una cierta alteración tisular que sería compatible con un entorno favorable a las bacteriemias.93 Tampoco se ha establecido la diferencia entre gingivitis y periodontitis en la producción de bacteriemias.94
Además, por epidemiología conocemos que la mayor parte de la población en cualquier edad presenta ciertos niveles de inflamación clínica y la encía sana se encuentra en porcentajes muy bajos de población.95
Análisis de la patología en edad infantil
La profilaxis antibiótica en los niños sigue los mismos principios que para el adulto, teniendo en cuenta únicamente las peculiaridades de farmacocinética y toxicidad. En este sentido y a modo de ejemplo la utilización de algunos antibióticos como las quinolonas no están recomendadas en la edad infantil. Del mismo modo las tetraciclinas no deberían administrarse en menores de 8 años.
Como punto de partida, consideramos necesario realizar una serie de particularidades diferenciales del tratamiento antibiótico en el niño: a) El niño en sus primeras etapas carece de antecedentes médicos que hagan sospechar de la presencia de posibles cuadros de reacciones adversas o de alergia a los fármacos; b) La mayor proporción de agua en los tejidos del niño, además de la mayor esponjosidad de los tejidos óseos, permiten una más rápida difusión de la infección de un lado, y de otro, se hace necesario el ajuste adecuado de las dosis del medicamento prescrito; c) los procedimientos anestésicos en dientes temporales en proceso de rizolisis pueden incluir la realización de inyecciones intraligamentarias, que aumentan sin embargo, la posibilidad de bacteriemia; d) la deficiente higiene oral en la mayoría de los niños y el consumo de alimentos ricos en sacarosa, contribuyen a aumentar el número de colonias de gérmenes en la cavidad oral, y con ello el riesgo de bacteriemia tras los tratamientos orales; y e) Las resistencias a los antibióticos en los niños presentan una extraordinaria complejidad tanto por su elevada incidencia como por sus circunstancias asociadas.46,47
Varios estudios han evaluado la prevalencia y la extensión de bacteriemias después de diferentes procedimientos dentales en niños. Se demostró que sólo el cepillado está asociado con bacteriemia en más de uno de cada tres niños.96 Los tratamientos conservadores odontológicos, en los que se colocan cuñas o matrices, o en el caso de procedimientos ortodóncicos como la colocación o retirada de bandas, pueden originar bacteriemia en un número significativo de niños.97 En una extracción sencilla de un diente, aparece bacteriemia en un 40-50% de los niños examinados.96 Los niveles más altos de bacteriemia se encuentran tras las inyecciones intraligamentarias en procedimientos de anestesia local (96,6% de los niños).98 En más del 50% de los casos se aislaron estreptococos del grupo viridans.
El nivel de higiene oral influye en los niveles de bacteriemia considerablemente. Por esta razón, una higiene oral óptima podría ser el factor más importante en la prevención de complicaciones como consecuencia de una bacteriemia; en opinión de algunos autores, más que cualquier pauta antibiótica.99
La patología traumática dentaria, constituye un factor etiológico de infección del área oral, máxime cuando se produce la exposición directa del tejido pulpar, y/o alteración del espacio periodontal. Las posibilidades de infección aumentarán cuando al traumatismo en el tejido dental duro o de soporte, se le sume la presencia de heridas abiertas en piel o mucosas.
Profilaxis de endocarditis bacteriana
Estas recomendaciones son un resumen de los acuerdos y documentos de consenso de la Academia Americana de Cardiología,37 que ha sido aceptado con posterioridad por la mayoría de sociedades científicas y profesionales.
Se hará en todo paciente con cardiopatía predisponente que vaya a ser sometido a un procedimiento con riesgo de bacteriemia en cirugía oral y maxilofacial. En función del riesgo de endocarditis podemos clasificar las cardiopatías en:37
1. De alto riesgo. Prótesis endovascular, endocarditis previa, cardiopatía congénita cianógena compleja o fístulas sistémico-pulmonares realizadas quirúrgicamente.
2. De riesgo moderado. Otras cardiopatías congénitas, valvulopatías adquiridas, prolapso mitral con insuficiencia, miocardiopatía hipertrófica.
3. De bajo riesgo. CIA ostium secundum, CIA o CIV intervenidos, by-pass previo, prolapso mitral sin regurgitación, marcapasos, desfibrilador implantable.
Requieren profilaxis antibiótica los pacientes de alto riesgo y riesgo moderado que vayan a ser intervenidos en el ámbito maxilofacial usando como pautas antibióticas 1 hora antes vía oral o 30 minutos antes vía intravenosa. En la
tabla 7 pueden verse los antibióticos recomendados en niños y adultos.
Adicionalmente, en los niños con historia de implementación de drogas intravenosas, y ciertos síndromes (ej. Down, Marfan), pueden tener riesgo de sufrir endocarditis bacteriana, por las anomalias cardiacas asociadas.
Aunque no está sustentado en la evidencia científica, la Academia Americana de Cardiología recomienda que "los individuos con riesgo de desarrollar endocarditis bacteriana deben mantener la mejor higiene oral posible". Otros autores han llegado a afirmar que "mantener un buen estado de salud oral, que reduzca las bacteriemias diarias, es probablemente más importante a la hora de prevenir la endocarditis que la administración preventiva de antibióticos antes de intervenciones dentales concretas". Es preciso hacer énfasis, por tanto, en el mantenimiento de una buena salud periodontal como forma de prevención delas bacteriemias y por tanto del riesgo de endocarditis.
Otro aspecto que deberá ser aclarado en el futuro es si las bacteriemias asociadas a periodontitis activas se reducen de forma significativa con el control de la infección periodontal y por tanto, si el tratamiento es una forma de profilaxis eficaz contra la endocarditis. Las bacterias periodontopatógenas raramente causan endocarditis aunque el grupo de microorganismos denominado HACEK entre los que se encuentran Actinobacillus actinomycetemcomitans y Eikenella Corrodens ha aumentado su importancia en la etiología, lo que sustentaría la hipótesis de un aumento relativo del peso de las enfermedades periodontales en la etiología de las endocarditis.
Conclusiones
1. La finalidad de la profilaxis antibiótica en cirugía es prevenir la posible aparición de infección a nivel de la herida quirúrgica, creando un estado de resistencia a los microorganismos mediante concentraciones antibióticas en sangre que eviten la proliferación y diseminación bacteriana a partir de la puerta de entrada que representa la herida quirúrgica.
2. El 10% de las prescripciones antibióticas se utiliza para infecciones odontogénicas, y una parte significativa de ellas se utiliza en profilaxis.
3. Los ensayos clínicos con antibióticos en patologías dentarias responden poco a los criterios metodológicos requeridos, y además no son lo suficientemente numerosos.
4. Como norma general, la profilaxis está indicada siempre que exista un riesgo importante de infección, ya sea por las características mismas de la operación o por las condiciones locales o generales del paciente.
5. El riesgo de contaminación del campo quirúrgico se incrementa con el tiempo de exposición y la complejidad del traumatismo producido y se minimiza con una adecuada técnica quirúrgica y con el buen estado del paciente. Pero el que se ha demostrado como factor más crítico y sujeto a debate es la profilaxis antibiótica.
6. En un estudio llevado a cabo en nuestro país se demostró que las complicaciones subsiguientes a la extracción del tercer molar son una enfermedad infecciosa y no exclusivamente inflamatoria, ya que se encontraron, con amoxicilina/ac. clavulánico 2000/125 mg, diferencias significativas en la frecuencia de complicaciones infecciosas entre los grupos que recibieron tratamiento (5 días), profilaxis preoperatoria (dosis única) y placebo (2,7; 5,3 y 16% respectivamente). Las tasas de complicación infecciosa eran mayores en caso de osteotomía o mayor duración del acto quirúrgico.
7. Las infecciones locales polimicrobianas son infecciones cutáneomucosas u óseas que se producen como consecuencia de procedimientos dentales invasivos.
8. Las infecciones sistémicas monomicrobianas son las infecciones que asientan en pacientes con focalidad susceptible de infectarse (alteraciones endocárdicas, prótesis óseas o articulares), en pacientes con mayor susceptibilidad.
9. El criterio del facultativo para la elección o no de profilaxis antibiótica debe basarse en el concepto de coste riesgo-beneficio. En última instancia la decisión de profilaxis es potestativa del facultativo que atenderá a la ecuación: riesgo = daño x probabilidad de sufrirlo. Este enfoque es subjetivo.
10.A tal fín, los pacientes podrían clasificarse en: a) pacientes sanos, b) pacientes con factores de riesgo de infección local o sistémica y c) pacientes con factores de riesgo de infección focal tras bacteriemia. En el sujeto sano la profilaxis se basa exclusivamente en el riesgo del procedimiento.
11.El antibiótico a elegir (en caso de considerar necesaria la profilaxis por el tipo de procedimiento y tipo de paciente) debe cumplir las siguientes características:
Espectro bacteriano adecuado, cubriendo todas las especies involucradas en las infecciones polimicrobianas locales o monomicrobianas focales distales, incluyendo microorganismos aerobios, microaerófilos, sin olvidar los anaerobios que debido a la dificultad en su aislamiento en ocasiones no son considerados prevalentes en bacteriemias de origen oral.
Espectro clínico amplio, para cubrir el mayor número de procedimientos odontológicos.
Espectro ecológico restringido para limitar al máximo los efectos sobre la flora saprófita habitual.
Farmacocinética y farmacodinamia adecuadas, para permitir su utilización en monodosis pre-operatoria en el caso de la profilaxis, o intervalos de dosificación amplios en el tratamiento preventivo de corta duración, con semividas o formulaciones de liberación prolongada que mantengan concentraciones adecuadas a nivel local (fluido gingival) o sistémico (suero) durante todo el tiempo que dure el procedimiento odontológico (profilaxis).
Perfil de seguridad adecuado, incluso en población infantil y tercera edad.
Agradecimientos
A los siguientes colaboradores por su ayuda con la búsqueda bibliográfica y participación en algunas de las secciones del documento: Lorenzo Aguilar Alfaro, Juan Carlos Asurmendi, Maria José Barra Soto, Antonio Bowen, Pedro Buitrago Vega, Alvaro Del Amo, Eva Santa Eulalia Troisfontaines, Pedro Fernández Palacios, Rafael Flores Ruiz, Manuel García Calderón, Ignacio García Moris, Maria José Giménez Mestre, Conchita González-Morán, Pilar Hita Iglesias, Luis Ilzarbe, Pedro Infante Cossío, Amparo Jimenez Planas, Carlos Labaig, Natale Magallanes Abad, Jose E. Martín Herrero, Manuel Menéndez Núñez, Francisco Pina, Rafael Poveda Roda, José Quijada,, Daniel Torres Lagares, Manuel Zaragoza.
A GlaxoSmithKline por su apoyo para hacer realidad el documento.
Bibliografía
1. Bascones A, Aguirre JM, Bermejo A, Blanco A, Gay-Escoda C, González-Moles MA, Gutiérrez Pérez JL, Jiménez Soriano Y, Liébaba Ureña J, López-Marcos JF, Maestre Vera JR, Perea Pérez EJ, Prieto Prieto J, de Vicente Rodríguez JC. Documento de consenso sobre el tratamiento antimicrobiano de las infecciones bacterianas odontogénicas. Med Oral Patol Oral Cir Bucal 2004;9:363-76. [ Links ]
2. Prescription des antibiotiques en odontologie et stomatologie. Recommandations et argumentaire. Agence Française de Sécurité Sanitaire des Produits de la Santé. 2001 (www.afssaps.sante.fr). [ Links ] 3. Martínez Lacasa J, Jiménez J, Ferrás VA, García-Rey C, Bosom M, Solá-Morales O, Aguilar L, Garau J. A double blind, placebo-controlled, randosmised, comparative phase III clinical trial of pharmacokinetically enhanced amoxicillin/clavulanate 2000/125, as prophylaxis or as treatment versus placebo for infectious and inflammatory morbidity after third mandibula removal. Program and Abstracts of the 43rd InterScience Conference on Antimicrobial Agents and Chemotherapy, Chicago 2003. American Society for Microbiology, Washington, DC. [ Links ] 4. Esposito M, Coulthard P, Oliver R, Thomsen P, Worthington HV. Antibiotics to prevent complications following dental implant treatment. Cochrane Database Syst Rev 2003;(3):CD004152. [ Links ] 5. Esposito M, Hirsch JM, Lekholm U, Thomsen P. Biological factors contributing to failures of osseointegrated oral implants. (I). Success criteria and epidemiology. Eur J Oral Sci 1998;106:527-51. [ Links ] 6. Esposito M, Hirsch JM, Lekholm U, Thomsen P. Biological factors contributing to failures of osseointegrated oral implants. (II). Etiopathogenesis. Eur J Oral Sci 1998;106:721-64. [ Links ] 7. Offenbacher S, Katz V, Fertik G, Collins J, Boyd D, Maynor G, McKaig R, Beck J. Periodontal infection as a possible risk factor for preterm low birth weight. J Periodontol 1996;67(10 Suppl):1103-13. [ Links ] 8. Overholser CD, Moreillon P, Glauser MP. Experimental bacterial endocarditis after dental extractions in rats with periodontitis. J Infect Dis 1987;155:107-12. [ Links ] 9. Tomás Carmona I, Diz Dios P, Scully C. An update on the controversies in bacterial endocarditis of oral origin. Oral Surg Oral Med Oral Pathol 2002;93:660- 70. [ Links ] 10. Longman LP, Preston AJ, Martin MV, Wilson NH. Endodontics in the adult patient: the role of antibiotics. J Dent 2000;28:539-48. [ Links ] 11. Drucker DB, Gomes BP, Lilley JD. Role of anaerobic species in endodontic infection. Clin Infect Dis 1997;25:S220-1. [ Links ] 12. Sixou JL, Magaud C, Jolivet-Gougeon A, Cormier M, Bonnaure-Mallet M. Evaluation of the mandibular third molar pericoronitis flora and its susceptibility to different antibiotics prescribed in france. J Clin Microbiol 2003;41:5794-7. [ Links ] 13. Sixou JL, Magaud C, Jolivet-Gougeon A, Cormier M, Bonnaure-Mallet M. Microbiology of mandibular third molar pericoronitis: incidence of beta-lactamaseproducing bacteria. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2003; 95:655-9. [ Links ] 14. Sobottka I, Cachovan G, Sturenburg E, Ahlers MO, Laufs R, Platzer U, Mack D. In vitro activity of moxifloxacin against bacteria isolated from odontogenic abscesses. Antimicrob Agents Chemother 2002;46:4019-21. [ Links ] 15. Loesche WJ, Grossman NS. Periodontal disease as a specific, albeit chronic, infection: diagnosis and treatment. Clin Microbiol Rev 2001;14:727-52. [ Links ] 16. Okell CC, Elliott D. Bacteremia and oral sepsis with special reference to aetiology of bacterial endocarditis. Lancet 1935;2:869-72. [ Links ] 17. Fine DH, Hammond BF, Loesche WJ. Clinical use of antibiotics in dental practice. Int J Antimicrob Agents 1998;9:235-8. [ Links ] 18. Jacobson JJ, Patel B, Asher G, Woolliscroft JO, Schaberg D. Oral staphylococcus in older subjects with rheumatoid arthritis. J Am Geriatr Soc 1997;45:590-3. [ Links ] 19. Berbari EF, Cockerill FR 3rd, Steckelberg JM. Infective endocarditis due to unusual or fastidious microorganisms. Mayo Clin Proc 1997;72:532-42. [ Links ] 20. Okabe K, Nakagawa K, Yamamoto E. Factors affecting the occurrence of bacteremia associated with tooth extraction. Int J Oral Maxillofac Surg 1995;24:239-42. [ Links ] 21. Rajasuo A, Perkki K, Nyfors S, Jousimies-Somer H, Meurman JH. Bacteremia following surgical dental extraction with an emphasis on anaerobic strains. J Dent Res 2004;83:170-4. [ Links ] 22. Stone HH, Haney BB, Kolb LD, et al. Prophylactic and preventive antibiotic therapy: Timing, duration and economic. Ann Surg 1979;189:691-99. [ Links ] 23. Dipiro JT, Cheung RPF, Borden TA Jr. Single dose systemic antibiotic prophylaxis of surgical wound infections. Am J Surg 1986;152:552-9. [ Links ] 24. Cisneros JM, Rodríguez-Baño J, Mensa J, y cols. Profilaxis con antimicrobianos en cirugía. Enferm Infecc Microbiol Clin 2002;20:335-40. [ Links ] 25. García-Rodríguez JA, Prieto J, Gobernado M, y cols. Documento de consenso sobre quimioprofilaxis quirúrgica. Rev Esp Quimioterap 2000;13:205-13. [ Links ] 26. French Health Products Safety Agency (Afssaps). Prescribing antibiotics in odontology and stomatology. Recommendations by the French Health Products Safety Agency. Fundam Clin Pharmacol 2003;17:725-9. [ Links ] 27. Martin MV, Butterworth ML, Longman LP. Infective endocarditis and the dental practitioner: a review of 53 cases involving litigation. Br Dent J 1997;182: 465-8. [ Links ] 28. Wynn RL, Meiller TF, Crossley H, Overholser CD. Recent reports calling for reduction of antibiotic prophylaxis in dental procedures: a response. Gen Dent 1999; 47:124-30. [ Links ] 29. Aguilar L, García-Rey G, Giménez MJ. Presión antibiótica, desarrollo de resistencias en Streptococcus pneumoniae y fracaso clínico. Un círculo no tan viciosos para algunos antibióticos. Rev Esp Quimioterap 2001;14:17-21. [ Links ] 30. Baquero F, Baquero-Artigao G, Canton R, Garcia-Rey C. Antibiotic consumption and resistance selection in Streptococcus pneumoniae. J Antimicrob Chemother 2002;50(Suppl S2):27-37. [ Links ] 31. Schrag SJ, Peña C, Fernández J, Sánchez J, Gómez V, Pérez E, Feris JM, Besser RE. Effect of short-course, high-dose amoxicillin therapy on resistant pneumococcal carriage: a randomized trial. JAMA 2001;286:49-56. [ Links ] 32. Tong DC, Rothwell BR. Antibiotic prophylaxis in dentistry: a review and practice recommendations. J Am Dent Assoc 2000;131:366-74. [ Links ] 33. Westerman EL. Postsplenectomy sepsis and antibiotic prophylaxis before dental work. Am J Infect Control 1991;19:254-5. [ Links ] 34. Sandre RM, Shafran SD. Infective endocarditis: review of 135 cases over 9 years. Clin Infect Dis 1996;22:276-86. [ Links ] 35. Hall G, Heimdahl A, Nord CE. Effects of prophylactic administration of cefaclor on transient bacteremia after dental extraction. Eur J Clin Microbiol Infect Dis 1996;15:646-9. [ Links ] 36. Hall G, Nord CE, Heimdahl A. Elimination of bacteraemia after dental extraction: comparison of erythromycin and clindamycin for prophylaxis of infective endocarditis. J Antimicrob Chemother 1996;37:783-95. [ Links ] 37. Dajani AS, Taubert KA, Wilson W, Bolger AF, Bayer A, Ferrieri P, Gewitz MH, Shulman ST, Nouri S, Newburger JW, Hutto C, Pallasch TJ, Gage TW, Levison ME, Peter G, Zuccaro G Jr. Prevention of bacterial endocarditis: recommendations by the American Heart Association. JAMA 1997;277:1794-1801. [ Links ] 38. Seymour RA, Lowry R, Whitworth JM, Martin MV. Infective endocarditis, dentistry and antibiotic prophylaxis; time for a rethink? Br Dent J 2000;189:610-6. [ Links ] 39. Shrout MK, Scarbrough F, Powell BJ. Dental care and the prosthetic joint patient: a survey of orthopedic surgeons and general dentists. J Am Dent Assoc 1994; 125:429-36. [ Links ] 40. Altemeier WA, Burke JP, Pruitt BA, Sandusky WR. Manual of control on infection in surgical patients. JB Lippincott Co., Philadelphia, 1976. [ Links ] 41. Liñares J, Martin-Herrero JE. Bases farmacomicrobiológicas del tratamiento antibiótico de las enfermedades periodontales y periimplantarias. Av Odontoestomatol 2003;(especial):23-33. [ Links ] 42. Barberán J, Giménez MJ, Aguilar L, Prieto J. Evidencia científica y concepción global del tratamiento empírico de la infección de vías respiratorias bajas en la comunidad. Rev Esp Quimioterap 2004;17:317-24. [ Links ] 43. Isla A, Canut A, Rodriguez-Gascon A, Labora A, Ardanza-Trevijano B, Solinis MA, Pedraz JL. Análisis farmacocinético/farmacodinámico (PK/PD) de la antibioterapia en odontoestomatología. Enferm Infecc Microbiol Clin 2005;23:116-21. [ Links ] 44. Granizo JJ, Aguilar L, Casal J, Garcia-Rey C, Dal-Re R, Baquero F. Streptococcus pneumoniae resistance to erythromycin and penicillin in relation to macrolide and beta-lactam consumption in Spain (1979-1997). J Antimicrob Chemother 2000;46:767-73. [ Links ] 45. Granizo JJ, Aguilar L, Casal J, Dal-Re R, Baquero F. Streptococcus pyogenes resistance to erythromycin in relation to macrolide consumption in Spain (1986-1997). J Antimicrob Chemother 2000;46:959-64. [ Links ] 46. Garcia-Rey C, Aguilar L, Baquero F, Casal J, Martin JE. Pharmacoepidemiological analysis of provincial differences between consumption of macrolides and rates of erythromycin resistance among Streptococcus pyogenes isolates in Spain. J Clin Microbiol 2002;40:2959-63. [ Links ] 47. Garcia-Rey C, Aguilar L, Baquero F, Casal J, Dal-Re R. Importance of local variations in antibiotic consumption and geographical differences of erythromycin and penicillin resistance in Streptococcus pneumoniae. J Clin Microbiol 2002; 40:159-64. [ Links ] 48. Gomez-Lus R, Granizo JJ, Aguilar L, Bouza E, Gutierrez A, Garcia-de- Lomas J. Is there an ecological relationship between rates of antibiotic resistance of species of the genus Streptococcus? The Spanish Surveillance Group for Respiratory Pathogens. J Clin Microbiol 1999;37:3384-6. [ Links ] 49. Rodriguez-Avial I, Rodriguez-Avial C, Culebras E, Picazo JJ. In vitro activity of telithromycin against viridans group streptococci and Streptococcus bovis isolated from blood: antimicrobial susceptibility patterns in different groups of species. Antimicrob Agents Chemother 2005;49:820-3. [ Links ] 50. Rodriguez-Avial I, Rodriguez-Avial C, Culebras E, Picazo JJ. Distribution of tetracycline resistance genes tet(M), tet(O), tet(L) and tet(K) in blood isolates of viridans group streptococci harbouring erm(B) and mef(A) genes. Susceptibility to quinupristin/dalfopristin and linezolid. Int J Antimicrob Agents 2003;21:536-41. [ Links ] 51. Tomás I, Limeres J, Diz P. Antibiotic prophylaxis. BDJ 2005;198:60-61. [ Links ] 52. Tomas I, Alvarez M, Limeres J, Otero JL, Saavedra E, Lopez-Melendez C, Diz P. In vitro activity of moxifloxacin compared to other antimicrobials against streptococci isolated from iatrogenic oral bacteremia in Spain. Oral Microbiol Immunol 2004;19:331-5. [ Links ] 53. Bascones A, Mansó F. Infecciones odontógenas en la cavidad bucal y región maxilofacial. Av Odontoestomatol 1994;10(Supl. A):5-26. [ Links ] 54. Tenenbaum JF, Gallion C, Dahan M. Amoxicillin and clavulanic acid concentrations in gingival crevicular fluid. J Clin Periodontol 1997;24: 804-7. [ Links ] 55. Poulet PP, Duffaut D, Barthet P, Brumpt I. Concentrations and in vivo antibacterial activity of spiramycin and metronidazole in patients with periodontitis treated with high-dose metronidazole and the spiramycin/ metronidazole combination. J Antimicrob Chemother 2005;55:347- 51. [ Links ] 56. Isla A, Canut A, Gascon AR, Labora A, Ardanza-Trevijano B, Solinis MA, Pedraz JL. Pharmacokinetic/Pharmacodynamic evaluation of antimicrobial treatments of orofacial odontogenic infections. Clin Pharmacokinet 2005;44:305-16. [ Links ] 57. Isla A, Canut A, Rodríguez-Gascón A, Pedraz JL. Farmacocinética/farmacodinámica de la formulación de amoxicilina/ácido clavulánico 2000/125 mg en odontoestomatología. Enferm Infecc Microbiol Clin 2005;23:387. [ Links ] 58. Liébana J, Ponton J, Benito L. Bacilos grampositivos anaerobios facultativos de interés oral. En Liébana J. Ed. Micro-biología Oral. 2ª ed. Madrid, Interamericana McGraw-Hill. 2002;345-54. [ Links ] 59. Liébana J, Baca P, Rodriguez-Avial C. Microbiología de las placas dentales. En Liébana J. Ed. Microbiología Oral. 2ª ed. Madrid, Interamericana McGraw-Hill. 2002;541-59. [ Links ] 60. Mejàre I, Brännström M : Deep bacterial penetration of early proximal caries lesions in young human premolars. J Dent Children 1985;103-107. [ Links ] 61. Seppä L, Alakuijala P, Karvonen I : A scanning electron microscopic study of bacterial penetration of human enamel in incipient caries. Archs Oral Biol 1985; 30:595-598. [ Links ] 62. Bruchner D, Colonna P, Berrazo B. Nomenclatura for aerobic and facultative bacteria. Clin Infect Dis 1999;29:713-23. [ Links ] 63. Lundeen TF, Roberson TM. Cariología. Lesión, etiología, prevención y control. En: Studervant CM, Roberson TM, Heymann HO, Studervant JR: Arte y Ciencia. Operatoria Dental. 3ª Ed. Madrid, Mosby 1996;60-128. [ Links ] 64. Pumarola J. Microbiología Endodóntica. En: CANALDA C, BRAU E: Endodoncia. Técnicas clínicas y bases científicas. Barcelona, Masson 2001;29-41. 65. Figueres KH, Douglas CWI. Actinomycosis associated with a roottreated tooth: report of case. Int Endod J 1991;24:326-9. [ Links ] [ Links ] 66. Molander A, Reit C, Dahlen G, Kvist T. Microbiological status of rootfilled teeth with apical peridontitis. Int Endod J 1998;31:1-7. [ Links ] 67. Barnard D, Davies J, Figdor D. Susceptibility of Actinomyces israelli to antibiotics, sodium hypochlorite and calcium hydroxide. Int Endod J 1996;29:320-6. [ Links ] 68. Vigil GV, Wayman BE, Dazey SE, Fowler CB, Bradley Jr DV. Identification and antaibiotic sensitivity of bacteria isolated from periapical lesions. J Endod 1997; 23:110-4. [ Links ] 69. Sands T, Pynn BR, Nenniger S. Third molar surgery: current concepts and controversies. Part 2. Oral Health 1993;83:19, 21-2, 27-30. [ Links ] 70. Zeitler DL. Prophylactic antibiotics for third molar surgery: a dissenting opinion. J Oral Maxillofac Surg 1995;53:61-4. [ Links ] 71. Kaziro GS. Metronidazole (Flagyl) and Arnica Montana in the prevention of post-surgical complications, a comparative placebo controlled clinical trial. Br J Oral Maxillofac Surg 1984;22:42-9. [ Links ] 72. Mitchell DA. A controlled clinical trial of prophylactic tinidazole for chemoprophylaxis in third molar surgery. Br Dent J 1986;160:284-6. [ Links ] 73. Macgregor AJ, Addy A. Value of penicillin in the prevention of pain, swelling and trismus following the removal of ectopic mandibular third molars. Int J Oral Surg 1980;9:166-72. [ Links ] 74. Piecuch JF, Arzadon J, Lieblich SE. Prophylactic antibiotics for third molar surgery: a supportive opinion. J Oral Maxillofac Surg 1995;53:53- 60. [ Links ] 75. Esposito M, Coulthard P, Oliver R, Thomsen P, Worthington HV. Antibiotics to prevent complications following dental implant treatment. The Cochrane Database of Systematic Reviews 2003. [ Links ] 76. Gynther G, Kondell P, Moberg L, Heimdahl A. Dental implant installation without antibiotic prophylaxis. Oral Sug Oral Med Oral Pathol Oral Radiol Endo 1998;85:509-11. [ Links ] 77. Binanhmed A, Stoykewych A, Peterson L. Single preoperative dose versus long-term prophylactic antibiotic regimens in dental implant surgery. Int J Oral Maxillofac Implants 2005;20:115-7. [ Links ] 78. Sindet-Pedersen. The prophylactic use of antibiotics in periodontics. In Proceedings of the 2nd European Workshop on Periodontology. Quintassence. Berlin 1997;30-37. [ Links ] 79. Daly C, Mitchell D, Grossberg D, Highfield J, Stewart D. Bacteraemia caused by periodontal probing. Aust Dent J 1997;42:77-80. [ Links ] 80. Daly CG, Mitchell DH, Highfield JE, Grossberg DE, Stewart D. Bacteremia due to periodontal probing: a clinical and microbiological investigation. Periodontol 2001;72:210-4. [ Links ] 81. Bowersock TL, Wu CC, Inskeep GA, Chester ST. Prevention of bacteremia in dogs undergoing dental scaling by prior administration of oral clindamycin or chlorhexidine oral rinse. J Vet Dent 2000;17:11-6. [ Links ] 82. Allison C, Simor AE, Mock D, Tenenbaum HC. Prosol-chlorhexidine irrigation reduces the incidence of bacteremia during ultrasonic scaling with the Cavi-Med: a pilot investigation. J Can Dent Assoc 1993;59:676-82. [ Links ] 83. Lofthus JE, Waki MY, Jolkovsky DL, Otomo-Corgel J, Newman MG, Flemmig T, Nachnani S. Bacteraemia following subgingival irrigation and scaling and root planing. J Periodontol 1991;62:602-7. [ Links ] 84. Witzenberger T, OLeary TJ, Gillette WB. Effect of a local germicide on the occurrence of bacteremia during subgingival scaling. J Periodontol 1982;53:172-9. [ Links ] 85. Appleman MD, Sutter VL, Sims TN. Value of antibiotic prophylaxis in periodontal surgery. J Periodontol 1982;53(5):319-24. [ Links ] 86. Powell CA, Mealey BL, Deas DE, McDonnell HT, Moritz AJ. Post-surgical infections: prevalence associated with various periodontal surgical procedures. J Periodontol 2005;76:329-33. [ Links ] 87. Wampole HS, Allen AL, Gross A. The incidence of transient bacteremia during periodontal dressing change. J Periodontol 1978;49:462-4. [ Links ] 88. Schlein RA, Kudlick EM, Reindorf CA, Gregory J, Royal GC. Tootbrushing and transient bacteraemia in patients undergoing orthodontic treatment. Am J Orthod Dentof Orthop 1991;99:466-72. [ Links ] 89. Sconyers JR, Crawford JJ, Moriarity JD. Relationship of bacteraemia to toothbrishing in patients with periodontitis. J Am Dent Assoc 1971;83:1294-6. [ Links ] 90. Bender IB, Naidorf IJ, Garvey GJ, Bacterial endocarditis: a consideration for physicians and dentists. J Am Dent Assoc 1984;109:415-20. [ Links ] 91. Everett ED, Hirschmann JV. Transient bacteraemia and endocarditis prophylaxis: a review. Medicine 1977;56:61-77. [ Links ] 92. Guntheroth WG. How important are dental procedures as a cause of infective endocarditis? Am J Cardiol 1984;54:797-801. [ Links ] 93. Schroeder HE, Theilade J. Electrón microscopy of normal human gingival epithelium. J Perio Res 1966;1:95-119. [ Links ] 94. Lockhart PB. The risk for endocarditis in dental practice. Periodontology 2000 2000;23:127-35. [ Links ] 95. Seiham A, Netuvelli GS. Periodontal diseases in Europe. Periodontology 2000 2002;29:104-21. [ Links ] 96. Roberts GJ, Holzel HS, Sury MRJ, Simmons NA, Gardner P, Longhurst P. Dental bacteremia in children. Pediatr Cardiol 1997;18:24-27. [ Links ] 97. Khurana M, Martin MV. Orthodontics and Infective Endocarditis. Br J Orthodontics 1999;26:295-8. [ Links ] 98. Roberts GJ, Simmons NB, Longhurst P, Hewitt PB. Bacteraemia following local anaesthetic injections in children. Br Dent J 1998;185:295-8. [ Links ] 99. Guggenheimer J, Orchard TJ, Moore PA, Myeres DE, Rossie KM. Reliability of self-reported heart murmur history : possible impact on antibiotic use in dentistry. JADA 1998;129:861-6.
![]() Dirección para correspondencia:
Dirección para correspondencia:
José Luis Gutiérrez Pérez
Servicio de Cirugía Maxilofacial. Hospital Virgen del Rocío
Av/ Manuel Siurot s/n
41013 Sevilla. España
E-mail: jlgp@us.es
Recibido:13.06.2006
Aceptado: Aceptado:14.06.2006











 text in
text in