Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Cirugía Oral y Maxilofacial
versión On-line ISSN 2173-9161versión impresa ISSN 1130-0558
Rev Esp Cirug Oral y Maxilofac vol.29 no.2 Madrid mar./abr. 2007
Reconstrucción craneal con biomateriales. Revisión histórica y estado actual
Cranial reconstruction with biomaterials. Historical revision and current state
I. Zubillaga Rodríguez1, G. Sánchez Aniceto1, J.J. Montalvo Moreno2
1 Médico Adjunto.
2 Jefe de Servicio.
Servicio de Cirugía Oral y Maxilofacial. Hospital Universitario 12 de Octubre, Madrid, España
Dirección para correspondencia
RESUMEN
La reconstrucción de defectos craneofaciales es todavía hoy día un proceso desafiante. Se define craneoplastia como la reparación de un defecto o deformidad craneal.
La persistencia de traumatismos craneofaciales y procedimientos neuroquirúrgicos aporta un número importante de casos que permiten un fascinante progreso y desarrollo de nuevos materiales.
El objetivo de este artículo es la revisión histórica de los distintos métodos reconstructivos craneales empleados, comentando sus ventajas e inconvenientes según el tamaño y forma del defecto a reparar. Se presentan casos clínicos recientes reconstruidos con diversos biomateriales.
Palabras clave: Craneoplastia; Biomateriales.
ABSTRACT
Craniofacial defect reconstruction is still a challenging procedure. A cranioplasty is the treatment of a cranial defect or a deformity.
Cranial injuries and neurosurgical procedures provide an important group of cases that allow the development of new materials and fascinating progress.
The aim of this article is a historic review of the different cranial reconstructive techniques used, describing advantages and drawbacks. The biomaterials applied in recent cases are presented.
Key words: Cranioplasty; Biomaterials.
Introducción
La reconstrucción de defectos craneofaciales es todavía hoy día un proceso desafiante. Diferentes técnicas y materiales han sido empleados en la remodelación craneal. Especialmente la elección del material a implantar ha sido controvertida. Ésta depende del tamaño del defecto y de las condiciones del área receptora.
Se define craneoplastia como la reparación de un defecto o deformidad craneal. Las diversas técnicas de reconstrucción craneal o craneoplastias mezclan sin lugar a dudas los conceptos de arte y ciencia quirúrgica. Los distintos métodos propuestos para la reconstrucción craneal desde la prehistoria hasta la moderna medicina tratan de solucionar defectos craneales de múltiples etiologías. La persistencia de traumatismos craneofaciales y procedimientos neuroquirúrgicos aporta un número importante de casos que permiten un fascinante progreso y desarrollo de nuevos materiales.
Revisión histórica
Los trépanos craneales, procedimiento quirúrgico más antiguo conocido, fueron practicados por muchas civilizaciones en la antigüedad. En Perú existe una amplia evidencia que los "cirujanos" preincaicos realizaron dicho tratamiento 3000 años antes de Cristo (Fig. 1). Se han descubierto cráneos trepanados incaicos junto a conchas y placas de plata y oro. También existen evidencias de cráneos con estos materiales colocados in situ cubriendo el defecto craneal. El ejemplo más notable es un cráneo que data de 2000 antes de Cristo hallado en Cerro Colorado (región de Paracas, Perú).1 Presentaba un defecto frontal izquierdo cubierto con una placa de oro de 1 mm de espesor. Se comenta que en dichas civilizaciones la reconstrucción con metales preciosos quedaba reservada para las clases sociales altas mientras que el empleo de elementos más débiles y comunes se aplicaba a las clases sociales deprimidas.
En la cultura celta neolítica se han encontrado fragmentos de cráneo redondeados u ovalados presumiblemente procedentes de cráneos trepanados. En ocasiones presentaban un orificio central formando un "anillo", el cual poseía cierto carácter mágico. Un cráneo encontrado en Crichel Down (Reino Unido,1938) contenía un gran anillo que había sido recolocado en la cavidad trepanada original. Los márgenes craneales no demostraban evidencia de curación, de manera que la craneoplastia pudo ser realizada postmortem. Se demuestra, sin embargo, que el concepto de craneoplastia no era extraño a las antiguas culturas europeas.
Autores de la antigua Asia, Egipto, Grecia y Roma aportan pocas innovaciones respecto a las culturas previas. Es a partir del siglo XVI cuando se plantean nuevas "ideas" respecto a la reconstrucción craneal. Fallopius proponía que el hueso del trépano podía ser repuesto tras el procedimiento inicial si la duramadre no había sido violada. Si existían desgarros durales, el hueso era eliminado y se empleaba una plancha de oro. Ésta es quizá la primera descripción recogida de una verdadera craneoplastia. Algunos contemporáneos suyos como Paré no daban crédito a sus prácticas.
La primera craneoplastia exitosa con injerto óseo fue descrita por Job Janszoon van Meekeren, un cirujano holandés que trató a un noble ruso que había sufrido una pérdida de una porción craneal tras el impacto de una espada. Se procedió a la reconstrucción con un fragmento craneal de un perro muerto adaptándolo al defecto. El conocimiento del caso por parte de las autoridades competentes de la época significó la excomunión del paciente del país, sin tomar medida alguna contra el cirujano.1
A comienzos del siglo XIX, los nativos de los mares del Sur utilizaban la cáscara del coco como material para craneoplastia y en el reciente siglo XX se empleó cuerno de búfalo como material reconstructivo.
Una gran variedad de materiales han sido empleados a lo largo de la Historia en la reconstrucción de defectos craneales. Ya desde el siglo pasado, se trata de encontrar el sustituto óseo ideal a emplear y se describen algunas de sus características como resistencia, maleabilidad, térmicamente no conductivo, esterilizable, inerte, radiolúcido, no magnético, disponible y barato.
Sin duda alguna, los sustitutos óseos metálicos han supuesto un gran avance en los biomateriales disponibles para la reparación craneal. El aluminio fue el primer metal en la historia reciente en emplearse. Inicialmente descrito por Booth y Curtis (1893),2 provocaba una importante reacción tisular, era epileptógeno y sufría una lenta desintegración, de manera que su uso no se generalizó.
Metales preciosos como el oro y la plata también fueron empleados a finales del siglo XIX. Gerster3 y Sebileau,4 respectivamente, describieron su aplicación como sustituto craneal. Entre sus desventajas destacaban el alto coste, la debilidad del metal en estado puro y, aplicado a la plata, la tinción del tejido adyacente.
El uso de plomo (Mauclaire, 1908),5 provocó en algunos casos intoxicación sistémica por dicho metal implicando la retirada de las placas, decreciendo significativamente su popularidad.
Otros metales utilizados fueron el platino, vitalio, ticonio, cromo, molibdeno, caracterizados todos por su falta de maleabilidad.
El tantalio fue descubierto en 1802. Fue propuesto como agente para craneoplastias en 1942, tras experimentos en perros que no mostraban reacción tisular. Es radiopaco y las pruebas de imagen postoperatorias eran difícilmente valorables. Su empleo fue sustituido por compuestos acrílicos y por titanio.
Al finalizar la II Guerra Mundial, Boldrey,6 introdujo las mallas de acero, recomendadas inicialmente para defectos de pequeño tamaño dada su escasa resistencia a los traumatismos. Comparte muchas propiedades con el tantalio y su gran ventaja era su bajo coste.
Estado actual
El titanio es un elemento que fue descubierto en 1796 pero no llegó a estar disponible comercialmente hasta 1946, tras el proceso de reducción del tetraclorhidro de titanio. Simpson,7 en 1965, fue el primero en emplearlo en reconstrucción craneal. Comparado con el tantalio, es mucho más radiolúcido y considerablemente menos caro. Otras ventajas son su biocompatibilidad y su alta resistencia mecánica. Es inerte, no carcinogénico ni alergénico.
La reconstrucción de defectos craneales con titanio se realiza con mallas. Fueron originalmente desarrolladas durante la Guerra de Vietnam. Con el paso del tiempo se han introducido refinamientos como la reducción del grosor, aumento de resistencia y maleabilidad. Previamente han sido empleadas en reconstrucción mandibular y en maxilares atróficos. Los buenos resultados obtenidos propiciaron un incremento en el número de aplicaciones.
Su uso está indicado en áreas que no soporten cargas y se emplea en las siguientes situaciones:8
1. reconstrucción inmediata en el tratamiento primario de fracturas conminutas craneales con pérdida de hueso en defectos de hasta 25 cm2. En estas situaciones las miniplacas no permiten habitualmente la fijación de todos los fragmentos óseos y por tanto la obtención de resultados estéticos óptimos.
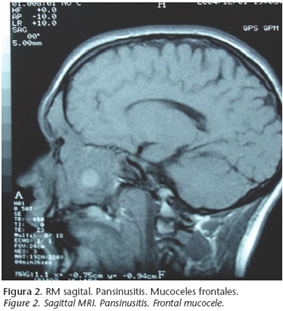
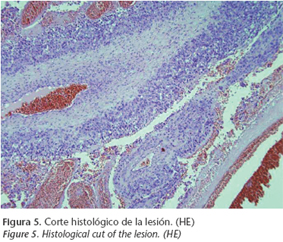
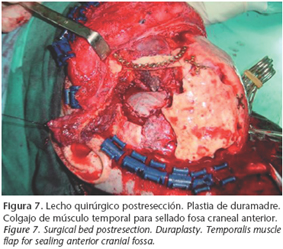
2. tratamiento de irregularidades en el contorno craneal (Figs. 2 a 5).
Entre las ventajas de esta técnica reconstructiva destacan su alta biocompatibilidad y aplicabilidad (incluso en contacto directo con senos paranasales), fácil manejo, combinación posible con hueso u otros biomateriales, mínima alteración en las pruebas de imagen postoperatorias; presenta reconstrucciones tridimensionalmente estables en estructuras anatómicas complejas, sin morbilidad de la zona donante y con baja susceptibilidad de infección.
Janecka,9 presenta una amplia experiencia en empleo de mallas de titanio en cirugía de la base craneal. La tasa de complicaciones es del 5%, si bien en gran parte aplicable a la calidad de los tejidos blandos.
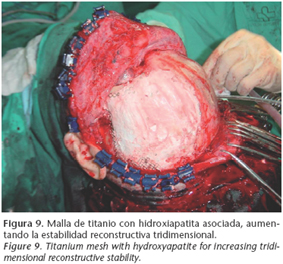
Como ya hemos comentado, es posible la combinación de mallas de titanio con otros biomateriales como la hidroxiapatita (Figs. 6 a 9). La malla desempeña el papel de soporte estructural en la reconstrucción y el efecto osteoconductivo que aporta la hidroxiapatita permite un crecimiento óseo progresivo en el defecto craneal.10 Se crea así un ajuste tridimensional más preciso en el contorno craneal, aumentando la estabilidad y la resistencia a fuerzas de tensión. Permite la reconstrucción de defectos craneales moderados-extensos, mayores incluso de 25 cm2.
Algunos autores,11 defienden el empleo de una malla de titanio o reabsorbible interpuesta entre la duramadre y el cemento de hidroxiapatita para evitar que las pulsaciones cerebrales y de la dura puedan interferir en el fraguado del cemento. Sin la malla se provocarían pequeñas microfracturas en la hidroxiapatita que desencadenarían una inflamación local, infección y posterior extrusión y fracaso del implante. La combinación malla-hidroxiapatita no tiene un impacto negativo en la biocompatibilidad, osteoconductividad y capacidad de remodelado del cemento.
La incapacidad para obtener antiguamente radiografías fácilmente interpretables con el uso de metales para craneoplastia era un gran handicap y fue una de las primeras razones por la que muchos cirujanos trataron de descubrir y emplear nuevos sustitutos óseos no metálicos.
El desarrollo de nuestra especialidad y, en concreto, de la reconstrucción craneal se encuentra íntimamente relacionado con las grandes guerras a nivel mundial. Durante la II Guerra Mundial se produjeron una gran cantidad de defectos craneales. Aunque el tantalio era uno de los materiales de elección en dicha época, existía un creciente interés por las resinas de acrílico. Justo tras finalizar la II Guerra Mundial, dichas resinas eran empleadas como material para prótesis dentales con buenos resultados. A partir de ahí se propuso que podrían tener un papel importante en la reconstrucción craneal. Una de sus ventajas iniciales era su mayor radiolucidez.
Así, el metilmetacrilato fue descubierto en 1939. Entre sus cualidades incluía gran resistencia a la tensión y al calor. Es un material inerte. Fue empleado por primera vez de forma experimental como material para craneoplastia en un ratón en 1940. Zander,1 fue el primero en emplearlo en humanos en octubre del mismo año. En su evolución se han desarrollado placas preformadas y preesterilizadas que facilitan su empleo.
Actualmente es uno de los biomateriales más empleados en la reconstrucción craneal, quizá por su elevada resistencia a las fuerzas externas, su biodisponibilidad y bajo coste. Presenta una excelente biocompatibilidad con los tejidos adyacentes; sin embargo, se han descrito reacciones a cuerpo extraño tras su empleo con la consiguiente infección en el área quirúrgica de implantación.12 A nivel intraoperatorio, la polimerización del polimetilmetacrilato da lugar a una reacción exotérmica significativa alcanzando temperaturas de hasta 80º. Se crea una reacción térmica que puede lesionar los tejidos adyacentes. Esto puede ser evitado empleando las previamente citadas placas moldeadas y preformadas (diseño tridimensional computerizado).
Es un material inerte (ausencia de sustitución ósea); no existe una integración efectiva con el hueso receptor. Persiste a largo plazo una interfase hueso-implante. Algunos estudios muestran una mejora en la osteointegración tras sumergir el implante en gel de ácido poliláctico-glicólico.13
La tasa de infección global se aproxima al 5% según los distintos estudios. Sin embargo, Manson,14 muestra un éxito total sin infecciones en su serie de 42 craneoplastias con metilmetacrilato. Pacientes con reconstrucción simultánea craneal, orbitaria o nasal presentan una tasa de infección del 23%. Los pacientes que desarrollan infección del implante han presentado previamente infección de la zona donde se coloca el metilmetacrilato. Para Manson dicho material es de elección en pacientes adultos con buena calidad de tejidos blandos sin historia previa de infección local.
HTR (Hard Tissue Replacement) es un polímero de polimetilmetacrilato- polihidroximetilmetacrilato. Presenta una alta resistencia a las fuerzas de compresión y biocompatibilidad. Contiene microporos en su estructura de 250-300 micrones, permitiendo teóricamente la invasión inicial de tejido fibrovascular y la posterior sustitución ósea. En su superficie existe una cubierta hidrófila con carga negativa que evita la adhesión bacteriana y disminuye por tanto el riesgo de infección.
Se realiza una TC tridimensional de alta resolución (cortes cada mm) que determine el defecto de forma precisa y permita el diseño del implante. Se precisa un software compatible con el de la empresa que manufactura el producto y 6-8 semanas de espera para la recepción del mismo. La fijación al cráneo se realiza con placas de titanio o reabsorbibles.15 Permite la reconstrucción de defectos craneales de más de 100 cm2 (Figs. 10 a 13).
Son muchos los biomateriales empleados a lo largo de la historia en la reconstrucción craneal. La búsqueda del biomaterial ideal es objeto de numerosos estudios clínicos. Parece lógico pensar que la sustitución ósea progresiva del implante es una condición indispensable para la obtención del biomaterial idóneo.
Ha sido introducida en las últimas décadas la hidroxiapatita como material útil en las distintas craneoplastias. Es el componente mineral primario del hueso, compuesto por moléculas de fosfato cálcico interconectadas formando una estructura hexagonal.
Inicialmente (mediados del siglo XX) estuvo disponible en formas cerámicas, creadas tras someter las preparaciones de fosfato cálcico a altas temperaturas. Poseen una porosidad limitada y su gran desventaja es que se trata de implantes preformados.16
En consecuencia, existió un gran ímpetu por desarrollar formas no cerámicas de hidroxiapatita (cementos) que pudieran ser moldeadas intraoperatoriamente hasta alcanzar el tamaño deseado. Fueron desarrollados en 1986 por la Asociación Dental Americana y aprobados por la FDA en 1996 para su aplicación en humanos. Estos implantes no son sometidos a altas temperaturas para su génesis (cristalización de la hidroxiapatita). Soporta inicialmente fuerzas de compresión menores que el PMMA. No es recomendado su uso en áreas que soporten cargas dado que su resistencia a las fuerzas de tensión es baja. Sus microporos favorecen la progresiva tendencia a la incorporación y posterior sustitución por el hueso nativo que lo rodea. Actúa como un material osteoconductor, debiendo estar en contacto con el hueso sano que lo rodea. Su composición implica ausencia de reacciones a cuerpo extraño, disminuyendo así el riesgo de infección y posterior extrusión. Puede ser empleada para la reparación de defectos craneales completos o en forma de injerto onlay sobre la cortical interna o díploe remanente (Fig.14). Si la reconstrucción craneal es de espesor total, es preciso asociar mallas que eviten la fragmentación de la hidroxiapatita en el proceso de fraguado por las pulsaciones durales. Además, facilitan el proceso de regeneración ósea guiada. Se han descrito tasas de infección de hasta un 5%.
Es controvertido el efecto de este biomaterial en el crecimiento craneal. Aunque estudios en animales no han demostrado un efecto negativo en el crecimiento craneal, parece adecuado evitar su uso en los 4-5 primeros años de vida (el cerebro alcanza el 80% del tamaño adulto a los 2-3 años), periodo de crecimiento craneal más rápido.16
Aunque la hidroxiapatita tiene un papel importante en la reconstrucción craneal, el sustituto óseo ideal no ha sido hallado. Hasta la fecha no existe evidencia histológica de crecimiento óseo significativo en humanos tras un periodo de seguimiento de 3 años. Se están desarrollando estudios que aumenten el potencial osteogénico innato de la hidroxiapatita (osteoinducción) combinándola con otros biomateriales tipo proteínas óseas morfogenéticas como la osteogenina o con el fosfato beta tricálcico. 17
Sin duda, el futuro de la reconstrucción craneal está en las técnicas de biología molecular, tratando de desarrollar el proceso de osteoinducción mediado por las proteínas óseas morfogenéticas. En el futuro dichas proteínas impregnarán el implante, aportando así propiedades osteoconductivas-osteinductivas.
Discusión
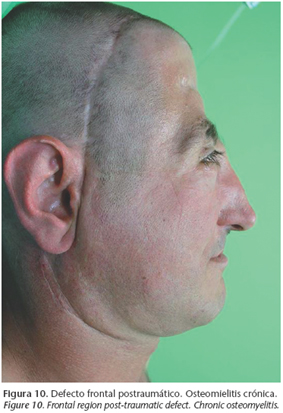
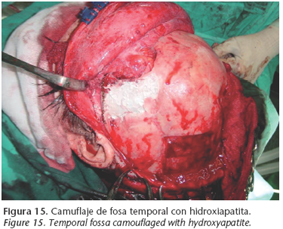
Los defectos craneales pueden ser divididos en congénitos y adquiridos, siendo estos últimos los más frecuentes. En la mayoría de los casos se trata de defectos postraumáticos. Entre las patologías congénitas a reconstruir se encuentran los meningoceles, encefaloceles, forámenes parietales masivos, aplasia cutis con agenesia craneal, cráneos bífidos. Sin embargo, las técnicas quirúrgicas reconstructivas han de emplearse con más frecuencia en la corrección de los defectos craneales que surgen tras la corrección quirúrgica de las craneosinostosis. Dentro de la patología adquirida incluimos casos postraumáticos (craniectomías descompresivas), oncológicos (tras exéresis de hueso craneal o para relleno de fosa temporal tras empleo de músculo temporal) (Fig. 15), osteomielitis craneal La región craneal más frecuentemente reconstruida es la región frontal.
En general, con la excepción de defectos craneales en niños menores de 3-4 años, no existe osteoneogénesis craneal propiamente dicha. Defectos pequeños, particularmente aquellos cubiertos por músculo (excepto en la región frontal) pueden no requerir craneoplastias . Tampoco está indicado en áreas que soporten cargas. En el resto de los casos son planteables técnicas reconstructivas craneales por dos motivos claros:
1. Consideraciones estéticas.
2. Protección frente a traumatismos.
Muchos factores pueden retrasar la corrección quirúrgica craneal. Sin embargo, se recomienda un mínimo de 3 meses de espera en casos postraumáticos y un mínimo de 6 meses en casos con infecciones locales, previa instauración de tratamiento antibiótico crónico.
Son muchas las características descritas que debe poseer un biomaterial, si bien no se ha encontrado el ideal. Entre ellas se encuentra la biocompatibilidad, fuerza, resistencia a la fractura y a la conducción térmica, inerte, esterilizable, bajo coste, radiolucidez, maleabilidad, osteoactividad.18
Asimismo, presentan ventajas frente a los injertos autógenos, como ausencia de morbilidad en la zona donante, disponibilidad, ausencia de reabsorción, fáciles de moldear, resultado cosmético superior. La mayor desventaja es que no dejan de ser cuerpos extraños, desencadenando ocasionalmente reacciones inflamatorias locales que pueden dar lugar a infecciones locales, provocando la extrusión y el fracaso del implante.
Es difícil atribuir muchas de las complicaciones exclusivamente al material que vamos a implantar, estando íntimamente asociadas a la técnica quirúrgica, respuesta del huésped y condiciones locales de la zona a recontruir.19 Quizá no sea tan importante el biomaterial a emplear y sí la calidad de las partes blandas de la región receptora del implante y el adecuado manejo de los senos paranasales que pudieran estar implicados.
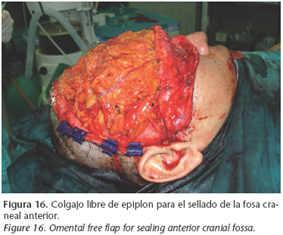
La creación de un espacio muerto intracraneal puede surgir tras la realización de una craneoplastia, bien por retracción dural cicatricial bien por pérdida de masa encefálica. El manejo de dicha situación es controvertido, pudiendo optar por el aislamiento estricto de los senos paranasales con colgajos locales,20 frente a la obliteración completa del espacio muerto mediante colgajos libres microvascularizados (Fig. 16).21
Conclusiones
La obtención de un resultado clínico satisfactorio en la reconstrucción craneal depende de:
1. Selección de un biomaterial que reproduzca la estructura rígida craneal según el tamaño y forma del defecto.
2. Lecho receptor óptimo que favorezca la estabilidad de la reconstrucción a largo plazo y la vascularización del implante, manteniendo el resultado estético perseguido.
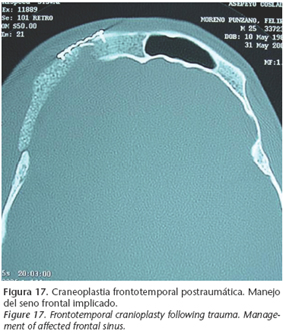
3. Manejo adecuado de los senos paranasales (Fig. 17).
Bibliografía
1. Sanan A, Haines S. Repairing holes in the head: a history of craneoplasty. Neurosurgery 1997; 40: 588-603. [ Links ]
2. Booth JA, Curtis BF. Report of a case of tumor of the left frontal lobe of the cerebrum: Operation-Recovery. Ann Surg 1893;17:128-39. [ Links ]
3. Gerster AG. Heteroplasty for defect of skull. Trans Am Surg Assoc 1895;13:485-6. [ Links ]
4. Sebileau S. Réparations craniennes par plaques osseuses. Lyon Med 1903;126:140-1. [ Links ]
5. Mauclaire P. Prosthese d´ivore pour reparer les pertes de substance du crane. Soc Chir Bull Mem 1914;40:113-5. [ Links ]
6. Boldrey E. Stainless steel wire-mesh in the repair of small cranial defects. Ann Surg 1945;121: 821-825. [ Links ]
7. Simpson D. Titanium in cranioplasty. J Neurosurg 1965;22:292-3. [ Links ]
8. Kuttenberger J, Hardt N. Long-term results following reconstruction of craniofacial defects with titanium micro-mesh systems. J Craniomaxilofac Surg 2001;29:75-81. [ Links ]
9. Janecka I. New reconstructive technologies in skull base surgery. Arch Otolaryngol Head Neck Surg 2000;126:396-401. [ Links ]
10. Ducic Y. Titanium mesh and hydroxyapatite cement cranioplasty: a report of 20 cases. J Oral Maxillofac Surg 2002;60:272-6. [ Links ]
11. Losee J y cols. Reconstruction of the inmature craniofacial skeleton with a carbonated calcium phosphate bone cement: interaction with bioresorbable mesh. J Craniofac Surg 2003;14:117-24. [ Links ]
12. Feith R. Side –effects of acrilic cements implanted into bone: a histological, angiografic, fluorescence-microscopic and autoradiografic study in the rabbit femur. Acta Orthop Scand 1975;161:3. [ Links ]
13. Dean D y cols. Osseointegration of preformed polymethylmethacrylate craniofacial prostheses coated with bone marrow impregnated poly foam. Plast Reconstr Surg 1999;104:705-12. [ Links ]
14. Manson P,Crawley W,Hoopes J. Frontal craneoplasty: risk factor and choice of cranial vault reconstructive material. Plast Reconstr Surg 1986;77:888. [ Links ]
15. Eppley B. Craniofacial reconstruction with computer-generated HTR patient matched implants: use in primary bony tumor excision. J Craniofac Surg 2002;13:650-7. [ Links ]
16. Hollier L, Stal S. The use of hydroxyapatite cements in craniofacial surgery. Clin Plastic Surg 2004 ;31:423-8. [ Links ]
17. Gosain A y cols. A 1 year study of osteoinduction in hydroxyapatite derived biomaterials in an adult sheep model: part II. Plast Reconstr Surg 2004;114:1155- 63. [ Links ]
18. Gosain A. Biomaterials for reconstruction of the cranial vault. Plast Reconstr Surg 2005;116:663-6. [ Links ]
19. Younghoon R. Biomaterials in craniofacial reconstruction. Clin Plastic Surg 2004;31:377-85. [ Links ]
20. Lee Ch, Antonyshyn O, Forrest C. Cranioplasty: indications, technique and early resuls of autogenous split skull cranial vault reconstruction. J Craniomaxillofac Surg 1995;23:133-42. [ Links ]
21. Netscher d. Management of residual cranial vault deformities. Clin Plast Surg 1992;19:301-3. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Ignacio Zubillaga Rodríguez
Servicio de Cirugía Oral y Maxilofacial.
Hospital Universitario 12 de Octubre
Avda. de Córdoba s/n.
28041 Madrid, España
E-mail: ignaciozubillaga@yahoo.es
Recibido: 19.01.05
Aceptado: 06.10.06











 texto en
texto en