My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Clínica y Salud
On-line version ISSN 2174-0550Print version ISSN 1130-5274
Clínica y Salud vol.19 n.3 Madrid Jan./Dec. 2008
ARTÍCULO
Simulación del dolor en el contexto médico-legal
Malingered pain in the medico-legal setting
Héctor González Ordi1
Pilar Capilla Ramírez2
Blanca Matalobos Veiga3
1Universidad Complutense de Madrid.
2FREMAP Madrid II
3CIPSO, Centro Integral Psico-Somático, SLP.
RESUMEN
Se presenta una revisión del estado actual de la literatura científica en relación a la detección de la simulación del dolor crónico en el contexto médicolegal. De acuerdo con los criterios diagnósticos propuestos por Bianchini, Greve y Glynn (2005) sobre la simulación del dolor y discapacidad, se exponen las diferentes estrategias médicas y psicológicas para la detección de simulación dentro de un marco de actuación multidimensional, incluyendo la existencia de beneficios externos y la evidencia convergente de los datos prevenientes de la evaluación física (médica), neuropsicológica y mediante autoinforme para establecer el diagnóstico de simulación.
ABSTRACT
This paper reviews the state-of-the-art of scientific literature on the detection of malingered pain in a medico-legal setting. Based on Bianchini, Greve & Glynn (2005), criteria for detecting malingered pain-related disability, medical and psychological assessment strategies and procedures within a multidimensional framework are addressed, including evidence of external benefits and physical (medical), neuropsychological, and self-report convergent data for the diagnostic of malingering.
Palabras clave
Simulación, Dolor, Discapacidad, Criterios diagnósticos, Evaluación.
Key words
Malingering, Pain, Disability, Diagnostic Criteria, Assessment.
Introducción
El concepto de simulación se incorpora como entidad clínica diagnóstica en la tercera edición del Manual Diagnóstico y Estadístico de los Trastornos Mentales editado por la Asociación Americana de Psiquiatría en 1980, el DSM-III; actualmente, en el DSM-IV-TR, se incluye dentro de la sección dedicada a "problemas adicionales que pueden ser objeto de atención clínica". Así, se entiende por simulación la producción intencional de síntomas físicos y/o psicológicos falsos o exagerados motivados por incentivos externos. La simulación implica la existencia de recompensas externas (cobro de seguros e indemnizaciones, etc.), a diferencia de los trastornos facticios, y se realiza consciente y deliberadamente, a diferencia de los trastornos somatomorfos (American Psychiatric Association, 2000).
Adicionalmente, el DSM-IV-TR sugiere que debe sospecharse de simulación si existe alguna de las combinaciones presentes: (1) presentación en un contexto medicolegal; (2) discrepancia acusada entre el estrés o la alteración explicados por la persona y los datos objetivos de la exploración médica; (3) falta de cooperación durante la valoración diagnóstica e incumplimiento del régimen de tratamiento prescrito y (4) presencia de trastorno antisocial de la personalidad.
Los esfuerzos por operativizar el concepto de simulación por parte del DSM contribuyeron clarificar que la simulación no podía considerarse un trastorno mental per se, zanjando un viejo debate nosológico (Widows y Smith, 2005). No obstante, los criterios diagnósticos para considerar sospecha de simulación propuestos resultaban demasiado limitados en su definición para ser considerados suficientemente fiables (Gerson, 2002). De hecho, el empleo aislado de los criterios diagnósticos DSM-IV puede llevar a incrementar el diagnóstico de falsos positivos por simulación hasta en un 80% (Rogers, 1990). Además, uno de los aspectos de mayor controversia, la presencia de trastorno de personalidad antisocial como indicador potencial de simulación, no ha recibido suficiente apoyo empírico hasta el momento (Rogers, Gillis y Bagby, 1990). En definitiva, los criterios DSM-IV-TR son necesarios pero no suficientes.
Como respuesta a las limitaciones de los criterios DSM-IV en la evaluación de la simulación, se han propuesto modelos alternativos que enfatizan específicamente el examen detallado de los datos de las pruebas y la concurrencia de la información antecedente disponible (ver Rogers y Bender, 2003). La simulación es un fenómeno multideterminado y multidimensional por lo que requiere de más que una estrategia unidimensional para su detección (González Ordi y Gancedo Rojí, 1999; Hutchinson, 2001). La detección de la simulación se fundamenta en la idea central de la convergencia de los datos que provienen de distintas fuentes de información: entrevista, historia clínica, pruebas médicas, pruebas psicológicas, evaluación conductual, etc. La mejor práctica clínica implica el uso de criterios diagnósticos múltiples en oposición a la utilización de un único test (Slick, Sherman y Iverson, 1999), así como la utilización de enfoques evaluativos que incluyan la combinación de tests especializados e indicadores de validez (Iverson, 2003).
Esto es tanto más cierto cuando consideramos la evaluación de la simulación en el dolor crónico, ya que es comúnmente aceptado que el dolor crónico es un fenómeno complejo, multifacético y multidimensional, que requiere un abordaje multidisciplinar de carácter eminentemente biopsicosocial (Gatchel, Peng, Peters, Fuchs y Turk, 2007; Melzack y Katz, 2006); por consiguiente, la detección de la simulación en el dolor crónico debería ser necesariamente multidimensional (Bianchini, Greve y Glynn, 2005; McDermott y Feldman, 2007).
Incidencia de la simulación en dolor crónico
Diversos estudios han tratado de determinar la incidencia de la simulación del dolor crónico, aunque ciertamente resulta difícil proporcionar datos precisos debido a que existe una gran variabilidad en función del campo de estudio o la patología que se aborda en cuestión. Uno de los estudios epidemiológicos más clásicos en el campo médico-legal es el de Mittenberg, Patton, Canyock y Condit, (2002).
Respecto al campo de estudio o ámbito de referencia, Mittenberg et al. (2002), establecen las siguientes tasas de incidencia: (1) lesiones personales un 29%; (2) discapacidad o indemnización laboral entorno a un 30%; (c) casos criminales en un 19%; y (d) casos procedentes de la medicina general o psiquiatría un 8%.
Como puede apreciarse, el ámbito de actuación médico-legal, vinculado a la valoración de la discapacidad y a los posibles beneficios laborales y socioeconómicos derivados de la misma, es el que registra una mayor tasa de incidencia de simulación, sin contar con que muchos de los casos procedentes de otros ámbitos pueden implicar posteriormente bajas laborales, procesos de rehabilitación prolongados y valoración de discapacidad con implicaciones económicas.
Por patologías, Mittenberg et al. (2002) informan de las siguientes tasas de incidencias: traumatismo craneoencefálico (TCE) leve un 38,5%, fibromialgia o fatiga crónica un 34,7%, dolor o trastornos somatoformes alrededor de un 31,4%, trastornos neurotóxicos un 26,5%, lesión por accidente con electricidad un 21,9%, trastornos por depresión un 14,9%, trastornos de ansiedad 13,5%, trastornos disociativos un 10,5%, trastorno con base epiléptica un 9,3%, TCE moderado o severo un 8,8% y demencia vascular un 2,4%.
Como puede observarse, los trastornos asociados al dolor crónico (fibromialgia, fatiga crónica, dolor o trastornos somatoformes) se encuentran a la cabeza de los índices de incidencia y representan en total más de la mitad de la incidencia de simulación por patologías, entorno al 66%; sin contar con que, a menudo, los TCE cursan también con cervicalgia y omalgia. De hecho, otros estudios sugieren que la incidencia de simulación de dolor es significativamente alta, estimándose los rangos de prevalencia entre un 25% y un 30% tanto para fibromialgia (Gervais, Russell, Green et al., 2001) como para dolor crónico en general (Gervais, Green, Allen et al., 2001). Hamilton y Feldman (2001) incluyen además la cervicalgia y el esguince cervical entre las patologías dolorosas más simuladas. No en vano, el DSM-IV-TR (APA, 2000) advierte que un aspecto a considerar en el diagnóstico diferencial del trastorno por dolor es que el síntoma o déficit no sea simulado o producido intencionalmente (p. 565).
En general, los datos indican que en el contexto médico-legal los patrones de simulación están más relacionados con la exageración de síntomas, como el dolor, y la discapacidad relacionada con trastornos y enfermedades físicas con la posibilidad de obtener incentivos económicos; mientras que, la simulación de sintomatología psicopatológica sería más prevalente en contextos forense o criminales, con el fin de reducir o evitar el pago de indemnizaciones, condenas y encarcelamientos (McDermott y Feldman, 2007).
Detección multidimensional de simulación en dolor crónico
Un principio fundamental en la detección de simulación es que cuantas más inconsistencias presente un paciente a lo largo de la realización de diferentes pruebas relativamente independientes y en diferentes dimensiones, más plausible resultará pensar que su rendimiento refleja un esfuerzo deliberado por dar una imagen falsa de sus capacidades o sintomatología (Bianchini, Greve y Glynn, 2005). De ahí que la convergencia de datos provenientes de diferentes fuentes de información sea crucial para asegurar el diagnóstico de simulación.
Desde el momento en que el dolor es un fenómeno multidimensional complejo de difícil objetivación (al no existir "dolorímetros" precisos y fiables que nos indiquen "exactamente" cuánto dolor experimenta una persona, la fuente de información principal sigue siendo el autoinforme), la simulación del dolor no se centra tanto en si existe o no dolor y cuánto dolor debería experimentar una persona en un momento determinado, sino cómo influye el dolor en la realización o no de diferentes actividades de la vida cotidiana, incluyendo por supuesto la actividad laboral. Así, el problema no es cuánto dolor experimenta la gente sino cuán incapacitante resulta el dolor para las personas.
En el contexto clínico y laboral, el tipo de simulación más frecuente es el que Resnick (1997) denomina "simulación parcial"; esto es, la exageración de sintomatología o discapacidad preexistente o la referencia al mantenimiento de síntomas que ya habían remitido. En otras palabras, el problema no es si los individuos presentan discapacidad genuina o simulada atribuible a las causas que subyacen al dolor crónico, el problema es si las personas que presentan lesiones o daños físicos, y que experimentan dolor crónico, además pueden y consiguen exagerarlos para obtener un beneficio.
La discapacidad relacionada con simulación de dolor (Malingered Pain-Related Disability) es la exageración o fabricación intencional de síntomas cognitivos, emocionales, conductuales o físicos disfuncionales, que son atribuidos al dolor con el propósito de obtener un beneficio económico, evitar el alta laboral u obtener otro tipo de incentivos (Bianchini, Greve y Glynn, 2005).
Criterios de sospecha clínica
Identificar y determinar la existencia de simulación es el punto final de un largo proceso de evaluación y diagnóstico que se inicia con la "sospecha clínica" por parte de los profesionales de la salud implicados en el tratamiento y rehabilitación del paciente. En buena medida, las sospechas clínicas de simulación están fundamentadas en las discrepancias e inconsistencias entre el diagnóstico previo y la evolución del paciente, en comparación con la evolución habitual de los pacientes en relación a la patología diagnosticada. Así mismo, la sospecha clínica de simulación se establece de forma contextual, atendiendo otros aspectos de carácter motivacional, sintomatológico, personal y conductual. Samuel y Mittenberg (2006) destacan aquellos aspectos que contribuyen a la sospecha de presencia de simulación en el contexto médico-legal:
1. Motivación y circunstancias: incentivos económicos, solución a problemas socioeconómicos, conducta antisocial, insatisfacción profesional, conflictos laborales, situación cercana a la jubilación e historia previa de engaño, simulación o actos deshonestos.
2. Sintomatología: presencia de síntomas atípicos o inusuales, exageración de la sintomatología, resultados en los tests psicológicos y sintomatología incongruente con el curso normal de la enfermedad.
3. Presentación ante la entrevista: falta de cooperación con el evaluador y con la divulgación de la información y discrepancias entre los datos de la entrevista y la historia clínica o la documentación preexistente.
4. Actividad/conducta fuera de la entrevista: actividad laboral durante el período de reclamación, realización de actividades lúdicas, no relacionadas con el trabajo, buen funcionamiento excepto en aquello relacionado con el desempeño de la actividad laboral, falta de compromiso con el tratamiento y estar bajo vigilancia.
Adicionalmente, en la Tabla 1 proponemos algunos aspectos específicos o indicadores clínicos de sospecha de simulación que se presentan comúnmente en pacientes con patologías que cursan con dolor crónico en el contexto médico-legal. Cuantos más indicadores clínicos presente el caso en cuestión, más relevante resultará realizar una evaluación pormenorizada para detectar simulación.
Criterios diagnósticos
Recientemente, Bianchini, Greve y Glynn (2005) han propuesto una serie de estándares diagnósticos referidos a la discapacidad relacionada con simulación de dolor. Sin duda, estos criterios contribuyen a operativizar considerablemente la detección de la simulación y lo hacen desde una perspectiva multidimensional, considerando un proceso de evaluación multimétodo/ multisistema.
Criterio A. Evidencia de incentivos externos significativos contingentes con un patrón de exageración o fabricación de síntomas (estatus de litigancia, pensión por discapacidad, indemnizaciones por parte de aseguradoras, prolongación de bajas laborales, obtención de más medicación psicoactiva, etc).
Criterio B. Evidencia procedente de la evaluación física. Evidencia de que las habilidades, capacidades y/o limitaciones demostradas a lo largo de una evaluación física formal son consistentes con la exageración de las quejas y síntomas somáticos y la disminución exagerada de la capacidad física. Este aspecto puede operativizarse mediante la detección de: (1) sesgos en el rendimiento físico: realización de pruebas de rendimiento que evidencian la existencia de una disminución de la capacidad física que no resulta concordante con la patología diagnosticada; (2) discrepancia entre la valoración subjetiva de dolor (v.g. EVA) y la reactividad psicofisiológica concomitante; (3) los síntomas o las quejas informadas por el paciente son sustancialmente divergentes con la evidencia patofisiológica existente; y (4) discrepancia entre la actividad física mostrada por el paciente durante la evaluación formal con la actividad física demostrada cuando el individuo no sabe que está siendo evaluado.
Criterio C. Evidencia procedente de la evaluación neuropsicológica. Evidencia de que los déficits neurocognitivos (v.g. capacidad de concentración, percepción, memoria, etc) demostrados a lo largo de una evaluación formal son consistentes con la exageración o el falseamiento de la discapacidad cognitiva. Este criterio se operativiza en: (1) rendimiento por debajo del azar en pruebas de elección forzada que evalúan funciones cognitivas o perceptivas; (2) rendimiento consistente con la exageración de la discapacidad en pruebas que evalúan funcionamiento cognitivo o perceptivo; (3) discrepancias entre los resultados de las pruebas neuropsicológicas y el conocimiento existente del funcionamiento cerebral; (4) discrepancias entre los resultados de las pruebas neuropsicológicas y la conducta observable y objetivable del paciente.
Criterio D. Evidencia procedente de la evaluación mediante autoinforme. Evidencia que los síntomas, quejas y limitaciones autoinformadas por el paciente son consistentes con un patrón de exageración de síntomas y discapacidad a nivel físico, cognitivo y/o emocional. Este criterio puede operativizarse a través de: (1) la discrepancia de la conducta del paciente cuando es formalmente evaluado versus cuando no sabe que está siendo evaluado; (2) las quejas autoinformadas no son consistentes con la evolución de la historia clínica del paciente; (3) los síntomas autoinformados por el paciente son discrepantes con los patrones conocidos de funcionamiento fisiológico y neurológico del dolor y la discapacidad referida a la patología en cuestión; (4) los síntomas autoinformados por el paciente son discrepantes con la conducta observable y objetivable; (5) presentación de un patrón de exageración de síntomas en pruebas de personalidad de amplio espectro y pruebas de screening de simulación de síntomas.
Criterio E. Los criterios mencionados no se explican mejor por factores psicopatológicos, neurológicos o evolutivos. La simulación se entiende como un patrón de conductas de carácter intencional y dirigido a la obtención de un beneficio externo, generalmente de tipo económico. A continuación, procederemos a describir brevemente las diversas pruebas, instrumentos y tests disponibles para la evaluación de las distintas dimensiones o criterios de evaluación física, neuropsicológica y de autoinforme.
Evaluación física (médica)
La falta de convergencia entre la sintomatología referida y los signos clínicos dificulta el diagnóstico de certeza, obligándonos en la práctica clínica diaria, a realizar pruebas complementarias con el fin de realizar un correcto diagnóstico diferencial con entidades nosológicas poco frecuentes antes de plantearnos la existencia de exageración de síntomas. Entre las pruebas de imagen más utilizadas se encuentran las radiografías o la resonancia magnética nuclear, que es actualmente la prueba de imagen por excelencia (Jensen, Brant-Zawadzki y Obuchowski, 1994). En cualquier caso, la interpretación de la imagen y del informe radiológico debería ser realizada siempre por el clínico que trata al paciente con el fin de asegurar la convergencia de distintas fuentes de información, ya que los hallazgos patológicos encontrados no tienen por qué ser los responsables de la sintomatología, lo que en el caso de exageración de síntomas y en especial, en el contexto médico- legal, complica aún más la situación. Así mismo, actualmente la resonancia magnética funcional (fMRI) aporta información interesante sobre las estructuras implicadas en el procesamiento del dolor, como el cortex cingulado anterior (Davis, Taylor, Crawley, Wood y Mikulis, 1997; Bantick, Wisw, Ploghaus, Clare, Smith y Tracey, 2002), y su consideración puede resultar ilustrativa en el caso de que el paciente refiera experimentar dolor pero no se encuentre evidencia neurofisiológica concomitante.
La realización de analíticas específicas o de rutina de diferentes marcadores bioquímicos puede resultar de utilidad en aquellas patologías que cursen con cansancio crónico (como la fibromialgia o el síndrome de fatiga crónica) y que nos descartaran la existencia de estados carenciales, tumorales, infecciosos, etc.
Para la evaluación de posibles trastornos funcionales es recomendable la consideración de los signos de Waddel (Waddel, McCullogh, Kummel y Venner, 1980). Los signos de Waddel son sensibles a la simulación de dolor lumbar, especialmente si se aprecian al menos tres de los 5 signos siguientes: (1) dolor a la palpación difusa superficial y no congruente anatómicamente; (2) test de simulación positivo (sobrecarga axial y rotación); (3) test distractorios positivos; (4) alteraciones regionales diferentes a las distribuciones neurológicas; y (5) hiperreacción o "conducta de dolor".
Para aquellos casos en que el paciente refiere pérdida de fuerza, podemos utilizar los tests isocineticos (Hislop y Perrine, 1967) que constituyen un modo más preciso y objetivo de valoración funcional de la fuerza realizada tanto articular como en un movimiento complejo que implique a varias articulaciones, respecto a la valoración clásica de función que se realizaba con las pruebas isométricas. Esta prueba está admitida como sistema de valoración en simulación de pérdida de fuerza, si bien en patología de columna su fiabilidad es menor que en el resto del organismo (Huesa, y Carabias,1999).
A menudo, la simulación de discapacidad provocada por una patología dolorosa suele conllevar que el paciente informe de la existencia vértigos, mareos o alteraciones del equilibrio (v.g. cervicalgia y esguince cervical), que le incapacitan para desarrollar una vida cotidiana activa. La posturografía dinámica (Bowman y Mangham, 1989) es una prueba que nos permite objetivar más precisamente esta sintomatología. Utiliza una plataforma dinamométrica montada sobre un soporte capaz de trasladarse horizontalmente, inclinarse adelante o atrás, y/o rotar alrededor de un eje alineado con los tobillos. El estudio mediante posturografía dinámica proporciona los siguientes patrones en las alteraciones del equilibrio (Barona de Guzmán, 2003): (1) patrón vestibular; (2) patrón visual; (3) patrón somatosensorial; (4) patrón de disfunción multisensorial, que es una combinación de los anteriores; (5) patrón afisiológico, que es un patrón poco consistente con la existencia de lesión orgánica, en el que el sujeto presenta mejor equilibrio en situaciones más complejas y que suele aparecer en casos de simulación o estados de ansiedad severa; y (6) patrón de normoequilibrio.
La electromiografía de inserción (aguja) y la electromiografía de superficie son técnicas útiles para evaluar la respuesta global del músculo y grupos musculares, proporcionando datos objetivables sobre la funcionalidad, la carga de trabajo en relación con diferentes niveles de esfuerzo, la fatigabilidad muscular, etc (De Luca, 1997). El EMG permite valorar la existencia de lesiones musculares o no asociadas a la presentación de dolor intenso y discapacidad, por lo que son útiles en patologías susceptibles de simulación de dolor crónico como cefaleas tensionales, migrañas, síndrome del túnel carpiano, síndrome cervicobraquial y ciatalgias.
Finalmente, el estudio con potenciales evocados acústicos, visuales y somatosensoriales puede proporcionarnos información sobre las discrepancias entre el procesamiento neurofisiológico de la información y la valoración autoinformada del paciente, ya que existe evidencia de que el estudio de la amplitud de la onda P300 ante diferentes estímulos parece discriminar entre pacientes con déficits genuinos y simulados (Rosenfeld, Ellwanger, Nolan, Wu, Bermann y Sweet, 1999).
Junto con estas técnicas y pruebas clínicas, la utilización de diferentes autoinformes específicos de medida de salud, calidad de vida e incapacidad nos permite valorar la utilidad de los tratamientos, y contrastar con los signos clínicos objetivables. Los autoinformes son utilidad en el caso de exageración de síntomas/simulación, ya que cuando los administramos en diferentes estadios de la patología dolorosa, sería esperable una convergencia con los datos clínicos; por otra parte, diferentes estudios demuestran que hay instrumentos que correlacionan entre sí, por lo que datos divergentes entre pruebas que correlacionan nos debe hacer sospechar de la existencia de falseamiento y profundizar en su estudio.
Entre ellos, destacamos el Cuestionario de Salud SF-36 (Alonso, Prieto y Anto, 1995) es uno de los instrumentos más usados a nivel nacional tanto como medida descriptiva del impacto de la enfermedad sobre la calidad de vida, como instrumento de evaluación de diferentes procedimientos terapéuticos y como referencia para validar nuevos instrumentos de medición.
El Cuestionario sobre el Impacto de la Fibromialgia – FIQ (Monterde et al., 2004) que es, hasta ahora, el único instrumento específico para medir el impacto del síndrome fibromiálgico en la capacidad funcional y calidad de vida. El FIQ además presenta una alta correlación con el SF-36, considerando que ambos cuestionarios presentan formatos de respuesta diferente, lo que resulta útil para evaluar la inconsistencia de respuestas a través de diferentes medidas, que suele presentarse en los sujetos simuladores.
La Escala de Severidad de Fatiga (Krupp et al., 1989) es un instrumento creado en neurología y su aplicación más extensa es en Esclerosis Múltiple y Lupus Eritematoso Sistémico. Consta de 9 items valorados de 0 a 7 puntos. Todos ellos hacen referencia expresa a la fatiga. Se obtienen los valores medios de las puntuaciones. Se consideran puntuaciones normales en adulto sano 2,3+/-0,7 puntos. Conociendo las puntuaciones en patologías como la Esclerosis Múltiple en fases avanzadas (con una clara severidad de fatiga objetivable), podemos sospechar la existencia de simulación/exageración de síntomas cuando las puntuaciones en esta escala se aproximan a estas puntuaciones y se alejan de la normalidad, en patologías mucho más banales.
El Neck Pain Questionnaire - NPQ (González, Balsa et al, 1999) es un cuestionario dirigido de forma específica a evaluar cómo afecta el dolor cervical a las actividades de la vida cotidiana, consta de 10 items, con 5 opciones de respuesta, puntuándose de 0-4 de menor a mayor intensidad y gravedad. Es muy utilizado en esguince cervical como medida repetida para evaluar la eficacia del tratamiento; en este sentido, la puntuación en el NPQ debería ir disminuyendo a medida que el paciente presenta una mejor movilidad de columna cervical y menos contracturas, ya que este cuestionario valora específicamente aspectos para los cuales es preciso una buena movilidad del cuello. Si esto no ocurre debe hacernos pensar en un patrón de exageración de síntomas y mantenimiento intencional de la discapacidad.
El Índice de Discapacidad de Oswestry - IDO (Fairbank y cols, 1980) permite evaluar el impacto del dolor lumbar en las actividades de la vida cotidiana. Esta es una prueba que proporciona valores en porcentajes de incapacidad. En este sentido, valores iguales o mayores al 80% sugieren la posibilidad de exageración de síntomas, lo que exige una valoración más pormenorizada de la existencia de simulación.
Finalmente, el Índice de Discapacidad Cronica de Waddel (Waddel y cols., 1984) evalúa si una actividad cotidiana concreta se ha visto reducida, si se evita o si se necesita ayuda como consecuencia del dolor lumbar. El IDC de Waddel correlaciona con el IDO, lo que puede resultar útil para valorar la inconsistencia de respuestas del paciente simulador a través de pruebas diferentes.
En general, los sujetos simuladores presentarán en las pruebas de autoinforme comentadas puntuaciones altas en índices de incapacidad, peor calidad de vida y peor estado de salud. Por otra parte, veremos que las puntuaciones de los diferentes instrumentos varían poco con los diferentes tratamientos aplicados, no correlacionan con los datos clínicos objetivables ni con otros instrumentos que valoran aspectos similares. El conjunto de pruebas, la divergencia entre ellas, la normalidad de las mismas o patrones que no se encuadran en lo esperado desde el punto de vista fisiológico es lo que, junto a la exploración física y los datos obtenidos en los instrumentos de evaluación de calidad de vida e incapacidad, nos orientará hacia la sospecha de exageración de síntomas.
Evaluación neuropsicológica
La patología dolorosa cronificada y la discapacidad asociada (v.g. esguince cervical y cervicalgia) a menudo cursa con déficits neurocognitivos relacionados con dificultades en concentración, percepción y memoria. Este aspecto debe tenerse en cuenta de forma relevante porque los simuladores suelen exagerar la presentación del deterioro neurocognitivo con el fin de mantener la imagen de discapacidad. No obstante, hemos de señalar que la evaluación neuropsicológica se ha considerado en la detección de simulación en dolor crónico de forma mucho menos extensiva que en otras patologías como el traumatismo craneoencefálico, donde naturalmente resulta la estrategia evaluativa de elección.
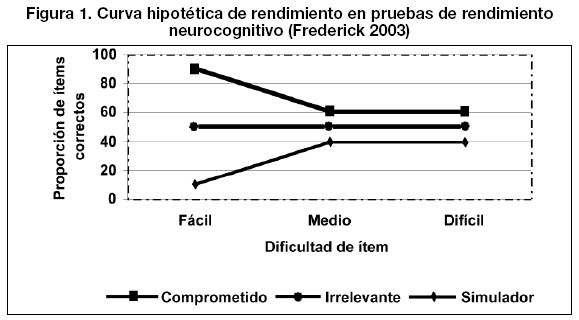
El rendimiento neurocognitivo en pruebas de evaluación neuropsicológica de los sujetos simuladores se caracteriza, entre otros patrones de ejecución, por presentar un menor porcentaje de respuestas correctas en los ítems fáciles o simples que en los ítems medios o difíciles (rendimiento subóptimo), por debajo del nivel esperado por azar (comprobación de validez de síntomas o SVT), y significativamente menor que los sujetos comprometidos honestamente con la realización de la prueba, presentado además un nivel de deterioro más severo que los pacientes con deterioro neuropsicológico genuino moderado o grave, tal y como puede apreciarse en la Figura 1 (Frederick, 2003).
Es por ello que, aunque existen diversas estrategias para detectar el engaño en pruebas neuropsicológicas (ver Bender y Rogers, 2004), el tipo de instrumentos neuropsicológicos que se más utilizan en la detección de simulación se basan en el denominado "efecto suelo"; esto es, pruebas sencillas pero que presentan una validez aparente de mayor complejidad, lo que lleva a los simuladores a sobrestimar su nivel de dificultad y a obtener un rendimiento inferior al de personas con una disfunción cerebral más grave (Muñoz Céspedes y Paúl Lapedriza, 2001).
De hecho, en una encuesta realizada a neuropsicólogos expertos en evaluación de la simulación en el contexto médicolegal, Slick, Tan, Strauss y Hultsch (2004) encontraron que, aunque eran partidarios de usar baterias neuropsicológicas de forma flexible, los instrumentos específicos más comúnmente utilizados para detectar rendimiento subóptimo eran el Test of Memory Malingering – TOMM (Tombaugh, 1996) y el test de los 15 items de Rey (Lezak, 1995).
El Test of Memory Malingering – TOMM (Tombaugh, 1996) es una prueba de screening diseñada específicamente para detección de simulación neurocognitiva y consta de dos series o ensayos con 50 dibujos/estímulos más 50 paneles de reconocimiento donde el sujeto debe identificar visualmente (no nombrar) los dibujos previamente presentados versus un dibujo distractor. Quince minutos después se administran 50 paneles de reconocimiento sobre los dibujos presentados previamente (ensayo de retención). Los simuladores presentan un porcentaje de identificación correcta de dibujos significativamente menor en la segunda serie/ensayo y en el ensayo de retención que los sujetos controles y los pacientes con deterioro cerebral genuino (Rees, 1996; Rees y Tombaugh, 1996); igualmente los pacientes litigantes con deterioro cerebral traumático presentan un peor rendimiento, por debajo del azar, que los pacientes no litigantes (Gansler, Tombaugh, Moczynski y Rees, 1995). El TOMM ha resultado ser eficaz en la clasificación correcta de pacientes con dolor crónico que exageran deliberadamente déficits neurocognitivos (Etherton, Bianchini, Greve y Ciota, 2005; Greiffenstein, Greve, Bianchini y Baker, 2008).
Otros instrumentos que se han utilizado eficazmente en la detección de simulación de deterioro neurocognitivo en pacientes con dolor crónico son el Índice de Memoria de Trabajo del WAIS-III (Etherton, Bianchini, Ciota, Heinly y Greve, 2006), el Victoria Symptom Validity Test, el Validity Indicador Profile o el Pórtland Digit Recognition Test, entre otros (ver Slick et al., 2004).
Finalmente, algunos estudios han informado del empleo de diversas pruebas neuropsicológicas combinadas para incrementar la validez predictiva a la hora de discriminar entre pacientes simuladores y no simuladores. Meyers y Volbrecht (2003) utilizaron nueve instrumentos de evaluación neuropsicológica, obteniendo un 83% de sensibilidad y un 100% de especificidad, con una tasa igual a cero de falsos positivos, en una muestra de 796 sujetos litigantes. Aunque esta es una estrategia interesante, incrementa considerablemente el tiempo dedicado a la evaluación de la detección de simulación.
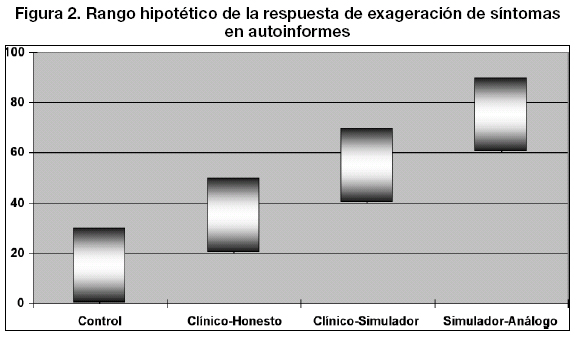
Evaluación mediante autoinformeEn la investigación clínica sobre detección de simulación utilizando pruebas de autoinforme suelen considerarse cuatro tipos de grupos de investigación: (1) grupo control, formado por sujetos sin patología previa diagnosticada, generalmente equiparados en edad y sexo, nos permiten observar cuál sería la respuesta honesta de sujetos que no evidencian la patología objeto de investigación y nos proporciona el "suelo" teórico en el rango hipotético de la respuesta de exageración de síntomas para dicha prueba o cuestionario; (2) grupo clínico-honesto, formado por pacientes clínicos que manifiestan la patología investigada pero que no se encuentran en situación litigante, por lo que es esperable que respondan honestamente al test; (3) grupo clínico-simulador, formado por pacientes clínicos que manifiestan la patología investigada y se encuentran en situación litigante, por lo que es esperable que exageren o fabriquen sintomatología para reflejar "la peor imagen posible", en nuestro caso, incremento del dolor y de la discapacidad; (4) grupo simulador-análogo, grupo de sujetos que no presentan patología alguna pero se les instruye específicamente para que simulen la patología investigada; aunque no suele ser un grupo clínico real, nos permite controlar experimentalmente la conducta de exageración de síntomas porque sabemos a ciencia cierta que están "mintiendo"; generalmente este grupo sirve también para establecer el "techo" teórico en el rango hipotético de la respuesta de exageración de síntomas para la prueba o cuestionario objeto de la investigación. En la Figura 2 puede verse una representación gráfica teórica de la distribución de la respuesta de exageración de síntomas para cada uno de los grupos comentados.
Aunque no siempre suele ser así, lo deseable es que la investigación clínica sobre la capacidad de discriminación de un instrumento psicológico en el rango de la respuesta de exageración de síntomas incluya los cuatro grupos de forma comparativa (Rogers y Bender, 2003).
En cualquier caso, cualquier prueba o cuestionario que pretenda detectar simulación, deberá mostrar una buena capacidad predictiva y exactitud (área bajo la curva), clasificando correctamente al mayor porcentaje de clínico-simuladores posible (sensibilidad) y, en especial, excluyendo correctamente al mayor porcentaje de clínico-honestos posible (especificidad), con el fin de reducir en lo posible el porcentaje de falsos positivos.
En su mayoría, estos instrumentos pretenden detectar con mayor o menor precisión patrones de "mala imagen" o estilos de respuesta sobredimensionados, o bien patrones sintomatológicos infrecuentes o excepcionales, improbables y bizarros; en otras palabras, detectar la tendencia del sujeto a crear la impresión deliberada de sufrir alguna alteración o deterioro mediante la exageración o fabricación de síntomas y problemas, maximizando las características negativas de si mismo (Baer, Rinaldo y Berry, 2003).
Entre los instrumentos de evaluación objetiva de la personalidad presentan índices de validez que han demostrado ser útiles en la detección de la simulación en dolor crónico, destacamos el MMPI-2, el Pain Patient Profile, el SCL-90-R y el Modified Somatic Perception Questionnaire. Sin embargo, otros como el Inventario Clínico Multiaxial de Millon III han demostrado resultados menos prometedores (McDermott y Feldman, 2007).
El Inventario Multifásico de Personalidad de Minnesota 2 (Butcher, Dahlstrom, Graham, Tellegen y Kaemmer, 1999) es uno de los cuestionarios más ampliamente utilizados para evaluar alteraciones psicopatológicas en el ámbito clínico en general y en el ámbito medicolegal en particular (Arbisi y Butcher, 2004; Butcher y Ben-Porath, 2004). Entre los indicadores de validez del MMPI-2 más utilizados y contrastados empíricamente para la detección de exageración de síntomas se encuentran las escalas de Infrecuencia F y Fb, la escala F-psicopatológica o Fp, el índice F-K de Gough, la Fake Bad Scale o FBS y la escala de disimulación revisada o DsR (para una revisión detallada de estas escalas consultar González Ordi e Iruarrizaga Díez, 2005).
Recientemente, Aguerrevere, Greve, Bianchini y Meyers (2008) han informado de un índice discriminante (Índice Abreviado de Meyers, IAM) para la detección de simulación basado en la combinación de pesos específicos en función de las puntuaciones obtenidas en las escalas de validez del MMPI-2 F, Fp, F-K, FBS, DsR, O-S y la escala suplementaria del MMPI-2 Es (Fuerza del Yo). Basado en estudios anteriores con dichas escalas del MMPI- 2 (Meyers, Millis y Volkert, 2002), el IAM presenta un número más reducido de escalas (F-K, F, FBS, Fp y Es), más fáciles de computar para el evaluador, pero manteniendo su capacidad predictiva para discriminar entre simuladores y no simuladores. En concreto, en pacientes con dolor crónico, el Índice Abreviado de Meyers presenta una sensibilidad del 50%, una especificidad del 95% y una exactitud predictiva (AUC) de .923, a la hora de discriminar entre pacientes simuladores y no simuladores (Aguerrevere et al., 2008).
El Pain Patient Profile o P3 (Tollison y Langley, 1995) es un cuestionario que evalúa emocionalidad negativa asociada al dolor y proporciona información sobre el grado a o nivel de depresión, ansiedad y somatización autoinformada por paciente de dolor crónico, además de incluir una escala de validez. El P3 se ha utilizado para discriminar entre pacientes simuladores y no simuladores con resultados prometedores. McGuire y Shores (2001), comparando las puntuaciones en el P3 entre un grupo clínico de dolor crónico y un grupo de simuladores análogos encontraron unos valores de sensibilidad del 70%, el 65% y el 60% para las escalas de depresión, ansiedad y somatización, respectivamente, siendo los valores de especificidad correspondientes del 85%, 72% y 87%. McGuire, Harvey y Shores (2001) en un estudio similar, pero incluyendo un grupo de dolor crónico honesto, un grupo de dolor crónico simulador y un grupo general en rehabilitación, encontraron valores predictivos muy interesantes especialmente entre los grupos de dolor honesto y simulador; así, respecto a la sensibilidad, los valores fueron del 77%, 69% y 85% para depresión, ansiedad y somatización, respectivamente; los valores de especificidad correspondieron en ese mismo orden de escalas al 77%, 73% y 87%, con un índice de exactitud global de la prueba (AUC) de .81, .79 y .89, respectivamente. En ambos estudios, los simuladores puntuaban significativamente más alto en todas las escalas clínicas que los restantes grupos.
El SCL-90-R (Derogatis, 2002) se ha utilizado para discriminar simulación en pacientes con esguince cervical litigantes y no litigantes. En concreto, Wallis y Bogduk (1996) encontraron que los pacientes litigantes puntuaban significativamente más alto en todas las escalas que los no litigantes, mostrando un claro patrón de exageración de síntomas o perfil clínico sobredimensionado.
Finalmente, el Modified Somatic Perception Questionnaire (Main, 1983) se ha utilizado también para discriminar entre pacientes simuladores y no simuladores con una sensibilidad y especificidad del 90%.
No obstante, a pesar de que tanto los instrumentos de evaluación objetiva de la personalidad como los instrumentos de evaluación neuropsicológica pueden resultar eficaces en la detección de la simulación, existen ciertas limitaciones también respecto a su utilización: (a) su administración conlleva mucho tiempo, (b) es necesario un entrenamiento especializado para su administración y (c) a menudo son pruebas complejas de interpretar (Schinka y Borum, 1993).
Razón por la cual, en los últimos años, se han desarrollado un cierto número de instrumentos de screening, rápidos y sencillos en su administración, corrección e interpretación, para detectar simulación. Entre ellos, es especialmente destacable el Inventario Estructurado de Simulación de Síntomas – SIMS.
El Inventario Estructurado de Simulación de Síntomas - SIMS (Widows y Smith, 2005 y 2009) es un instrumento de evaluación mediante autoinforme que pretende detectar patrones de exageración de síntomas de carácter psicopatológico y neuropsicológico. Su aplicación puede resultar útil, administrando como medida de screening o formando parte de una batería de evaluación más completa y pormenorizada, tanto en contextos clínicos como médico-legales o forenses.
Permite obtener una puntuación total que se refiere al perfil de simulación general que presenta el sujeto y cinco escalas específicas referidas a la simulación de síntomas de distintos trastornos psicopatológicos y neuropsicológicos: (1) Psicosis: evalúa el grado en que el sujeto presenta síntomas psicóticos inusuales o extravagantes que no son típicos de la patología psicótica real; (2) Deterioro Neurológico: evalúa el grado en que el sujeto presenta síntomas de tipo neurológico ilógicos o muy atípicos; (3) Trastornos Amnésicos: evalúa el grado en que el sujeto presenta síntomas relacionados con trastornos de memoria que son inconsistentes con los patrones de deterioro producidos por disfunción o daño cerebral real; (4) Baja Inteligencia: evalúa el grado en que el sujeto exagera su déficit intelectual al fallar preguntas sencillas de conocimiento general; y (5) Trastornos Afectivos: evalúa el grado en que el sujeto informa de síntomas atípicos de depresión y ansiedad.
González Ordi y Santamaría Fernández (2008) señalan que los resultados de los estudios de la adaptación española resultan prometedores, ya que el SIMS presenta una aceptable consistencia interna (a de Cronbach para la escala total de .94, n=934) y una adecuada validez predictiva para discriminar entre simuladores y no simuladores, con un 94,8% de sensibilidad, un 94,5% de especificidad y un índice de exactitud global de la prueba (AUC) de .97.
A su vez, los resultados del SIMS son concordantes con las escalas de validez del MMPI-2 que son sensibles a la exageración de síntomas (F, Fb, Fp, F-K, FBS y DsR) y están inversamente relacionados con las escalas de defensividad (escala K), proporcionando una adecuada evidencia de validez convergente (González Ordi y Santamaría Fernández, 2008). Además, el SIMS presenta correlaciones positivas y significativas con indicadores de exageración de síntomas o "mala imagen" de otras pruebas objetivas de personalidad, como es el caso de la Escala Z (mala imagen) del Inventario Clínico Multiaxial de Millon II y III (González Ordi y Santamaría Fernández, 2008) y el Índice Global de Gravedad o Índice Sintomático General (GSI) del SCL-90-R (Edens, Otto y Dwyer, 1999). En este sentido, el SIMS es un instrumento de screening que puede resultar muy útil a la hora de proporcionar información que favorezca la convergencia de los datos para determinar simulación.
Recientemente, Capilla Ramírez, González Ordi y Santamaría Fernández (2008) han presentado un estudio utilizando el SIMS como herramienta para discriminar entre pacientes con dolor crónico litigantes y no litigantes. En concreto, se administró esta prueba a cuatro grupos distintos: un grupo control (sin patología dolorosa diagnosticada), dolor crónico de espalda no litigante, dolor crónico de espalda litigante y fibromialgia litigante, encontrando que los grupos litigantes puntuaban significativamente más alto en el SIMS que el grupo no litigante y el grupo control, y que entre estos dos últimos, no existían diferencias significativas; el SIMS fue capaz de discriminar entre litigantes y no litigantes con una sensibilidad del 80%, una especificidad del 100% y un índice de exactitud global de .987. Los pacientes litigantes presentaron un patrón de exageración de síntomas con el fin de reflejar "su peor imagen posible", mucho más deteriorada que los individuos que presentan una patología similar pero que responden honestamente, siguiendo el principio de "cuanto más, mejor" (Rogers, Gillis y Bagby, 1990).
A lo largo de este artículo hemos presentado una concepción multidimensional de la detección de la simulación en dolor crónico, centrada en la evaluación pormenorizada multimétodo/multisistema en tres grandes dimensiones: física (médica), neuropsicológica y mediante autoinforme. Hemos hecho mención a algunos instrumentos, pruebas, estrategias más utilizadas en el campo y hemos hecho hincapié en la necesidad de la convergencia de los datos provenientes de distintas fuentes de información, a partir de la sospecha clínica, para poder determinar con la mayor seguridad posible el diagnóstico de simulación.
Parafraseando a DeClue (2002), "ninguna puntuación aislada o combinación de puntuaciones en un test" puede determinar por sí misma la presencia de simulación" (p.724); es la exploración e investigación clínica cuidadosa, la detección de inconsistencias del paciente en diversas pruebas psicológicas y físicas, o de la observación de su conducta en distintos ámbitos médico, psicológico, fisioterapéutico y rehabilitador y la convergencia de los datos disponibles, lo que al final contribuye a la determinación de simulación.
Como acertadamente señala Ruano Hernández (2009), identificar el fraude contribuye a su vez a defender los derechos justos de quienes de verdad sufren la adversidad de una enfermedad o de un accidente, o bien de otros problemas que afectan a la calidad de vida de las personas.
Lo deseable es que, tal y como parece deducirse de la producción científica existente en los últimos años en el campo de la detección de la simulación, se vayan generando instrumentos cada vez más precisos y fiables, con buena capacidad predictiva, que ayuden a los profesionales de la salud a determinar objetivamente sus sospechas clínicas de simulación.
Referencias
Aguerrevere, L.E., Greve, K.W., Bianchini, K.J. y Meyers, J.E. (2008). Detecting malingering in traumatic brain injury and chronic pain with an abbreviated version of the Meyers Index for the MMPI-2. Archives of Clinical Neuropsychology, 23, 831-838. [ Links ]
Alonso J, Prieto L, Antó J.M. (1995). La versión española del SF-36 Health Survey (Cuestionario de Salud SF-36): un instrumento para la medida de los resultados. Medicina Clínica, 104 (20), 771-766. [ Links ]
American Psychiatric Association (2000). Diagnostic and statistical manual of mental disorders (DSM-IV-TR). Washington, DC: APA. [ Links ]
Arbisi, P.A. y Butcher, J.N. (2004). Relationship between personality and health symptoms: Use of the MMPI-2 in medical assessments. International Journal of Clinical and Health Psychology, 4, 571-595. [ Links ]
Baer, R. A., Rinaldo, J. C. y Berry, D. T. R. (2003). Self-report distortions (including faking, lying, malingering, social desirability). En R. Fernández-Ballesteros (Ed.), Encyclopedia of Psychological Assessment, Vol. 2 (pp. 861-866). London: SAGE. [ Links ]
Bantick, S., Wisw, R.G., Ploghaus, A., Clare S., Smith, S.M. y Tracey, I. (2002). Imaging how attention modulates pain in humans using functional MRI. Brain, 125, 310-319. [ Links ]
Barona de Guzman, R. (2003). Interés clínico del sistema Ned SUE/IBV en el diagnóstico y valoración de las alteraciones del equilibrio. Revista de Biomecánica del Instituto de Biomecánica de Valencia (Monográfico: posturografía ¿algo se mueve?). Febrero de 2003, 43-51. [ Links ]
Bender, S.D. y Rogers, R. (2004). Detection of neurocognitive feigning: development of a multi-strategy assessment. Archives of Clinical Neuropsychology, 19, 49-60. [ Links ]
Bianchini, K.J., Greve, K.W. y Glynn, G. (2005). On the diagnosis of malingered pain-related disability: lessons from cognitive malingering research. The Spine Journal, 5, 404-417. [ Links ]
Bowman, C. y Mangham, C. (1989). Clinical use of moving platform posturography. Seminars in Hearing, 10, 161-171. [ Links ]
Butcher, J.N. y Ben-Porath, Y.S. (2004). Use of the MMPI-2 in medico-legal evaluations: An alternative interpretation for the Senior and Douglas (2001) critique. Australian Psychologist, 39, 44-50. [ Links ]
Butcher, J.N., Dahlstrom, W.G., Graham, J.R., Tellegen, A. y Kaemmer, B. (1999). MMPI-2: Inventario Multifásico de Personalidad de Minnesota-2. Manual. (Adaptación española realizada por A. Avila-Espada y F. Jiménez-Gómez). Madrid: TEA Ediciones. [ Links ]
Capilla Ramírez, P., González Ordi, H. y Santamaría Fernández, P. (2008). Detección de simulación en dolor crónico. Comunicación presentada en el VIII Congreso Nacional de la Sociedad Española de Traumatología Laboral – SETLA. Logroño, 27-29 de Noviembre de 2008. [ Links ]
Davis, K., Taylor, S.I., Crawley, A.P., Wood, M.L. y Mikulis, D.I. (1997). Functional MRI pain and attention-related activations in the human cingulated cortex. Journal of Neurophysiology, 77, 3370-3380. [ Links ]
DeClue, G. (2002). Practitioner's corner: Feigning Malingering: A case study. Behavioral Sciences and the Law, 20, 717-726. [ Links ]
De Luca, C.J. (1997). The use of surface electromyography in biomechanics. Boston: Delsys. [ Links ]
Derogatis, L.R. (2002). Cuestionario de 90 síntomas SCL-90-R. Madrid: TEA Ediciones. [ Links ]
Edens, J.F., Otto, R.K. y Dwyer, T. (1999). Utility of the Structured Inventory of Malingered Symptomatology in identifying persons motivated to malinger psychopathology. Journal of the American Academy of Psychiatry and the Law, 27, 387-396. [ Links ]
Etherton, J.L., Bianchini, K.J., Ciota, M.A., Heinly, M.T. y Greve, K.W. (2006). Pain, malingering and the WAIS-III Working Memory Index. The Spine Journal, 6, 61-71. [ Links ]
Etherton, J.L., Bianchini, K.J., Greve, K.W. y Ciota, M.A. (2005). Test of Memory Malingering performance is unaffected by laboratory-induced pain: implications for clinical use. Archives of Clinical Neuropsychology, 20, 375-384. [ Links ]
Fairbank, J.C.T., Davies, J.B., Couper, J. y O'Brien, J.P. (1980). The Oswestry low back pain disability questionnaire. Physiotherapy, 66, 271-73. [ Links ]
Frederick, R.I. (2003). Neuropsychological tests and techniques that detect malingering. En P.W. Halligan, C. Bass y D.A. Oakley (Eds.), Malingering and illness deception (pp. 323-335). Oxford: Oxford University Press. [ Links ]
Gansler, D., Tombaugh, T.N., Moczynski, N.P. y Rees, L.M. (1995). Test of Memory Malingering (TOMM): initial validation in a traumatic braining injury cohort. Comunicación presentada en el Annual Meeting of the National Academy of Neuropsychology, San Francisco, CA. [ Links ]
Gatchel, R.J., Peng, Y.B., Peters, M.L., Fuchs, P.N. y Turk, D.C. (2007). The biopsychosocial approach to chronic pain: scientific advances and future directions. Psychological Bulletin, 133, 581-624. [ Links ]
Gerson, A.R. (2002). Beyond DSM-IV: A meta-review of the literature on malingering. American Journal of Forensic Psychology, 20, 57-69. [ Links ]
Gervais, R.O., Green, P., Allen, L.M. et al (2001). Effects of coaching on symptom validity testing in chronic pain patients presenting for disability assessment. Journal of Forensic Neuropsychology, 2,1-19. [ Links ]
Gervais, R.O., Russell, A.S., Green, P. et al (2001). Effort testing in patients with fibromyalgia and disability incentives. Journal of Rheumatology, 28,1892-1899. [ Links ]
González, T., Balsa, A., González, I., Zamorano, E., Sainz de Murieta, J., Perez, J. y Martin, E. (1999). Adaptación del Northwick Park Neck Questionnaire a la población española. Revista Española de Reumatología, 5, 176-179. [ Links ]
González Ordi, H. y Gancedo Rojí, M. (1999). Evaluación de la simulación de respuesta: diagnóstico, técnicas y procedimientos. En A. Ruano, J. M. Muñoz Céspedes y C. Cid Rojo (Coords.), Psicología de la Rehabilitación (pp. 405-441). Madrid: Fundación MAPFRE-Medicina. [ Links ]
González Ordi, H. e Iruarrizaga Díez, I. (2005). Evaluación de las distorsiones de respuesta mediante el MMPI-2. Papeles del Psicólogo, 26, 129-137. [ Links ]
González Ordi, H. y Santamaría Fernández, P. (2008). Detection of Malingering in Clinical, Medicolegal, and Forensic Settings. Comunicación presentada en la 29th Stress and Anxiety Research Society (STAR) Conference. Londres, 16-18 de Julio de 2008. [ Links ]
Greiffenstein, M.F., Greve, K.W., Bianchini, K.J. y Baker, W.J. (2008). Test of Memory Malingering and Word Memory Test: a new comparison of failure concordance rates. Archives of Clinical Neuropsychology, 23, 801-807. [ Links ]
Hamilton, J.C. y Feldman, M.D. (2001). "Chest pain" in patients who are malingering. En J.W. Hurst y D.C. Morris (Eds.), Chest pain (pp. 443-456). Armork, NY: Futura Publishing Co. [ Links ]
Hislop, H.J. y Perrine, J.J. (1967). Isokinetic concept of exercice. Physical Therapy, 47,114-117. [ Links ]
Huesa, F. y Carabias, A. (1999). Evaluación comparativa isométrica, isotónica e isocinética de la musculatura flexo extensora de columna lumbar en sujetos sanos y afectos de lumbalgia. Mapfre Medicina, 10, 213-218. [ Links ]
Hutchinson, G.L. (2001). Disorders of simulation: Malingering, factitious disorders, and compensation neurosis. Madison, CT: Psychosocial Press. [ Links ]
Iverson, G.L. (2003). Detecting malingering in civil forensic evaluations. En H.A. Jr. Mac-Neill y L.C. Hartlage (Eds.), Handbook of forensic neuropsychology (pp. 137-177). New York: Springer. [ Links ]
Jensen, M.C., Brant-Zawadzki, M.N. y Obuchowski, N. (1994). Magnetic Resonance Imaging of the lumbar spine in people without back pain. New England Journal of Medicine, 331, 69-73. [ Links ]
Krupp, L.B., LaRocca, N.G., Muir Nash, J. y Steinberg, A.D. (1989). The fatigue severity scale. Application to patients with multiple sclerosis and systemic lupus erythematosus. Archives of Neurology, 46, 1121-1123. [ Links ]
Larrabee, G.J. (2003). Exaggerated MMPI-2 symptom report in personal injury litigants with malingered neurocognitive deficit. Archives of Clinical Neuropsychology, 18, 673-686. [ Links ]
Lezak, M.D. (1995). Neuropsychological assessment. New York: Oxford University Press. [ Links ]
Main, C.J. (1983). The modified somatic perception questionnaire (MSPQ). Journal of Psychosomatic Research, 27, 503-514. [ Links ]
McDermott, B.E. y Feldman, M.D. (2007). Malingering in the medical setting. Psychiatric Clinics of North America, 30, 645-662. [ Links ]
McGuire, B.E., Harvey, A.G. y Shores, E.A. (2001). Simulated malingering in pain patients: a study with the Pain Patient Profile. British Journal of Clinical Psychology, 40, 71-79. [ Links ]
McGuire, B.E. y Shores, E.A. (2001). Pain Patient Profile and the assessment of malingered pain. Journal of Clinical Psychology, 57, 401-409. [ Links ]
Melzack, R. y Katz, J. (2006). Pain in the 21st Century: the neuromatrix and beyond. En G. Young, A.W. Kane y K. Nicholson (Eds.), Psychological knowledge in court: PTSD, Pain, and TBI (pp. 129-148). New York: Springer. [ Links ]
Meyers, J.E., Millis, S.R. y Volkert, K. (2002). A validity index for the MMPI-2. Archives of Clinical Neuropsychology, 17, 157-169. [ Links ]
Meyers, J.E. y Volbrecht, M.E. (2003). A validation of multiple malingering detection methods in a large clinical sample. Archives of Clinical Neuropsychology, 18, 261-276. [ Links ]
Mittenberg, W., Patton, C., Canyock, E.M. y Condit, D.C. (2002). Base rates of malingering and symptom exaggeration. Journal of Clinical and Experimental Neuropsychology, 24, 1094-1102. [ Links ]
Monterde, S. Salvat, I., Montull, S. y Fernández Ballart, J. (2004). Validación de la versión española del Fibromyalgia Impact Questionnaire. Revista Española de Reumatología, 31, 507-513. [ Links ]
Muñoz Céspedes, J.M. y Paúl Lapedriza, N. (2001). La detección de los posibles casos de simulación después de un traumatismo craneoencefálico. Revista de Neurología, 32, 773-778. [ Links ]
Rees, L.M. (1996). A test of memory malingering: A simulation study and clinical validation. Tesis doctoral no publicada. Carleton University, Ottawa, Ontario (Cánada). [ Links ]
Rees, L.M. y Tombaugh, T.N. (1996). Validation of the Test of Memory Malingering (TOMM) using a simulation paradigm. Comunicación presentada en el Annual Meeting of the International Neuropsychological Society, Chicago, Ill. [ Links ]
Resnick, P.J. (1997). Malingering of posttraumatic disorders. En R. Rogers (Ed.), Clinical Assessment of Malingering and Deception (pp. 130-152). New York: The Guilford Press. [ Links ]
Rogers, R. (1990). Development of a new classificatory model of malingering. Bulletin of the American Academy of Psychiatry and the Law, 18, 323-333. [ Links ]
Rogers, R. y Bender, S. D. (2003). Evaluation of Malingering and Deception. En A. M. Goldstein (Ed.), Handbook of Psychology. Vol. 11: Forensic Psychology (pp.109-129). New Jersey: Wiley. [ Links ]
Rogers, R., Gillis, J.R. y Bagby, R.M. (1990). The SIRS as a measure of malingering: A validation study with a correctional sample. Behavioral Sciences and the Law, 8, 85-92. [ Links ]
Rosenfeld, J.P., Ellwanger, J.W., Nolan, K., Wu, S., Bermann, R.G. y Sweet, J. (1999). P300 scalp amplitude distribution as an index of deception in a simulate cognitive deficit model. International Journal of Psychopsysiology, 33, 3-19. [ Links ]
Ruano Hernández, A. (2009). Prólogo. Simulación. En Widows, M.R. y Smith, G.P. (2009). Inventario Estructurado de Simulación de Síntomas – SIMS [Adaptación española realizada por H. González Ordi y P. Santamaría Fernández]. Madrid: TEA Ediciones. [ Links ]
Samuel, R.Z., y Mittenberg, W. (2006). Determination of malingering in disability evaluations. Primary Psychiatry, 12. Obtenido el 7 de Enero de 2008, de http://www.primarypsychiatry.com/aspx/articledetail.aspx?articleid=122 [ Links ]
Schinka, J.A. y Borum, R. (1993). Readability of adult psychopathology inventories. Psychological Assessment, 5, 384-386. [ Links ]
Slick, D.J., Sherman, E.M. e Iverson, G.L. (1999). Diagnostic criteria for malingering neurocognitive dysfunction: Proposed standards for clinical practice and research. The Clinical Neuropsychologist, 13, 545-561. [ Links ]
Slick, D.J., Tan, J.E., Strauss, E.H. y Hultsch, D.F. (2004). Detecting malingering: a survey of experts’ practices. Archives of Clinical Neuropsychology, 19, 465-473. [ Links ]
Tollison, D.C. y Langley, J.C. (1995). Pain Patient Profile manual. Minneapolis: National Computer Services. [ Links ]
Tombaugh, T.N. (1996). Test of Memory Malingering. North Tonawanda, NY: MHS. [ Links ]
Waddel, G., Bircher, M., Finlayson, D. y Main, C.J. (1984). Symptoms and signs: physical disease or illness behavior?. British Medical Journal: Clinical, Research & Education, 289, 739-41. [ Links ]
Waddel, G., McCullogh, J.A., Kummel, E. y Venner, R.M. (1980). Nonorganic physical sign in low back pain. Spine, 5, 117. [ Links ]
Widows, M. R. y Smith, G. P. (2005). SIMS: Structured Inventory of Malingered Symptomatology. Professional manual. Lutz, FL: PAR: Psychological Assessment Resources. [ Links ]
Widows, M.R. y Smith, G.P. (2009). Inventario Estructurado de Simulación de Síntomas – SIMS [Adaptación española realizada por H. González Ordi y P. Santamaría Fernández]. Madrid: TEA Ediciones. [ Links ]