Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.40 no.1 Toledo ene./feb. 2016
https://dx.doi.org/10.7399/fh.2016.40.1.9059
ORIGINALES
Evaluación de dos sistemas cerrados en el proceso de elaboración de quimioterapia parenteral
Evaluation of two closed-system drug transfer device in the antineoplastic drug elaboration process
Sandra Gómez-Álvarez, Begoña Porta-Oltra, Marta Hernández-Griso, Francisca Pérez-Labaña y Mónica Climente-Martí
Sevicio de Farmacia Hospital Universitario Doctor Peset, Valencia. España.
Aceptado como póster en el 59 congreso nacional SEFH. Localizador: zgy8835509.
Dirección para correspondencia
RESUMEN
Objetivo: evaluar el impacto del uso de dos sistemas cerrados sobre el proceso de preparación de quimioterapia parenteral, con respecto al sistema estándar, en términos de contaminación local y ambiental, y tiempos de preparación.
Método: estudio observacional prospectivo. Se compararon dos proveedores distintos de sistemas cerrados, Icu Medical® y Care Fusion®, frente al sistema estándar de preparación de quimioterapia parenteral. Quince enfermeros del Servicio de Farmacia elaboraron cada uno de ellos 5 preparaciones, una siguiendo el procedimiento estándar y cuatro usando los sistemas cerrados. Para evaluar la aparición de contaminación se elaboró una solución de fluoresceína al 0,5%. Se evaluaron dos tipos de contaminación: local (en tres puntos: sistema acoplado a vial, jeringa y envase final) y ambiental (guantes y mesa de trabajo), obteniéndose el porcentaje de preparaciones contaminadas en cada uno de ellos. Se registró el tiempo empleado por cada enfermero en cada una de las preparaciones.
Resultados: se elaboraron 75 preparaciones. Se produjo una reducción global de la contaminación local para los SC Icu Medical® y Care Fusion® del 24% y 74%, respectivamente. En el sistema cerrado Care Fusion® la contaminación local fue significativamente menor que en el sistema estándar en vial, jeringa y envase final; mientras que en el sistema cerrado Icu Medical® solo fue significativamente menor en la conexión al vial. Se produjo un incremento significativo del tiempo de preparación con la utilización de sistemas cerrados de los entre 23,4 y 30,5 segundos.
Conclusiones: ambos sistemas cerrados han mostrado un beneficio con respecto a la utilización del sistema estándar. Sin embargo, se han visto incrementados significativamente los tiempos de preparación con ambos sistemas.
Palabras clave: Fármaco citostáticos; Exposición ocupacional; Sistema cerrado de transferencia de fármacos.
ABSTRACT
Objective: to assess the impact of two closed-system drug transfer device on the local and environmental contamination and preparation times in the process of preparation of parenteral chemotherapy compared to the standard system.
Method: prospective observational study. Two different closed-systems providers, Care Fusion® and Icu Medical®, were compared to standard preparation. 15 nurses of Pharmacy Department prepared 5 preparations each one, one with the standard procedure and four using closed-systems. To evaluate the contamination, a fluorescein solution 0.5% was prepared. Two kind of contamination were evaluated, local (three points connection: closed-system connect vial, syringe and final infusion bags) and environmental (gloves and countertop). Percentage of contaminated preparations was obtained in each one. Time taken by each nurse in each preparation was recorded.
Results: 75 preparations were prepared. Local contamination was reduced 21% and 75% in closed-system Icu Medical® and Care Fusion® respectively. Care Fusion® closed system, local contamination was significantly lower than the standard system to the vial, syringe and final package, while Icu Medical® closed-systems only was significantly lower in the connection to the vial. Time of preparation was increased significantly with the use of closed-system between 23.4 and 30.5 seconds.
Conclusions: both closed-systems drug transfer device have shown an improvement in contamination than the use of the standard system. However, preparation time has been significantly increased with the use of both systems.
Key words: Cytotastic drug; Occupational exposure; Closed system drug transfer device.
Aportación a la literatura científica
La mayoría de los estudios realizados hasta el momento, han evaluado y demostrado la efectividad del uso del sistema cerrado PhaSeal® en la preparación de fármacos citostáticos. En este contexto, el objetivo de este estudio es evaluar el impacto del uso de dos sistemas cerrados, Care Fusion® e Icu Medical®, sobre el proceso de preparación de quimioterapia parenteral, con respecto al sistema estándar de transferencia, en términos de contaminación local y ambiental, así como su impacto en los tiempos de preparación en una unidad centralizada de preparación de quimioterapia.
El uso de estos sistemas cerrados ha conseguido reducir la contaminación local, lo que conlleva una disminución de la exposición de los trabajadores a los fármacos citostáticos durante su manipulación y por tanto una mayor seguridad del proceso de elaboración.
Introducción
Los citostáticos son sustancias citotóxicas que se utilizan para causar un daño celular mediante la alteración del metabolismo o el bloqueo de la división y reproducción celular, inhibiendo así el crecimiento de las células. Este efecto no es selectivo de las células cancerosas, sino que afecta a todas las células del organismo, pudiendo provocar efectos mutagénicos, carcinogénicos, teratogénicos y/o tóxicos para la reproducción1-3.
Los riesgos del manejo de fármacos citostáticos para la salud del personal sanitario involucrado en su preparación y administración fueron reconocidos por primera vez en el año 1970. Desde entonces, no se han obtenido datos indicativos del nivel a partir del cual es significativa la exposición crónica a estos fármacos, ya que éste personal no está expuesto a una exposición puntual sino a múltiples exposiciones a lo largo del tiempo. Tampoco se ha podido establecer de forma clara los efectos tóxicos a largo plazo de la exposición a estos fármacos, pero diversos estudios han demostrado la presencia de fármacos citostáticos, como ciclofosfamida, en la orina o sangre del personal sanitario involucrado en el proceso de elaboración o administración de este tipo de medicación4-6, casos de abortos o nacimientos con anormalidades7-8, y de aumento del riesgo de cáncer (1,4 - 986 casos adicionales por cada millón de trabajadores expuestos) en el personal sanitario expuesto9-10.
En consecuencia, la exposición de los profesionales sanitarios durante el manejo de estos fármacos ha ido limitándose en las últimas décadas con la introducción de nuevas medidas de seguridad. En 1980, es incorporado al proceso de preparación el uso de cabinas de seguridad biológica (CSB) y equipos de protección individual11. Aunque la exposición fue reducida tras la implementación de estas medidas, estudios posteriores seguían mostrando contaminación fuera de la CSB, en el suelo, mesa de trabajo y aire4,12. Debido al potencial riesgo de los antineoplásicos, el creciente uso de estos, y la continua presencia de contaminación el National Institute for Occupational Safety and Health (NIOSH) publicó una alerta13, que fue apoyada por la American Society of Health-System Pharmacists (ASHP) con la actualización de sus guías sobre manejo de citostáticos14. Ambas instituciones consideraban dentro de sus recomendaciones el uso de sistemas cerrados (SC) de transferencia para la elaboración y administración de citostáticos. Éstos, son definidos por el NIOSH, como dispositivos que no intercambian aire no filtrado o contaminantes con el entorno adyacente13.
Otros organismos también se han pronunciado en cuanto a las recomendaciones de uso de estas nuevas técnicas. Así la International Society of Oncology Pharmacy Practitioners (ISOPP) en 2007, recomienda además de la presencia de una unidad centralizada de preparación, con una sala de acondicionamiento semilimpia, una sala de paso y una sala limpia provista de CSB, el uso de dispositivos de transferencia de fármacos durante la preparación y la administración de fármacos citotóxicos que deben ser herméticos y estancos15. También se une a esta recomendación la Farmacopea de Estados Unidos en la vigente edición USP 79716 y en su proyecto USP 80017. Asimismo, la Directiva 2004/37/EC del parlamento europeo y del consejo establece 4 niveles para la manipulación segura y protección del trabajador a la exposición a carcinógenos, donde los sistemas cerrados se consideran en un nivel 2 de seguridad (Aislamiento del riesgo o control de la fuente), jerárquicamente en una categoría superior a los Controles de ingeniería/ ventilación y controles administrativos/medidas organizativas (nivel 3) y a los Equipos de protección personal (nivel 4)18.
En España, el Instituto Nacional de Seguridad e Higiene establecía en la nota técnica de prevención 740 el uso de estos sistemas únicamente para la administración19. No ha sido hasta el año 2014 cuando la guía de buenas prácticas para trabajadores profesionalmente expuestos a agentes citostáticos, publicada por el Instituto de Salud Carlos III, el Ministerio de Economía y Competitividad y la Escuela Nacional de Medicina del Trabajo, ha incorporado como recomendación el uso se estos sistemas no solo en la administración sino también en la preparación de medicamentos citostáticos20.
La implementación de estos sistemas ha resultado en una disminución de la contaminación tanto ambiental como en las superficies de trabajo, y por tanto, una disminución de la exposición a fármacos citostáticos por parte de los profesionales sanitarios21-24. Un reciente estudio realizado en 22 hospitales de EE UU media la presencia de ciclofosfamida, ifosfamida y 5-fluorouracilo, en diferentes superficies de la CSB, mostrando que la contaminación superficial había sido reducida de forma significativa tras la implementación de los sistemas cerrados21.
La mayoría de los estudios realizados hasta el momento, han evaluado y demostrado la efectividad del uso del sistema cerrado PhaSeal® en la preparación de fármacos citostáticos21,25-27. En este contexto, el objetivo de este estudio es evaluar el impacto del uso de dos sistemas cerrados, Care Fusion® e Icu Medical®, sobre el proceso de preparación de quimioterapia parenteral, con respecto al sistema estándar de transferencia, en términos de contaminación local y ambiental, así como su impacto en los tiempos de preparación en una unidad centralizada de preparación de quimioterapia.
Material y métodos
Estudio observacional prospectivo realizado en un hospital que dispone de una unidad centralizada de preparación de quimioterapia parenteral en el Servicio de Farmacia, que en el año 2013 realizó un total de 17028 preparaciones de antineoplásicos. El servicio de Farmacia dispone de una antesala destinada al almacenamiento y acondicionamiento del material, una sala de paso y dos salas consideradas limpias donde se ubican las dos CSB de clase II para la elaboración de la quimioterapia que cumplen con el RD 485/199728. Los enfermeros preparan todas las mezclas parenterales de quimioterapia en las CSB, aplicando una adecuada técnica aséptica y siguiendo las recomendaciones para la protección y el manejo seguro de citostáticos18,20, bajo la supervisión y validación final de los farmacéuticos de la unidad.
En el estudio se compararon dos proveedores distintos de sistemas cerrados, Icu Medical® y Care Fusion®, frente al sistema estándar de preparación de quimioterapia parenteral. El sistema estándar es un sistema abierto compuesto por jeringas, y filtros Mini-Spyke®. Los filtros Mini-Spyke® son filtros de venteo de membrana hidrófoba (diámetro medio de poro de 0,22 mcm) para evitar la sobrepresión en el interior del vial y por tanto la formación de aerosoles. Los sistemas cerrados, Care Fusion® e Icu Medical®, estaban compuestos:
1. Adaptador para la jeringa.
2. Punzón para el vial, con adaptador (SCPA) el cual queda anclado al vial o universal (SCPU) que a diferencia del anterior únicamente queda fijado al vial sin una sujeción externa a éste.
3. Punzón para el envase final, con alargadera en el sistema cerrado Care Fusion®, y sin alargadera en el sistema cerrado Icu Medical®.
Tanto en el sistema estándar como en el sistema cerrado se utilizó como envase final un Viaflex® 50 ml glucosa 5%.
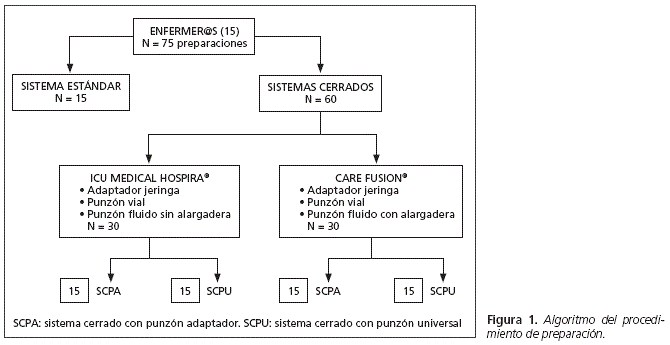
15 enfermeros del Servicio de Farmacia fueron invitados a participar en el estudio. Cada uno de ellos elaboró un total de 5 preparaciones consecutivas, una preparación siguiendo el procedimiento estándar establecido en el hospital y cuatro preparaciones usando los sistemas cerrados Care Fusion® e Icu Medical® (dos con cada SC: una con el punzón universal y otra con el punzón adaptador) como se muestra en la figura 1. Todos los enfermeros fueron instruidos para realizar los mismos movimientos y usar la misma técnica, y así minimizar las diferencias entre ellos.
Para evaluar la aparición de contaminación durante el proceso de preparación se elaboró una solución de fluoresceína al 0,5% a partir de viales de fluoresceína al 10%, que se introdujo una vez preparada en el interior de viales vacíos. La fluoresceína es una sustancia inocua para el manipulador, que emite fluorescencia cuando es expuesta a la luz UV (365 nm). Esta propiedad permite evidenciar la formación de gotas, y por tanto, es de gran utilidad para detectar la presencia de contaminación25. Una vez elaborados los viales con fluoresceína al 0,5% se determinó la estanqueidad mediante la simulación del proceso de preparación. Un farmacéutico se encargó de supervisar el procedimiento y comprobar la presencia o ausencia de contaminación mediante el uso de luz UV en diferentes puntos de la preparación. Antes de cada preparación se realizó un blanco para comprobar la ausencia de contaminación en el material y superficie de trabajo. El procedimiento llevado a cabo se muestra en la figura 2. Se evaluó la presencia de dos tipos de contaminación:
1. Ambiental, a través de la presencia de fluoresceína en guantes y mesa de trabajo.
2. Local, a través de la presencia de fluoresceína en el vial, jeringa y preparación final. Se determinó la presencia de contaminación en las conexiones entre los diferentes componentes del sistema, y en el exterior de los mismos.
Se obtuvo el porcentaje de preparaciones con contaminación local y ambiental, de forma global y en cada uno de los puntos, para el sistema estándar y los dos sistemas cerrados evaluados. Asimismo, se calculó el porcentaje de reducción de la contaminación para cada uno de los sistemas cerrados con respecto al sistema estándar, a partir del número de contaminaciones globales en cada sistema. (Dividiendo el número de contaminaciones globales en cada uno de los 4 sistemas cerrados entre el número de contaminaciones globales del sistema estándar).
Por último, el farmacéutico registró el tiempo empleado por cada enfermera en cada una de las preparaciones, para determinar el impacto de la incorporación de los sistemas cerrados en la duración de la elaboración de quimioterapia.
Análisis estadístico
Los resultados obtenidos se presentan de forma descriptiva, como frecuencias para las variables categóricas (presencia o ausencia de contaminación) y, con sus respectivas medidas de tendencia central y dispersión para las variables cuantitativas (tiempos de preparación). Se realizo un análisis comparativo entre los diferentes SC con respecto al estándar para cada tipo de contaminación, ambiental y local, diferenciando en el caso de la contaminación local entre vial, jeringa y envase final y del tiempo de preparación. Se comparó la presencia de contaminación en el punzón con adaptador y universal en ambos SC. Para las variables respuesta cuantitativas se utilizó la prueba T-test de Student y para las variables respuesta categóricas el test de Chi-cuadrado. Se aplicó un valor α=5% (p<0,05) para contrastar posibles diferencias entre variables.
Resultados
Se elaboraron un total de 75 preparaciones. Ninguna preparación presentó contaminación ambiental, ni con el sistema estándar ni con los sistemas cerrados.
La tabla 1 muestra la frecuencia con la que se presentó la contaminación local en el vial, jeringa y envase final para cada uno de los cinco sistemas estudiados. Se produjo una reducción global significativa de la contaminación local para el SCPU de Icu Medical® del 24% (p=0,001) y para los SCPA y SCPU de Care Fusion® del 74% (p<0,0001). La reducción global de la contaminación para el SCPA de Icu Medical® fue del 7%, no siendo significativa (p>0,05). Con relación a la utilización del punzón con adaptador o universal para el vial, no se encontraron diferencias significativas entre ambos tipos de anclaje en ninguno de los dos sistemas cerrados. En el caso del sistema cerrado Care Fusion® la contaminación local fue significativamente menor que en el sistema estándar tanto para el vial (p<0,0001), como para la jeringa (p=0,001) y el envase final (p<0,0001), dato no hallado en el sistema cerrado Icu Medical® donde sólo se obtuvo una reducción significativa de la contaminación en la conexión al vial (p=0,006 y p=0,003 en el SCPA y SCPU respectivamente).
En cuanto a los tiempos de preparación como se observa en la tabla 2, cuando la preparación se realizó utilizando los sistemas cerrados se produjo un incremento significativo del tiempo de preparación con respecto al tiempo empleado en la preparación estándar. Se emplearon un mínimo de 21,87 (DE: 5,24) segundos más cuando se utilizó el SCPU Icu Medical® y de 24,13 (DE: 5,11) segundos más en el caso del SCPU Care Fusion®, no siendo significativas las diferencias de tiempo entre ambos sistemas cerrados (p>0,05).
Discusión
A lo largo del tiempo se han ido incorporando diversas medidas para reducir el potencial riesgo de la preparación y administración de fármacos citostáticos para el personal sanitario, como son el uso de CSB, equipos de protección personal y recientemente, el uso de sistemas cerrados.
Nuestro estudio muestra la efectividad del uso de los sistemas cerrados en términos de reducción de la contaminación local en comparación con el sistema de preparación estándar con filtro de venteo y jeringa. Se obtuvieron reducciones en la contaminación de hasta el 74% cuando se empleó el sistema cerrado en el proceso de preparación, lo que muestra el beneficio adicional del uso de estos sistemas para disminuir la exposición de los trabajadores a los fármacos citostáticos durante su manipulación.
Estos resultados confirman los resultados obtenidos en estudios previos en los que se utilizaba como sistema cerrado, el sistema PhaSeal®21,25-27. Aunque es difícil hacer una comparación por la diferente metodología llevada a cabo en cada uno de ellos, se ha comparado los resultados obtenidos en el presente estudio con los de Favier y cols. Estos autores utilizaron una solución de fluoresceína para simular el proceso de preparación y detectar la presencia de contaminación, metodología también llevada a cabo en nuestro estudio25. Es importante resaltar como se define en el estudio de Favier y cols la contaminación ambiental para evitar errores en la interpretación de los datos. La contaminación ambiental se describe como la suma de contaminación en los puntos de conexión y la presencia de derrames, a diferencia de nuestro estudio donde la contaminación ambiental implica tan solo la presencia de contaminación en guantes y mesa de trabajo, entendido como derrames y salpicaduras, pero no en los puntos de conexión. En nuestro estudio, en estos casos se ha consensuado que esta medición representa principalmente una contaminación local.
En nuestro estudio ninguna preparación presentó contaminación ambiental (guantes y mesa de trabajo), ni cuando se empleó el sistema estándar, por lo que la reducción de este tipo de contaminación fue nula. Esto puede ser explicado por la formación recibida en técnica aséptica de preparaciones parenterales y el grado de experiencia del personal de enfermería de nuestro Servicio de Farmacia, el cual lleva años trabajando y llevando a cabo la elaboración de fármacos citostáticos, lo que hace que la contaminación ambiental esperada sobre todo con el uso del sistema estándar no esté presente y no suponga una mejora en este punto. Entre las posibles fuentes de contaminación ambiental podemos citar los derrames, la contaminación externa y los errores del operador, en nuestro caso la experiencia de los trabajadores hace que el error del operador no sea un factor a añadir en la incidencia de derrames y por tanto de contaminación ambiental. En el estudio de Favier y cols., se obtuvieron reducciones de la contaminación ambiental del 93%25.
En cuanto a la contaminación local, descrita como la presencia de fluoresceína en los puntos de conexión del vial, jeringa y envase final, se produjo una reducción significativa para ambos tipos de sistemas cerrados, al igual que en el estudio de Favier y cols, donde la contaminación en el sistema cerrado Phaseal® fue del 0% con una reducción de la contaminación del 100% comparado con el sistema estándar25. En nuestro caso al analizar la presencia de contaminación en los diferentes puntos de conexión se pudo observar como en el caso del sistema cerrado Icu Medical® sólo eran significativas las diferencias para el punto de conexión del vial, independientemente del punzón utilizado. Sin embargo, en el sistema cerrado Care Fusión® estas reducciones fueron halladas en los 3 puntos de conexión, observándose por tanto una disminución de la contaminación local del 74%.
Es importante destacar que el punto donde se producen con mayor frecuencia las fugas independientemente del sistema cerrado empleado es en el adaptador de la jeringa. En este punto la frecuencia de aparición de la contaminación fue del 100% y 93% para el sistema cerrado Icu Medical® en el punzón adaptador y punzón universal respectivamente y del 47% para el sistema cerrado Care Fusion® con ambos punzones. Estos datos sugieren hasta un 40% más de fugas cuando se compara con los otros dos puntos de conexión (vial y envase final), por lo que durante la elaboración de citostáticos se deberá prestar una especial atención en este punto para minimizar el riesgo de contaminación y exposición.
El objetivo secundario de nuestro estudio fue analizar el impacto del uso de los sistemas cerrados en la duración de la preparación. Se produjo un incremento significativo en los tiempos de preparación cuando se emplearon los sistemas cerrados para simular el proceso de preparación. Este aumento significativo también fue observado en el estudio de Favier y cols, donde fueron necesarios una media de 33 segundos más para la preparación cuando el envase final eran jeringas y 38 segundos más cuando eran bolsas25. El incremento de los tiempos de preparación puede ser explicado por la falta de experiencia del personal en la utilización de estos sistemas, los enfermeros han desarrollado aptitudes en la elaboración de citostáticos mediante el sistema estándar pero en lo que respecta al sistema cerrado muchos de ellos nunca antes habían utilizado este sistema para la preparación de mezclas, a pesar de haber recibido todos instrucciones de cómo proceder. Es por ello, que estos tiempos de preparación esperan verse reducidos con la práctica y adquisición de experiencia.
Las principales limitaciones de este trabajo se centran en que la presencia de contaminación ambiental y local fue medida de forma cualitativa a través de la detección de fluorescencia, siendo realizada esta medición por un único farmacéutico, lo que reduce la variabilidad interindividual presente si hubiera sido medida por varios operadores pero a su vez, incrementa la probabilidad de aparición del error sistemático. Además cada enfermero elaboro únicamente una preparación con cada tipo de sistema, lo que conlleva una ausencia de reproducibilidad y repetitividad de las mediciones. Por último, destacar que solamente se midió el impacto del uso de sistemas cerrados en el proceso de preparación, siendo necesario también evaluar su impacto en el proceso de administración.
Conclusión
En nuestro estudio, el uso de sistemas cerrados ha conseguido reducir la contaminación local entre un 24 y 74%, lo que conlleva una disminución del potencial riesgo de exposición de los trabajadores a los fármacos citostáticos durante su manipulación y por tanto una mayor seguridad del proceso de elaboración. Ambos sistemas cerrados han mostrado una beneficio con respecto a la utilización del sistema estándar con filtro de venteo y jeringa, ICU Medical® presentó menor contaminación en uno de los tres puntos de conexión evaluados (vial) mientras que el sistema cerrado Care Fusion® en los tres (vial, jeringa y envase final). En lo que respecta a los tiempos de preparación se ha producido un incremento significativo, el cual espera verse reducido con la práctica y la adquisición de experiencia por parte del personal.
Bibliografía
1. Valanis BG, Vollmer WM, Labuhn KT, Glass AG. Acute symptoms associated with antineoplastic drug handling among nurses. Cancer Nurs. 1993;16(4):288-95. [ Links ]
2. Valanis BG, Vollmer WM, Labuhn KT, Glass AG. Association of antineoplastic drug handling with acute adverse effects in pharmacy personnel. Am J Hosp Pharm. 1993;50(3):455-62. [ Links ]
3. Hemminki K, Kyyrönen P, Lindbohm ML. Spontanius abortions and malformations in the offspring of nurses exposed to anaesthetic gases, cytotstatic drugs and other potencial hazards in hospital, based on registered information of outcome. J Epidemiol Community Health. 1985;39(2):141-7. [ Links ]
4. Sessink PJ, Boer KA, Scheefhals AP, Anzion RB, Bos RP. Occupational exposure to antineoplastic agents at several departments in a hospital. Environmental contamination and excretion of cyclophosphamide and iphosfamide in urine of exposed workers. Int Arch Occup Environ Health.1992;64(2):105-12. [ Links ]
5. Pethran A, Schierl R, Hauff K, Grimm CH, Boos KS, Nowak D. Uptake of antineoplastic agents in pharmacy and hospital personnel. Part I: Monitoring of urinary concentrations. Int Arch Occup Environ Health. 2003;76(1):11-16. [ Links ]
6. Minoia C, Turci R, Sottani C, Schiavi A, Perbellini L, Angeleri S, et al. Application of high performance liquid chromatograohy/tan-dem mass spectrometry in the environmentl and biological monitoring of health care personnel occupationally exponed to cy-clophosphamide and ifosfamide. Rapid Commun Mass Spectrom. 1998;12(20):1485-93. [ Links ]
7. Dranitsaris G, Jonhston M, Poirier S, Schueller T, Milliken D, Green E, et al. Are health care providers who work with cancer drugs at an increased risk for toxic events? A systematic review and meta-analysis of the literature. J Oncol Pharm Pract. 2005;11(2):69-78. [ Links ]
8. Selevan SG, Lindbohm ML, Hornung RW, Hemminki K. A study of occupational exposure to antineoplastic drugs and fetal loss in nurses. N Engl J Med. 1985;313(19):1173-8. [ Links ]
9. Wick C, Slawson MH, Jorgenson JA, Tyler LS. Using a closed system protective device to reduce personnel exposure to antineoplastic agent. Am J Health Syst Pharm. 2003;60(22):2314-20. [ Links ]
10. Vanderbroucke J, Robays H. How to protect environment and employees against cytostatic agents, the UZ Ghent experience. J Oncol Pharm Pract. 2001;6(4):146-52. [ Links ]
11. American Society of Health System Pharmacists. ASHP technical assistance bulletin on handling citotoxic and hazardous drugs. Am J Hosp Pharm. 1990;47:1033-49. [ Links ]
12. Connor TH, Anderson RW, Sessink PJM, Broadfield L, Power LA. Surface contamination with antineoplastic agents in six cancer treatment centers in Canada and the United States. Am J Health Syst Pharm. 1999; 56(14):1427-32. [ Links ]
13. National Institute for Occupational Safety and Health. Preventing occupational exposures to antineoplastic and other hazardous drugs in healthcare settings. Washington DC: US Centers for Disease Control and Prevention; 2004. DHHS (NIOSH) Publication No. 2004-165. Accedido 22 Febrero 2014: http://www.cdc.gov/niosh/docs/2004-165/pdfs/2004-165.pdf. [ Links ]
14. American Society of Health System Pharmacists. ASHP guidelines on handling hazardous drugs. Am J Health Syst Pharm. 2006;63:1172-93. [ Links ]
15. International Society of Oncology Pharmacy Practicioners Standards Committee. ISOPP standards of practice. Safe handling of cytotoxics. J Oncol Pharm Pract. 2007;13 Suppl:1-81. [ Links ]
16. Pharmaceutical compounding-sterile preparations (general information chapter 797). In: 36th rev., and the National Formulary 31 ed. Rockville, MD: The United States Pharmacopeial Convention; 2013: 361-98. [ Links ]
17. The Compounding Expert Committee. General Chapter 800 Hazardous drugs - handling in healthcare settings. The United States Pharmacopeial Convention.2014. Disponible en: http://www.usp.org/sites/default/files/usp_pdf/EN/m7808_pre-post.pdf Accedido mayo 2015. [ Links ]
18. Directiva 2004/37/CE del parlamento europeo y del consejo, 29 abril 2004, relativa a la protección de los trabajadores contra los riesgos relacionados con la exposición a agentes carcinógenos o mutágenos durante el trabajo (sexta Directiva específica con arreglo al apartado 1 del artículo 16 de la Directiva 89/391/ CEE del Consejo). Acceso en enero 2014: http://www.boe.es/doue/2004/229/L00023-00034.pdf. [ Links ]
19. NTP 740: Exposición laboral a citostáticos en el ámbito sanitario. Ministerio de Trabajo y Asuntos Sociales. Instituto Nacional de Seguridad e Higiene en el Trabajo, 2006. Acceso en febrero de 2014: http://www.insht.es/portal/site/Insht/menuitem.a82abc159115c-8090128ca10060961ca/?vgnextoid=db2c46a815c83110VgnVCM100000dc0ca8c0RCRD&do=Search&idPalabra=xujbba. [ Links ]
20. Guía de Buenas Prácticas para Trabajadores Profesionalmente Expuestos a Agentes Citostáticos. Ministerio de Economía y Competitividad, Instituto de Salud Carlos III, Escuela Nacional de Medicina de Trabajo. 2014. Acceso en junio de 2014: http://gesdoc.isciii.es/gesdoccontroller?action=download&id=26/03/2014-199edf956b. [ Links ]
21. Sessink PJ, Connor TH, Jorgenson JA, Tyler TG. Reduction in surface contamination with antineoplastic drugs in 22 hospital pharmacies in the US following implementation of a closed-system drug transfer device. J Oncol Pharm Pract. 2010;17(1): 39-48. [ Links ]
22. Harrison BR, Peters BG, Bing MR. Comparison of surface contamination with cyclophosphamide and fluorouracil using a closed system drug transfer device versus standard preparation techniques. Am J Health Syst Pharm. 2006;63(18):1736-44. [ Links ]
23. Connor TH, Anderson RW, Sessink PJ, Spivey SM. Effectiveness of a closed-system device in containing surface contamination with cyclophosphamide and ifosfamide in an i.v. admixture area. Am J Healh Syst Pharm. 2002;59(1):68-72. [ Links ]
24. Siderov J, Kirsa S, McLauchlan R. Reducing workplace cytotoxic surface contamination using closed-system drug transfer device. J Oncol Pharm Pract. 2010;16(1):19-25. [ Links ]
25. Favier B, Labrosse H, Gilles-Afchain L, Cropet C, Perol D, Chaumard N, et al. Tha Phaseal® system: Impact of its use on workplace contamination and duration of chemotherapy preparation. J Oncol Pharm Pract. 2012;18(1):37-45. [ Links ]
26. Wick C, Slawson MH, Jorgenson JA, Tyler LS. Using a closed-system protective device to reduce personnel exposure to antineoplastic agents. Am J Health Syst Pharm. 2003;60(22):2314-20. [ Links ]
27. Nygren O, Gustavsson B, Ström L, Eriksson R, Jarneborn L, Friberg A. Exposure to anti-cancer drugs during preparation and administration. Investigations of an open and a closed system. J Environ Monit. 2002;4(5):739-42. [ Links ]
28. Real Decreto 485/1997, de 14 de abril, por el que se establecen las disposiciones mínimas de seguridad y salud en los lugares de trabajo. Acceso en enero de 2014: http://www.boe.es/boe/dias/1997/04/23/pdfs/A12918-12926.pdf. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: gomal.sandra@gmail.com
(Sandra Gómez Álvarez).
Recibido: el 8 de abril de 2015;
Aceptado: el 26 de octubre de 2015.