Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.42 no.3 Toledo may./jun. 2018
https://dx.doi.org/10.7399/fh.10931
REVISIÓN
El reto del envejecimiento y la complejidad farmacoterapéutica en el paciente VIH +
1Servicio de Farmacia Hospitalaria, Hospital Universitario de Valme, AGS Sur de Sevilla, Sevilla, Spain.
2Servicio de Enfermedades Infecciosas, Hospital San Pedro, Logroño-La Rioja, Spain.
3Servicio de Farmacia, Hospital Universitario Virgen del Rocío, Sevilla, Spain.
4Facultad de Farmacia, Universidad de Sevilla, Sevilla, Spain.
Introducción
Actualmente, la infección por VIH se considera ya una enfermedad crónica gracias a la extraordinaria disminución de la mortalidad producida tras la introducción del tratamiento antirretroviral de gran actividad (TAR) y la llegada posterior de nuevos fármacos más potentes y con mejores pautas posológicas1. El aumento de la supervivencia ha llevado aparejado un envejecimiento paralelo de la población VIH + . De hecho, se han publicado ya datos de diferentes cohortes de pacientes VIH + , a nivel mundial, en las que más del 50% de los individuos en tratamiento tienen ya más de 50 años y la perspectiva para 2030 va en aumento2.
El envejecimiento de la población ha tenido como consecuencia el incremento en la aparición de numerosas comorbilidades. Se sabe, incluso, que esta prevalencia es mayor entre los pacientes con infección por VIH que en la población general y presentándose, también, de forma más precoz. Se estima que, con diez años de antelación, sugiriendo, pues, un envejecimiento acelerado3-6. En paralelo al incremento de comorbilidades, ha tomado cada vez más presencia el concepto de polifarmacia en el ámbito del VIH +7, aumentando la prevalencia de la misma, a pesar de no existir un consenso unánime sobre su definición, según la mayoría de los autores, en los últimos años8. En esta línea, recientemente, con la intención de dar una visión más exacta, no tanto numérica, de la farmacoterapia de los pacientes, se ha acuñado el término complejidad farmacoterapéutica, con diferentes herramientas para su medición, conociéndose ya su relación con diferentes resultados en la salud de los pacientes9-12.
La experiencia y la evidencia científica obtenida con la población general están sirviendo ya como punto de partida para la valoración y abordaje del paciente de edad avanzada con infección por VIH13-16. Sin embargo, aún quedan muchos aspectos claves por conocer y consensuar, dentro del equipo multidisciplinar que atiende a este tipo de pacientes, de manera que sirvan para reorientar y mejorar la asistencia a esta población.
El objetivo de esta revisión es describir el estado actual del conocimiento y manejo del envejecimiento y la complejidad farmacoterapéutica en el paciente VIH + .
Métodos
Se realizó una revisión bibliográfica de la literatura. Para ello, se llevó a cabo una búsqueda bibliográfica diseñada a tal efecto en las siguientes bases de datos: Medline (vía Pubmed), Scopus, Web of Science, The Cochrane Library y Google Académico.
Se incluyeron todos los artículos, originales o revisiones, publicados en lengua inglesa o española, desde el año 2007 al 2017, que analizaron el manejo del envejecimiento y la complejidad farmacoterapéutica en pacientes VIH + , mayores de 50 años.
La búsqueda en la base de datos Medline se realizó empleando términos Medical Suject Heading (MeSH), thesaurus de la US National Library of Medicine. Par ello, se combinaron los siguientes términos: “Polypharmacy”/“Polifarmacia”, “Aging”/“Envejecimiento”, términos: “Polypharmacy”/“Polifarmacia”, “Aging”/“Envejecimiento”, Regimen Complexity” y “HIV”/”VIH”.
La revisión de los artículos se realizó de forma independiente por dos de los autores de la revisión. Las discordancias se resolvieron por consenso. Para valorar el grado de concordancia entre los autores, en la inclusión de los artículos seleccionados, se utilizó el índice Kappa (se admitió y utilizó un umbral de 0,80 como de buena correlación).
Posteriormente se analizaron y sintetizaron los datos de los artículos que cumplieron los criterios de inclusión.
Resultados
Se analizaron un total de 208 referencias bibliográficas identificadas y relacionadas con los objetivos del estudio. El diagrama de flujo de la bibliografía revisada según los criterios de inclusión y exclusión previstos se observa en la Figura 1. Finalmente, los estudios seleccionados, que incluyen datos relevantes en el ámbito del paciente VIH + , se incluyeron en la Tabla 1-1 y la Tabla 1-2.
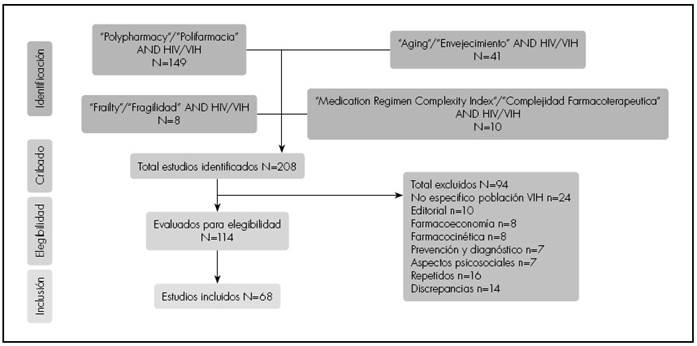
Figura 1. Diagrama de flujo de la bibliografía revisada e inclusión y exclusión de estudios analizados.
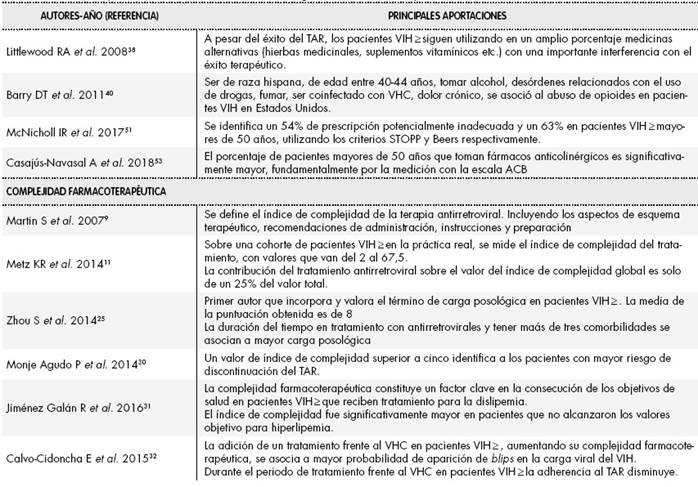
TABLA 1. Principales conclusiones de los artículos originales realizados en pacientes VIH + incluidos en la revisión.
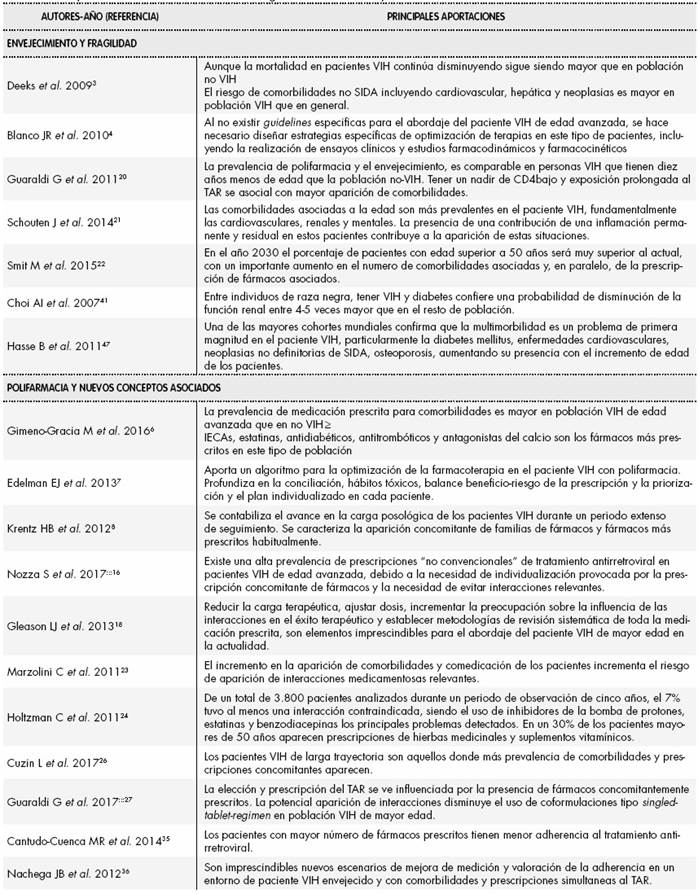
Tabla 1(cont.) Principales conclusiones de los artículos originales realizados en pacientes VIH + incluidos en la revisión.
En términos generales, la polifarmacia se ha definido como el uso concomitante de numerosos fármacos de manera simultánea. Sin embargo, existen múltiples definiciones del término, entre las que se incorporan aspectos como el uso de medicación potencialmente inapropiada (MPI), infrautilización del uso de fármacos o duplicidad farmacoterapéutica. A nivel del umbral numérico, se han utilizado en los diferentes estudios publicados distintos puntos de cortes, aunque la mayoría han usado el valor de cinco fármacos concomitantemente prescritos17,18. Sin embargo, desde la publicación del Documento de VIH y edad avanzada del Plan Nacional del SIDA y la Sociedad Española de Geriatría y Gerontología en 2015, que incluyó esta definición, al menos en nuestro entorno, se ha consensuado que un paciente está polimedicado si usa ≥ 6 principios activos simultáneamente, siendo esa la definición a utilizar para poder correlacionar y comparar los diferentes estudios que en un futuro se lleven a cabo19.
Desde el punto de vista más cualitativo, diferentes estudios han puesto de manifiesto ya la importancia del problema. El estudio de Guaraldi et al. fue el primero, en 2011, en identificar que el número de pacientes VIH + mayores de 50 años, con más de dos comorbilidades crónicas, era superior al de los sujetos de la misma edad no infectados por el VIH20. Asimismo, Schouten et al., en 2014, confirmó los datos21. Por otra parte, el modelo desarrollado por Smit et al., proyectó que, en 2030, el 84% de los pacientes tendrán más de dos comorbilidades22. Marzolini et al. publicaron el primer estudio que demostró que es a la edad de 50 años en pacientes VIH + donde se encuentra el punto de inflexión. A partir de esa edad, se observa, significativamente, la necesidad de más prescripciones de fármacos, apareciendo un porcentaje del 20% con más de cuatro fármacos prescritos23. La cohorte americana HOPS de 2013 también categorizó esos datos, confirmando un 95% de sus pacientes mayores de 60 años con polifarmacia, siendo el 73% debido a medicación concomitante24.
Otro concepto análogo, recientemente introducido, fue el de carga posológica, que incluyó no solo el número de medicamentos, sino también el unmero de tomas. Así, el estudio de Zhou et al. fue el primero en hablar de ello en pacientes VIH +25. Para los autores, la mediana de medicamentos prescritos fue de ocho (IQR: 6-11) y la mediana de formas farmacéuticas prescritas también de ocho (IQR: 5-15), tres (IQR: 2-5) de antirretrovirales y cinco (IQR: 3-12,5) de medicación concomitante. La duración del tiempo en tratamiento con antirretrovirales (por cada dos años en tratamiento) y tener más de tres comorbilidades se asociaban significativamente a la mayor carga posológica (más de 10 formas farmacéuticas al día). Cuzin et al., en un análisis similar para una cohorte francesa, encontró un 62% de comorbilidades y un 71% de comedicación en pacientes mayores de 50 años26. Ya en nuestro entorno, el estudio de Gimeno-Gracia et al. hablaba de la relevancia de la medicación concomitante en pacientes VIH + comparativamente con la población general, identificándose los inhibidores de la enzima convertidora de angiotensina, antidiabéticos, estatinas, agentes antitrombóticos y antagonistas del calcio, por ese orden, como las familias de fármacos más comúnmente prescritas6. En esta línea, las estrategias de TAR también se han visto afectadas por la aparición de la polifarmacia. El estudio de Guaraldi et al. demostró cómo las estrategias single-tablet-regimens son menos prescritas en aquellos pacientes con prescripción simultánea de varios fármacos concomitantes, debido, entre otros factores, a la posibilidad de interacciones27. La cohorte italiana GEPPO también ha confirmado cómo los tratamientos antirretrovirales en pacientes VIH de edad más avanzada se ven condicionados por la existencia de polifarmacia16.
Dando un paso más en el manejo del paciente polimedicado, particularmente el VIH + , en los últimos tiempos se ha querido cuantificar la importancia de la polifarmacia. Pasando, así, de un aspecto cualitativo, a uno más cuantitativo, valorando cifras y asociando ese valor a la obtención de resultados en salud. Este aspecto se analizó en el documento de la Sociedad Americana de Farmacia Hospitalaria (ASHP) Pharmacy Practice Model Summit-2011, en el que se recomendó que el seguimiento farmacoterapéutico a los pacientes debía llevarse a cabo, en base a un índice de complejidad (IC) de la farmacoterapia. El índice debía incluir factores como la gravedad de la enfermedad, el número de medicamentos y las comorbilidades28. Hasta ese momento, el único IC publicado era el de Martin et al., en 2007, precisamente para valorar la medicación antirretroviral9. Básicamente se trataba de un score basado en la ponderación de 15 variables agrupadas en cuatro grandes bloques: esquema terapéutico, recomendaciones de administración, instrucciones y preparación. Desde entonces, la Universidad de Colorado ha seguido desarrollando la herramienta para simplificar su cálculo y extrapolarlo a cualquier otra patología. Lo que ha dado lugar al desarrollo de los índices Patient-level Medication Regimen Complexity Index (pMRCI) y el Antiretroviral Medication Regimen Complexity Index (ARCI)10,11,29, que incluyen puntaciones que van desde el 0,75 hasta el infinito, en función de la medicación prescrita.
En el ámbito del VIH, el estudio de Metz et al. analizó las puntuaciones de este índice obtenidas en su cohorte, variando entre 2-67,5 (siendo el peso del TAR aproximadamente solo un 25% del valor total)11. Diversos autores han analizado la relación entre el IC y diferentes resultados en salud. Así, Monje-Agudo et al. identificaron que un IC con un valor de cinco, marcaba el umbral a partir del cual los pacientes tienen mayor riesgo de discontinuación del TAR30. Jiménez-Galán et al. analizaron la influencia del IC sobre el control clínico de pacientes VIH + con dislipemia, observando que mientras que la mayoría de los pacientes presentan un adecuado control viroinmunológico prácticamente la mitad de los mismos no cumplen objetivos terapéuticos de la dislipemia, especialmente aquellos con un IC más elevado31. Por otro lado, Calvo-Cidoncha et al. confirmaron como, en pacientes coinfectados con VIH-VHC adicionar la terapia anti-VHC incrementa la complejidad farmacoterapéutica y el riesgo de blips. Asociándose, además, a un descenso en la adherencia al TAR32.
Sin duda, uno de los principales aspectos a considerar sobre la repercusión del concepto de complejidad farmacoterapéutica, desde la perspectiva del paciente, ha sido la adherencia terapéutica. Algunos estudios en población general ya han examinado este factor, con resultados interesantes que hay que considerar por su posible influencia en la población VIH +33. En una revisión sistemática reciente, la falta de adherencia estuvo asociada con la existencia de polifarmacia12. Aunque algunos de esos estudios indiquen que existe una tendencia en los pacientes VIH + de mayor edad, de tener mejores tasas de adherencia, comparado con individuos jóvenes, se ha observado que el deterioro cognitivo puede dificultar este objetivo. También la polifarmacia puede contribuir a la fatiga farmacoterapéutica34. Específicamente en población VIH + , el estudio de Cantudo-Cuenca et al. demostró como el uso concomitante de medicación disminuye la adherencia a la medicación antirretroviral35.
Por otra parte, otro factor destacado en la bibliografía fue el riesgo de interacciones farmacológicas, que puede verse incrementando en individuos VIH + de edad avanzada, debido a los tratamientos para las múltiples comorbilidades que aparecen en esta población36-38. Además, es conocido ya, como la mayoría de los antirretrovirales comparten ruta de metabolización con la de otros fármacos habitualmente utilizados, tanto a nivel de citocromo (P450), como de glicoproteína P39.
La polifarmacia y su impacto en la aparición de interacciones ha sido descrita en estudios como el de Holtzman et al. realizado sobre una cohorte americana de pacientes atendidos de forma ambulatoria24. Entre los más de 3.800 pacientes analizados durante un periodo de observación de cinco años, el 7% tuvo al menos una interacción contraindicada, siendo el uso de inhibidores de la bomba de protones, estatinas y benzodiacepinas los principales responsables. Otro de los aspectos claves y llamativos de estudio fue la aparición, en casi un 30% de los pacientes VIH mayores de 50 años de prescripciones de hierbas medicinales, suplementos vitamínicos y de otro tipo, que pueden interaccionar con la medicación antirretroviral, como también se ha visto en otros estudios40-44.
Desde un punto de vista más clínico, un aspecto básico, a este respecto, ha sido conocer cómo la combinación de medicamentos utilizados para tratar enfermedades crónicas y el TAR en adultos mayores infectados con VIH aumenta la posibilidad de interacciones clínicamente relevantes, lo que puede conducir a la pérdida de eficacia de los medicamentos, el fracaso virológico y la toxicidad. Se ha identificado como los pacientes de edad más avanzada son aún más susceptibles a las interacciones que los individuos más jóvenes19. En primer lugar, por padecer un número mayor de comorbilidades relacionadas con el envejecimiento. En segundo lugar, los cambios fisiológicos relacionados con la edad afectan las propiedades farmacocinéticas y farmacodinámicas de los medicamentos. Estos cambios fisiológicos, vistos también en pacientes VIH + , se pueden explicar por una serie de factores que incluyen la genética del paciente, el estilo de vida y su entorno específico. Las alteraciones farmacocinéticas relacionadas con el envejecimiento se deben a cambios, tanto en la composición corporal de una persona como en la función de los órganos que eliminan los fármacos. El volumen hepático y el flujo sanguíneo hepático se ha confirmado que disminuyen con la edad19, así como el aclaramiento de creatinina, lo que puede provocar una disminución de la eliminación de los fármacos y la consecuente acumulación de los mismos. Por otro lado, la tasa de filtración glomerular disminuye alrededor de 1% por año con la edad. Se ha descrito cómo los métodos para estimar la función renal pueden sobreestimarla en adultos mayores, al no tener en cuenta la baja masa muscular45-46. En adultos infectados por VIH, este problema se ha complicado aún más porque esta población tiene característicamente una masa muscular inferior a la de personas no VIH + y, a menudo, pueden existir otras patologías o elementos a tener en cuenta, que actúen de factores de confusión y que pueden contribuir a disminuir aún más la función renal como, por ejemplo, diabetes mellitus, hipertensión, bajo recuento de células CD4, raza y uso de antirretrovirales47-48. La estimación de la función renal, por tanto, ha resultado más difícil en adultos mayores infectados por el VIH, afectando a la dosificación y la prescripción de medicamentos excretados por vía renal19.
Otro concepto clave y cada vez más importante en el abordaje del paciente VIH de edad avanzada es la fragilidad. Un síndrome emergente, que ha demostrado ser un buen predictor de un peor estado de salud y de eventos adversos en la población general13,14. La fragilidad engloba un síndrome biológico de disminución en la reserva funcional homeostática y en la capacidad de respuesta a agentes de estrés externos. Es el resultado de una acumulación de carencias en distintos sistemas fisiológicos y condiciona una vulnerabilidad para diversos efectos adversos, incluyendo caídas, delirium, hospitalización, discapacidad y muerte15. Hoy en día ya se conoce cómo los pacientes VIH + experimentan cambios inmunológicos similares a los que provoca el envejecimiento en la población anciana no infectada, aspectos que se producen a consecuencia, fundamentalmente, de un estado basal de activación inmune e inflamación persistente que de forma gradual llevan al envejecimiento del sistema inmune de forma precoz, lo que se conoce como inmunosenescencia. Esta activación crónica del sistema inmune viene marcada por la persistente replicación viral en reservorios, las coinfecciones con otros virus y fundamentalmente por la presencia de traslocación bacteriana por alteración persistente de la barrera intestinal47.
Si tenemos en cuenta estos aspectos comentados anteriormente, aparece un nuevo concepto: el de “prescripción inadecuada de fármacos” (PIF)48-49. Esta situación podría definirse como el riesgo de sufrir efectos adversos mayores al beneficio clínico, especialmente cuando existen alternativas terapéuticas más seguras y/o eficaces. La PIF también incluye el uso de fármacos con mayor frecuencia o mayor duración que la indicada, así como el uso de fármacos con elevado riesgo de interacciones medicamentosas y la duplicidad de fármacos de la misma clase. Igualmente incluye la incorrecta selección del medicamento o de la dosis y la no utilización o subutilización de fármacos beneficiosos que sí que están clínicamente indicados.
En la última década se ha manifestado un creciente interés en buscar los mecanismos para definir la adecuación de los tratamientos farmacológicos en los adultos mayores. Se han desarrollado diferentes grupos de criterios para la detección de MPI en pacientes mayores como los criterios de Beers y los STOPP-START50. La utilización de estos criterios para mejorar la utilización de medicamentos y evitar la PIF en la población VIH + está siendo ya estudiado y validado en algunos estudios, en este ámbito. El más reciente, publicado por McNicholl et al. encontró un 54% de prescripción potencialmente inadecuada y un 63% en pacientes VIH + mayores de 50 años, utilizando los criterios STOPP y Beers respectivamente51. El estudio de Greene et al.52, aunque más modesto en cuanto a tamaño muestral, dejó entrever, por primera vez, aspectos como la MPI. Este concepto se midió a través del uso de los criterios de Beers, incluyendo una lista guía de medicación y clases de medicamentos que deberían ser evitados en pacientes mayores de 65 años. Asimismo, se valoró el denominado riesgo colinérgico, a través de la escala validada ARS. En la misma se otorgaba una asignación de puntos de 0-3, donde tres indicaba alto riesgo y cero el nulo. El valor más alto otorgaba una predicción elevada de caídas y desórdenes mentales en población envejecida. En el estudio se identificó un 52% de MPI y un 17% de pacientes con un riesgo colinérgico de tres puntos. En nuestro entorno, el estudio de Casajús-Navasal et al. ha identificado el riesgo anticolinérgico, en una cohorte de práctica clínica real, de mayores de 50 años, según la escala ACB y ARS. Así, el 43,3% de los pacientes presentaba alto riesgo anticolinérgico con la escala ACB y el 36,4% según la escala ARS53.
De lo anteriormente indicado se ha identificado un interés por profundizar en un concepto ya conocido en población no VIH envejecida como es el de la desprescripción54-57. Según la definición de Scott et al.58, se trata de un proceso sistemático de identificación y discontinuación de fármacos en aquellos casos en los que los daños existentes o potenciales exceden los beneficios existentes o potenciales en un contexto de atención individualizada que tiene en cuenta su funcionalismo, su esperanza de vida, y sus valores y preferencias. Este proceso de retirada de fármacos tendría el potencial beneficio de poder reducir los efectos nocivos asociados con la polifarmacia, pero garantizando la capacidad de que el paciente continúa recibiendo la terapia más apropiada59. Se han identificado numerosas barreras para reducir el número de medicamentos y facilitar la desprescripción60,61. En la actualidad, también en el paciente VIH + , existe mucha información sobre cuándo iniciar una terapia, pero muy poca sobre cómo y cuándo suspenderla. Pese a la ausencia de evidencia que avale el mantenimiento de la terapia lo habitualmente descrito en la bibliografía es mantener los tratamientos pautados60,61.
El enfoque de todo este nuevo manejo de la medicación ha derivado en el concepto de optimización de la farmacoterapia y la inclusión y aplicación de estos nuevos términos, lo que ha llevado al consenso sobre la necesidad de llevar a cabo la revisión de toda la medicación prescrita, al menos cada seis meses en individuos que tengan prescrito ≥ 4 medicamentos, y al menos una vez al año para el resto19. Se ha determinado como prioritario identificar y establecer estrategias para De igual forma se recomienda realizar la revisión de la farmacoterapia prescrita de forma sistematizada y mediante una metodología secuencial y estructurada. Las recomendaciones, extraídas de la bibliografía, para introducir estrategias de optimización de la prescripción y la revisión de la polifarmacia en la práctica clínica diaria se detallan en la Tablas 2 y la Tabla 3.
Discusión
El abordaje del paciente VIH +, especialmente el de edad avanzada, es una preocupación creciente por cuanto el número de artículos que abordan esta problemática se está incrementando en los últimos años. No obstante, los nuevos conceptos identificados requieren aún de una mayor profundización y confirmación de los resultados, por cuanto aún no se han homogeneizado ni las definiciones utilizadas, particularmente los de polifarmacia y complejidad farmacoterapéutica, así como la metodología de análisis comparativo. Adicionalmente, estos nuevos conceptos, identificados como retos por los profesionales que atienden a esta población, requieren de un reenfoque en el manejo asistencial, en todos los ámbitos profesionales. Parece prioritario no ceñirse exclusivamente al tratamiento de la infección y al manejo de los fármacos antirretrovirales (adherencia, interacciones y/o efectos adversos) La bibliografía analizada manifiesta la, cada vez mayor, presencia de otros problemas emergentes asociados al envejecimiento como el manejo de comorbilidades y los deterioros funcional y cognitivo. Adicionalmente, los cambios fisiológicos que se producen con el envejecimiento deben ser tenidos en cuenta, para llevar a cabo un proceso de optimización de la farmacoterapia y el seguimiento clínico a este tipo de pacientes. Estos cambios identificados no se han manifestado como lineales ni uniformes, según la bibliografía. Por eso, es preciso realizar un abordaje global que permita detectar a aquellas personas de edad avanzada con infección por VIH, que están en riesgo de envejecer con un peor estado de salud o lo que es lo mismo: quiénes están en riesgo de tener una peor calidad de vida. Los primeros datos disponibles sobre la identificación de estos conceptos analizados en población no VIH envejecida, confirman la alta presencia de prescripciones potencialmente inadecuadas y presencia de un importante riesgo colinérgico.
No existe ningún estudio que haya abordado la desprescripción en esta población, pero dados los resultados publicados por los diversos autores, se hace necesario establecer una estrategia para su implantación y medición de su utilidad.
La principal limitación identificada del análisis realizado radica en las diferentes poblaciones, umbrales de edad y metodología de estudio llevada a cabo. Análogamente las diferentes definiciones utilizadas, así como la falta de estandarización de estas, dificulta la comparativa entre diferentes estudios que han abordado conceptos similares, especialmente la polifarmacia y la complejidad farmacoterapéutica.
Futuros estudios permitirán confirmar cómo el enfoque de abordaje propuesto por algunos autores, conducirá a una nueva visión del paciente y de su manejo. Resulta ya necesario y prioritario generar evidencias que demuestren la mejora, para el ámbito sanitario y los propios pacientes, que aportan esta nueva forma de entender la patología, ya que actualmente no están disponibles.
En conclusión, existe un interés creciente en profundizar en la relación entre la infección por VIH y el envejecimiento. La complejidad farmacoterapéutica está empezando a utilizarse como criterio de seguimiento farmacoterapéutico, por su influencia en resultados en salud. Es necesario manejar e incorporar nuevos conceptos que ayuden a la optimización farmacoterapéutica en esta población.
Bibliography
Antiretroviral Therapy Cohort Collaboration. Survival of HIV-positive patients starting antiretroviral therapy between 1996 and 2013: a collaborative analysis of cohort studies. Lancet HIV. 2017;4:e349-e356. DOI: 10.1016/S2352-3018(17)30066-8 [ Links ]
Centers for Disease Control - CDC (USA). Persons aged 50 and older. (Citado 07/10/2017). Disponible en: http://www.cdc.gov/hiv/topics/over50/index.htm [ Links ]
Deeks SG, Phillips AN. HIV infection, antiretroviral treatment, ageing, and non-AIDS related morbidity. BMJ. 2009;338:a3172 DOI: 10.1136/bmj.a3172 [ Links ]
Blanco JR, Caro AM, Pérez-Cachafeiro S, Gutiérrez F, Iribarren JA, González-García J, et al. HIV infection and aging. AIDS Rev. 2010;12(4):218-30. [ Links ]
HIV and Aging: State of Knowledge and Areas of Critical Need for Research: A report to the NIH Office of AIDS Research by the HIV and Aging Working Group J Acquir Immune Defic Syndr. 2012;60(Supl. 1):S1-18. DOI: 10.1097/QAI.0b013e31825a3668 [ Links ]
Gimeno-Gracia M, Crusells-Canales MJ, Armesto-Gómez FJ, Compaired-Turlan V, Rabanaque-Hernández MJ. Polypharmacy in older adults with human immunodeficiency virus infection compared with the general population. Clin Interv Aging. 2016;11:1149-57. DOI: 10.2147/CIA.S108072.eCollection 2016 [ Links ]
Edelman EJ, Gordon KS, Glover J, McNicholl IR, Fiellin DA, Justice AC. The next therapeutic challenge in HIV: polypharmacy. Drugs Aging. 2013;30:613-28. DOI 10.1007/s40266-013-0093-9 [ Links ]
Krentz HB, Cosman I, Lee K, Ming JM, Gill MJ. Pill burden in HIV infection: 20 years of experience. Antivir Ther. 2012;17:833-40. DOI: 10.3851/IMP2076 [ Links ]
Martin S, Wolters PL, Calabrese SK, Toledo-Tamula MA, Wood LV, Roby G, et al. The Antiretroviral Regimen Complexity Index: a novel method of quantifying regimen complexity. J Acquir Immune Defic Syndr. 2007;45(5):535-44. [ Links ]
Libby AM, Fish DN, Hosokawa PW, Linnebur SA, Metz KR, Nair KV, et al. Patientlevel medication regimen complexity across populations with chronic disease. Clin Ther. 2013;35(4):385-98. DOI: 10.1016/j.clinthera.2013.02.019 [ Links ]
Metz KR, Fish DN, Hosokawa PW, Hirsch JD, Libby AM. Patient-Level Medication Regimen Complexity in Patients With HIV. Ann Pharmacother. 2014;48(9):1129-37. [ Links ]
Wimmer BC, Cross AJ, Jokanovic N, Wiese MD, George J, Johnell K, et al. Clinical outcomes associated wiht medication regimen complexity in order people: a systematic review. J Am Geriatr Soc. 2017;65:747-53. DOI: 10.1111/jgs.14682 [ Links ]
Moulis F, Moulis G, Balardy L, Gerard S, Sourdet S, Rouge-Bugat ME, et al. Searching for a polypharmacy threshold associated with frailty. J Am Med Dir Assoc. 2015;16:259-61. DOI: 10.1016/j.jamda.2014.11.016 [ Links ]
Moulis F, Moulis G, Balardy L, Gerard S, Montastruc F, Sourdet S, et al. Exposure to atropinic drugs and frailty status. J Am Med Dir Assoc. 2015;16:253-7. DOI: 10.1016/j.jamda.2014.11.017 [ Links ]
Fried LP, Tangen CM, Walston J, Newman AB, Hirsch C, Gottdiener J, et al. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci. 2001;56:146-56. [ Links ]
Nozza S, Malagoli A, Maia L, Calcagno A, Focà E, De Socio G, et al. Antiretroviral therapy in geriatric HIV patients: the GEPPO cohort study. J Antimicrob Chemother. 2017;72(10):2879-86. DOI: 10.1093/jac/dkx169 [ Links ]
Gnjidic D, Hilmer SN, Blyth FM, Naganathan V, Waite L, Seibel MJ, et al. Polypharmacy cutoff and outcomes: five or more medicines were used to identify community-dwelling older men at risk of different adverse outcomes. J Clin Epidemiol. 2012;65:989-95 DOI: 10.1016/j.jclinepi.2012.02.018 [ Links ]
Gleason LJ, Luque AE, Shah K. Polypharmacy in the HIV-infected older adult population. Clin Interv Aging. 2013;8:749-63. DOI: 10.2147/CIA.S37738 [ Links ]
. Grupo de expertos de la Secretaría del Plan Nacional sobre el sida (SPNS), Sociedad Española de Geriatría y Gerontología (SEGG). (Noviembre 2015). Documento de consenso sobre Edad Avanzada e Infección por el Virus de la Inmunodeficiencia Humana. (Citado 22/10/2017). Disponible en http://www.msssi.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/publicaciones/profSanitarios/docEdadAvanzadaVIH.pdf [ Links ]
Guaraldi G, Orlando G, Zona S, Menozzi M, Carli F, Garlassi E, et al. Premature age-related comorbidities among HIV-infected persons compared with the general population. Clin Infect Dis. 2011;53(11):1120-6 DOI: 10.1093/cid/cir627 [ Links ]
Schouten J, Wit FW, Stolte IG, Kootstra NA, van der Valk M, Geerlings SE, et al. Cross-sectional comparison of the prevalence of age-associated comorbidities and their risk factors between HIV-infected and uninfected individuals: the AGEhIV Cohort Study. Clin Infect Dis. 2014;59:1787-97. DOI: 10.1093/cid/ciu701 [ Links ]
Smit M, Brinkman K, Geerlings S, Smit C, Thyagarajan K, Sighem AV, et al. Future challenges for clinical care of an ageing population infected with HIV: amodelling study. Lancet Infect Dis. 2015;15(7):810-8. DOI: 10.1016/S1473-3099(15)00056-0 [ Links ]
Marzolini C, Back D, Weber R, Furrer H, Cavassini M, Calmy A, et al. Ageing with HIV: medication use and risk for potential drug-drug interactions. J Antimicrob Chemother. 2011;66:2107-11. DOI: 10.1093/jac/dkr248 [ Links ]
Holtzman C, Armon C, Tedaldi E, Chmiel JS, Buchacz K, Wood K, Brooks JT, and the HOPS Investigators. Polypharmacy and Risk of Antiretroviral Drug Interactions Among the Aging HIV-Infected Population J Gen Intern Med. 2013. 28(10):1302-10. DOI: 10.1007/s11606-013-2449-6 [ Links ]
Zhou S, Martin K, Corbett A, Napravnik S, Eron J, Zhu Y, et al. Total Daily Pill Burden in HIV-Infected Patients in the Southern United States. AIDS Patient Care STDS. 2014;28:311-7. DOI: 10.1089/apc.2014.0010 [ Links ]
Cuzin L, Katlama C, Cotte L, Pugliese P, Cheret A, Bernaud C, et al. Ageing with HIV: do comorbidities and polymedication drive treatment optimization? HIV Med. 2017 18(6):395-401. DOI: 10.1111/hiv.12441 [ Links ]
Guaraldi G, Menozzi M, Zona S, Calcagno A, Silva AR, Santoro A, et al. Impact of polypharmacy on antiretroviral prescription in people living with HIV. J Antimicrob Chemother. 2017;72:511-4. DOI: 10.1093/jac/dkw437 [ Links ]
The consensus of the Pharmacy Practice Model Summit. Am J Health Syst Pharm. 2011. Jun 15;68(12):1148-52. DOI : 10.2146/ajhp110060. (Citado 29/10/2017). Disponible en: http://www.ajhp.org/content/68/12/1148.full.pdf+html [ Links ]
Patient-level medication regimen complexity in defined clinical populations. (Citado 21-10-2017). Disponible en: http://www.ucdenver.edu/academics/colleges/pharmacy/Research/researchareas/Pages/MRCTool.aspx. [ Links ]
Monje Agudo P, Calvo Cidoncha E, Gómez Fernández E, Almeida González CV, Morillo Verdugo R. Predictor and complexity indexes as predictors of antiretroviral therapy discontinuation. Eur J Clin Pharm. 2014;16(3):189-93. [ Links ]
Jiménez Galán R, Montes Escalante I, Morillo Verdugo R. Influencia de la complejidad farmacoterapéutica en el cumplimiento de los objetivos terapéuticos en pacientes VIH + con tratamiento antirretroviral y concomitante para la dislipemia. Proyecto INCOFAR. Farm Hosp. 2016;40(2):90-101. DOI: 10.7399/fh.2016.40.2.9932 [ Links ]
Calvo-Cidoncha E, González-Bueno J, Almeida-González C, Morillo-Verdugo R. Influence of Treatment Complexity on Adherence and Incidence of Blips in HIV/HCV Coinfected Patients. J Manag Care Pharm. 2015;21(2):153-57. [ Links ]
Patton DE, Hughes CM, Cadogan CA, Ryan CA. Theory-Based Interventions to Improve Medication Adherence in Older Adults Prescribed Polypharmacy: A Systematic Review. Drugs Aging. 2017;34(2):97-113. DOI 10.1007/s40266-016-0426-6 [ Links ]
Usherwood T. Encouraging adherence to long-term medication. Aust Prescr. 2017;40:147-50. DOI: 10.18773/austprescr.2017.050 [ Links ]
Cantudo-Cuenca MR, Jiménez-Galán R, Almeida-Gonzalez CV, Morillo-Verdugo R. Concurrent use of comedications reduces adherence to antiretroviral therapy among HIV-infected patients. J Manag Care Spec Pharm. 2014;20(8):844-50. [ Links ]
Nachega JB, Hsu AJ, Uthman OA, Spinewine A, Pham PA. Antiretroviral therapy adherence and drug-drug interactions in the aging HIV population. AIDS. 2012;26(Supl. 1):S39-53. [ Links ]
Tseng A, Szadkowski L, Walmsley S, Salit I, Raboud J. Association of Age With Polypharmacy and Risk of Drug Interactions With Antiretroviral Medications in HIV-Positive Patients. Ann Pharmacother. 2013;47:1429-39. DOI: 10.1177/1060028013504075 [ Links ]
Littlewood RA, Vanable PA. Complementary and alternative medicine use among HIV-positive people: research synthesis and implications for HIV care. AIDS Care. 2008;20:1002-18. DOI: 10.1080/09540120701767216 [ Links ]
HIV drug interactions. (Citado 27-10-2017). Disponible en https://www.hiv-druginteractions.org/ [ Links ]
Barry DT, Goulet JL, Kerns RK, Becker WC, Gordon AJ, Justice AC, et al. Nonmedical use of prescription opioids and pain in veterans with and without HIV. Pain. 2011;152:1133-8. [ Links ]
Choi AI, Rodriguez RA, Bacchetti P, Bertenthal D, Volberding PA, O’Hare AM. Racial differences in end-stage renal disease rates in HIV infection versus diabetes. J Am Soc Nephrol. 2007;18(11):2968-74. [ Links ]
Mocroft A, Kirk O, Gatell J, Gargalianos P, Zilmer K, et al. Chronic renal failure among HIV-1-infected patients. AIDS. 2007;21(9):1119-27. [ Links ]
Scherzer R, Estrella M, Li Y. Association of tenofovir exposure with kidney disease risk in HIV infection. AIDS. 2012;(7):867-75. DOI: 10.1097/QAD.0b013e328351f68f [ Links ]
Kalayjian RC, Franceschini N, Gupta SK. Suppression of HIV-1 replication by antiretroviral therapy improves renal function in persons with low CD4 cell counts and chronic kidney disease. AIDS. 2008;(4):481-7. DOI: 10.1097/QAD.0b013e3282f4706d [ Links ]
Cohen C, Elion R, Ruane P, Shamblaw D, DeJesus E, Rashbaum B, et al. Randomized,phase 2 evaluation of two single-tablet regimens elvitegravir/cobicistat/emtricitabine/tenofovir disoproxil fumarate versus efavirenz/emtricitabine/tenofovir disoproxil fumarate for the initial treatment of HIV infection. AIDS. 2011;25(6):F7-12. DOI: 10.1097/QAD.0b013e328345766f [ Links ]
Elion R, Cohen C, Gathe J, Shalit P, Hawkins T, Liu HC, et al.; for GS-US-216-0105 Study Team. Phase 2 study of cobicistat versus ritonavir each with once-daily atazanavir and fixed-dose emtricitabine/tenofovir df in the initial treatment of HIV infection. AIDS. 2011;25(15):1881-6. DOI: 10.1097/QAD.0b013e32834b4d48 [ Links ]
Hasse B, Ledergerber B, Furrer H, Battegay M, Hirschel B, Cavassini M, et al. Morbidity and aging in HIV-infected persons: the Swiss HIV cohort study. Clin Infect Dis. 2011;53:1130-9. DOI: 10.1093/cid/ciw495 [ Links ]
Anderson K, Stowasser D, Freeman C, Scott I. Prescriber barriers and enablers to minimising potentially inappropriate medications in adults: a systematic review and thematic synthesis. BMJ Open. 2014;4:e006544. DOI: 10.1136/bmjopen-2014-006544 [ Links ]
American Geriatrics Society 2012 Beers Criteria Update Expert Panel. American Geriatrics Society updated Beers Criteria for potentially inappropriate medication use in older adults. J Am Geriatr Soc. 2012; 60:616-31. DOI: 10.1111/j.1532-5415.2012.03923.x [ Links ]
Gallagher P, Ryan C, Byrne S, Kennedy J, O’Mahony D. STOPP (Screening Tool of Older Person’s Prescriptions) and START (Screening Tool to Alert doctors to Right Treatment). Consensus validation. Int J Clin Pharmacol Ther. 2008;46:72-83. [ Links ]
McNicholl IR, Gandhi M, Hare CB, Greene M, Pierluissi E. A Pharmacist-Led Program to Evaluate and Reduce Polypharmacy and Potentially Inappropriate Prescribing in Older, HIV-Positive Patients. Pharmacotherapy. 2017;37(12):1498-1506. DOI: 10.1002/phar.2043 [ Links ]
Greene M, Justice AC, Lampiris HW, Valcour V. Management of Human Immunodeficiency Virus Infection in Advanced Age. JAMA. 2013;309:1397-1405. DOI: 10.1001/jama.2013.2963 [ Links ]
Casajús-Navasal A, Marín-Gorricho R, Gallardo-Anciano J, Nebot-Villacampa MJ, Zafra-Morales R, González-Pérez Y. Prevalence of the consumption of anticholinergic drugs in HIV patients. Farm Hosp. 2018;42(1):1-4. DOI: 10.7399/fh.10842 [ Links ]
Reeve E, Wiese MD. Benefits of deprescribing on patients’ adherence to medications. Int J Clin Pharm. 2014;36:26-9. DOI: 10.1007/s11096-013-9871-z. [ Links ]
Reeve E, To J, Hendrix I, Shakib S, Roberts MS, Wiese MD. Patient barriers to and enablers of deprescribing: a systematic review. Drugs Aging. 2013;30:793-807. DOI:: 10.1007/s40266-013-0106-8 [ Links ]
Jyrkka J, Enlund H, Korhonen MJ, Sulkava R, Hartikainen S. Polypharmacy status as an indicator of mortality in an elderly population. Drugs Aging. 2009;26:1039-48. DOI: 10.2165/11319530-000000000-00000 [ Links ]
Palagyi A, Keay L, Harper J, Potter J, Lindley RI. Barricades and brickwalls-a qualitative study exploring perceptions of medication use and deprescribing in long-term care. BMC Geriatr. 2016;16:15. DOI: 10.1186/s12877-016-0181-x [ Links ]
Scott IA, Hilmer SN, Reeve E, Potter K, Le Couteur D, Rigby D, et al. Reducing inappropriate polypharmacy: the process of deprescribing. JAMA Intern Med. 2015;175:827-34. DOI: 10.1001/jamainternmed.2015.0324 [ Links ]
Garfinkel D, Ilhan B, Bahat G. Routine deprescribing of chronic medications to combat polypharmacy. Ther Adv Drug Saf. 2015;6:212-33. DOI: 10.1177/2042098615613984 [ Links ]
Bemben NM. Deprescribing: An Application to Medication Management in Older Adults. Pharmacotherapy. 2016;36:774-80. DOI: 10.1002/phar.1776 [ Links ]
Cullinan S, Fleming A, O’Mahony D, Ryan C, O’Sullivan D, Gallagher P, et al. Doctors’ perspectives on the barriers to appropriate prescribing in older hospitalized patients: a qualitative study. Br J Clin Pharmacol. 2015;79:860-9. DOI 10.1111/bcp.12555 [ Links ]
Recibido: 05 de Noviembre de 2017; Aprobado: 28 de Enero de 2018











 texto en
texto en