My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Farmacia Hospitalaria
On-line version ISSN 2171-8695Print version ISSN 1130-6343
Farm Hosp. vol.42 n.6 Toledo Nov./Dec. 2018 Epub Nov 09, 2020
https://dx.doi.org/10.7399/fh.10932
ORIGINALES
Determinación del pH como criterio de calidad en la elaboración de fórmulas magistrales orales líquidas
1Pharmacy Unit. Complejo Hospitalario Universitario de Pontevedra, Pontevedra. Spain.
Objetivo:
El pH es un factor crítico para todos aquellos medicamentos que se encuentran en formas líquidas acuosas, ya que puede ejercer un efecto sobre la solubilidad del principio activo condicionando la estabilidad de los medicamentos, la tolerancia biológica de la forma farmacéutica y la actividad del principio activo. El objetivo de este trabajo es establecer el rango óptimo de pH de las fórmulas orales líquidas más frecuentemente elaboradas en el Servicio de Farmacia para estandarizar e incorporar dicho valor en los protocolos normalizados de trabajo como criterio de control de calidad.
Método:
El estudio se desarrolló en tres fases. En una primera fase se realizó un estudio retrospectivo de los registros de elaboración de las fórmulas orales líquidas elaboradas, al menos 5 veces, desde enero de 2015 a diciembre de 2016 en nuestro Servicio de Farmacia, y se calculó el valor medio y la desviación estándar de los valores de pH registrados para cada fórmula. En una segunda fase se realizó una búsqueda bibliográfica para conocer el pH de máxima estabilidad del principio activo y comprobar si esta característica se registra como requisito de control de calidad en los procedimientos descritos en los formularios de referencia. En una tercera fase se comprobó si los pH determinados se correspondían con el de máxima estabilidad descrito en la literatura y se establecieron rangos de aceptación.
Resultados:
Se revisaron un total de 31 fórmulas (14 soluciones/17 suspensiones). Se conocía el valor del pH de máxima estabilidad de 19 (61,3%) de los principios activos y/o fórmulas orales líquidas evaluadas, de las cuales 15 (78,9%) se encontraban dentro del mismo y las 4 restantes (21,1%) presentaron una desviación estándar de ± 0,5 con respecto al valor de pH referenciado en la bibliografía. El rango de pH para un mismo procedimiento normalizado de trabajo oscilaba entre 0,32 y 1,51. Se estableció como control de calidad un rango de aceptación de pH de ± 0,75.
Conclusiones:
Se ha establecido un rango óptimo de pH para las 31 fórmulas orales líquidas de mayor prescripción en nuestro hospital. Esta característica debería formar parte de la validación galénica de estas preparaciones, así como de su control de calidad rutinario, para asegurar la calidad y eficacia de las mismas
PALABRAS CLAVE: Control de calidad; Estabilidad; Formulación magistral; Formularios; Indicador de calidad; pH
Introducción
El pH de una solución acuosa es un factor crítico que se ha de tener en cuenta para todos aquellos medicamentos que se encuentran en formas líquidas acuosas. El efecto que el pH puede ejercer sobre la solubilidad condiciona de manera decisiva la estabilidad de los medicamentos a administrar. Además, puede verse comprometida la tolerancia biológica de la forma farmacéutica y la actividad del principio activo (PA)1.
La solubilidad de los fármacos ácidos y básicos es pH dependiente y está en función de su constante de ionización, lo cual origina un equilibrio entre la especie ionizada y la no ionizada, produciendo la disolución del ácido y/o de la base. Las reacciones acuosas son generalmente catalizadas por el pH. Se han hecho estudios que miden las velocidades de degradación a distintos pH, manteniendo constante la temperatura, fuerza iónica y concentración del solvente. En estos estudios se concluye que, si el pH no se encuentra dentro de un rango de máxima estabilidad, predomina la forma no ionizada del fármaco, dando lugar a la formación de precipitados insolubles2.
Cada PA tiene un rango de pH en el que presenta su máxima estabilidad y fuera de ese rango puede perder actividad, debido a transformaciones físicas y químicas. La combinación con diluyentes, excipientes y otros medicamentos que posean un pH diferente puede desencadenar efectos no deseados y comprometer la estabilidad de la formulación. Se ha comprobado que, por ejemplo, el ácido fólico y la furosemida precipitan a pH inferior a 8 y a 7, respectivamente; el omeprazol se degrada a valores de pH inferiores a 7,8; el propranolol se descompone si está expuesto a valores de pH alcalinos y el captopril sufre degradación oxidativa en medios que presenten valores de pH superiores a 43.
Por tanto, la determinación del pH es importante en la elaboración de formulaciones orales líquidas (FOL), ya que afecta a la solubilidad, actividad, absorción, tolerancia biológica y estabilidad del PA4,5.
Sin embargo, la mayor parte de los formularios de reconocido prestigio sobre FOL para pacientes pediátricos: “Formulación Pediátrica Manuela Atienza”, “Standardised formulations for New Zealand”, “Nation-wide Children´s Hospital”, “Hospital for Sick Children” and “University of Michigan College of Pharmacy”, no recogen valores de pH de máxima estabilidad de las preparaciones descritas en ellos. Por otro lado, el Formulario Nacional Español (FNE) incluye en su procedimiento PN/L/ CP7001/00 la determinación de pH como control de calidad de soluciones, suspensiones y jarabes, pero exclusivamente para las formulaciones elaboradas en lotes6 7 8 9 10-11.
Ante la falta de datos de compatibilidad entre los componentes de las FOL, planteamos que conocer los pH de máxima estabilidad de los medicamentos a administrar es un factor predictivo que puede evitar serios problemas de estabilidad y cuya determinación asegura la calidad y eficacia de las preparaciones elaboradas.
El objetivo de este trabajo es establecer el rango óptimo de pH de las FOL más frecuentemente elaboradas en el Servicio de Farmacia para estandarizar e incorporar dicho valor en los protocolos normalizados de trabajo (PNT) como criterio de control de calidad.
Métodos
Se realizó un estudio retrospectivo de los registros de elaboración de todas las FOL preparadas en el Servicio de Farmacia desde enero de 2015 a diciembre de 2016. Se seleccionaron aquellas FOL que se habían elaborado con una frecuencia igual o superior a 5 y se recogieron los valores de pH evaluados. Se calculó el valor medio y la desviación estándar para cada preparación, así como el rango, obtenido a través de la diferencia entre el valor máximo y el mínimo registrado. Estas determinaciones de pH se realizaron con un medidor sensIONTMpH31®.
Para conocer el pH de máxima estabilidad del PA, se revisaron como fuentes bibliográficas: la ficha técnica de la materia prima de nuestro principal proveedor (www.acofarma.com/es/formulación-magistral/ fichas- tecnicas) y los libros Trissel´s “Stability of Compounded Formulations”, 2.ª edición, y Handbook of Extemporaneous Preparation (2010), así como las fichas técnicas de la Agencia Española del Medicamento y Productos Sanitarios (AEMPS) de medicamentos comerciales para administración en solución por vía intravenosa y el United States Pharmacopeia 32th edition and National Formulary 27th edition (USP 32- NF27)12-16.
También se consultaron los formularios de referencia más relevantes en formulación pediátrica anteriormente citados6 7 8 9-10.
Finalmente, los valores de pH registrados se contrastaron con los valores de máxima estabilidad contemplados en la bibliografía y se estableció rango de aceptación para cada una de las FOL evaluadas.
Resultados
Se revisaron un total de 31 FOL según los criterios de la primera fase del estudio, de las cuales 14 eran soluciones y 17 eran suspensiones (Tabla 1.1) (Tabla 1.2) (Tabla 1.3). Para todas las FOL que se elaboraron durante el periodo de estudio y que cumplían los criterios de inclusión, se recogieron los datos de valor medio de pH, desviación estándar y rangos de pH para un mismo PNT (Tabla 2). Este último valor oscilaba entre 0,32 y 1,51.
Tabla 1. Forma farmacéutica y composición de las formulaciones orales líquidas elaboradas en el Servicio de Farmacia

Tabla 1. (cont.). Forma farmacéutica y composición de las formulaciones orales líquidas elaboradas en el Servicio de Farmacia

Tabla 1. (cont.). Forma farmacéutica y composición de las formulaciones orales líquidas elaboradas en el Servicio de Farmacia

amp: ampollas; cáps: cápsulas; comp: comprimidos; cs: cantidad suficiente; csp: cantidad suficiente para.
Tras consultar las diferentes fuentes bibliográficas para conocer el pH de máxima estabilidad del PA, sólo se conocía el valor de 19 (61,3%) de los PA y/o FOL evaluadas.
En cuanto a los formularios de referencia consultados, se establecía un valor de pH como control de calidad para 3 (9,7%) de las FOL seleccionadas en “Formulación Pediátrica Manuela Atienza”; 10 (32,3%) en el “Standardised formulations for New Zealand”, 1 (3,2%) en el “Nation-wide Children´s Hospital”, 1 (3,2%) en el “University of Michigan College of Pharmacy” y ninguna en el “Hospital for Sick Children”.
Los datos de pH de máxima estabilidad de PA y de FOL referenciados en la bibliografía seleccionada se recogen en laTabla 3.
Tabla 3. Valores de pH de máxima estabilidad del principio activo y valores de pH de formulaciones orales líquidas descritos en la bibliografía consultada
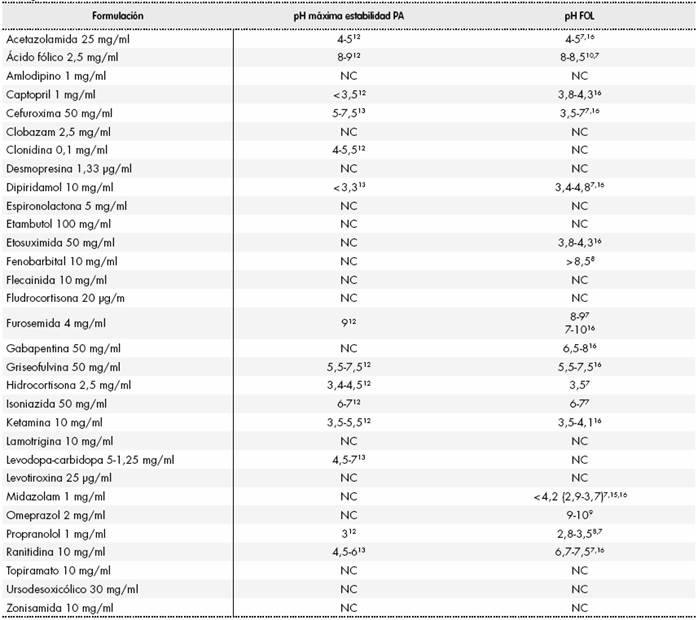
FOL: fórmulas orales líquidas; NC: no conocido; PA: principio activo.
De las 19 FOL y/o PA para los que se conoció el rango de pH de máxima estabilidad, 15 (78,9%) se encontraban dentro del mismo y las 4 (21,1%) restantes presentaron una desviación estándar de ± 0,5.
Basándonos en los datos recogidos en la bibliografía consultada y en la variabilidad de las determinaciones evaluadas, se estableció incluir el pH como control de calidad habitual en los PNT con un rango de aceptación de ± 0,75.
Discusión
El pH es uno de los factores que más influyen en la estabilidad de una forma farmacéutica en solución acuosa. Conocer el pH de máxima estabilidad de un PA de las FOL es primordial para garantizar la calidad de la formulación elaborada y éste debe mantenerse estable durante todo el periodo de validez y conservación establecidas1.
En la mayor parte de los formularios revisados no se incluye el pH como control a realizar, ni un rango de aceptación, sólo en el USP 32-NF 27 se describe un rango de pH para cada monografía. En el FNE se describe la determinación de pH (PN/L/CP/001/00) como procedimiento de control de producto y se exige para todas las soluciones, suspensiones, jarabes y geles elaborados en lotes11,16.
Es de destacar la escasa bibliografía que aporta datos sobre los valores de pH de máxima estabilidad para un PA y/o FOL.
Puesto que hay muchos medicamentos como furosemida, propranolol, omeprazol y captopril que tienen un pH de máxima estabilidad conocido y muy delimitado, fuera del cual la formulación no es estable, consideramos que es un valor que debe ser conocido y evaluado, aunque sea una fórmula individualizada y no se elabore en lotes5. El PNT establecido debería incluir este criterio.
Para aquellas FOL para las cuales no se conoce un rango de pH de máxima estabilidad o el PA es insoluble, la determinación del pH sigue siendo un indicador de calidad, puesto que debe mantenerse estable y reproducible para un mismo PNT, como se ha demostrado en el estudio.
Aunque el Servicio de Farmacia evaluaba y registraba el pH de forma rutinaria para todas las FOL individualizadas, no estaba establecido un rango de aceptación para cada PNT. Este trabajo nos ha servido para protocolizar este criterio e incluir su evaluación como control de calidad.
Conocer el pH de máxima estabilidad en la elaboración de una FOL y establecer un rango de aceptación como control de calidad son requisitos indispensables para una correcta validación galénica y garantizar la eficacia del tratamiento.
Aportación a la literatura científica
La mayor parte de los formularios de referencia pediátricos no incluyen la determinación del pH como control de calidad en la elaboración de fórmulas orales líquidas.
La búsqueda bibliográfica realizada en este estudio pone en evidencia la influencia que tiene el pH en la estabilidad de estas formulaciones y la importancia de conocer el rango de pH de máxima estabilidad del PA. El poder establecer dicho valor como control de calidad nos permitirá garantizar la reproducibilidad de un mismo procedimiento normalizado de trabajo y una correcta validación galénica de la fórmula elaborada.
REFERENCIAS
Loyd V, Allen Jr, Edmon OK. pH and Solubility, Stability and Absortion Part II. Science and Technology. 2011;1(8) (consultado 25/1/2017). Disponible en: https://compoundingtoday.com/Newsletter/Science_and_Tech_1112.cfm [ Links ]
Veiga Ochoa MD, Gil Alegre ME, Torrado Duran J. Preformulacion. En: Vila Jato JL, editor. Tecnologia Farmaceutica Volumen I: Aspectos fundamentales de los sistemas farmaceuticos y operaciones basicas. Madrid: Sintesis; 2001; p. 27-73. [ Links ]
Allen LV. Preservatives, Antioxidants and pH. Secundum Artem. 2014;18(1):1-8 (consultado 25/1/2017). Disponible en: https://www.perrigo.com/business/pdfs/Sec%20Artem%2018.1.pdf [ Links ]
Garcia Palomo M, Canete Ramirez C. Vehiculos en formulaciones orales liquidas para pacientes pediatricos preparaciones esteriles. Boletin de Farmacotecnia. 2014;4(3):1-7 (consultado 25/1/2017). Disponible en: http://gruposdetrabajo.sefh.es/farmacotecnia/images/stories/Boletines/BOLETIN32014final.pdf [ Links ]
Davila MC. Estabilidad, caducidad y conservacion de Formulas Magistrales. En: Pineiro Corrales G, coordinadora. Aspectos practicos de la farmacotecnia en un servicio de farmacia. Madrid: Astellas Pharma; 2011; p. 133-48. [ Links ]
Atienza Fernandez M, Martinez Atienza J. Formulacion en Farmacia Pediatrica (pagina web en internet). Madrid: Manuela Atienza; 2011 (2/5/2011, consultado 25/1/2017). Disponible en: http://formulacionpediatrica.es/procedimientos-pnt/ [ Links ]
Pharmaceutical Society of New Zealand incorporated. Standardised formulations for New Zealand (Base de datos en internet). New Zeland: Chris Jay; 2010 (consultado 30/1/2017). Disponible en: https://www.psnz.org.nz/Category?Action=View&Category_id=284 [ Links ]
Nationwide Children’s Hospital. Compounding Formulas (base de datos en internet). Ohio: Nationwide Children´s Hospital (consultado 30/1/2017). Disponible en: http://www.nationwidechildrens.org/outpatient-pharmacycompounding-formulas [ Links ]
Walsh K, Hook R. Sickkids (Base de datos en Internet). Toronto: The Hospital for Sick Children; 1999 (2014; consultado 30/01/2017). Disponible en: http://www.sickkids.ca/pharmacy/compounding-service/index.html [ Links ]
Arenz B. State-Wide initiative to standardize the compounding of oral liquids in Pediatrics. Michigan College (base de datos en internet). Michigan; 2014 (2017; consultado 2/2/2017). Disponible en: http://www.mipedscompounds.org/about-initiative [ Links ]
Sintas Ponte E, Vardulaki Operman A, Tarno Fernandez ML, Nunez Velazquez A. Formulario Nacional Espanol. Madrid: Ministerio de Sanidad y Consumo, Secretaria General Tecnica y Boletin Oficial del Estado; 2003. [ Links ]
Acofarma Distribucion S.A. Fichas tecnicas-Formulacion Magistral (base de datos de internet). Madrid: Carmen Bau; 2017 (consultado 29/1/2017). Disponible en: http://www.acofarma.com/es/formulacion-magistral/fichas-tecnicas [ Links ]
Trissel LA. Stability of Compounded Formulations. 2a ed. Washington: American Pharmaceutical Association; 2000. [ Links ]
Jackson M, Lowey A. Handbook of Extemporaneous Preparation, a guide to pharmaceutical compounding. London: Pharmaceutical Press; 2010. [ Links ]
Agencia Espanola de Medicamentos y Productos Sanitarios (AEMPS). Centro de informacion online de medicamentos de la AEMPS (base de datos de internet). Madrid: Ministerio de Sanidad, Servicios Sociales e Igualdad (consultado 29/01/2017). Disponible en: https://www.aemps.gob.es/cima/inicial.do [ Links ]
Food and Drug Administration. United States Pharmacopeia 32th edition and National Formulary. 27th edition. Washington DC: Silver Spring; 2008. [ Links ]
Cómo citar este artículo:Vázquez-Blanco S, González-Freire L, Dávila-Pousa MC, Crespo-Diz C. pH determination as a quality standard for the elaboration of oral liquid compounding formula. Farm Hosp. 2018;42(6):221-227.
Aportación a la literatura científica :La mayor parte de los formularios de referencia pediátricos no incluyen la determinación del pH como control de calidad en la elaboración de fórmulas orales líquidas. La búsqueda bibliográfica realizada en este estudio pone en evidencia la influencia que tiene el pH en la estabilidad de estas formulaciones y la importancia de conocer el rango de pH de máxima estabilidad del PA. El poder establecer dicho valor como control de calidad nos permitirá garantizar la reproducibilidad de un mismo procedimiento normalizado de trabajo y una correcta validación galénica de la fórmula elaborada.
Recibido: 05 de Noviembre de 2017; Aprobado: 30 de Junio de 2018











 text in
text in 



