Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Farmacia Hospitalaria
versión On-line ISSN 2171-8695versión impresa ISSN 1130-6343
Farm Hosp. vol.43 no.3 Toledo may./jun. 2019 Epub 14-Oct-2019
https://dx.doi.org/10.7399/fh.11127
ORIGINALES
Estudio piloto para desarrollar y validar un cuestionario basado en el índice de síntomas de VIH
1Servicio de Farmacia, Hospital de Urdúliz-Alfredo Espinosa, Urdúliz. España.
2Servicio de Farmacia. Hospital Galdakao-Usansolo, Galdakao. España.
3Unidad de Investigación, Hospital Galdakao-Usansolo, Galdakao. España.
4Servicio de Farmacia, Hospital Universitario Marqués de Valdecilla, Santander. España.
5Servicio de Farmacia, Hospital Universitario Virgen de Valme, Sevilla. España.
Objetivo
El objetivo principal es validar el cuestionario de Índice de Síntomas de VIH en población española, en cuanto a comprensión y aceptabilidad. Objetivos secundarios: describir síntomas referidos por el paciente, tolerancia y calidad de vida.
Método
Fase piloto de un estudio observacional y multicéntrico no comparativo, para la validación del cuestionario de Índice de Síntomas de VIH en población española. Se incluyeron pacientes mayores de 18 años, diagnosticados de infección por el VIH en tratamiento. Se calculó el índice de síntomas, la adherencia según los registros de dispensación y la calidad de vida con el cuestionario MOS-HIV. Los cálculos estadísticos se realizaron en el SAP System V9.2.
Resultados
Se aplicó el cuestionario de Índice de Síntomas de VIH en 75 pacientes, durante los años 2013 y 2014. El 95% consideró el cuestionario como de fácil aplicación y comprensión. La mediana de la puntuación total del cuestionario fue de nueve síntomas (RIQ 1-18); y los síntomas más frecuentes fueron: nervios o ansiedad (45%), hinchazón, dolor o gas en el estómago (40%), dificultad para dormir (39%) y cansancio o falta de energía (37%). La presencia de síntomas se relacionó con un peor resultado en el cuestionario MOS-HIV. Según la escala visual analógica, cuanto mayor era la puntuación en el cuestionario, menor era el nivel de tolerancia (R = -0,51; p < 0,0001) y mayor el número de días con síntomas (R = 0,51; p < 0,0001).
Conclusiones
La aplicación del cuestionario fue sencilla. Se constata un nivel de tolerancia alto; y una correlación consistente y significativa con el MOS-HIV, así como con la escala visual analógica.
PALABRAS CLAVE: Efectos adversos; Medicamentos antirretrovirales; Resultados comunicados por los pacientes; Validación del cuestionario; VIH
Introducción
El tratamiento antirretroviral (TAR) de gran actividad ha contribuido enormemente al control de la infección por el virus de la inmunodeficiencia humana (VIH), disminuyendo significativamente su morbimortalidad1. Para ello es necesario un elevado cumplimiento del tratamiento prescrito. La aparición de efectos adversos, tanto a corto como a largo plazo, ha resultado ser un factor determinante y claramente relacionado con el incumplimiento terapéutico, principalmente por estar fuertemente asociados a la calidad de vida del paciente2 3 4 5 6-7.
La mejor manera de evaluar los efectos adversos del paciente es realizando entrevistas directas, lo que se conoce como patient reported outcomes o resultados comunicados por el paciente. El cuestionario elaborado por Justice et al., “HIV Symptom Index”8, es el único cuestionario validado para la determinación y seguimiento de los síntomas referidos por los pacientes con TAR, y su uso está avalado por el AIDS Clinical Trials Group (ACTG) estadounidense, al que se refiere como “Symptoms distress module”8.
Debido a la falta de cuestionarios validados en población española para medir los síntomas percibidos por el paciente con infección por VIH, este equipo de investigación se propone validar el cuestionario de Índice de Síntomas de VIH (ISV) de Justice. Todo ello con el fin de que su aplicación en la práctica clínica habitual pueda servir para mejorar la detección y manejo de efectos adversos relacionados con el tratamiento9.
El cuestionario ISV consta de 20 preguntas sobre síntomas específicos de VIH, y considera tanto los síntomas referidos por el paciente como la intensidad del mismo.
El objetivo principal del estudio es evaluar el cuestionario ISV, en cuanto a su comprensión, aceptabilidad y claridad. Como objetivo secundario se plantea describir los síntomas referidos por el paciente y su nivel de tolerancia, así como su calidad de vida.
Métodos
Se llevó a cabo la fase piloto de un estudio observacional y multicéntrico no comparativo, denominado “Tolerómetro”, para la validación del cuestionario de 20 preguntas ISV del ACTG, al que se añadió una pregunta para indicar cualquier otro síntoma no recogido y dos más para valorar el grado de tolerancia global y el número de días con mala tolerancia, a través de una escala visual analógica (EVA).
Se incluyó a pacientes mayores de 18 años, diagnosticados de infección por VIH con TAR (mínimo un mes), que dieran su consentimiento informado por escrito; que acudían personalmente a las consultas de los Servicios de Farmacia, y capaces de entender y responder los cuestionarios.
Para el cálculo del tamaño muestral, se siguió el criterio extendido en la literatura y propuesto por Conelly para el estudio piloto, que debería ser al menos un 10% de la muestra estimada para el trabajo de campo; se estimó que para el estudio que se realizará posteriormente harán falta al menos 115 pacientes para la validación del cuestionario10.
Los pacientes se reclutaron de manera prospectiva y consecutiva de julio del 2013 a febrero del 2014, en cinco hospitales. Tras el reclutamiento se recogió información tanto directamente de los pacientes como de la historia clínica.
Inicialmente, para valorar la comprensión del cuestionario original, se realizó un pretest del cuestionario, al que contestaron 17 pacientes del centro del investigador principal. Posteriormente, se les realizó una entrevista cognitiva, para evaluar la comprensión de las preguntas y su relevancia según la opinión de las personas que lo contestaron.
Se recogieron variables sociodemográficas: sexo, edad, nivel de estudios, situación laboral; variables relacionadas con la enfermedad: tiempo desde el diagnóstico, grupo de riesgo, clasificación de los Centers for Disease Control and Prevention (CDC), presencia de hepatitis C, nivel de CD4 y carga viral. Así como variables relacionadas con TAR actual: no tratado previamente o pretratado, tiempo con TAR, tratamiento actual (fármacos, dosis, número de comprimidos y frecuencia de administración), duración del tratamiento actual, otros tratamientos concomitantes (especialmente el tratamiento de la hepatitis C).
Se realizó un análisis descriptivo de la muestra analizada, estimándose medias y desviaciones estándares (medianas y rangos intercuartílicos en caso de que no siguiera una distribución normal) para las variables continuas, así como frecuencias y porcentajes para las categóricas.
El ISV se calculó sumando el resultado de cada una de las 20 preguntas, cuyos valores oscilan entre 0 ante ausencia de síntoma y 4 si el síntoma molesta mucho, pudiéndose alcanzar un valor total entre 0 y 80. Se consideró “síntoma molesto” aquel síntoma valorado como “me molesta” o “me molesta mucho”. Al cuestionario ISV se le añadió una pregunta más para recoger cualquier síntoma no reflejado en el cuestionario, además se acompañó de dos escalas analógicas para detectar el nivel de tolerancia y la frecuencia. El cuestionario considera los síntomas ocurridos en las cuatro semanas previas.
Los pacientes también respondieron un cuestionario cualitativo de opinión para conocer el tiempo de aplicación y la dificultad y nivel de comprensión del cuestionario, así como sugerencias para mejorarlo.
Partiendo de la hipótesis de que cuanto mayor es el número de síntomas, peor será la calidad de vida del paciente, se aplicó el cuestionario de calidad de vida específico MOS-HIV. Dicho cuestionario es uno de los más utilizados para evaluar la calidad de vida relacionada con la salud en la infección por VIH, incluso se ha utilizado como modelo de referencia para desarrollar y validar otros cuestionarios11.
El cuestionario MOS-HIV consta de 35 preguntas sobre 11 dimensiones de salud, con una puntuación global que va de 0 a 100, donde una mayor puntuación indica un mejor estado de salud; además se obtienen dos índices, uno de salud mental y otro de salud física. Hace referencia a las últimas dos semanas, es de aplicación rápida y puede autoadministrarse. Ha demostrado validez, fiabilidad y sensibilidad al cambio12. Además, está traducido y validado en población española, donde se ha utilizado ampliamente.
Se evaluó la asociación de las puntuaciones obtenidas en la presencia/ ausencia de síntomas de cada ítem del cuestionario de síntomas específicos según el grado de sintomatología reportado por cada componente físico y mental del MOS-HIV. Para tal fin, se aplicó el test no paramétrico de Wilcoxon para muestras independientes. Se halló el coeficiente de correlación de Pearson para evaluar la asociación entre los valores de cada ítem y el índice total de síntomas específicos con el nivel de tolerancia y la frecuencia del EVA.
Se estimó la adherencia mediante la tasa de posesión de la medicación (TPM) obtenida de los registros de dispensación de farmacia en un periodo previo a la aplicación del cuestionario de mínimo tres meses, y preferiblemente en un intervalo de seis meses. Además, se aplicó el cuestionario de adherencia SMAQ (Simplified Medication Adherence Questionnaire) validado en población VIH española, que mide la adherencia en las cuatro semanas previas, mismo periodo que el ISV13.
Los cálculos estadísticos se realizaron con el paquete estadístico SAS System V9.2. Se asumió significación estadística cuando p < 0,05.
Este estudio se realizó de acuerdo con los principios de la Declaración de Helsinki, además de ser autorizado por el Comité Ético de Investigación Clínica del País Vasco y ser clasificado como estudio postautorización de tipo observacional de seguimiento prospectivo.
Resultados
En la fase piloto, el cuestionario ISV se aplicó en 75 pacientes en el Servicio de Farmacia de los cinco hospitales. La edad media de la población fue de 43,5 (desviación estándar (DE) 12,1) años y predominantemente masculina (73%), tal y como se recoge en la Tabla 1.
Tabla 1. Análisis descriptivo de variables sociodemográficas y clínicas
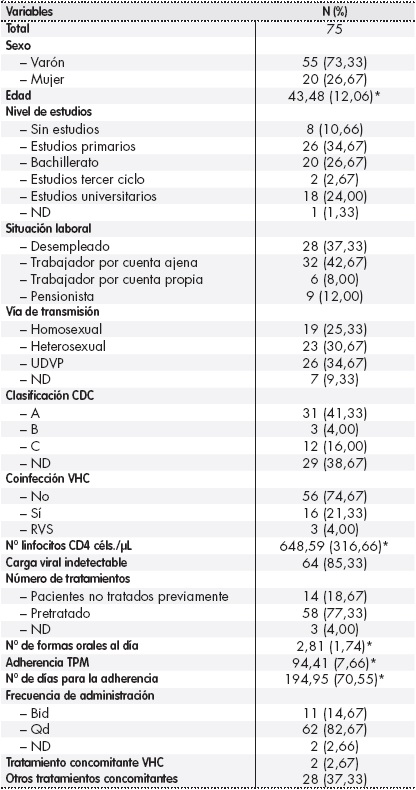
*Desviación estándar. Bid: dos veces al día; CDC: Centers for Disease Control and Prevention; ND: no disponible; Qd: una vez al día; RVS: respuesta viral sostenida; TPM: tasa de posesión de la medicación; UDVP: usuarios de drogas por vía parenteral; VHC: virus de la hepatitis C.
En relación con los datos clínicos, el 85% de los pacientes presentaban una carga viral indetectable y el nivel medio de CD4 fue de 648,6 céls./µL (DE 316,7). El 19% eran pacientes no tratados previamente, con un número medio de formas orales al día de 2,8 (DE 1,7), la mayoría administrados una vez al día (83%). El 37% de los pacientes tenían otros tratamientos concomitantes además del TAR, y el 2,7% de los pacientes estaban con tratamiento para la hepatitis C.
La mayoría tenían un tratamiento basado en dos análogos de nucleósidos inhibidores de la transcriptasa inversa más un no nucleósido (37), 19 pacientes asociado a un inhibidor de la proteasa potenciado (IPr), y 2 a un inhibidor de la integrasa (II). De los 17 restantes, ocho pacientes en monoterapia con un IPr, cuatro en biterapia basada en IPr y cinco con al menos tres fármacos de diferentes familias.
La mediana de la puntuación total del ISV fue de 9 (RIQ 1-18) en una escala de 0 a 80. El 19% de los pacientes no indicaron ningún síntoma y el 57% de los pacientes no tuvo ningún síntoma molesto. Mientras que la mediana del número de síntomas referido por paciente fue de 5 (RIQ 1-10), la mediana del número de síntomas molestos por paciente fue de 0 (RIQ 0-3).
El síntoma más frecuente detectado en el cuestionario ISV fue nervios o ansiedad (45%), seguido de hinchazón, dolor o gas en el estómago (40%), dificultad para dormir (39%) y cansancio o falta de energía (37%). Cuando sólo se consideraban los síntomas molestos, los más frecuentes fueron la ansiedad e hinchazón de estómago (20%) y la dificultad para dormir (17%). En la Tabla 2se recoge cada síntoma con su frecuencia de notificación.
Tabla 2. Análisis descriptivos del cuestionario de Índice de Síntomas de VIH (ISV)

*Resultados como mediana (RIQ). EVA: escala visual analógica; ISV: Índice de Síntomas de VIH.
Fueron cuatro los pacientes que indicaron síntomas que no se recogían en el cuestionario original con su grado de molestia: artritis-artrosis (me molesta mucho), sueños intensos (me molesta un poco), irritabilidad (me molesta un poco), y calor y sudores (no me molesta).
Según los resultados del cuestionario cualitativo de opinión, el tiempo medio en completar el cuestionario fue de 11 minutos (rango de 1 a 33 minutos). Un total de 58 pacientes (77%) lo completaron solos. La mayoría de los pacientes consideraron el cuestionario como fácil y que se entendía bien (94,7%), mientras que a tres les resultó difícil. El 89% de los pacientes consideraron el cuestionario útil.
Solamente tres pacientes respondieron que algunas preguntas no las relacionaban con el tratamiento, y otras les resultaban muy parecidas entre sí; y no indicaban ningún síntoma concreto que no entendieran bien, ni hacían ninguna sugerencia para mejorar las preguntas.
Hubo 4 pacientes que echaron en falta alguna cuestión o síntoma importante, entre ellos las molestias gástricas y los golpes de calor.
Se recogieron las sugerencias aportadas por 12 pacientes. A cinco les resultó largo y con preguntas repetidas, aunque hay quien lo consideró corto. Algún paciente sugirió repetir el cuestionario de forma periódica; y otro propuso la opción de apuntar hasta las pequeñas cosas.
La mediana del nivel de tolerancia según la EVA fue de 9 (RIQ 8-10) y el número de días con mala tolerancia fue de 0 (RIQ 0-2).
La mediana de la EVA nivel de tolerancia fue de 10 (RIQ 9-10) en el grupo de pacientes con ausencia de síntomas frente a 9 (RIQ 7-10) entre los pacientes que refirieron algún síntoma, siendo la diferencia significativa (p = 0,008). Este dato se repite en la EVA frecuencia de tolerancia (p = 0,02), tal y como se aprecia en la Tabla 3.
Tabla 3. Asociación entre la tolerancia y frecuencia con la EVA y los síntomas específicos. Resultados como Mediana (Rango intercuartil=p25-p75)

ISV: índice de síntomas de VIH; EVA: escala analógica visual.
Finalmente, el análisis de la asociación entre el ISV y el EVA demostró que cuanto mayor era la puntuación en el ISV, menor era el nivel de tolerancia según EVA (R = −0,51; p < 0,0001) y mayor el número de días afectados por los síntomas según EVA (R = 0,51; p < 0,0001).
La puntuación total del cuestionario de calidad de vida MOS-HIV fue de 45,71 (DE 2,37) en el componente físico en el grupo de pacientes con ausencia de síntomas, frente a 42,01 (DE 5,97) entre los pacientes que refirieron algún síntoma, siendo la diferencia significativa (p = 0,04). En cuanto al componente mental, fue de 57,08 (DE 4,14) en ausencia de síntomas y 51,23 (DE 9,21) en presencia, también significativa (p = 0,02); confirmándose que la calidad de vida fue significativamente inferior en pacientes con presencia de síntomas, más aún cuando se consideraban sólo los síntomas molestos.
La puntuación en el cuestionario MOS-HIV se relacionó con la puntuación del ISV (r = 0,74; p < 0,0001) en la escala de salud física y en la de salud mental (r = 0,67; p < 0,0001), en ambos casos fue significativa. Cuanto mayor fue el número de síntomas referidos, menor fue la calidad de vida en el componente físico y mental en todas las áreas del cuestionario, oscilando el coeficiente de correlación entre 0,34 y 0,74.
La presencia de síntomas en el ISV se relacionó de forma significativa con un peor resultado tanto en el componente físico como mental del MOS-HIV, tal y como se aprecia en la Tabla 4.
Tabla 4. Asociación entre el componente físico y mental del MOS-HIV y los síntomas específicos

Resultados como media (desviación estándar).
La adherencia media, o TPM, en el periodo anterior a la aplicación del cuestionario (mediana de intervalo de cálculo de adherencia: 180 días, RIQ 150-243) fue de 94,4% (intervalo de confianza 95%: 92,7-96,2) medida por los registros de dispensación de farmacia.
Según el cuestionario SMAQ, el 40% de los pacientes se clasificaron como no adherentes (30/75). Considerando la pregunta 5 semicuantitativa (olvidos en la última semana), el 92% se consideraba adherente.
Discusión
El cuestionario ISV elaborado por Justice et al., es el único cuestionario que ha sido validado para la determinación y seguimiento de los síntomas referidos por los pacientes con TAR, y por ello fue elegido para esta fase piloto y una posterior validación en población española14.
En nuestro estudio se observó que el cuestionario era de fácil aplicación y de cumplimentación rápida, de aproximadamente cinco minutos por parte del paciente. Aunque hubo pacientes que echaron en falta alguna cuestión o síntoma importante, por lo que se consideró necesario añadir la pregunta de otros síntomas para que el paciente los reflejara con sus palabras, aunque luego se pudieran reclasificar entre los ya existentes o pudiera servir para detallar más las preguntas.
Además, presentó una buena asociación con las dimensiones física y mental de la escala MOS-HIV, así como con el grado de tolerancia según la EVA. Se constató la utilidad de incluir una pregunta de otros síntomas para que el paciente pudiera notificar aquel síntoma no reflejado en el cuestionario.
La mediana de síntomas referidos por los pacientes en nuestro estudio piloto fue inferior a la indicada en el estudio original de Justice, 5 (RIQ 1-10) frente a 15 (RIQ 8-19), probablemente debido a la diferencia temporal donde los tratamientos eran peor tolerados. Los síntomas más frecuentes en el estudio de Justice son fatiga (81%), diarrea (78%), tristeza (76%), dificultad para dormir (75%) y ansiedad (74%), no tan distintos de los referidos por nuestros pacientes, aunque de nuevo en un porcentaje inferior. El estudio de Justice también demuestra una buena asociación con las dimensiones física y mental de la escala MOS-HIV, al igual que ocurría en nuestro estudio.
En otros estudios más recientes donde se utiliza el mismo cuestionario, el número de síntomas es de 8,2, más parecido a nuestro estudio, y los síntomas más frecuentemente indicados por los pacientes son fatiga, tristeza, nerviosismo, insomnio, mialgias y cambios en la apariencia física15 16-17.
En el estudio de Braithwaite, de 1.864 pacientes de la cohorte de veteranos VACS, el 66% percibe efectos adversos relacionados con el TAR, aunque el 39% tiene dudas sobre si realmente están asociadas al medicamento18. Entre nuestros pacientes, el 81,3% indicó algún síntoma, aunque de estos sólo el 57% se identificaron como molestos.
Existen otras escalas como la Memorial Symptom Assesment Scale‑Short Form (MSAS-SF), que mide la frecuencia, gravedad y molestia asociadas a 32 síntomas; se ha utilizado en distintas patologías, y especialmente en el cáncer19. En un estudio de Wakeham K et al., se aplicó el MSAS-SF en 212 pacientes VIH con una media de 14 síntomas, siendo los más frecuentes dolor, pérdida de peso, prurito, cansancio, entumecimiento, tos, cambio en la piel, preocupación y falta de apetito20. Síntomas que coinciden con los recogidos entre los pacientes de nuestro estudio piloto. Aun así, el MSAS-SF es un cuestionario más extenso y más detallado y con menor experiencia en VIH.
Una de las limitaciones más importantes de este estudio tiene que ver con la confusión existente entre los síntomas de la enfermedad y los producidos por los medicamentos. El cuestionario ISV recoge los signos y síntomas que el paciente manifiesta, pero no necesariamente significa que sean causados por la medicación antirretroviral. Además, los síntomas también pueden verse influidos por la propia enfermedad o comorbilidades asociadas que presenta el paciente.
Otra de las limitaciones del estudio es que, al igual que ocurre con cualquier estudio piloto, no podemos llegar a conclusiones definitivas sobre las propiedades psicométricas del cuestionario evaluado. Por ello, debemos esperar a los resultados del trabajo de campo para poder establecer la validez y fiabilidad de este instrumento.
Respecto a la adherencia media, se observaron diferencias entre la calculada mediante TPM y el SMAQ, aunque si se tiene en cuenta la pregunta 5 semicuantitativa del SMAQ (olvidos en la última semana), el resultado se asemejó más a la TPM.
Finalmente, los resultados obtenidos están ligados al tipo de tratamiento que se evalúa en esta población; actualmente es mayor la utilización de inhibidores de la integrasa y la biterapia21, por lo que una vez validado propiamente el cuestionario, las futuras líneas de investigación deberían orientarse a aplicarlo en los tratamientos actuales.
Se trata de un cuestionario de aplicación fácil y rápida, con una buena valoración y nivel de comprensión por parte de los pacientes; y que, además, presentó una correlación consistente y significativa con las dimensiones físicas y mentales de la escala MOS-HIV, así como con la EVA de tolerancia.
Los resultados de nuestro estudio sugieren que cuanto mayor es la puntuación del cuestionario de síntomas ISV, peor es la tolerancia según la EVA, mayor la frecuencia de días con mala tolerancia según la EVA y peor la puntuación del MOS-HIV en todas sus dimensiones. Aunque teniendo en cuenta que se trata de un estudio piloto, consideramos necesario esperar a los resultados del estudio definitivo.
Agradecimentos
A Nerea González Hernández, de la Unidad de Investigación del Hospital de Galdakao, por su asesoramiento en el diseño, desarrollo y validación de cuestionarios.
REFERENCIAS
GESIDA. Documento de consenso de GESIDA/Plan Nacional sobre el Sida respecto al tratamiento antirretroviral en adultos con infección por el virus de la inmunodeficiencia humana (Actualización enero 2012) 2012 (consultado 25/02/2019). Disponible en: http://gesida-seimc.org/wp-content/uploads/2017/02/gesidadcyrc2012-Documentoconsenso-TAR-adulto-verimprimir.pdf [ Links ]
Escobar I, Knobel H, Polo R, Ortega L, Martín-Conde MT, Casado JL, et al. Recomendaciones GESIDA/ SEFH/ PNS para mejorar la adherencia al tratamiento antirretroviral en el año 2004. Farm Hosp 2004;28:6-18. [ Links ]
Martín MT, Cacho del E, López E, Codina C, Tuset M, Lazzari de E, et al. Reacciones adversas del tratamiento antirretroviral: relación entre los síntomas percibidos y el cumplimiento terapéutico. Med Clin (Barc). 2007;129:127-33. DOI: 10.1157/13107497 [ Links ]
Ammassari A, Murri R, Pezzotti P, Trotta MP, Ravasio L, De Longis P, et al. Self-reported symptoms and medication side effects influence adherence to highly active antiretroviral therapy in persons with HIV infection. J Acquir Immune Defic Syndr. 2001;28:445-9. DOI: 10.1097/00042560-200112150-00006 [ Links ]
Duran S, Spire B, Raffi F, Walter V, Bouhour D, Journout V, et al. Self-reported symptoms after initiation of a protease inhibitor in HIV-infected patients and their impact on adherence to HAART. HIV Clin Trials. 2001;2:38-45. DOI:10.1310/R8M7-EQ0M-CNPW-39FC [ Links ]
Duran S, Savès M, Spire B, Cailleton V, Sobel A, Carrieri P, et al. Failure to maintain long-term adherence to highly active antiretroviral therapy: the role of lipodistrophy. AIDS. 2001;15:2441-4. DOI: 10.1097/00002030-200112070-00012 [ Links ]
Cooper V, Gellaitry G, Hankins M, Fisher M, Horne R. The influence of symptom experiences and attributions on adherence to highly active antiretroviral therapy (HAART): a six-month prospective, follow-up study. AIDS Care. 2009;21:520-8. DOI: 10.1080/09540120802301824 [ Links ]
Justice AC, Holmes W, Gifford AL, Rabeneck L, Zackin R, Sinclair G, et al. Development and validation of a self- completed HIV symptom index. J Clin Epidemiol. 2001;54(Supl 1):S77-90. DOI: https://doi.org/10.1016/S0895-4356(01)00449-8 [ Links ]
Morillo Verdugo R, Fernández Lisón LC, Huertas Fernández MJ, Martín Conde MT, Roldán Morales JC, Ruano Camps R, et al. Papel del farmacéutico de hospital en la prevención, identificación y manejo de los efectos adversos asociados al tratamiento antirretroviral. Farm Hosp. 2010;34:237-50. DOI:10.1016/j.farma.2010.01.012 [ Links ]
Connelly LM. Pilot studies. Medsurg Nurs. 2008;17:411-2. [ Links ]
Clayson DJ, Wild DJ, Quarterman P, Duprat-Lomon I, Kubin M, Coons SJ. A comparative review of health-related quality-of-life measures for use in HIV/AIDS clinical trials. Pharmacoeconomics. 2006;24:751-65. DOI:10.2165/00019053-200624080-00003 [ Links ]
Badia X, Podzamczer D, López-Lavid C, García M, Grupo Español de Validación de los cuestionarios MOS-HIV y MQOL-HIV. Medicina basada en la evidencia y la validación de cuestionarios de calidad de vida: la versión española del cuestionario MOS-HIV para la evaluación de la calidad de vida en pacientes infectados por VIH. Enf Infecc Microbiol Clin. 1999;17(Supl 2):103-13. [ Links ]
Knobel H, Alonso J, Casado JL, Collazos J, González J, Ruiz I, et al. Validation of a simplified medication adherence questionnaire in a large cohort of HIV-infected patients: the GEEMA Study. AIDS. 2002;16:605-13. DOI: 10.1097/00002030-200203080-00012 [ Links ]
Justice AC, Rabeneck L, Hays RD, Wu AD, Bozzette SA. Sensitivity, specificity, reliability, and clinical validity of provider reported symptoms: a comparison with self-report symptoms. Outcomes Committee of the AIDS Clinical Trials Group. J Acquir Immune Defic Syndr. 1999;21:126-33. [ Links ]
Skiest DJ, Krambrink A, Su Z, Robertson KR, Margolis DM; A5170 Study Team. Improved measures of Qualify of life, lipid profile and lipoatrophy after treatment interruption in HIV-infected patients with immune preservation: results of ACTG 5170. J Acquir Immune Defic Syndr. 2008;49:377-83. DOI:10.1097/QAI.0b013e31818cde21 [ Links ]
Dejesus E, Young B, Morales-Ramírez JO, Sloan L, Ward DJ, Flaherty JF, et al. Simplification of antiretroviral therapy to a single-tablet regimen consisting of Efavirenz, Emtricitabine, and Tenofovir versus unmodified antiretroviral therapy in virologically suppressed HIV-1 infected patients. Acquir Immune Defic Syndr. 2009;51:163-74. DOI:10.1097/QAI.0b013e3181a572cf [ Links ]
Spire B, Arnould B, Barbier F, Durant J, Gilquin J, Landman R, et al. Simplification and first validation of a short battery of patient questionnaires for clinical management of HIV-infected patients: the HIV-SQUAD (Symptom Quality of life Adherence) questionnaire. HIV Clin Trials. 2009;10:215-32. DOI: 10.1310/hct1004-215 [ Links ]
Braithwaite RS, Goulet J, Kudel I, Tsevat J, Justice AC. Quantifying the decrement in utility from perceived side effects of combination antiretroviral therapies in patients with HIV. Value Health. 2008;11:975-9. DOI: 10.1111/j.1524-4733.2007.00315.x [ Links ]
Chang VT, Hwang SS, Feuerman M, Kasimis B . The Memorial Symptom Assessment Scale Short Form (MSAS-SF). Validity and reliability. Cancer. 2000;89:1162-71. DOI: 10.1002/1097-0142(20000901)89:53.0.CO;2-Y [ Links ]
Wakeham K, Harding R, Bamukama-Namakoola D, Levin J, Kissa J, Parkes-Ratanshi R, et al. Symptom burden in HIV-infected adults at time of HIV diagnosis in rural Uganda. J Palliat Med. 2010;13:375-80. DOI: 10.1089/jpm.2009.0259 [ Links ]
GESIDA. Documento de consenso de GESIDA/Plan Nacional sobre el Sida respecto al tratamiento antirretroviral en adultos con infección por el virus de la inmunodeficiencia humana. 2018 (consultado 25/02/19). Disponible en: http://gesida-seimc.org/wp-content/uploads/2018/01/gesida_TAR_adultos_v3-1.pdf [ Links ]
Cómo citar este trabajo:Ibarra-Barrueta O, Mora-Atorrasagasti O, Aguirre U, Legarreta MJ, Illaro-Uranga A, Morillo-Verdugo R. Estudio piloto para desarrollar y validar un cuestionario basado en el índice de síntomas de VIH. Farm Hosp. 2019;43(3):87-93.
Presentación en CongresosLos resultados fueron presentados parcialmente en el 59 Congreso de la SEFH, celebrado en Valladolid del 30 de septiembre al 3 de octubre de 2014. Ibarra Barrueta O, Mora Atorrasagasti O, Illaro Uranga A, Morillo Verdugo R, Martín Conde M, Serrano López-De-Las-Hazas J. Estudio piloto para el desarrollo de una herramienta de valoración de la tolerancia al tratamiento antirretroviral. 59 Congreso de la SEFH, Valladolid 30 septiembre-3 octubre 2014.
Aportación a la literatura científica:Debido a la falta de cuestionarios validados en población española para medir los síntomas percibidos por el paciente con infección VIH, se propone desarrollar y validar un cuestionario basado en el Índice de Síntomas de VIH. Su aplicación en la práctica clínica habitual puede servir para mejorar la detección y manejo de efectos adversos relacionados con el tratamiento.
Recibido: 18 de Julio de 2018; Aprobado: 11 de Diciembre de 2018











 texto en
texto en 


