Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Farmacia Hospitalaria
versão On-line ISSN 2171-8695versão impressa ISSN 1130-6343
Farm Hosp. vol.44 no.4 Toledo Jul./Ago. 2020 Epub 28-Jun-2021
https://dx.doi.org/10.7399/fh.11441
DOCUMENTOS DE CONSENSO
Documento de consenso para mejorar la adherencia a la farmacoterapia en pacientes con infección por el virus de la inmunodeficiencia humana en tratamiento antirretroviral
1Specialist Pharmacist. Hospital Universitario de Valme. Southern Healthcare Area, Sevilla. Spain.
2Clinical and Research Division. Secretariat of the Spanish AIDS Plan, Ministerio de Sanidad, Madrid. Spain.
3Department of Infectious Diseases, Hospital del Mar, Barcelona. Spain.
Introducción
En el año 19991,2, el Plan Nacional sobre el Sida (PNS), la Sociedad Española de Farmacia Hospitalaria (SEFH) y el Grupo de Estudio del SIDA (GeSIDA) publicaron por primera vez una serie de recomendaciones para mejorar la adherencia, que fueron actualizadas en 2004 y 20083,4. La adherencia al tratamiento sigue siendo foco de atención de profesionales sanitarios e investigadores, por lo que se ha considerado oportuno efectuar una revisión y actualización de dicho documento de consenso, basada en las actuales recomendaciones respecto al tratamiento antirretroviral (TAR)5.
La adherencia inadecuada, no solo al TAR en el adulto, sino también a otros fármacos prescritos en un paciente con infección por el virus de la inmunodeficiencia humana (VIH), sigue siendo la principal causa de fracaso terapéutico. Existen diversos factores asociados a la mala adherencia y otros que facilitan la misma, de ahí que antes de iniciar el TAR conviene preparar al paciente, identificar las situaciones que puedan dificultar la adherencia e intentar corregirlas. Asimismo, se deberá evaluar periódicamente la adherencia durante el seguimiento del TAR y del resto de los fármacos prescritos.
Presentamos un resumen del documento que actualiza las recomendaciones publicadas en 2008, tras una revisión de la literatura científica, que ha permitido emitir unas recomendaciones consensuadas para la mejora de la adherencia. Se hace hincapié en aquellos aspectos más novedosos o no incluidos en recomendaciones anteriores. El objetivo es ayudar a todos los profesionales sanitarios dedicados al control clínico y terapéutico de los pacientes con el VIH a mejorar la adherencia a toda la farmacoterapia prescrita.
El PNS, en colaboración con las diferentes sociedades científicas implicadas, seguirá actualizando este documento periódicamente en función de la evolución de los conocimientos sobre la adherencia al tratamiento. No obstante, se recuerda que, dado que éstos cambian muy rápidamente, es conveniente que los lectores consulten también otras fuentes de información.
Métodos
El panel redactor estuvo integrado por clínicos expertos en la infección por el VIH y el TAR designados por el PNS y las Juntas Directivas de GeSIDA y de la SEFH. Estos expertos se distribuyeron en grupo redactor y revisor, que se responsabilizaron de actualizar el documento. Tres miembros del Panel (representando al PNS, GeSIDA y SEFH) han actuado, adicionalmente, como coordinadores, cuyo cometido ha sido revisar el documento. El coordinador del PNS se ha encargado de ordenar todas las secciones del documento, redacción y edición final del mismo. Los redactores revisaron los datos más relevantes de las publicaciones científicas (PubMed y Embase; español e inglés), desde la ultima actualización del documento, en 2008, hasta el 30 de noviembre de 2019. El texto elaborado por los redactores se sometió a la consideración de los revisores, incorporándose las aportaciones aceptadas por consenso. Una vez ordenadas todas las secciones, el documento se ha discutido y consensuado en una reunión por audioconferencia del panel. Tras la incorporación de las modificaciones aprobadas en dicha reunión, el documento se expuso durante 15 días en las páginas web del PNS, GeSIDA y SEFH para que cualquier interesado pudiera hacer sugerencias, que tras su estudio y debate se integraban o no en el documento final. Cada una de las recomendaciones se basaron en la evidencia científica y la opinión de expertos, clasificándose con una letra que indica su necesidad de implantación (A (debe ofrecerse siempre), B (en general debe ofrecerse) o C (debe ofrecerse opcionalmente)) y un número que expresa las pruebas que sustentan la recomendación (I (resultados obtenidos a partir de uno o más ensayos clínicos aleatorizados o un metaanálisis), II (uno o más ensayos no aleatorizados o datos observacionales de cohortes) o III (basado en la opinión de expertos)).
Resultados
Aunque no existe una definición universalmente aceptada, dado el nuevo perfil y enfoque de trabajo con el paciente con infección por el VIH, se podría definir adherencia como: “la capacidad del paciente de implicarse correctamente en la elección, inicio y control de toda la farmacoterapia que tenga prescrita, permitiendo así alcanzar, en la medida de lo posible, los objetivos farmacoterapéuticos planteados en cada momento, acorde a su situación clínica y expectativas de salud”.
Esta definición que pivota sobre el TAR como elemento fundamental de la terapéutica en el paciente con infección por el VIH pone de manifiesto la cada vez más frecuente e importante toma de medicación concomitante prescrita6.
La adherencia incorrecta no se refiere solamente a las dosis de medicamentos no tomadas, sino que intervienen otros factores que se comentan a continuación7. La adherencia a corto y medio-largo plazo es el resultado de un proceso que se desarrolla a través de diferentes etapas: la aceptación del diagnóstico, la percepción de la necesidad de realizar el tratamiento correctamente, la motivación para hacerlo, la disposición y entrenamiento de habilidades para realizarlo, la capacidad de superar las barreras o dificultades que aparezcan y el mantenimiento de los logros alcanzados con el paso del tiempo8.
Anteriormente, para hablar de no adherencia se había clasificado la misma en intencionada y no intencionada, para hacer referencia a la voluntariedad del paciente en la toma incorrecta de los fármacos. En la actualidad, la no adherencia puede dividirse en primaria (el tiempo que pasa desde que se realiza la prescripción hasta que el paciente dispone del fármaco prescrito) y secundaria (mide el grado de utilización del medicamento por el paciente a lo largo del tiempo, de acuerdo con las recomendaciones realizadas). Es importante tener en cuenta que la falta de adherencia puede ocurrir en cualquiera de estos ámbitos o en ambos a la vez9. Por tanto, a la hora de llevar a cabo evaluaciones para mejorar la adherencia al tratamiento se debe incluir no sólo la terapia antirretroviral, sino también todos los fármacos prescritos al paciente.
Este documento consta de los siguientes apartados:
Factores que influyen en la adherencia.
Métodos para valorar la adherencia.
Estrategias del equipo interdisciplinar para mejorar la adherencia.
Procedimiento para la prescripción, dispensación y seguimiento del tratamiento.
Factores que influyen en la adherencia
Existen muchas limitaciones que hacen difícil generalizar los resultados de los diferentes estudios sobre los factores que influyen en la adherencia, el método utilizado para medirla, los aspectos evaluados, la población estudiada y el diseño del estudio. Los factores pueden clasificarse en: relacionados con el individuo, con el tratamiento y con el equipo asistencial y sistema sanitario (Tabla 1). En la Tabla 2 se resumen las recomendaciones y grado de implantación de medidas para afrontar los factores relacionados con la adherencia al tratamiento en el paciente adulto y adolescente.
Tabla 1. Factores relacionados con la adherencia incorrecta al tratamiento antirretroviral
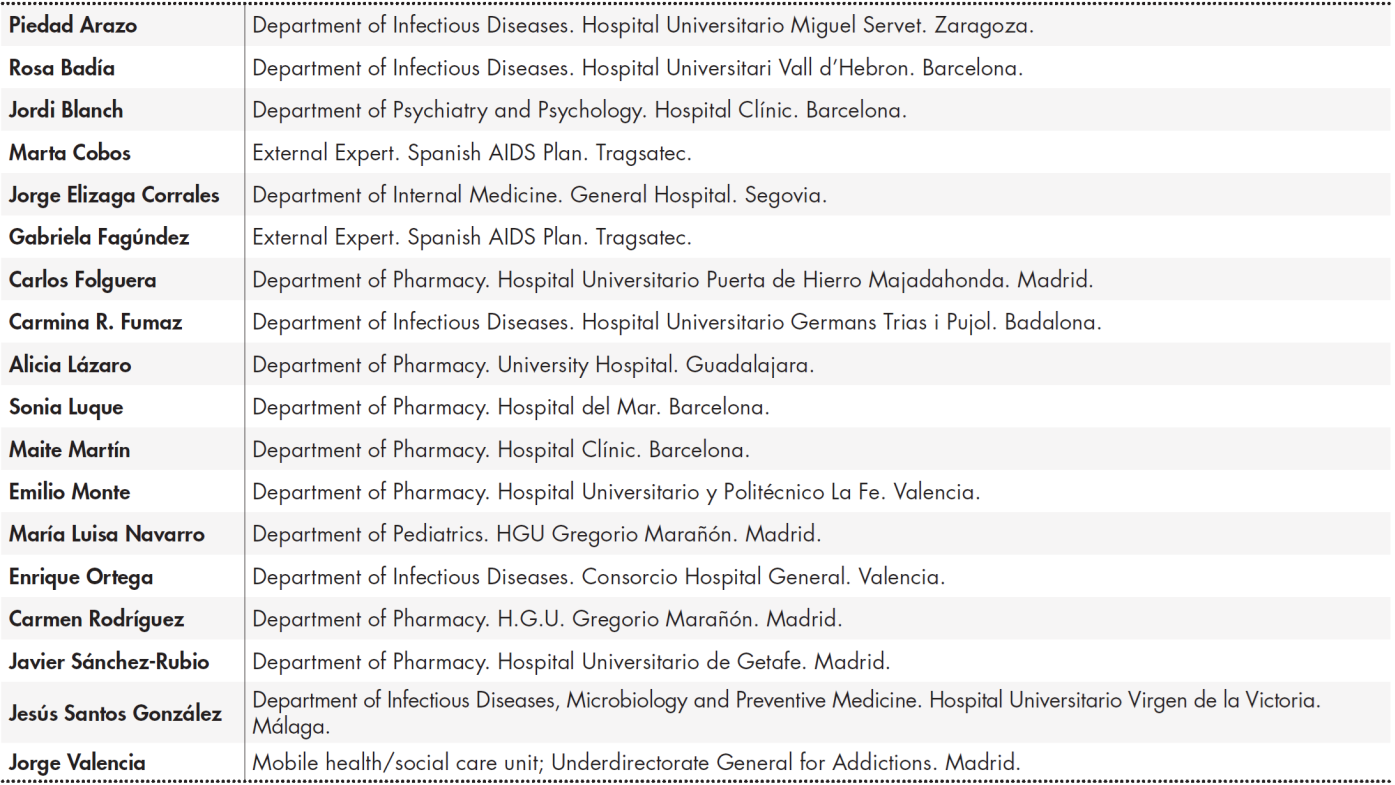
* Características que de forma más contundente se han relacionado con dificultad para la adherencia.
** Además del desconocimiento del idioma, se consideran las barreras de acceso al sistema sanitario (cultura sanitaria diferente, desconocimiento del sistema).
Tabla 2. Recomendaciones y grado de implantación de medidas para afrontar los diferentes factores relacionados con la adherencia al tratamiento en el paciente adulto y adolescente
TAR: tratamiento antirretroviral.
Es importante indicar que el paciente adolescente con infección por el VIH tiene más dificultades para la adherencia al tratamiento y al sistema de salud que el adulto debido a una menor autonomía y privacidad10. Los adolescentes tienen comprometida la adherencia debido a que conceden gran importancia al presente inmediato y a su aceptación de su grupo de iguales, sin priorizar ni valorar el riesgo que conlleva para su salud la falta de adherencia2. Además, la infección supone un estigma en la sociedad, lo cual, a su vez, puede influir en la toma del TAR. Se debe priorizar un tratamiento que permita realizar una actividad igual que sus pares, intentar simplificarlo a una toma diaria y menor número de comprimidos que los que tomaba en su infancia, coformulaciones y sin efectos secundarios11,12.
El adolescente de infección perinatal se le hace difícil tomar la medica-
ción. Estos han mostrado riesgos de factores psicosociales y salud conductual, lo cual se ha asociado a un peor cumplimiento13-15.
Se pueden usar terapias directamente observadas, ayuda psicológica, apoyo de programa de pares, seguimiento de farmacia, herramientas de la tecnología de la información y la comunicación (TIC) consistentes en alarmas en los dispositivos electrónicos, mensajes de texto, programas gratuitos para aplicaciones móviles16,17.
Métodos para valorar la adherencia
El método ideal debería ser altamente sensible y específico, permitir una medida cuantitativa y continua, fiable, reproducible, capaz de detectar cambios de adherencia en el tiempo y aplicable en diferentes situaciones, rápido y económico. Sin embargo, el método ideal no existe, por lo que debemos conocer las fortalezas y limitaciones de cada uno de los métodos que aplicamos.
Los métodos para valorar la adherencia pueden clasificarse en directos e indirectos.
Directos
Concentraciones plasmáticas
Aunque se considera el método más objetivo, presenta muchas e importantes limitaciones. De acuerdo con los estudios publicados, hay controversias con este método. A pesar de observarse niveles de fármaco inferiores en los pacientes no adherentes y una buena correlación entre las concentraciones y los cuestionarios, se han encontrado niveles plasmáticos considerados como adecuados en un porcentaje importante de pacientes con una baja adherencia autorreferida18,19. En otros estudios, considerando exclusivamente este método como criterio de adherencia, no se han encontrado diferencias significativas respecto al control virológico20-22. Algunos, sin embargo, demuestran que el nivel de fármacos es una variable que predice de forma independiente la respuesta virológica, mientras que otros han encontrado una aceptable sensibilidad, pero baja especificidad para identificar la respuesta virológica23-25.
Es importante también considerar que existen muchas variables intra e interindividuales que condicionan el comportamiento cinético de los fármacos antirretrovirales. El establecimiento de un umbral estándar para clasificar a los pacientes como adherentes o no adherentes resulta cuestionable. Serían necesarias varias determinaciones en cada paciente, estudios farmacocinéticos poblacionales y un conocimiento preciso de aquellos factores que afectan al perfil cinético de cada fármaco o, al menos, a los grupos farmacológicos a los que pertenezcan. Si bien se han conseguido avances en estos campos, aún no es posible disponer de datos precisos fuera del ámbito de la investigación26.
Por último, cabe destacar que este método requiere unas técnicas analíticas caras y complejas, por lo que no es aplicable en la práctica diaria. Se han ensayado otros métodos de determinación analítica para estimar adherencia y/o exposición acumulativa de medicamentos en muestras de sangre: gota de sangre seca y/o cabello con resultados variables, pero
con utilidad potencial en zonas cuyos recursos son limitados.
Evolución clínica y datos analíticos
La evolución clínica y el resultado virológico e inmunológico no deberían considerarse métodos de estimación de la adherencia, sino más bien la consecuencia de ésta.
La carga viral indetectable no es un indicador perfecto de alta adherencia al TAR y además no informa de los patrones de adherencia. En pacientes con supresión virológica y una adherencia subóptima se han observado niveles más altos de marcadores de inflamación y coagulopatía27. Por último, el seguimiento inmunovirológico como medida de estimación de adherencia no aplica al uso de Profilaxis Pre-exposición (PrEP).
Indirectos
En la Tabla 3 se incluyen cada uno de los métodos indirectos con sus ventajas y limitaciones.
Tabla 3. Recomendaciones, grado de necesidad de implantación, ventajas y limitaciones de los métodos de medición de la adherencia en el paciente VIH

Modelos predictivos
Numerosos estudios han intentado explorar las diferentes variables explicativas de la falta de adherencia al tratamiento en personas con infección por el VIH, aunque no muchos de ellos con el objetivo de desarrollar modelos predictivos validados que permitan diseñar estrategias dirigidas28-30. Además, hasta ahora, la capacidad predictiva de estos modelos en general no ha sido óptima y existe una significativa heterogeneidad entre ellos, haciendo difícil su aplicación generalizada. Se han desarrollado en poblaciones concretas con tamaños muestrales pequeños, diferencias en la definición y en el umbral de adherencia, los tratamientos utilizados en el momento, la forma de medir la adherencia y los tipos de variables incluidas.
Los métodos estadísticos clásicos no resultan adecuados para el análisis de grandes volúmenes de datos (big data), por lo que se ha desarrollado el denominado análisis predictivo, incluyendo técnicas como el aprendizaje automático (machine learning) y la minería de datos (data mining), que permiten analizar un elevado número de variables en amplios conjuntos de pacientes y detectar asociaciones inesperadas31. La aplicación de este nuevo enfoque en el entorno de la adherencia al tratamiento de la infección por el VIH en el futuro podrá contribuir al desarrollo de modelos de predicción útiles. En nuestro entorno, se ha elaborado una escala predictiva de adherencia, muy sencilla de utilizar y con alta sensibilidad y especificidad, destacando su alto valor predictivo negativo (http://artshiv-calculator.humimar.org/es), aunque para su uso generalizado debería ser evaluada en diferentes escenarios clínicos32.
Estrategias del equipo interdisciplinar para mejorar la adherencia
Se consideran las siguientes:
Apoyo y ayuda.
Intervención, educativas, motivacionales y conductuales.
Pauta terapéutica.
TIC, Tecnologías de aprendizaje y conocimiento (TAC) y 2.0.
Específicas para la PrEP.
Estrategias de apoyo y ayuda
Papel del médico especialista
Prescripción del TAR y medicación concomitante
Es importante valorar de forma individual el momento de inicio del TAR y los fármacos que deben formar parte del régimen inicial, sopesando las ventajas e inconvenientes de cada una de las opciones. En su elección hay que considerar las comorbilidades que presenta el paciente, los fármacos concomitantes, así como el consumo de drogas de uso recreativo valorando de forma exhaustiva la posibilidad de interacciones. Se debe seleccionar el esquema terapéutico que mejor se adapte al estilo de vida y comorbilidades, valorando el riesgo de mala adherencia33. Tomada la decisión de iniciar el TAR, la prescripción pasa por tres fases diferenciadas: informativa, consenso y compromiso y mantenimiento y soporte.
Seguimiento del TAR y medicación concomitante
El envejecimiento de la población con infección por el VIH ha aumentado la aparición de comorbilidades no relacionadas específicamente con la infección como la enfermedad cardiovascular, diabetes mellitus, insuficiencia renal, osteopenia y osteoporosis o trastornos psiquiátricos34. Como consecuencia, ha aumentado la prescripción crónica de fármacos no antirretrovirales y la polifarmacia. A pesar de que la polifarmacia puede estar justificada, su uso se asocia con un potencial riesgo de interacciones medicamentosas, acontecimientos adversos, falta de adherencia al tratamiento, un mayor riesgo de hospitalizaciones, caídas y muerte. Actualmente, el abordaje del paciente VIH debe ir más allá del tratamiento de la infección y manejo de su TAR. Es fundamental realizar una revisión completa de toda la medicación y la complejidad del tratamiento, monitorizar la adherencia de todos los medicamentos que toma el paciente de forma periódica y fomentar hábitos de vida saludable.
Papel del farmacéutico especialista
Uno de los temas prioritarios en las consultas de atención farmacéutica (AF) es el abordaje de la adherencia. En los últimos años se han desarrollado el “Mapa Estratégico de Atención al paciente Externo” y el modelo de “Atención Farmacéutica CMO” (capacidad-motivación-oportunidad), que han reforzado la importancia en la orientación farmacéutica hacia las necesidades individuales de cada paciente35,36.
El farmacéutico especialista es clave en la valoración sistemática y en la mejora de la adherencia tanto al TAR como al resto de medicación. La AF especializada en el momento de la dispensación del tratamiento es una intervención esencial para monitorizar la adherencia y desarrollar intervenciones educativas, motivacionales y conductuales que permitan reforzarla37. En la consulta, el farmacéutico especialista ofrece un clima de confidencialidad y confianza con el paciente que facilita la comunicación, así como la identificación y manejo precoz de todos los factores de riesgo que puedan relacionarse con una adherencia subóptima. Para el desarrollo adecuado de esta labor resulta fundamental la estratificación de sus necesidades, la entrevista de motivación y el uso de las nuevas tecnologías para un contacto permanente, de manera que puedan identificarse y solucionarse aquellas situaciones que puedan comprometer una adherencia óptima.
El farmacéutico debe ejercer un papel de consultor y asesor, motivando al paciente y ofreciendo la información necesaria para que pueda tomar las decisiones adecuadas. Es fundamental generar vínculos de confianza suficientes para que el paciente exprese sus dudas, dificultades y preocupaciones y poder así individualizar las intervenciones en función de las barreras detectadas. Para ello, es muy importante la formación en entrevista motivacional. Durante la consulta de AF se debe resaltar la importancia que tiene la adherencia al tratamiento en su totalidad, no únicamente al TAR, identificar posibles barreras y potenciar los aspectos positivos para mantener una buena adherencia. Asimismo, reforzará la necesidad de realizar un correcto seguimiento en las consultas programadas38.
Es clave disponer de una herramienta de estratificación que permita la identificación de subgrupos con diferentes niveles de riesgo y perfiles de necesidad de AF diferenciados, y definir recomendaciones para cada uno de estos subgrupos. Por último, las nuevas tecnologías permiten realizar AF a distancia, de forma continua y adaptada a las necesidades del paciente, monitorizar la adherencia y ayudar al paciente con la toma de su medicación mediante alarmas y servicios de mensajería39-41.
En la Tabla 4 se resumen los objetivos de la consulta de AF.
Papel del profesional de enfermería
La consulta de enfermería especializada debe crear una relación de empatía, confidencialidad, confianza y respeto para entender al paciente en todo su contexto, permitiéndose conocer su disposición y recursos para abordar las causas, factores o barreras que puedan condicionar la adherencia y el cumplimiento terapéutico, mejorando, por tanto, la eficacia del mismo. La disponibilidad y flexibilidad que se proporciona facilita la accesibilidad y conexión del paciente con el resto del equipo multidisciplinar, favoreciendo la vinculación a las unidades de VIH, resultando de gran ayuda la aparición y uso generalizado de las nuevas tecnologías, que facilitan la comunicación continuada. Se aplican planes de cuidados dirigidos a educar y empoderar en el autocuidado con intervenciones que modifiquen conductas y comportamientos para promover la autonomía, compromiso, responsabilidad, autocontrol y refuerzo conductual, con estrategias centradas en la realidad y necesidades, tanto física como psíquica y social de cada paciente42.
Papel del psicólogo y/o psiquiatra
El psicólogo puede intervenir para que el paciente pueda realizar un proceso adecuado de adaptación a la enfermedad a través de las distintas situaciones que se presenten. Al inicio, la intervención psicológica puede ayudar a un mejor ajuste del diagnóstico, previniendo así la posibilidad de que se instauren estrés, ansiedad o depresión que puedan influir en que el/la paciente no cuide bien de su salud. El desarrollo de un crecimiento postraumático tras recibir el diagnóstico se ha relacionado con un mejor ajuste y una mayor satisfacción43.
En cuanto al psiquiatra, su intervención será fundamental cuando se diagnostique patología psiquiátrica asociada o no a la enfermedad que requiera control farmacológico. Los pacientes con enfermedades psiquiátricas que no están estables no podrán alcanzar ni mantener la necesaria adherencia al tratamiento. Además, debe colaborar con el resto de profesionales para detectar precozmente la patología psiquiátrica.
Estrategias de intervención, educativas, motivacionales y conductuales
Son numerosos los estudios que se han desarrollado a lo largo del tiempo para evaluar la eficacia de las diferentes estrategias de intervención en la mejora o mantenimiento de una adecuada adherencia al TAR.
Un resumen de las intervenciones del equipo interdisciplinar para mejorar la adherencia se ofrece en la Tabla 5.
Estrategias en la pauta terapéutica
En los últimos años, los esquemas de TAR han evolucionado, mayoritariamente, a pautas con fármacos coformulados en un solo comprimido y con una farmacocinética que soporta el uso de una sola toma al día (QD). La excelente tolerancia y la escasa toxicidad de estos tratamientos hacen que se facilite enormemente la adherencia con respecto a los antiguos.
Por otra parte, pacientes que por razones múltiples tienen prescritos esquemas de tratamiento más complejos se pueden beneficiar de simplificar su tratamiento asegurando la supresión virológica (fundamental a la hora de simplificar un régimen terapéutico).
La nanotecnología y la posibilidad de coformular principios activos en forma de nanopartículas permiten tratamientos parenterales de larga duración (long acting)44,45. En la actualidad se están realizando ensayos clínicos en los que pautas de dos fármacos por vía intramuscular cada mes o cada dos meses demuestran la no inferioridad frente a esquemas en triple terapia por vía oral. Está por dilucidar qué tipo de pacientes se beneficiarían de estas pautas y cuál será el beneficio en la adherencia.
Estrategias TIC, TAC y 2.0
Las intervenciones basadas en tecnología digital han surgido como una herramienta de utilidad para la asistencia al paciente con infección por el VIH combinadas con la asistencia estándar. Entre ellas, iniciativas basadas en eSalud (utilización de Internet en el ámbito de la salud),
 mSalud (uso de dispositivos móviles) o telesalud (tecnologías de la comunicación para dar soporte sanitario a larga distancia), demostrando potencial utilidad en la adherencia al tratamiento. En relación con la adherencia, además de registrarla y medirla, existe consenso en considerar que la tecnología digital puede ser efectiva para mejorarla, si bien las evidencias publicadas ofrecen resultados contradictorios. En general, se considera que las intervenciones basadas en mSalud, especialmente a través de mensajes de texto o llamadas telefónicas, son las más eficaces. Algunas intervenciones basadas en vídeos, cuestionarios o iniciativas en el entorno web también han demostrado su utilidad46-48. Por otra parte, diversos estudios llevados a cabo con poblaciones específicas han demostrado que los usuarios demandan un perfil más social de las intervenciones, que permita la interacción entre iguales y con los profesionales sanitarios49. En este sentido, algunas intervenciones basadas en redes sociales pretenden crear grupos y comunidades útiles para motivar a los pacientes a mantener una buena adherencia al tratamiento. También las redes sociales pueden ayudar a la monitorización de la adherencia, ya que muchos pacientes comparten información personal (incluyendo comportamientos relacionados con el VIH y el tratamiento) que, analizada de forma agregada, puede aportar información valiosa para entender y predecir comportamientos en relación con la adherencia al tratamiento50. Otra posibilidad que brindan los canales digitales es la puesta en marcha de programas online entre iguales (programas de paciente experto), cuya eficacia sobre la mejora de la adherencia ha sido puesta de manifiesto en algunas evaluaciones preliminaries51-53.
mSalud (uso de dispositivos móviles) o telesalud (tecnologías de la comunicación para dar soporte sanitario a larga distancia), demostrando potencial utilidad en la adherencia al tratamiento. En relación con la adherencia, además de registrarla y medirla, existe consenso en considerar que la tecnología digital puede ser efectiva para mejorarla, si bien las evidencias publicadas ofrecen resultados contradictorios. En general, se considera que las intervenciones basadas en mSalud, especialmente a través de mensajes de texto o llamadas telefónicas, son las más eficaces. Algunas intervenciones basadas en vídeos, cuestionarios o iniciativas en el entorno web también han demostrado su utilidad46-48. Por otra parte, diversos estudios llevados a cabo con poblaciones específicas han demostrado que los usuarios demandan un perfil más social de las intervenciones, que permita la interacción entre iguales y con los profesionales sanitarios49. En este sentido, algunas intervenciones basadas en redes sociales pretenden crear grupos y comunidades útiles para motivar a los pacientes a mantener una buena adherencia al tratamiento. También las redes sociales pueden ayudar a la monitorización de la adherencia, ya que muchos pacientes comparten información personal (incluyendo comportamientos relacionados con el VIH y el tratamiento) que, analizada de forma agregada, puede aportar información valiosa para entender y predecir comportamientos en relación con la adherencia al tratamiento50. Otra posibilidad que brindan los canales digitales es la puesta en marcha de programas online entre iguales (programas de paciente experto), cuya eficacia sobre la mejora de la adherencia ha sido puesta de manifiesto en algunas evaluaciones preliminaries51-53.
Estrategias para mejorar la adherencia a la PrEP
La eficacia de la PrEP está estrechamente vinculada a niveles elevados de adherencia1. Los ensayos clínicos sobre eficacia de la PrEP en las poblaciones diana han medido de diversas formas esta adherencia, y en ocasiones ha resultado subóptima, por lo que es necesario desarrollar estrategias para mejorarla54.
Existen limitaciones en la fuerza de la evidencia sobre la eficacia real de estas intervenciones, dado que hay pocos ensayos clínicos publicados hasta el momento. Se han pilotado intervenciones de tipo cognitivo-conductual como el counseling y el seguimiento personalizado, indicando que este tipo de intervenciones influyen positivamente en la adherencia55.
Estudios cualitativos indican que otras estrategias, como la integración de la PrEP en una rutina diaria, utilización de pastilleros, recordatorios a través de smartphones, llevar la medicación en todo momento o el apoyo de parejas o pares, tienen cierta efectividad. En función de las dificultades para una correcta adherencia, se podría considerar implementar en cada paciente una o varias de las estrategias56. Las intervenciones del tipo mSalud a través de mensajes de texto han logrado una buena aceptación de los usuarios y efectividad, observándose en algunos casos una disminución de hasta el 50% en el olvido de las tomas54.
Al prescribir la PrEP se debe orientar al paciente en la toma de decisiones informadas sobre el uso del preservativo, e identificar estrategias individualizadas para maximizar la adherencia en este contexto. En el caso de usuarios de chemsex, algunos estudios encuentran que una forma de favorecer la adherencia sería tener en cuenta los patrones de uso de drogas sexuales y recreativas, realizando una recomendación de PrEP personalizada54.
Otros colectivos en los que se ha encontrado una mayor frecuencia de interrupción de la PrEP son los de mujeres y los de personas jóvenes. En cambio, las mujeres adherentes indicaron, además de motivaciones personales como la reducción del riesgo y el interés por el resultado de la investigación, otras estrategias como recordatorios y el apoyo de su entorno familiar y comunitario54.
Se deben tener en cuenta la dinámica de los comportamientos y el riesgo de adquirir infección por el VIH a la hora de establecer la estrategia más adecuada para un individuo determinado, con intervenciones adaptadas que aborden, a diferentes niveles, las barreras a las que puedan enfrentarse.
Procedimiento para la prescripción,
dispensación y seguimiento del tratamiento
El tiempo que transcurre entre el diagnóstico hasta la primera visita con el médico para evaluar al paciente y prescribir el tratamiento debe ser corto (se aconseja que sea inferior a dos semanas, aunque lo óptimo sería menos de una semana). El acortar el tiempo mejora la retención de la información recibida, facilita el apoyo psicológico de forma rápida y el acceso a una información rápida y veraz. Se debe atender de forma rápida a la(s) pareja(s) y planificar los estudios complementarios, analíticas y resto de pruebas, studio de contactos, cribado de infecciones de transmisión sexual, etc. Debe pactarse con el paciente la forma de comunicación en el futuro.
El siguiente punto es el inicio del TAR. Aunque en algunas ocasiones se podría iniciar el primer día, las guías recomiendan que se comience cuando el paciente esté preparado, lo cual ocurre en la mayoría de los pacientes en la segunda visita, y no debería demorarse más de dos semanas, para disminuir lo antes posible el riesgo de transmisión. Durante estas dos visitas el médico debe comprobar si el paciente presenta un perfil que dificultará la adherencia y continuación del tratamiento33.
La consulta médica y la de atención farmacéutica deberían estar coordinadas y compartir información para evitar visitas innecesarias o adicionales, es decir, potenciando el acto único asistencial.
Para los pacientes con factores de mala adherencia es recomendable introducir herramientas informáticas de alerta activa a partir de los sistemas de información, prescripción y dispensación para identificarlos. Dicha información debe compartirse entre todos los profesionales implicados para establecer las medidas individualizadas más adecuadas que permitan revertir dicha situación. Asimismo, debe estar establecida la forma de actuación y haberse definido perfectamente la persona asignada para ello. Todo ello debe ser registrado en la historia clínica del paciente33,57.
Por otra parte, la actuación farmacéutica para la mejora de la adherencia puede dividirse en tres etapas: valoración inicial del paciente, educación terapéutica y planificación personalizada del seguimiento.
En la valoración inicial se debe tener en cuenta que una buena comunicación entre el farmacéutico y el paciente es un requisito necesario para lograr con éxito los objetivos farmacoterapéuticos propuestos. A través de la entrevista con el paciente debe obtenerse información útil que pueda favorecer o comprometer los objetivos farmacoterapéuticos propuestos con el paciente. Estos datos pueden agruparse en socioeconómicos, clínicos, farmacoterapéuticos, relacionados con el entorno sanitario y nivel de conocimiento sobre el tratamiento y la patología.
Recientemente se ha publicado el modelo CMO de atención farmacéutica para mejorar la adherencia en pacientes con infección por el VIH36,58,59.
La optimización de la adherencia terapéutica pasa por planificar las citas presenciales y no presenciales, intentando potenciar el acto único y las nuevas formas de comunicación. La dispensación no debe estar condicionada por el número de comprimidos de los envases de medicamentos, sino por aspectos clínicos, personales y de la relación con el sistema sanitario (citas en el hospital, distancia al hospital, etc.). Así, varios estudios recomiendan la dispensación multimensual teniendo en cuenta la estabilidad de la enfermedad, la tolerancia al tratamiento, la localización de los servicios sanitarios y el tiempo en TAR, con el objetivo de disminuir las barreras de acceso al tratamiento, facilitar el cumplimiento y mejorar la respuesta virológica33,60.
Finalmente, el seguimiento farmacoterapéutico especializado permite valorar el alcance de los objetivos terapéuticos, analizar la seguridad y la adherencia, detectar potenciales interacciones farmacológicas y reorientar el plan farmacoterapéutico si fuera necesario.
Para un correcto seguimiento resulta esencial la integración con el equipo multidisciplinar que atiende al paciente, comunicando la información relevante obtenida en la consulta, así como establecer un circuito óptimo para manejar los efectos adversos del tratamiento, la falta de adherencia al tratamiento, la pérdida de seguimiento del paciente y los reinicios de tratamiento. El feedback con los pacientes es un elemento muy importante, ya que permitirá adaptar el programa de seguimiento a sus necesidades y reorientar los objetivos farmacoterapéuticos. La evaluación de los patient-reported outcomes permite conocer los síntomas, el estado funcional y la calidad de vida relacionada con la salud, el bienestar o la satisfacción respecto al cuidado o tratamiento recibido desde la perspectiva del paciente.
En la Tabla 6 se observan las recomendaciones y grado de implantación de actuaciones a llevar a cabo por cada uno de los miembros del equipo interdisciplinar.
Tabla 6. Recomendaciones y grado de implantación de actuaciones a llevar a cabo por cada uno de los miembros del equipo interdisciplinary

TAR: tratamiento antirretroviral; VIH: virus de la inmunodeficiencia humana.
El algoritmo de seguimiento recomendado para la mejora de la adherencia en el entorno multidisciplinar se observa en la Figura 1.
Bibliography
Codina C, Knobel H, Miró JM, Carmona A, García B, Antela A, et al. Recomendaciones GESIDA/SEFH/PNS para mejorar la adherencia al tratamiento antirretroviral. Farm Hosp. 1999;23(4):215-29. [ Links ]
Recomendaciones GESIDA/SEFH/PNS para mejorar la adherencia al tratamiento antirretroviral. Enferm Infecc Microbiol Clin. 2000;18(1):27-39. [ Links ]
Knobel H, Escobar I, Polo R, Ortega L, Martín-Conde MT, Casado JL, et al. Recommendations from GESIDA/SEFH/PNS to improve adherence to antiviral treatment (2004). Enferm Infecc Microbiol Clin. 2005;23(4):221-31. [ Links ]
Recomendaciones de GeSIDA/Plan Nacional sobre el Sida respecto al tratamiento antirretroviral en adultos infectados por el virus de la inmunodeficiencia humana (updated january 2008) (accessed 12/11/2019). Available at: http://www.mscbs.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/docs/recomendacionesAdherenciaTrtoAntirr etroviral062008.pdf [ Links ]
Recomendaciones de GeSIDA/Plan Nacional sobre el Sida respecto al tratamiento antirretroviral en adultos infectados por el virus de la inmunodeficiencia humana (updated january 2019) (accessed 12/11/2019). Available at: http://www.mscbs.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/publicaciones/profSanitarios/docTAR2019vF inalCONresaltesTablas_V8feb19.pdf [ Links ]
Abdulrahman SA, Ganasegeran K, Rampal L, Martins OF. HIV treatment adherence -A shared burden for patients, health-care providers, and other stakeholders. AIDS Rev. 2019;21(1):28-39. DOI: 10.24875/AIDSRev.19000037 [ Links ]
Altice F, Evuarherhe O, Shina S, Beaubrun AC. Adherence to HIV treatment regimens: systematic literature review and meta-analysis. Patient Prefer Adherence. 2019;13:475-90. DOI: 10.2147/PPA.S192735. eCollection 2019. [ Links ]
Cramer JA, Roy A, Burrell A, Fairchild C, Fuldeore MJ, Ollendorf DA. Medication compliance and persistence: Terminology and definitions. Value Health. 2008;11(1):44-7. DOI: 10.1111/j.1524-4733.2007.00213.x [ Links ]
Vrijens B, De Geest S, Hughes DA, Przemyslaw K, Demonceau J, Ruppar T, et al. A new taxonomy for describing and defining adherence to medications. Br J Clin Pharmacol. 2012;73(5):691-705. DOI: 10.1111/j.1365-2125.2012.04167.x [ Links ]
Corless IB, Hoyt AJ, Tyer-Viola L. 90-90-90-Plus: Maintaining adherence to antiretroviral therapies. AIDS Patient Care STDS. 2017;31(5):227-36. DOI: 10.1089/apc.2017.0009 [ Links ]
Abdulrahman SA, Ganasegeran K, Rampal L, Martins OF. Conceptual framework for investigating and influencing adherence behavior among HIV-positive populations: An applied social cognition model. AIDS Rev. 2019;21(3):23-7. DOI: 10.24875/AIDSRev.19000069 [ Links ]
Bock P, James A, Nikuze A, Peton N, Sabapathy K, Mills E. Baseline CD4 count and adherence to antiretroviral therapy: a systematic review and meta-analysis. J Acquir Immune Defic Syndr. 2016;73(5):514-21. [ Links ]
Adelekan B, Andrew N, Nta I, Gomwalk A, Ndembi N, Mensah C. Social barriers in accessing care by clients who returned to HIV care after transient loss to follow-up. AIDS Res Ther. 2019;16(1):17. DOI: 10.1186/s12981-019-0231-5 [ Links ]
Carpenter BS, Hanass-Hancock J. Looking at antiretroviral adherence through a disability lens: a cross-sectional analysis of the intersection of disability, adherence, and health status. Disabil Rehabil. 2020 Mar; 42(6):806-13. DOI: 10.1080/09638288.2018.1510048 [ Links ]
Poku RA, Owusu AY, Mullen PD, Markham C, McCurdy SA. Antiretroviral therapy maintenance among HIV-positive women in Ghana: the influence of poverty. AIDS Care. 2019 Aug 12:1-6. DOI: 10.1080/09540121.2019.1653434 [ Links ]
Kanters S, Park J, Chan K, Socias ME, Ford N, Forrest JI. Interventions to improve adherence to antiretroviral therapy: a systematic review and network meta-analysis. Lancet HIV. 2017;4(1):e31-40. DOI: 10.1016/S2352-3018(16)30206-5 [ Links ]
Brittain K, Asafu-Agyei NA, Hoare J, Bekker LG, Rabie H, Nuttall J, et al. Association of adolescent-and caregiver-reported antiretroviral therapy adherence with HIV viral load among perinatally-infected South African adolescents. AIDS Behav. 2018;22(3):909-1. [ Links ]
Ibarra O, Morillo R. Lo que debes saber sobre la adherencia al tratamiento. Grupo de adherencia terapéutica ADHEFAR de la SEFH. Badalona: Euromedice Vivactis; 2017. [ Links ]
Tuldra A, Fumaz CR, Ferrer MJ, Bayés R, Arnó A, Balagué M. Prospective randomised two-arm controlled study to determine the efficacy of a specific intervention to improve long-term adherence to highly antiretroviral therapy. J Acquir Immune Defic Syndr. 2000;25(3):221-8. [ Links ]
Duran S, Solas C, Spire B, Carrieri MP, Fuzibet JG, Costagliola D. Do HIV-infected injecting drugs users over-report adherence to highly active antiretroviral therapy? A comparison between patient's self-reports and serum protease inhibitors concentrations in the French Manif 2000 cohort study. AIDS Behav. 2018;22(3):909-17. DOI: 10.1007/s10461-017-2004-2 [ Links ]
Alcoba M, Cuevas MJ, Pérez-Simón MR, Mostaza JL, Ortega L, Ortiz de Urbina J, et al.; HAART Adherence Working Group for the Province of Leon, Spain. Assessment of adherence to triple antiretroviral treatment including indinavir: role of the determination of plasma levels of indinavir. J Acquir Immune Defic Syndr. 2003;33(2):253-8. [ Links ]
Pérez-Simón MR, Cuevas MJ, Ortega L, Carro JA, Mostaza JL, Martín V. Valoración de la adherencia al tratamiento antirretroviral: papel de la determinación de la concentración plasmática de los fármacos no análogos de nucleósidos. Med Clin (Barc). 2003;120(18):701-3. [ Links ]
Quirós-Roldán E, Torti C, Lapadula G, Ladisa N, Micheli V, Patroni A. Adherence and plasma drug concentrations are predictors of confirmed virologic response after 24-week salvage highly active antiretroviral therapy. AIDS Patient CARE STDS. 2007;21(2):92-9. [ Links ]
Duong M, Piroth L, Peytavin G, Forte F, Kohli E, Grappin M. Value of patient selfreport and plasma human immunodeficiency virus protease inhibitor level as markers of adherence to antiretroviral therapy: relationship to virologic response. Clin Infect Dis. 2001;33(3):386-92. [ Links ]
Fernández X, Luque S, González E. Fracaso virológico de distintos tipos de tratamiento antirretroviral en una cohorte de pacientes con muy baja adherencia. Enferm Infecc Microbiol Clin. 2018;36(3):91-2. [ Links ]
Castillo-Mancilla JR, Haberar JE. Adherence measurements in HIV: New advancements in pharmacologic methods and real-time monitoring. Curr HIV/AIDS Rep. 2018;15(1):49-59. DOI: 10.1007/s11904-018-0377-0 [ Links ]
Castillo-Mancilla JR, Brown TT, Erlandson KM. Suboptimal adherence to combination antiretroviral therapy is associated with higher levels of inflammation despite HIV suppression. Clin Infect Dis. 2016;63(12):1661-7. [ Links ]
Cheng Y, Nickman NA, Jamjian C, Stevens V, Zhang Y, Sauer B. Predicting por adherence to antiretroviral therapy among treatment-naïve veterans infected with human immunodeficiency virus. Medicine (Baltimore). 2018;97(2):e9495. DOI: 10.1097/MD.0000000000009495 [ Links ]
Vitalis D. Predicting adherence to antiretroviral therapy among pregnant women in Guyana: Utility of the Health Belief Model. Int J STD AIDS. 2017;28(8):756-65. DOI: 10.1177/0956462416665989 [ Links ]
Harris RA, Haberer JE, Musinguzi N, Chang KM, Schechter CB, Doubeni CA. Predicting short-term interruptions of antiretroviral therapy from summary adherence data: Development and test of a probability model. PLoS One. 2018;13(3):e0194713. DOI: 10.1371/journal.pone.0194713. eCollection 2018. [ Links ]
Hernández I, Zhang Y. Using predictive analytics and big data to optimize pharmaceutical outcomes. Am J Health Syst Pharm. 2017;74(18):1494-500. DOI: 10.2146/ajhp161011 [ Links ]
Knobel H, Guelar A, Calzado S. Development of a risk score-based on patient's individual factors for predicting non-adherence to antiretroviral therapy. Abstract: TUPED1206, 9TH IAS Conference on HIV Science. 23-26 July 2017. Paris, France. [ Links ]
Panel de expertos de GeSIDA y Plan Nacional sobre el Sida. Documento de consenso de GeSIDA/Plan Nacional sobre el Sida respecto al tratamiento antirretroviral en adultos infectados por el virus de la inmunodeficiencia humana. Updated february 2020 (webpage) (accessed 12/11/2019). Available at: http://gesida-seimc.org/category/guias- clinicas/antirretroviral-vigentes/ [ Links ]
Greene M, Justice AC, Lampiris HW, Valcour Vl. Management of human immunodeficiency virus infection in advanced age. JAMA. 2013;309(13):1397-405. DOI: 10.1001/jama.2013.2963 [ Links ]
Mapa estratégico de Atención Farmacéutica al paciente externo de la SEFH (webpage) (accessed 01/11/2020). Available at: https://www.sefh.es/mapex/index.php [ Links ]
Morillo-Verdugo R, Calleja-Hernández MA, Robustillo Cortés MA. A new pharmaceutical care concept: more capable, motivated and timely. Hosp Pharm. 2019;54(6):348-50. DOI: 10.1177/0018578719867657 [ Links ]
Ryan KL, Jakeman B, Conklin J, Pineda LJ, Deming P, Mercier RC. Treatment of patients with HIV or hepatitis C by pharmacist clinicians in a patient-centered medical home. Am J Health Syst Pharm. 2019;76(11):821-8. DOI: 10.1093/ajhp/zxz059 [ Links ]
Morillo-Verdugo R, Robustillo-Cortés MLA, Martín Conde MT, Callejón-Callejón G, Cid-Silva P, Moriel-Sánchez C, et al. Effect of a structured pharmaceutical care intervention versus usual care on cardiovascular risk in HIV patients on antiretroviral therapy: INFAMERICA study. Ann Pharmacother. 2018;52(11):1098-108. DOI: 10.1177/1060028018778045 [ Links ]
Morillo-Verdugo R, Martínez-Sesmero JM, Lázaro-López A, Sánchez-Rubio J, Navarro-Aznárez H, DeMiguel-Cascón M, et al. Desarrollo de un modelo de estratificación de atención farmacéutica destinado a pacientes VIH+. Farm Hosp. 2017;41(3):346-56. DOI: 10.7399/fh.2017.41.3.10655 [ Links ]
Alexander E, Butler CD, Darr A, Jenkins MT, Long RD, Shipman CJ. ASHP statement on telepharmacy. Am J Health Syst Pharm. 2017;74(9):e236-41. DOI: 10.2146/ajhp170039 [ Links ]
Quintana Y, González Martorell EA, Fahy D, Safran C. A systematic review on promoting adherence to antiretroviral therapy in HIV-infected patients using mobile phone technology. Appl Clin Inform. 2018;09(02):450-66. DOI: 10.1055/s-0038-1660516 [ Links ]
Pisano González M, González Pisano A. La modificación de los hábitos y la adherencia terapéutica, clave para el control de la enfermedad crónica. Enferm Clín. 2014;24(1):59-66. DOI: 10.1016/j.enfcli.2013.10.006 [ Links ]
Dibb B. Assessing stigma, disclosure regret and posttraumatic growth in people living with HIV. AIDS Behav. 2018;22(12):3916-23. DOI: 10.1007/s10461-018-2230-2 [ Links ]
Dionne B. Key principles of antiretroviral pharmacology. Infect Dis Clin North Am. 2019;33(3):787-805. DOI: 10.1016/j.idc.2019.05.006 [ Links ]
Gendelman HE, McMillan J, Bade AN, Edagwa B, Kevadiya BD. The promise of long-acting antiretroviral therapies: From need to manufacture. Trends Microbiol. 2019;27(7):593-606. DOI: 10.1016/j.tim.2019.02.009 [ Links ]
Cao B, Gupta S, Wang J, Hightow-Weidman LB, Muessig KE, Tang W. Social media interventions to promote HIV testing, linkage, adherence, and retention: Systematic review and meta-analysis. J Med Internet Res. 2017;19(11):e394. DOI: 10.2196/jmir.7997 [ Links ]
Vieira IC, Gimeniz MT, de Oliveira H. Information and communication technologies for adherence to antiretroviral treatment in adults with HIV/AIDS. Int J Med Inform. 2016;92:54-61. DOI: 10.1016/j.ijmedinf.2016.04.013 [ Links ]
Jongbloed K, Parmar S, van der Kop M, Spittal PM, Lester RT. Recent evidence for emerging digital technologies to support global HIV engagement in care. Curr HIV/AIDS Rep. 2015;12(4):451-61. DOI: 10.1007/s11904-015-0291-7 [ Links ]
Amico KR. Evidence for technology interventions to promote ART adherence in adult populations: A review of the literature 2012-2015. Curr HIV/AIDS Rep. 2015;12:441-50. DOI: 10.1007/s11904-015-0286-4 [ Links ]
Bychkov D, Young S. Social media as a tool to monitor adherence to HIV antiretroviral therapy. J Clin Transl Res. 2018;3(Suppl 3):407-10. [ Links ]
Simoni J, Huh D, Frick PA, Pearson CR, Andrasik MP, Dunbar PJ, et al. Peer support and pager messaging to promote antiretroviral modifying therapy in Seattle: a randomized controlled trial. J Acquir Immune Defic Syndr. 2009;52(4):465-73. [ Links ]
Horvath KJ, Oakes JM, Rosser S, Danilenko G, Vezina H, Amico KR, et al. Feasibility, acceptability and preliminary efficacy of an online peer-to-peer social support ART adherence intervention. AIDS Behav. 2013;17(6):2031-44. DOI: 10.1007/s10461-013-0469-1 [ Links ]
Morillo-Verdugo R, Robustillo-Cortés MA. Desarrollo de un programa de paciente experto 2.0 para pacientes VIH+. Revista Multidisciplinar del Sida. 2015;1(6): 40-52. [ Links ]
Plan Nacional Sobre el Sida-Grupo de Expertos PrEP. Ministerio de Sanidad, Servicios Sociales e Igualdad. Profilaxis Preexposición al VIH en España. Enero 2018 (webpage) (accessed 01/11/2020). Available at: https://www.mscbs.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/docs/PROFILAXIS_PREEXPOSICION_VIH .pdf [ Links ]
Haberer J. Current concepts for PrEP adherence in the PrEP revolution: from clinical trials to routine practice. Curr Opin HIV AIDS. 2016;11(1):10-7. DOI: 10.1097/COH.0000000000000220 [ Links ]
Mayer KH, Safren SA, Elsesser SA, Psaros C, Tinsley JP, Marzinke M, et al. Optimizing pre-exposure antiretroviral prophylaxis adherence in men who have sex with men: Results of a pilot randomized controlled trial of “Life-Steps for PrEP”. AIDS Behav. 2017;21(5):1350-60. DOI: 10.1007/s10461-016-1606-4 [ Links ]
Shubber Z, Mills EJ, Nachega JB, Vreeman R, Freitas M, Bock P, et al. Patientreported barriers to adherence to antiretroviral therapy: A systematic review and meta-analysis. PLoS Med. 2016;13(11):e1002183. DOI: 10.1371/journal.pmed.1002183. eCollection 2016 Nov. [ Links ]
Calleja MA, Morillo R. El modelo CMO en consultas externas de Farmacia Hospitalaria. Barcelona: Euromedice Vivactis; 2016. [ Links ]
Morillo-Verdugo R, Robustillo-Cortés MA, Manzano García M, Almeida-González CV. Influence of pharmacist intervention, based on CMO model, to improve activation in HIV patients. Rev Esp Quimioter. 2019;32(1):40-9. [ Links ]
Mutasa-Apollo T, Ford N, Wiens M, Socias ME, Negussie E, Wu P, et al. Effect of frequency of clinic visits and medication pick-up on antiretroviral treatment outcomes: a systematic literature review and meta-analysis. J Int AIDS Soc. 2017;20(Suppl 4):2164. DOI: 10.7448/IAS.20.5.21647 [ Links ]
Recibido: 11 de Marzo de 2020; Aprobado: 06 de Abril de 2020











 texto em
texto em 






