My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Farmacia Hospitalaria
On-line version ISSN 2171-8695Print version ISSN 1130-6343
Farm Hosp. vol.44 n.5 Toledo Sep./Oct. 2020 Epub July 26, 2021
https://dx.doi.org/10.7399/fh.11384
ORIGINALES
Centralización del plan de mantenimiento con metadona en un servicio de farmacia hospitalaria en la Comunidad de Madrid
1Servicio de Farmacia, Hospital Universitario Infanta Leonor, Madrid. Spain.
2Facultad de Farmacia, Universidad CEU San Pablo, Madrid. Spain.
Introducción
La metadona fue sintetizada en los años 40 del siglo pasado. Es un agonista opiáceo puro de origen sintético que presenta afinidad y una marcada actividad en los receptores µ. Muestra una potencia ligeramente superior a la de la morfina y mayor duración de acción, aunque con menor efecto euforizante1. Por ello es una alternativa a la morfina: mismas propiedades analgésicas pero con efectos adversos más leves2.
Fue en 1964 cuando comenzó a utilizarse en programas clínicos con fines de deshabituación a opiáceos como la heroína. Esta práctica fue desarrollada por un equipo de investigación de la Universidad Rockefeller de Nueva York3. Estos programas, denominados programas de mantenimiento con metadona (PMM), surgieron tras la Segunda Guerra Mundial con el objetivo de tratar la adicción a la heroína, en respuesta al aumento desorbitado del consumo y muertes relacionadas con esta sustancia de abuso que tuvo lugar a finales de los años 50 y comienzos de los 60 en la ciudad de Nueva York4,5.
La metadona fue, por tanto, la primera terapia de sustitución con opiáceos en Estados Unidos, Australia y Europa y continúa siendo la más usada en la actualidad. Ha demostrado claramente reducir el consumo ilícito de heroína, las muertes por sobredosis de esta droga, y disminuir la frecuencia de inyección y la transmisión del virus de la inmunodeficiencia humana6. Además, mejora la calidad de vida de los pacientes, incluyendo cambios positivos en la salud y el funcionamiento tanto social como físico7,8. Los tratamientos de mantenimiento con metadona oral han demostrado ser efectivos tanto para los pacientes individualmente como para la salud pública, además de ser coste-efectivos9,10.
En España, el consumo de heroína alcanzó su incidencia más alta en la década de los 8011. La primera normativa española relativa a la prescripción y dispensación de metadona para el tratamiento de la dependencia a opiáceos apareció en 1983, aunque hasta 1990 no se normalizaron los criterios de prescripción, generalizándose su uso. A partir de entonces comenzaron a ponerse en práctica toda una serie de leyes sobre la regulación e implantación de los PMM12-16 que han ido evolucionando hasta la actualidad17.
En la Comunidad de Madrid, mediante el Decreto 125/2017, de 17 de octubre, del Consejo de Gobierno, por el que se establece la estructura orgánica del Servicio Madrileño de Salud, se incorporó la estructura de la Dirección General de Coordinación de la Asistencia Sanitaria, la Subdirección General de Asistencia en Adicciones (SGAA), asumiendo dicha Dirección General las competencias sobre “la planificación y coordinación de los recursos de tratamiento, rehabilitación y reinserción de que disponen las Administraciones Públicas en materia de drogodependencias, así como de aquellos recursos pertenecientes a instituciones de titularidad privada que reciban fondos públicos en el ámbito de la Comunidad para tareas de asistencia a las adicciones”.
La SGAA coordina una red de centros y servicios con el objetivo de atender a los ciudadanos de la Comunidad Autónoma que presentan problemas de consumo y adicción de drogas y anualmente supone alrededor de 22.000. De todos ellos, aproximadamente el 16% tienen prescrito el medicamento metadona como un sustitutivo opiáceo indicado para el tratamiento de su trastorno adictivo por consumo de heroína.
A raíz de este cambio organizativo se publicó la Resolución 189/201818, en la que se encomendaban a un servicio de farmacia hospitalaria (SFH) las tareas de suministro diario de metadona a los Centros de Atención Integral a Drogodependientes (CAID) de la SGAA del Servicio Madrileño de Salud. Esta Resolución tiene por objetivo centralizar el procedimiento de adquisición, elaboración, distribución y dispensación de metadona gestionado por el SFH como primer paso que posibilite un cambio de modelo de la asistencia farmacoterapéutica para el tratamiento de los pacientes incluidos en este programa (entre 3.000 y 5.000), que reciben metadona en los 27 CAID que se distribuyen a lo largo de la Comunidad de Madrid.
En una primera fase debería asumirse la gestión de adquisición y elaboración de metadona siguiendo con el circuito actual de distribución, dosificación y administración personalizada en cada CAID.
En una segunda fase se asumirían las actuaciones dirigidas a la protocolización, estandarización y armonización de los tratamientos, mediante la elaboración de protocolos farmacoclínicos de prescripción y la atención farmacéutica, incluyendo la difusión de estrategias de información y formación dirigidas a profesionales y pacientes de los CAIDs.
Como resultado de lo anteriormente expuesto, así como de la Resolución 189/201818 y teniendo en el horizonte estos objetivos por fases, el SFH inició las actividades encomendadas en marzo de 2018, siendo la primera vez que farmacéuticos especialistas en farmacia hospitalaria son responsables de este tipo de funciones en el ámbito del tratamiento de las adicciones en la Comunidad de Madrid. Esto abre todo un abanico de posibilidades de actuación que permitirán no sólo aprovechar y optimizar recursos ya existentes, sino también posibilitar un cambio de modelo de asistencia farmacoterapéutica, incorporando las competencias, habilidades y conocimiento del farmacéutico especialista al proceso asistencial.
El objetivo de este artículo es describir el proceso de centralización del procedimiento de adquisición, elaboración, distribución y dispensación de metadona en el SFH que permita un cambio de modelo de la asistencia farmacoterapéutica para el tratamiento de los pacientes incluidos en el PMM incorporando al farmacéutico especialista al proceso asistencial.
Métodos
Para acometer la primera fase del proyecto se realizó un análisis del circuito previo a la Resolución 189/201818 para la adquisición de todos los medios y materiales necesarios para implementar la puesta en marcha de la Unidad de Farmacia Centralizada en el SFH.
Para ello, se habilitó en las instalaciones del servicio de farmacia un laboratorio de farmacotecnia, equipado con matraces aforados de 500 ml, 1.000 ml, 2.000 ml y 2.500 ml de volumen, una balanza de precisión, agitadores magnéticos, imanes, vasos de precipitados de 800 ml,
2.000 ml y 3.000 ml, varillas de vidrio, un ordenador de mesa y con los requerimientos de seguridad necesarios mediante control electrónico de acceso y almacenamiento de seguridad debido a la naturaleza estupefaciente de los medicamentos a utilizar.
Posteriormente, se estableció el procedimiento de adquisición de hidrocloruro de metadona a través de la Agencia Española del Medicamento y de metadona comprimidos al laboratorio proveedor para garantizar el suministro de los CAIDs. Asimismo, se estableció el nuevo circuito, horarios, ruta y procedimientos de seguridad para el transporte de los medicamentos a los CAIDs. Al inicio del programa, la adquisición se realizaba mediante compra directa al laboratorio proveedor. Posteriormente se diseñó y adjudicó, cumpliendo la Ley de Contratos de la Administración Pública, un procedimiento normalizado para la adquisición de hidrocloruro de metadona y metadona comprimidos mediante concurso público.
También se implementó un sistema de comunicación entre el SFH y los CAIDs, creando una nueva cuenta de correo electrónico exclusiva para este programa. Asimismo, se diseñaron dos formularios de solicitud, uno para metadona en solución oral (Figura 1) y otro para metadona comprimidos (Figura 2), mediante los cuales los diferentes CAIDs envían sus solicitudes individualizadas al SFH.
Se redactaron y aprobaron por la Comisión de Calidad del SFH seis procedimientos normalizados de trabajo de todos los procesos del programa, siguiendo la metodología implementada en el SFH y basada en la certificación del SFH por el Sistema de Gestión ISO 9001:2015 obtenida en el año 2012.
Asimismo, se formó al personal técnico del servicio de farmacia tanto en las cuestiones teóricas como prácticas del programa para incorporar esta actividad en sus tareas diarias.
Metadona en solución oral
Con respecto a los aspectos galénicos, la metadona en solución oral se elabora siguiendo la Guía de buenas prácticas de preparación de medicamentos en Servicios de Farmacia Hospitalaria19 a concentración 10 mg/ml, según Formulario Nacional20, en soluciones de diferentes volúmenes dependiendo de las necesidades de los CAIDs.
Las diferentes solicitudes pueden variar en función del número de pacientes y población atendida en el CAID o periodos vacacionales, solicitándose desde 5.000 mg hasta 200.000 mg de hidrocloruro de metadona (desde 0,5 hasta 20 litros). Esto obliga a que los lotes de solución de metadona elaborados se acondicionen en volúmenes múltiplos de 0,5 litros usando como material de acondicionamiento final frascos de vidrio topacio de 1 y/o 2,5 litros de capacidad. Durante la elaboración, se asignan los lotes correspondientes según el libro recetario, y se cumplimenta la ficha de control de elaboración correspondiente. En dicho formulario quedan registrados los lotes que se dispensan a cada CAID, garantizando así la trazabilidad de la elaboración. Una vez acondicionadas, las botellas se etiquetan, se sellan con parafilm y se custodian en cámara frigorífica a 2 ºC-8 ºC y en condiciones de seguridad (la cámara frigorífica dispone de una sonda que monitoriza la temperatura y su puerta permanece cerrada bajo llave hasta el momento de la dispensación).
Metadona en comprimidos
La metadona en comprimidos también se dispensa a los CAIDs mediante prescripciones individualizadas realizadas por los facultativos médicos de cada CAID. La dosis se acondiciona de forma individual por paciente y en función de la especialidad de metadona, proporcionando en cada una de ellas prospecto informativo.
Por último, se estableció una programación de trabajo semanal según la cual, cuatro días se emplean para elaborar metadona en solución y uno para preparar las prescripciones individualizadas de metadona comprimidos.
Transporte y distribución
Para la selección de la empresa responsable de la distribución y transporte del hidrocloruro de metadona y metadona comprimidos se diseñó y adjudicó, cumpliendo la Ley de Contratos de la Administración Pública, un procedimiento normalizado mediante concurso público.
En primer lugar, se definió la ruta de transporte asignando un día de la semana a cada CAID, y se establecieron las condiciones de seguridad y prevención de roturas de envases durante el mismo (se transportan en neveras flexibles con separadores acolchados entre las botellas para evitar que durante el transporte choquen entre sí y se rompan). Concretamente, y como mecanismo de control y seguridad, se estableció un formulario de control de transporte, entrega y devolución diario entre la empresa de transporte y sus profesionales y el SFH. Dicho formulario recoge el número de envases de metadona solución y su volumen, los miligramos totales solicitados por cada CAID y si han solicitado o no tratamientos individualizados de metadona en comprimidos. Asimismo, dicho formulario también contiene un último apartado para que el CAID selle y rubrique que la entrega ha sido correcta cuando ésta se produce.
Por otra parte, el SFH también se responsabiliza de revisar la contabilidad de los CAIDs mediante los cuadernos diarios de dispensación y balance de contabilidad que se envían vía correo electrónico, lo cual garantiza el correcto uso y control del medicamento.
Circuito diario
Con una semana de antelación cada CAID envía los formularios de solicitud, tanto de metadona solución como las prescripciones de metadona comprimidos, por correo electrónico. Los datos se anonimizan mediante el envío de ficheros encriptados con clave aparte facilitada previamente por los CAIDs. El personal administrativo del SFH recepciona, registra y archiva las solicitudes, y el farmacéutico las revisa, valida y define la programación semanal. Se elabora metadona en solución y se preparan los tratamientos individualizados de metadona comprimidos siguiendo dicha programación. Tras la validación farmacéutica del proceso de elaboración se cumplimentan las hojas de ruta, realizándose dos copias. Diariamente se entrega al transportista la metadona siguiendo la hoja de ruta establecida según la programación semanal. El transportista firma su conformidad en una de las copias, la cual se entrega al administrativo para su archivo. Posteriormente, se entrega al transportista la segunda copia, y comienza el circuito de transporte. A medida que realiza la entrega correspondiente a cada CAID, éstos comprueban que la dispensación de metadona se corresponde con lo que han solicitado. Si todo es correcto, el CAID sella la entrega en el apartado correspondiente. Este procedimiento se repite con cada CAID programado en la ruta de transporte, de tal manera que al finalizar el reparto diario, el impreso contiene el sello de cada CAID. Este formulario es devuelto al SFH por el transportista y se archiva, sirviendo como comprobante de que el envío y dispensación de metadona de ese día ha sido correcto. En caso de encontrar alguna discrepancia, el CAID se comunica con el SFH para que ésta sea resuelta.
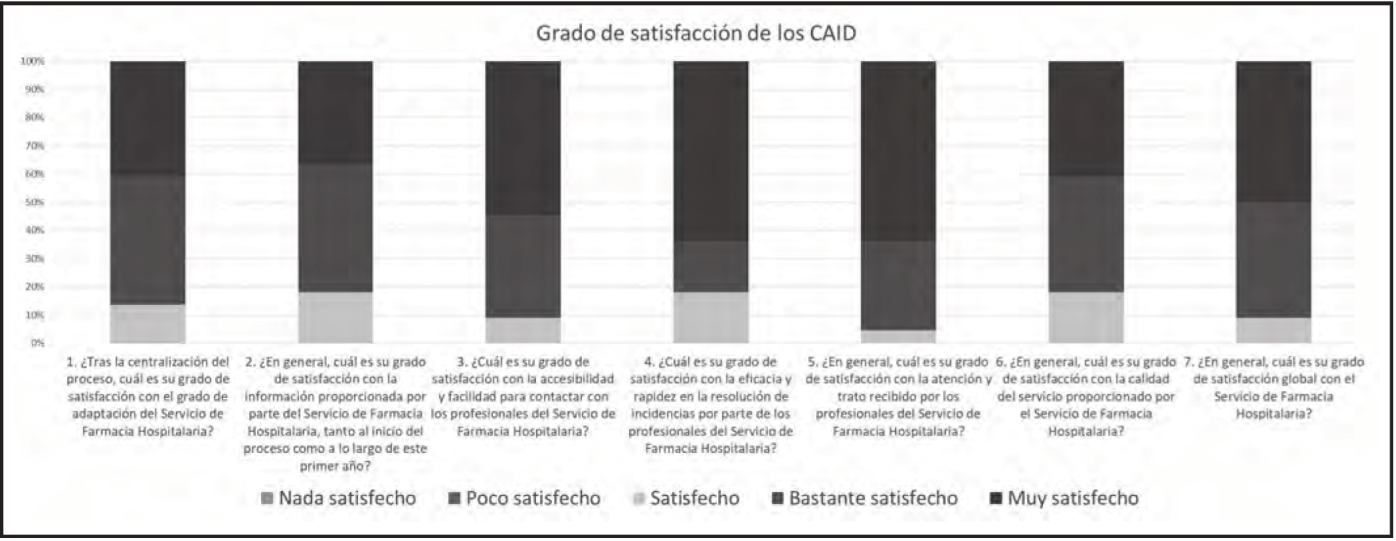
Por último, con motivo de conocer el grado de satisfacción del programa de centralización en los diferentes CAIDs, se diseñó una encuesta de calidad percibida que contenía siete preguntas (Tabla 1) con cinco posibles respuestas de escala de Likert (nada satisfecho, poco satisfecho, satisfecho, bastante satisfecho y muy satisfecho). Se envió a 24 CAIDs por correo electrónico mediante la plataforma de Formularios de Google®.
Resultados
Durante el primer año de implantación se han convocado y adjudicado, cumpliendo la Ley de Contratos de la Administración Pública, procedimientos para la adquisición de metadona, envases para la dosificación personalizada en los CAIDs y transporte de metadona desde el hospital a los CAIDs. Todas las especificaciones técnicas, necesidades y criterios de valoración han sido establecidos por el personal facultativo del SFH.
El SFH atiende a una red de 27 CAIDs, con un número estimado de entre 3.000 y 5.000 pacientes incluidos en el PMM.
Desde el inicio del proyecto, en el periodo abril de 2018-septiembre de 2019 se han elaborado un total de 5.293,5 litros de metadona solución. Más concretamente, 76 lotes de metadona 10 mg/ml solución de 1 litro y
2.087 lotes de metadona 10 mg/ml de 2,5 litros, lo cual supone un total de 5.217,5 litros. Esto se corresponde con un consumo de 52.935 g de metadona en forma de clorhidrato, es decir, prácticamente 53 kg. Del total elaborado se han dispensado 5.242,75 litros.
Se han dispensado un total de 151.579 comprimidos de metadona de 5 mg, 30 mg y 40 mg, lo que representa en unidades 32.857, 62.164 y 56.558, respectivamente. Estas cifras se corresponden con la dispensación de 2.844 peticiones individualizadas. Las causas y motivos de la dispensación de esta forma farmacéutica fueron el desarrollo de intolerancia a la metadona en solución, motivos personales de desplazamiento, de trabajo o vacacionales, o bien por ser pacientes con un buen control y adherencia.
La media mensual de peticiones dispensadas es de 138,7, aunque es de destacar que su valor se triplica en los meses de verano por cambio de metadona en solución a comprimidos para facilitar el desplazamiento y/o periodo vacacional de los pacientes.
El importe de adquisición ha sido de 63.110,9 € (hidrocloruro de metadona 43.993,8 € y metadona comprimidos 19.117,1 €).
Se han revisado un total de 7.934 archivos que contenían los cuadernos diarios de dispensación y balances de contabilidad de todos los CAIDs durante este año y medio, cumpliendo los requisitos legales en materia de control de medicamentos estupefacientes (Real Decreto 1675/2012, de 14 de diciembre, por el que se regulan las recetas oficiales y los requisitos especiales de prescripción y dispensación de estupefacientes para uso humano y veterinario21).
En una segunda fase del proyecto se ha convocado un concurso público para la adquisición de un sistema informático de gestión y sistemas automatizados de dispensación de metadona, el cual ha sido adjudicado en marzo de 2019 y que actualmente se encuentra en vías de implementación en los CAIDs. Asimismo, se está acometiendo la actualización del protocolo farmacoterapéutico del PMM de la Comunidad de Madrid en colaboración con un equipo multidisciplinar formado por diferentes profesionales de los CAIDs, del SFH, de la Subdirección de Farmacia y Productos Sanitarios y la Subdirección de Adicciones.
En cuanto a los resultados de la encuesta, contestaron 22 CAIDs, obteniendo una tasa de respuesta del 92%. El grado de satisfacción global obtenido fue: 50% muy satisfecho, 41% bastante satisfecho y 9% satisfecho. Los resultados obtenidos se recogen en la Figura 3.
Discusión
En España, los PMM han sido analizados en diferentes ámbitos sanitarios como son los centros ambulatorios, los centros de atención a drogodependientes y las oficinas de farmacia comunitaria. Las publicaciones relacionadas con estos PMM varían en función de la modalidad de cada comunidad autónoma, pero en general muestran resultados de sus experiencias desde diferentes perspectivas, analizando aspectos de efectividad, aspectos económicos y también aspectos de calidad percibida mediante encuestas de satisfacción a los pacientes tratados con metadona8,11,17,22-32. Sin embargo, estos datos responden a objetivos diferentes a los expuestos en este artículo, ya que se centran en los PMM, mientras que nuestro objetivo consiste en describir la centralización del proceso de adquisición, elaboración, distribución y dispensación de metadona a los CAIDs de la Comunidad de Madrid y el papel del farmacéutico en dicho proceso. Esto hace que no se puedan comparar nuestros resultados con los publicados dadas las funciones implementadas hasta el momento.
En la Comunidad de Madrid cabe destacar que la dispensación de metadona se puede realizar desde los CAIDs o desde las farmacias comunitarias que se encuentran dentro del Programa de Mantenimiento con metadona en oficinas de farmacia de Madrid, que se creó en 1997, gracias al convenio de colaboración firmado entre la Consejería de Sanidad y Asuntos Sociales (Agencia Antidroga) y el Colegio Oficial de Farmacéuticos de Madrid33.
Sin embargo, en la Comunidad de Madrid nunca antes se había centralizado el procedimiento de adquisición, elaboración, distribución y dispensación de metadona a los CAIDs. Este hecho, además de suponer una experiencia pionera en nuestra comunidad, se realiza bajo la dirección y responsabilidad de un SFH, siendo la primera vez que farmacéuticos especialistas realizan tareas asistenciales en el ámbito de las adicciones, lo cual ha permitido una serie de beneficios que se detallan a continuación. El primero de ellos ha sido la optimización de los recursos sanitarios del Servicio Madrileño de Salud, debido a que, por una parte, se han aprovechado, con mínimas adaptaciones, los recursos ya existentes en el propio SFH y, por otra parte, se han diseñado y adjudicado procedimientos para la adquisición de metadona, envases para la dosificación personalizada en los CAIDs y transporte de metadona. Todo ello ha supuesto una mayor eficiencia del proceso, lo que a su vez contribuye a la sostenibilidad del sistema de salud.
En segundo lugar destacamos la reducción de la variabilidad intercentros mediante la elaboración de los procedimientos normalizados de trabajo que han permitido la unificación y homogeneización de los procesos.
También se mejora la calidad del medicamento, al centralizar la elaboración de solución de metadona en un único centro, en este caso un SFH, que además de disponer de mejores instalaciones, incorpora la elaboración de fórmulas magistrales siguiendo la Guía de buenas prácticas de preparación de medicamentos en Servicios de Farmacia Hospitalaria19, y existiendo un sistema de trazabilidad durante el proceso de elaboración. Todo ello proporciona mayor seguridad para el paciente.
Por otra parte, y dada la alta complejidad en cuanto al elevado número de pacientes incluidos en el PMM y las grandes cantidades de metadona en solución que se tienen que elaborar y para garantizar un correcto suministro a todos los CAIDs, se justifica la necesidad de planificar por adelantado el proceso de elaboración de manera que sea viable para el SFH.
Los resultados de la encuesta de calidad percibida muestran un alto grado de satisfacción asistencial en los diferentes CAIDs. Cabe destacar que no se ha registrado ninguna puntuación inferior a satisfecho, obteniendo, como puede observarse, un predominio claro de resultados con la opción más satisfactoria “muy satisfecho”. Además, se destaca el alto grado de satisfacción (muy satisfecho o bastante satisfecho) del 81,8% con la eficacia y rapidez de la resolución de incidencias por parte de los profesionales del SFH, y del 95,4% (bastante o muy satisfecho) con la atención y trato recibido por los profesionales del SFH.
Como limitación al proceso de centralización del PMM destaca la falta de informatización de todo el proceso asistencial de prescripción, dispensación y administración de metadona que posibilite a los médicos prescriptores, farmacéuticos especialistas y otros profesionales de los CAIDs, entre otros beneficios, conocer la trazabilidad completa de las prescripciones, disponer de una historia clínica electrónica que recoja los aspectos clínicos del paciente e historia farmacoterapéutica, de la cual se pudiera obtener información sobre la efectividad, seguridad, eficacia y adherencia de la metadona.
De esta limitación surgen nuestros próximos retos y mejoras que queremos aportar, como son la implementación de un programa informático que integre todos los procesos relacionados con el uso de la metadona y aumentar la integración del farmacéutico especialista en los equipos clínicos multidisciplinares que atienden a los pacientes drogodependientes aportando un valor añadido en su atención y en la mejora de los resultados en salud32. El primero de ellos ya se está llevando a cabo y el segundo está en vías de desarrollo, ya que el farmacéutico especialista está trabajando en la actualización del protocolo farmacoterapéutico del PMM de la Comunidad de Madrid junto con otros profesionales del Servicio Madrileño de Salud.
Además, y debido al corto periodo de estabilidad que se asigna a la metadona en solución20, actualmente se están estudiando posibles mejoras en la formulación mediante la incorporación de conservantes, así como estudios de estabilidad fisicoquímica y microbiológica que permitan aumentar el periodo de validez de la fórmula. Estas mejoras permitirán no sólo una más óptima organización del circuito, sino además una mejor capacidad de adaptar la dispensación a las características individuales del paciente.
Por todo lo anteriormente expuesto, y a modo de conclusión, podemos afirmar que queda consolidada toda la primera fase del proyecto, que se han cumplido los objetivos iniciales que se pretendían asumir tras la publicación de la Resolución 189/201818 y que este circuito puede servir de modelo a otras comunidades autónomas. Por tanto, la centralización del PMM en los SFH posibilita un cambio de modelo de asistencia farmacoterapéutica al incorporar al proceso asistencial de los pacientes dependientes de opiáceos, las competencias, habilidades y conocimiento del farmacéutico especialista en farmacia hospitalaria. Además, permite disponer de la experiencia y los recursos para afrontar este reto asistencial de forma óptima, para beneficio de los pacientes y resto de profesionales sanitarios, contribuyendo a la sostenibilidad del sistema de salud.
Bibliography
Agencia Española de Medicamentos y Productos Sanitarios. Ficha técnica Metasedin 30 mg comprimidos y 40 mg comprimidos (Internet). Madrid. Centro de información de medicamentos (CIMA) (accessed 10/07/2019). Available at: https://cima.aemps.es/cima/pdfs/es/ft/62423/FT_62423.html.pdf [ Links ]
Payte JT. A brief history of methadone in the treatment of opioid dependence: a personal perspective. J Psychoactive Drugs. 1991;23(2):103-7. DOI: 10.1080/02791072.1991.10472226 [ Links ]
Dole VP, Nyswander M. A medical treatment for diacetylmorphine (heroin) addiction. A clinical trial with methadone hydrocloride. JAMA. 1965;193:646-50. DOI: 10.1001/jama.1965.03090080008002 [ Links ]
Kreek MJ, Borg L, Ducat E, Ray B. Pharmacotherapy in the treatment of addiction: Methadone. J Addict Dis. 2010;29(2):200-16. DOI: 10.1080/10550881003684798 [ Links ]
Joseph H, Stancliff S, Langrod J. Methadone maintenance treatment (MMT): a review of historical and clinical issues. MtSinai JMed. 2000;67(5-6):347-64. [ Links ]
Corsi KF, Lehman WK, Booth RE. The effect of methadone maintenance on positive outcomes for opiate injection drug users. J Subst Abuse Treat. 2009;37(2):120-6. DOI: 10.1016/j.jsat.2008.11.004 [ Links ]
Mattick RP, Breen C, Kimber J, Davoli M. Methadone maintenance therapy versus no opioid replacement therapy for opioid dependence. Cochrane Database Syst Rev. 2003;(2):CD002209. [ Links ]
Jiménez Treviño L, Sáiz Martínez PA, Gutiérrez Cienfuegos E, Bascarán Fernández MT, Carreño Rendueles E, González-Quiros Menéndez de Luarca M, et al. Valoración transversal tras quince años en una muestra de adictos a opiáceos en Asturias. Adicciones. 2000;12(4):507. DOI: 10.20882/adicciones.661 [ Links ]
Barnett PG, Hui SS. The cost-effectiveness of methadone maintenance. MtSinai JMed. 2000;67(5-6):365-74. [ Links ]
Kleber HD. Methadone maintenance 4 decades later. JAMA. 2008;300(19):2303. DOI: 10.1001/jama.2008.648 [ Links ]
Torrens M, Fonseca F, Castillo C, Domingo-Salvany A. Methadone maintenance treatment in Spain: the success of a harm reduction approach. Bull World Health Organ. 2013;91(2):136-41. DOI: 10.2471/BLT.12.111054 [ Links ]
Orden de 20 de mayo de 1983 por la que se regulan los tratamientos con metadona. Boletin Oficial del Estado, n.º 127 (28 de mayo de 1983). [ Links ]
Orden de 31 de octubre de 1985 por la que se regulan los tratamientos de deshabituación con metadona dirigidos a toxicómanos dependientes de opiáceos. Boletin Oficial del Estado, n.º 269 (9 de noviembre de 1985). [ Links ]
Real Decreto 1131/1990, de 14 de septiembre, por el que se modifica el artículo 3.3 del Real Decreto 75/1990, de 19 de enero, por el que se regulan los tratamientos con opiáceos de personas dependientes de los mismos. Boletín Oficial del Estado, n.º 224 (18 de septiembre de 1990). [ Links ]
Real Decreto 75/1990, de 19 de enero, por el que se regulan los tratamientos con opiáceos de personas dependientes de los mismos. Boletin Oficial del Estado, n.º 20 (23 de enero de 1990). [ Links ]
Real Decreto 5/1996, de 15 de enero, sobre modificación del Real Decreto 75/1990, de 19 de enero, por el que se regulan los tratamientos con opiáceos de personas dependientes de los mismos y de ampliación de su anexo. Boletin Oficial del Estado, n.º 44 (20 de febrero de 1996). [ Links ]
Meneses Falcón C, Charro Baena B. Los programas de mantenimiento con metadona en Madrid: evolución y perfil de los usuarios. Madrid: Universidad Pontificia Comillas; 2000. [ Links ]
Resolución del director general de coordinación de la asistencia sanitaria por la que se encomienda al Hospital Universitario Infanta Leonor las tareas de suministro diario de metadona a los centros de atención integral a drogodependientes de la Subdirección General de Asistencia en Adicciones del Servicio Madrileño de Salud. Dirección General de Coordinación de la Asistencia Sanitaria, n.º 189/2018 (27 de febrero de 2018). [ Links ]
Guía de buenas prácticas de preparación de medicamentos en servicios de farmacia hospitalaria (Internet). Madrid: Ministerio de Sanidad, Servicios Sociales e Igualdad; 2014 Available at: http://www.msssi.gob.es/profesionales/farmacia/pdf/GuiaBPP3.pdf [ Links ]
Agencia Española de Medicamentos y Productos Sanitarios, coord. Formulario Nacional (Internet). 2ª ed. Madrid: Ministerio de Sanidad, Consumo y Bienestar Social. 2019. Available at: https://www.boe.es/biblioteca_juridica/abrir_pdf.php?id=PUB-NT-2019-112 [ Links ]
Real Decreto 1675/2012, de 14 de diciembre, por el que se regulan las recetas oficiales y los requisitos especiales de prescripción y dispensación de estupefacientes para uso humano y veterinario. Boletín Oficial del Estado, n.º 313 (29 de diciembre de 2012). [ Links ]
Carbó PA. La perspectiva de los usuarios en un programa de mantenimiento con metadona: elementos evaluativos. Intervencion Psicosocial. 2000;9(2):217-31. [ Links ]
Díez J, Ramos E, Blas C, Fernández B, Fortes B. Evaluación del Programa de Mantenimiento con Metadona en Bizkaia en 2003: aspectos metodológicos. Pharmaceutical Care España. 2006;8(2):72-80. [ Links ]
Fernández Miranda JJ. Efectividad de los programas de mantenimiento con metadona. Adicciones. 2005;17(2):167-80. [ Links ]
Fernández Miranda J. Efectividad de los programas de mantenimiento con metadona. Una revisión de los resultados de los estudios de evaluación. Med Clín. 2001;116(4):150-4. DOI: 10.1016/S0025-7753(01)71753-8 [ Links ]
Markez Alonso I, Iraurgi Castillo I, Póo Ruiz M. Programas de mantenimiento con metadona en el País Vasco: dispositivos específicos y oficinas de farmacia. Trastornos Adictivos. 2002;4(3):171-80. DOI: 10.1016/S1575-0973(02)70073-1 [ Links ]
Puigdollers E, Cots F, Brugal MT, Torralba L, Domingo-Salvany A, Costas F. Methadone maintenance programs with supplementary services: a cost-effectiveness study. Gac Sanit. 2003;17(2):123-30. [ Links ]
Brugal MT, Domingo-Salvany A, Puig R, Barrio G, García de Olalla P, de la Fuente L. Evaluating the impact of methadone maintenance programmes on mortality due to overdose and aids in a cohort of heroin users in Spain. Addiction. 2005;100(7):981-9. DOI: 10.1111/j.1360-0443.2005.01089.x [ Links ]
Del Pozo Iribarría J, Soldevilla Íñiguez D, Murga García JA, Antoñanzas Villar F. Costs-analysis of methadone program in the autonomous community La Rioja, Spain. Rev Esp Salud Publica. 2012;86(5):543-9. DOI: 10.4321/S1135-57272012000500008 [ Links ]
Escudero Torras M. Evaluación a 4 años de una muestra de 40 participantes en un programa de mantenimiento con metadona en Barcelona. Adicciones. 2000;12(3):383. DOI: 10.20882/adicciones.649 [ Links ]
García Llaneza JA. Evaluación de los resultados de un programa de comunidad terapéutica con mantenimiento de metadona. Liberaddictus. 2009; 105:25-34. [ Links ]
Rodríguez Reinado C, Millán Carrasco A, Venegas Sánchez J, March Cerdá JC. Oportunidades de mejora del servicio de metadona en atención primaria, desde el punto de vista profesional. Adicciones. 2010;22(3):207-16. [ Links ]
Concierto entre la Consejería de Sanidad y el Colegio Oficial de Farmacéuticos de Madrid. 2015. Available at: http://www.madrid.org/bvirtual/BVCM017739.pdf [ Links ]
Recibido: 05 de Diciembre de 2019; Aprobado: 22 de Marzo de 2020











 text in
text in