Introducción
Según el ABC European Consensus, la adherencia al tratamiento incluye una participación cooperativa, voluntaria y activa por parte del paciente en realizar las recomendaciones establecidas por los profesionales sanitarios encargados de sus cuidados. Este proceso involucra tres etapas: la iniciación, incluyendo el momento donde el paciente toma la primera dosis del fármaco prescrito, la implementación, periodo en el que el cumplimiento de la terapia prescrita es correcto y, finalmente, la discontinuación, momento en que el paciente abandona el fármaco por algún motivo1.
La adherencia terapéutica es un factor determinante en la consecución de los resultados clínicos, especialmente para aquellas patologías crónicas. En términos generales, cuanto peor es la adherencia, peores son los resultados en salud y, consecuentemente, la calidad de vida. Asimismo, también es un determinante crítico en los costes sanitarios.
En los últimos años, algunos autores están replanteando las definiciones más tradicionales sobre la adherencia y su abordaje1. En este sentido aparece el concepto de adherencia primaria, en contraposición a la más clásica ahora considerado como adherencia secundaria1. De esta manera, la no adherencia primaria (NAP) es definida como no recoger la medicación prescrita de su farmacia en un periodo de tiempo corto desde su prescripción, lo cual supone una desviación relevante del plan farmacológico previsto. La prevalencia de la misma ha sido analizada en varios estudios a lo largo de la última década, especialmente en pacientes con enfermedades crónicas (diabetes, hipertensión, asma, etc.)2-4. En el paciente que vive con infección por VIH (PVVIH), el estudio de Borrego et al. realizado en España5 muestra que la prevalencia de esta situación ocurre en un tercio de los pacientes, lo que condiciona la consecución de los objetivos en relación con la farmacoterapia de estos sujetos, más, si cabe, en la actualidad, en un contexto en el que estos pacientes están envejeciendo y en el que las comorbilidades aparecen con mayor frecuencia y celeridad que en población no VIH6,7.
La nueva definición de la atención farmacéutica (AF) aboga por la vinculación de estos profesionales con los pacientes y el resto del equipo multidisciplinar para alinear y alcanzar objetivos en relación con la farmacoterapia, realizando un seguimiento longitudinal y llevando a cabo intervenciones en base a la complejidad asistencial que manifiestan los mismos. Esta metodología se conoce como CMO, de acuerdo con los tres pilares fundamentales en los que se asienta: la estratificación (Capacidad), los objetivos en relación con la farmacoterapia (Motivación) y la incorporación de las nuevas tecnologías en el seguimiento mantenido de los pacientes (Oportunidad)8,9.
Diferentes estudios han demostrado que la aplicación de esta metodología de trabajo en estos pacientes reporta mejoría en resultados de salud y experiencia asistencial, pero ningún estudio ha analizado, hasta ahora, su utilidad para el abordaje de la mejora respecto a la NAP10-12.
El objetivo de este estudio fue estimar la efectividad de la AF, basada en la metodología CMO (Capacidad, Motivación y Oportunidad), para la mejora de la NAP al tratamiento concomitante en PVVIH, en tratamiento antirretroviral activo (TAR).
Como objetivos secundarios se incluyeron también estimar la efectividad de la AF en la mejora de la adherencia secundaria al tratamiento concomitante y al TAR.
Métodos
Estudio longitudinal, prospectivo, multicéntrico, de intervención sanitaria estructurada, realizado entre septiembre de 2019 y septiembre de 2020.
Se incluyeron en el estudio PVVIH mayores de 18 años, en TAR, al menos, durante un año previo a la inclusión, que aceptaron participar en el estudio, otorgando el correspondiente consentimiento informado y con prescripción, por cualquier médico, de medicación concomitante al TAR 6 meses antes del inicio del estudio y, adicionalmente, nueva prescripción de fármacos concomitantes al inicio del periodo de investigación. Se excluyeron del mismo a aquellos pacientes participantes en ensayos clínicos durante el periodo completo de seguimiento, embarazadas y los que no firmaron el consentimiento informado.
Se recogieron las siguientes variables demográficas: edad, sexo, factor de riesgo de adquisición de la enfermedad y estatus económico (bueno, malo o muy malo), relación con los profesionales sanitarios (bueno, malo o muy malo), conocimiento del tratamiento y la patología (bueno, malo, muy malo); variables clínicas basales y relacionadas con el VIH: carga viral plasmática (cop/ml), cifra de CD4 (cél./µl), cociente C4/CD8, colesterol (mg/dl), HDL colesterol (mg/dl), triglicéridos (mg/dl), hemoglobina glicosilada (g/dl), tensión arterial (mmHg), y variables farmacoterapéuticas: TAR prescrito durante el estudio, tipo y número de fármacos concomitantes y presencia o no de polifarmacia (definido como prescripción de más de cinco medicamentos al día)13.
El periodo de seguimiento de cada sujeto fue de 6 meses tras la inclusión en el estudio. Aquellos pacientes que no acudieron a dos visitas consecutivas de seguimiento farmacoterapéutico establecidas fueron retirados del estudio y considerados abandonos, no reemplazándose por otros.
Todos los pacientes fueron seguidos según la metodología CMO (Figura 1). Inicialmente, todos los pacientes fueron estratificados en tres niveles, según las variables recogidas en el modelo publicado por la Sociedad Española de Farmacia Hospitalaria (SEFH) para el paciente VIH14. Se llevó a cabo una AF más o menos intensiva de acuerdo con las intervenciones predeterminadas para cada nivel de atención. En cada visita presencial al Servicio de Farmacia Hospitalaria se llevó a cabo una entrevista motivacional basada en el alineamiento y consecución de los objetivos en relación con la farmacoterapia que cada paciente tuviera, según el momento de la evolución de las patologías descritas y la experiencia previa que el paciente hubiera mostrado con su farmacoterapia prescrita. Cada entrevista motivacional se dividió en dos partes: la primera de identificación de resistencias y, a continuación, generación de discrepancias internas o mantenimiento de las fortalezas mostradas. En cada entrevista se establecieron o reevaluaron objetivos farmacoterapéuticos, en consenso con el resto del equipo médico responsable del cuidado del paciente en cada momento.
Para desarrollar el pilar de oportunidad, se creó y desarrolló una página web: http://www.proyecto-pricmo.com (inoperativa actualmente) (Figura 2). En ella se incorporaron contenidos informativos sobre la importancia de la adherencia, con vídeos, infografías, dípticos, enlaces a otras webs, artículos y otra información relevante en esta materia. Esta herramienta estuvo disponible y actualizada durante todo el proyecto, de manera que los pacientes pudieran acceder en cualquier momento a los contenidos publicados de acuerdo con sus competencias digitales.
A todos los pacientes se les facilitaron herramientas de contacto permanente con los farmacéuticos del estudio (teléfono, correo electrónico, etc.) para resolver cualquier incidencia en relación con su tratamiento en cualquier momento.
La variable principal fue el porcentaje de pacientes considerados adherentes primarios a la medicación concomitante prescrita en el momento basal, analizando los 6 meses previos, frente al mismo valor en los pacientes al finalizar el estudio.
Se definió adherencia primaria a la que tiene en cuenta el periodo entre que el tratamiento se prescribe y el paciente lo tiene en su poder, tras una dispensación en farmacia comunitaria. El límite temporal máximo para definir esta variable se limitó a un periodo de 14 días.
Para el objetivo secundario, se comparó el porcentaje de pacientes considerados adherentes secundarios al tratamiento concomitante durante los 6 meses previos al inicio del estudio frente al mismo valor en los pacientes al finalizar el estudio.
La adherencia secundaria al tratamiento concomitante se definió como el número total de días de toma de medicación de acuerdo con las pautas del prescriptor durante el periodo de seguimiento15. Para ser considerado adherente se valoraron, conjuntamente, tanto los registros de dispensación en oficina de farmacia (se consideró adherente sólo si el cociente adherencia multiintervalo de dispensación fue superior al 90%) como la valoración positiva del cuestionario ARMS-e16.
También se comparó el porcentaje de pacientes adherentes al TAR durante los 6 meses antes y después del inicio del estudio. Para ser considerado adherente se valoraron, conjuntamente, tanto los registros de dispensación de pacientes externos (se consideró adherente sólo si el cociente adherencia multiintervalo de dispensación era superior al 90% y la valoración del cuestionario validado SMAQ17 era positiva).
El tratamiento concomitante y las correspondientes dispensaciones en oficina de farmacia se recogieron de las aplicaciones informáticas de los diferentes sistemas de salud de los hospitales participantes. El resto de las variables se obtuvieron durante las respectivas entrevistas presenciales de los pacientes en las consultas de AF a pacientes externos de los servicios de farmacia participantes y la historia de salud única de los centros participantes.
Respecto al análisis estadístico, las variables cuantitativas se resumieron con medias y desviaciones típicas, o bien con medianas y percentiles P25 y P75 en caso de distribuciones asimétricas, y las variables cualitativas con frecuencias y porcentajes. Para comparar la media de las variables cuantitativas se realizó la prueba t de Student para muestras relacionadas y el test no paramétrico de Wilcoxon. Previamente se comprobó la normalidad de los datos con el test de Kolmogorov-Smirnov, con el fin de determinar la utilización de pruebas paramétricas o no paramétricas. Para analizar la relación entre variables cuantitativas se utilizó el test de McNemar. Para establecer la relación entre las diferentes variables cuantitativas se empleó el coeficiente de correlación de Spearman y el test no paramétrico de U de Mann-Withney para muestras no relacionadas. El análisis de los datos se realizó con el programa informático R studio v 1.1.456.
El estudio fue aprobado por el Comité de Ética de la Investigación de Sevilla-Sur (1841N-17).
Resultados
Un total de 65 pacientes fueron reclutados para participar en el estudio. Finalmente, 61 fueron incluidos en el análisis estadístico, excluyéndose 4 por pérdidas de seguimiento. Las características basales de los sujetos incluidos en el estudio se muestran en la tabla 1. El 72,0% fueron hombres, con una mediana de edad de 53 años (IQR: 51-58).
Tabla 1. Características basales de los pacientes del estudio.
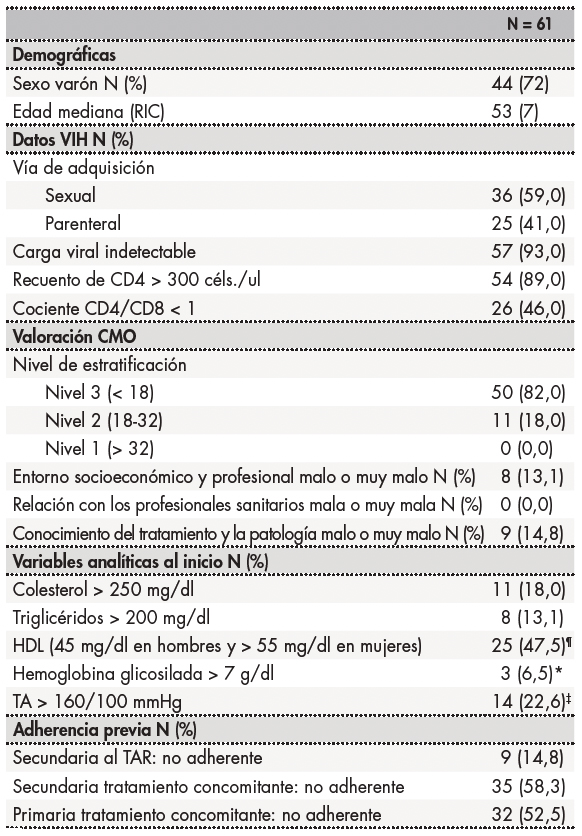
¶solo medido en 57 (93,4) pacientes;
*medido en 46 (75,4) pacientes;
‡medido en 52 (85,2) pacientes.
HDL: High Density Lipoprotein; RIC: rango intercuartílico; TA: tensión arterial; TAR: tratamiento antirretroviral.
Respecto al tipo de TAR prescrito, por familias fueron: dos análogos de la transcriptasa inversa (INTI)+ un inhibidor de la integrasa: 42,6%; dos INTI+ un no nucleósido: 16,4%; dos INTI+ un inhibidor de la proteasa: 11,5%, y otras combinaciones (mono/biterapias): 29,5%. Durante el seguimiento del estudio hubo tres cambios de TAR por decisión clínica, quedando la distribución de la prescripción en: dos INTI+ un inhibidor de la integrasa: 47,5%; dos INTI+ un no nucleósido: 11,5%; dos INTI+ un inhibidor de la proteasa: 11,5%, y otras combinaciones (mono/biterapias): 29,5%. No hubo diferencias significativas respecto a los porcentajes de prescripción.
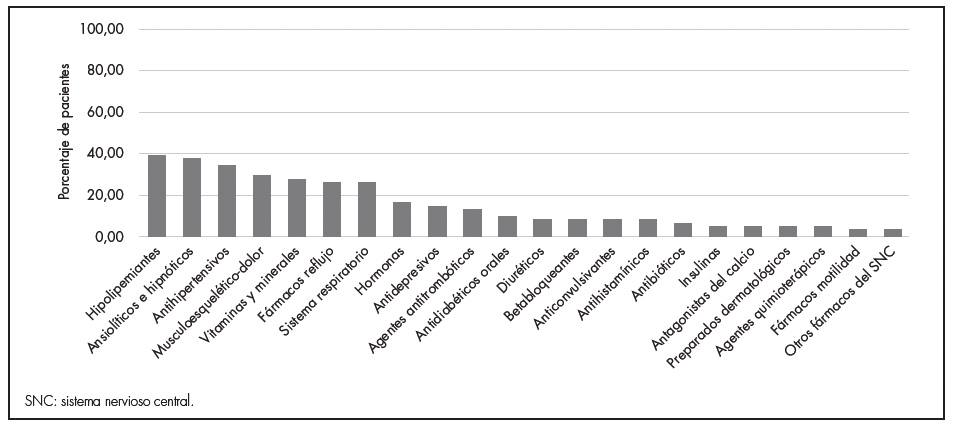
Respecto a la mediana de fármacos concomitantes, fue de 7 (IQR: 5-8). Los tratamientos más prescritos fueron hipolipemiantes, ansiolíticos e hipnóticos y antihipertensivos (Figura 3). El 60,6% de los pacientes tenían presencia de polifarmacia.
Respecto a la variable principal del estudio, el porcentaje de pacientes considerados no adherentes primarios al inicio fue del 52,5% (n = 32), mientras que a la finalización del seguimiento fue del 4,9% (n = 3, p < 0,001). La evolución de las variables secundarias de adherencia al tratamiento concomitante y al TAR se observan en la figura 4. En ambos casos se encontraron mejoras significativas a la finalización del seguimiento (p < 0,001).
Discusión
El presente estudio ha puesto de manifiesto cómo una intervención farmacéutica basada en la estratificación de pacientes, la entrevista motivacional y el uso de las nuevas tecnologías, consigue mejorar la adherencia primaria a la medicación concomitante en PVVIH en TAR activo.
Dependiendo de la definición, el contexto y la metodología utilizada, la NAP en pacientes con patologías crónicas ha alcanzado diferentes niveles de prevalencia según la bibliografía disponible, aunque la mayoría de los autores coinciden en situar alrededor del 20%18. Respecto a los fármacos más comúnmente implicados, las cifras oscilan en torno al 25% en hipolipemiantes, osteoporóticos y antiasmáticos, 16% en antihipertensivos, 12% en antidepresivos y 10% en antidiabéticos19,20. Estos fármacos coinciden, en su mayoría, con el perfil de prescripción concomitante de la población incluida en nuestro estudio, aunque el punto de partida inicial fuera, en nuestro caso, incluso, sustancialmente superior (52,5%), lo cual da una idea de la complejidad respecto a la situación basal de esta problemática en la población sobre la que se realizó la intervención y la fortaleza de los resultados de la misma.
Según la literatura publicada, en población crónica general, es conocido cómo la adherencia se ve modificada por numerosos factores. Entre los más descritos están los socioeconómicos (por ejemplo, disponibilidad de empleo), los relacionados con el sistema de salud (por ejemplo, acceso a fármacos o relación con profesionales sanitarios), con la enfermedad (como la presencia de síntomas) o, incluso, con el propio paciente (nivel educativo, aspectos cognitivos, creencias y actitudes sobre la salud). Más concretamente, en el PVVIH, particularmente el de edad avanzada, la creciente aparición del fenómeno de la polifarmacia y la complejidad farmacoterapéutica están relacionándose cada vez con mayor insistencia con la no adherencia al tratamiento concomitante21,22. En este caso, ambos factores también estuvieron presentes en nuestro estudio, ya que la edad mediana superaba el umbral considerado clave para el abordaje del PVVIH de edad avanzada, 50 años13, y la presencia de polifarmacia también fue superior a lo conocido en nuestro entorno, más del 60%23. Diferentes autores han propuesto intervenciones concretas para evitar esta problemática en diferentes tipos de pacientes. En los últimos años, además, muy orientadas a la incorporación de las nuevas tecnologías al seguimiento de los pacientes, por ejemplo, incorporando recordatorios diarios a través de servicio de mensajes cortos incluso en ensayos clínicos aleatorizados24. Otros enfoques también han incluido el uso de llamadas a través del teléfono móvil o aplicaciones específicas para abordar la importancia clínica del diagnóstico adecuado y el inicio inmediato de tratamiento adecuado como refuerzo de la adherencia primaria25,26.
También, en los últimos años, se identifica con mayor relevancia los beneficios, en el abordaje de la adherencia a fármacos en pacientes con patologías crónicas, de la entrevista motivacional27-29.
Dado el carácter cada vez más complejo y multidimensional de los PVVIH, el presente estudio ha planteado la necesidad de un abordaje diferente, no solo multidisciplinar o utilizando un determinado elemento de soporte de mejora, como las nuevas tecnologías o la entrevista motivacional, sino que, sobre todo, se ha centrado en conocer las características individuales de cada individuo y diseñar intervenciones específicas individualizadas y longitudinales de acuerdo con su complejidad21,30. Ello ha sido posible añadiendo y tomando como base la estratificación realizada, que analiza y tiene en cuenta la influencia de las diferentes variables divididas en dimensiones de salud específicas para cada individuo. A partir de las mismas, se realizó una atención individualizada y modulada en intensidad a lo largo del tiempo. Esta metodología ha sido ya contrastada en estudios anteriores en los que se observa mejoría en resultados en salud, basados en la mejora de la adherencia secundaria a los tratamientos10,11. En esta ocasión, la incorporación de un entorno web específico con material tanto escrito como en formato visual ha reforzado más si cabe el mensaje de una forma más dinámica y adaptada a cada tipología de paciente, aspecto que, hasta este proyecto, no se había realizado anteriormente. Ello ha reforzado el enfoque centrado en el paciente y no tanto en los problemas relacionados con el medicamento, indicando como prioridad la consecución de los objetivos relacionados con la farmacoterapia a alcanzar de manera más próxima para cada tipología de paciente incluido en el estudio. La misma, secundariamente, ha tenido como repercusión una mejora, también significativa, tanto en la adherencia secundaria a la medicación concomitante como al TAR, donde ya la situación de partida era muy alta.
Este estudio presenta varias limitaciones. La primera de ellas es que el mismo se diseñó considerando que hubiera sólo un grupo de intervención, careciendo de grupo control. Dada la creciente expansión, formación y conocimiento del modelo por parte de los farmacéuticos de hospital y los resultados obtenidos en estudios anteriores en los últimos años, se consideró que podría existir un sesgo en los participantes al asemejar intervenciones ante la existencia de un posible grupo control. Por ello, se estimó que la mejor forma de considerar la influencia de la intervención farmacéutica fuera un diseño antes-después en que cada paciente fuera su propio control. Adicionalmente, el periodo de seguimiento del estudio (6 meses) es considerado relativamente corto dentro de la vida de un PVVIH con tratamiento crónico. Sin embargo, metodológicamente, es lo suficientemente robusto como para determinar el impacto de una intervención sanitaria estructurada, así como la planificación y alcance de los objetivos establecidos en un periodo concreto de la vida de estos pacientes, ya que estos son dinámicos y están condicionados por las diferentes dimensiones de salud que manifiestan.
Adicionalmente, tampoco se indagó, por no existir clasificación previa publicada en la bibliografía, en los motivos por los cuales los pacientes no fueron adherentes primarios a la medicación (por ejemplo, falta de confianza en el diagnóstico, costes inasumibles, incompatibilidad con el estilo de vida, etc.). Al no tener disponible esa información para el periodo previo a la intervención y no existir una clasificación consensuada para categorizar esa situación, se consideró más adecuado para los fines del proyecto conocer exclusivamente la prevalencia.
Futuras líneas de investigación nos permitirán conocer sobre qué dimensiones de los pacientes (cognitiva, socioeconómica, nutricional, autocuidado, malestar y ansiedad, etc.) tiene mayor influencia la metodología aplicada o si existen umbrales de polifarmacia o complejidad farmacoterapéutica que predigan qué pacientes van a ser más no adherentes primarios y abordarlos de manera más individualizada si cabe, tanto con ayuda tecnológica en los sistemas de información sanitaria como con la metodología propuesta. Por otra parte, investigaciones con una secuencia temporal más larga nos permitirán identificar los resultados en salud y los beneficios asistenciales (ahorro en visitas a consultas extraordinarias, ingresos hospitalarios, etc.) que supone una estrategia basada en la referida metodología.
En conclusión, la intervención farmacéutica diseñada en base al modelo de AF CMO que utiliza modelos de estratificación de pacientes, el establecimiento de objetivos con relación a la farmacoterapia, el uso de la entrevista motivacional, así como el seguimiento longitudinal que permiten las nuevas tecnologías, mejora la adherencia primaria y secundaria a la medicación concomitante y al TAR.
Aportación a la literatura científica
La no adherencia primaria a la medicación concomitante es una problemática relevante en la asistencia al paciente con infección por VIH.
La metodología de atención farmacéutica CMO, basada en estratificación, entrevista motivacional y nuevas tecnologías consigue mejorar tanto la adherencia primaria como secundaria en estos pacientes.