My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Farmacia Hospitalaria
On-line version ISSN 2171-8695Print version ISSN 1130-6343
Farm Hosp. vol.46 n.3 Toledo May./Jun. 2022 Epub July 11, 2022
https://dx.doi.org/10.7399/fh.11724
ORIGINALES
Vancomicina frente a daptomicina como tratamiento de las bacteriemias asociadas a catéter y causadas por grampositivos en el paciente oncológico
1Servicio de Farmacia, Complejo Hospitalario Universitario de Canarias, Tenerife. España
2Servicio de Enfermedades Infecciosas, Complejo Hospitalario Universitario de Canarias, Tenerife. España
3Unidad de Oncología, Complejo Hospitalario Universitario de Canarias, Tenerife. España
Objetivo:
Analizar la eficacia y seguridad de la daptomicina frente a la vancomicina en el tratamiento de las infecciones del torrente sanguíneo asociadas a catéter vascular en pacientes oncológicos.
Método:
Se realizó un estudio retrospectivo que incluyó a los pacientes ingresados en la Unidad de Oncología-Médica entre 2010-2018 con infección del torrente sanguíneo asociada a catéter vascular causada por grampositivos, y que fueron tratados con vancomicina o daptomicina. Como objetivos principales se determinaron la tasa de mortalidad por todas las causas a los 30 días, el reingreso hospitalario a los 30 días y la duración de la estancia hospitalaria.
Resultados:
El estudio incluyó 70 pacientes con infecciones del torrente sanguíneo asociadas a catéter vascular: el 61,4% (n = 43) recibió vancomicina y el 38,6% (n = 27) daptomicina. El 78,5% (n = 55) de las bacterias aisladas presentaron una concentración mínima inhibitoria de vancomicina ≤ 1 μg/ml. No se observaron diferencias entre ambos grupos de pacientes en cuanto a la tasa de mortalidad a 30 días (32,6% [n = 14] frente al 29,6% [n = 8]; p = 0,797), la tasa de reingreso a 30 días (30,2% [n = 13] frente al 29,6% [n = 8]; p = 0,957) o la duración de la hospitalización (18,9 frente a 16,5 días; p = 0,562). La tasa de nefrotoxicidad fue equivalente en ambos grupos: 7% (n = 3) para vancomicina frente al 7,4% (n = 2) para daptomicina (p = 0,946).
Conclusiones:
Nuestros resultados muestran que ambos antibióticos son equivalentes en su seguridad y eficacia. Por ello, vancomicina debería seguir siendo el tratamiento de elección para la infección del torrente sanguíneo asociada a catéter vascular, especialmente en centros con una baja prevalencia de cepas con una susceptibilidad disminuida a vancomicina.
PALABRAS CLAVE Daptomicina; Vancomicina; Bacteriemia; Catéter venoso central
Introducción
Los catéteres venosos centrales se utilizan habitualmente para administrar tratamiento antineoplásico en pacientes oncológicos. No obstante, su uso no está exento de complicaciones, debidas principalmente a infecciones del torrente sanguíneo asociadas a catéter vascular (ITSAC), que provocan una mortalidad de entre el 12 y el 25%1,2. A menudo son causadas por bacterias grampositivas (75%)1,3. Puesto que un 80% de las cepas de Staphylococcus coagulasa-negativo son resistentes a meticilina y que se ha producido un aumento en la prevalencia del Staphylococcusaureus resistente a meticilina, la vancomicina y la daptomicina se han convertido en el tratamiento de elección en cuadros de ITSAC2,4,5. Aunque hasta ahora ambos antibióticos han demostrado ser eficaces en el tratamiento de las ITSAC, son pocos los estudios comparativos que aborden su efectividad y seguridad6.
En este estudio se presenta un análisis de la efectividad y seguridad de la daptomicina frente a la vancomicina en pacientes con tumores sólidos en el contexto de la práctica clínica diaria.
Métodos
Diseño del estudio y criterios de selección de los pacientes
En este estudio retrospectivo se evaluó la efectividad y seguridad de la vancomicina en comparación con la daptomicina en pacientes con tumores sólidos e ITSAC causadas por grampositivos. Todo paciente oncológico con ITSAC causada por grampositivos hospitalizado durante un período de ocho años (2010-2018) en un hospital de 822 camas situado en Tenerife (España) podía ser candidato a ser reclutado para el estudio. Para ser incluidos, los pacientes debían tener una edad ≥ de 18 años, un tumor sólido, presentar una infección por bacterias grampositivas y certeza de que el origen de la bacteriemia no pudiera ser otro que un catéter venoso central. Los pacientes debían estar recibiendo tratamiento con vancomicina o daptomicina. El tratamiento se consideró empírico cuando se administraba una pauta antimicrobiana dentro de las 24 horas de extracción de la muestra sanguínea, sin conocerse aún si existía susceptibilidad. La elección de vancomicina o daptomicina dependía de la preferencia de cada facultativo.
Los pacientes que presentaran malignidad hematológica o neutropenia quedaron excluidos del estudio, así como aquellos en los que ningún agente etiológico pudo ser identificado o en los que se confirmó la presencia de una ITSAC causada por gramnegativos. También se excluyeron los pacientes en los que se hubiera modificado el tratamiento antibiótico.
Debido al diseño retrospectivo y observacional del estudio, no se requirió consentimiento informado ni aprobación por el comité de ética del centro.
Variables clínicas evaluadas
Los resultados del estudio se evaluaron tomando en consideración datos demográficos y el índice de comorbilidad de Charlson, que permite hacerse una idea general de la gravedad de la enfermedad7. Se registraron la dosis de antibiótico administrada, así como la frecuencia de administración y la duración del tratamiento. A efectos de la evaluación de la seguridad, se definió la nefrotoxicidad como un incremento de la creatinina en sangre del 50% o de 0,5 mg/dl, si este último valor era mayor, en al menos dos mediciones consecutivas desde el comienzo del tratamiento antibiótico hasta el tercer día posterior al final del tratamiento8. Se midieron los valores de creatina-fosfocinasa en los sujetos tratados con daptomicina. Se consideró que la elevación era clínicamente significativa cuando se superaba el límite superior de la normalidad en cinco veces (es decir, 0,850 U/l).
La susceptibilidad al tratamiento antibiótico se confirmó por microdilución en caldo, según las guías del Clinical and Laboratory Standards Institute9. Las categorías clínicas se determinaron según los puntos de corte definidos en los criterios del European Committee on Antimicrobial Susceptibility testing10, retirándose los catéteres venosos centrales en pacientes con una ITSAC por Staphylococcusaureus documentada.
Definiciones y evaluación de los resultados
Las ITSAC se clasificaron según las guías clínicas vigentes de la Infectious Diseases Society of America5.
El criterio de evaluación primario se definió como la combinación de la tasa de mortalidad a 30 días (M30), la tasa de reingreso a 30 días (R30) y la duración de la hospitalización (DH). La M30 se definió como la tasa de mortalidad observada a partir del cultivo inicial, y la R30 como la tasa de reingresos por cualquier razón dentro de los 30 días posteriores al cultivo inicial.
Análisis estadístico
El análisis estadístico se llevó a cabo utilizando la prueba de chi cuadrado para comparar los valores de M30 y R30 de ambos grupos experimentales con el paquete SPSS Statistics v. 25.0 (IBM Corporation, Armonk, NY, Estados Unidos). Para el estudio de la nefrotoxicidad en los diferentes grupos también se seleccionó la prueba de chi cuadrado. Las diferencias entre las características basales de ambos grupos de pacientes fueron evaluadas mediante la prueba U de Mann-Whitney para las variables cuantitativas continuas y, alternativamente, la prueba de chi cuadrado para las variables dicotómicas. El nivel de significación estadística se estableció en un valor de p < 0,05.
Resultados
Características demográficas de la población estudiada
Un total de 558 pacientes oncológicos que habían sufrido un episodio compatible con ITSAC fueron tratados con vancomicina o daptomicina. Entre ellos, 70 cumplían con los criterios de inclusión y el 47,1% (n = 33) eran hombres, siendo la edad media de la muestra de 57,9 años (desviación estándar = 11,5). El 61,4% (n = 43) de estos pacientes fueron tratados con vancomicina y el 38,6% (n = 27) con daptomicina.
Las características basales de los dos grupos se detallan en la tabla 1. No se encontraron diferencias estadísticamente significativas en las características basales de ambos grupos; la única diferencia tuvo que ver con el porcentaje de infecciones causado por Staphylococcus aureus susceptible a meticilina, que era más elevado en el grupo de pacientes tratados con daptomicina (33,3% [n = 9] frente al 11,6% [n = 5]; p = 0,027) (Tabla 2).
Tabla 1. Características demográficas de los pacientes
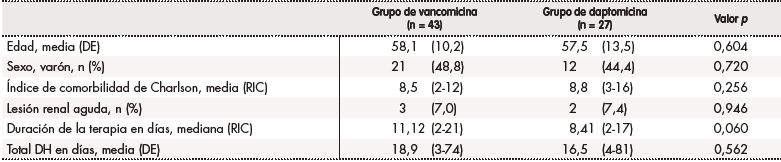
DE: desviación estándar; DH: duración de la hospitalización; n: número de pacientes; RIC: rango intercuartílico.
Tabla 2. Características de los microorganismos causantes de infecciones del catéter intravascular central
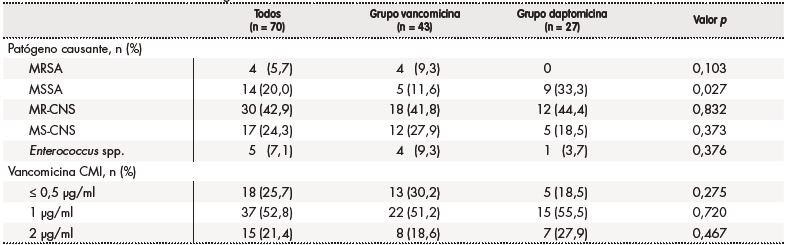
CMI: concentración mínima inhibitoria; MR-CNS: Staphylococcus coagulasa-negativo resistente a meticilina; MRSA: Staphylococcus aureus resistente a meticilina; MS-CNS:Staphylococcus coagulasa-negativo susceptible a meticilina; MSSA: Staphylococcus aureus susceptible a meticilina; n: número de pacientes.
Se realizó un seguimiento farmacológico de las concentraciones plasmáticas de vancomicina sólo en el 23,3% (n = 10) de los pacientes (dosis media: 14,1 mg/kg/12 h; rango intercuartílico [RIC]: 1,8-19,6). La dosis media diaria de vancomicina fue de 568,7 mg (dosis media: 7,43 mg/kg/día; RIC: 4,2-12,3).
Evaluación de la efectividad
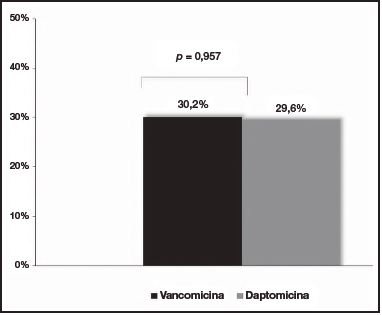
No se observaron diferencias en la M30 entre los pacientes tratados con vancomicina y aquellos que recibieron daptomicina (32,6% [n = 14] frente al 29,6% [n = 8], respectivamente [p = 0,797]) (Figura 1). Tampoco se encontraron diferencias en cuanto a la R30 (30,2% [n = 13] para el grupo de vancomicina frente al 29,6% [n = 8] para el de daptomicina (p = 0,957)] (Figura 2). Igualmente, la DH fue similar en ambos grupos de tratamiento (18,9 días [RIC: 3-74] para el grupo de vancomicina frente a 16,5 días [RIC: 4-81] para el de daptomicina (p =0,562)] (Tabla 1).
Evaluación de la seguridad
La tasa de nefrotoxicidad fue similar en ambos grupos de tratamiento: 7% (n = 3) de los pacientes tratados con vancomicina frente al 7,4% (n = 2) de los que recibieron daptomicina (p = 0,946) (Tabla 1). Uno de los pacientes tratados con vancomicina registró una insuficiencia renal y dos desarrollaron una enfermedad renal. En el caso del grupo de daptomicina, dos pacientes sufrieron enfermedad renal. No se observó un aumento significativo de los niveles de creatina-fosfocinasa en nuestra cohorte de pacientes.
Discusión
Son pocos los estudios que realizan una comparación directa entre el uso de vancomicina y daptomicina para el tratamiento de ITSAC en pacientes oncológicos6. Por lo tanto, aún no existe consenso sobre cuál es la mejor alternativa de tratamiento para estos pacientes.
Nuestro estudio demuestra que, en la práctica clínica rutinaria, la vancomicina presenta un grado de efectividad similar al de la daptomicina para el tratamiento de estas infecciones. Cabe destacar que la equivalencia en materia de efectividad observada en este análisis se ha alcanzado a pesar del uso de dosis infraterapéuticas de vancomicina en la mayoría de los pacientes y una optimización farmacocinética de la pauta de dosificación en el 76,6% de los casos, en línea con las recomendaciones vigentes11.
Chaftari et al. llevaron a cabo el único análisis comparativo entre ambas alternativas terapéuticas en pacientes oncológicos con ITSAC6. Estos autores compararon una cohorte de 38 pacientes oncológicos con sospecha o confirmación de ITSAC tratados con daptomicina con una cohorte histórica de 40 pacientes tratados con vancomicina. En este estudio, la daptomicina demostró ser capaz de una erradicación bacteriológica y de una resolución clínica más rápidas6.
Por el contrario, nuestro estudio evidenció que la daptomicina no presentaba ningún beneficio sobre la vancomicina en pacientes oncológicos con confirmación de ITSAC causada por grampositivos. Podría especularse que la diferencia en los resultados de nuestro estudio y el de Chaftari podría atribuirse, al menos en parte, a diferencias en las cepas bacterianas aisladas. En nuestro estudio, el 78,5% de las bacterias aisladas exhibieron una concentración mínima inhibitoria (CMI) de vancomicina ≤ 1 µg/ml, mientras que Chaftari et al. determinaron que el 74,3% de las cepas de Staphylococcusaureus presentaban una CMI de vancomicina de entre 1 y 2 µg/ml6.
Este estudio se llevó a cabo en una única institución y fue de naturaleza retrospectiva, lo que podría limitar su aplicabilidad en otros contextos. Estos resultados deberán ser validados en ensayos de eficacia comparativos de carácter prospectivo, aleatorizado y controlado. No obstante, variables tales como el índice de Charlson, que proporciona información sobre los factores que condicionan las comorbilidades y la gravedad de la enfermedad en distintos pacientes, fueron tomadas en consideración para reducir posibles sesgos. En definitiva, se procuró equilibrar al máximo las características basales de ambos grupos de tratamiento.
Este estudio presenta la que hasta la fecha es la mayor cohorte de pacientes oncológicos confirmada, comparando la efectividad y seguridad de ambas alternativas terapéuticas. Los resultados indican que ambos antibióticos son equivalentes tanto en materia de seguridad como de efectividad. Los datos recabados permiten concluir que la vancomicina debe seguir utilizándose para el tratamiento de estas infecciones, especialmente en centros caracterizados por una baja prevalencia de cepas con escasa susceptibilidad a la vancomicina.
REFERENCIAS
1. Ferrer C, Almirante B. Infecciones relacionadas con el uso de los catéteres vasculares. Enferm Infecc Microbiol Clin. 2014;32(2):115-24. DOI: 10.1016/j.eimc.2013.12.002 [ Links ]
2. Raad I, Hanna H, Maki D. Intravascular catheter-related infections: advances in diagnosis, prevention, and management. Lancet Infect Dis. 2007;7(10):645-57. DOI: 10.1016/S1473-3099(07)70235-9 [ Links ]
3. Raad I, Hachem R, Hanna H, Bahna P, Chatzinikolaou I, Fang X, et al. Sources and outcome of bloodstream infections in cancer patients: the role of central venous catheters. Eur J Clin Microbiol Infect Dis. 2007;26(8):549-56. DOI: 10.1007/ s10096-007-0320-6 [ Links ]
4. Becker K, Heilmann C, Peters G. Coagulase-negative staphylococci. Clin Microbiol Rev. 2014;27(4):870-926. DOI: 10.1128/CMR.00109-13 [ Links ]
5. Mermel LA, Allon M, Bouza E, Craven DE, Flynn P, O’Grady NP, et al. Clinical practice guidelines for the diagnosis and management of intravascular catheter-related infection: 2009 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2009; 49(1): 1-45. DOI: 10.1086/599376 [ Links ]
6. Chaftari AM, Hachem R, Mulanovich V, Chemaly RF, Adachi J, Jacobson K, et al. Efficacy and safety of daptomycin in the treatment of Gram-positive catheter-related bloodstream infections in cancer patients. Int J Antimicrob Agents. 2010; 36(2): 182-6. DOI: 10.1016/j.ijantimicag.2010.03.015 [ Links ]
7. Charlson ME, Pompei P, Ales KL, MacKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chronic Dis. 1987;40(5):373-83. DOI: 10.1016/0021-9681(87)90171-8 [ Links ]
8. Ricci Z, Cruz D, Ronco C. The RIFLE criteria and mortality in acute kidney injury: A systematic review. Kidney Int. 2008; 73(5): 538-46. DOI: 10.1038/sj.ki.5002743 [ Links ]
9. Clinical and Laboratory Standards Institute. Performance standards for antimicrobial susceptibility testing. 27th ed. CLSI supplement M100. Wayne, PA: CLSI; 2017. [ Links ]
10 European Committee on Antimicrobial Susceptibility Testing (EUCAST). Breakpoint tables for interpretation of MICs and zone diameters. Version 11.0, 2021 [página web] [01/01/2021; 05/05/2021]. Disponible en: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Breakpoint_tables/v_11.0_Breakpoint_Tables.pdf [ Links ]
11. Rybak M, Lomaestro B, Rotschafer JC, Moellering R Jr, Craig W, Billeter M, et al. Therapeutic monitoring of vancomycin in adult patients: A consensus review of the American Society of Health-System Pharmacists, the Infectious Diseases Society of America, and the Society of Infectious Diseases Pharmacists. Am J Health-Syst Pharm. 2009; 66: 82-98. DOI: 10.2146/ajhp080434 [ Links ]
Aportación a la literatura científica:
En este trabajo se han analizado la efectividad y la seguridad de daptomicina frente a vancomicina en pacientes oncológicos con infecciones del torrente sanguíneo asociadas a catéter vascular. Puesto que, hasta la fecha, pocos estudios han comparado ambas alternativas terapéuticas en cuanto a su idoneidad para el manejo de ese tipo de infecciones, queda aún por determinar cuál de las dos es la más adecuada para este grupo de pacientes.
Este estudio supone la mayor cohorte de pacientes oncológicos con infecciones relacionadas con el catéter comparando la efectividad y seguridad de vancomicina versus daptomicina. El estudio añade nueva evidencia mostrando equivalencia.
Cómo citar este trabajo:Del Rosario-García B, Nazco-Casariego GJ, Gómez-Sirvent JL, García-Marrero R, García-Rosado D, López-Lirola AM, Oramas-Rodríguez JM, González-García J. Vancomicina frente a daptomicina como tratamiento de las bacteriemias asociadas a catéter y causadas por grampositivos en el paciente oncológico. Farm Hosp. 2022;46(3):105-8.
Recibido: 12 de Mayo de 2021; Aprobado: 06 de Diciembre de 2021; : 14 de Abril de 2022











 text in
text in