Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista de la Sociedad Española del Dolor
versión impresa ISSN 1134-8046
Rev. Soc. Esp. Dolor vol.11 no.5 Madrid jul. 2004
NOTA CLÍNICA
Estudio de eficacia y coste en la electroestimulación medular como
tratamiento de la angina refractaria
M. Mayo1, J. Pallarés2, C. Villalaín1, A. Moreno-Gázquez1, M. A. Canos3 y L. Almenar4
| Mayo M, Pallarés J, Villalaín C, Moreno-Gázquez A, Canos MA, Almenar L. Cost-effectiveness study of medullary electrostimulation for the management of refractory angina. Rev Soc Esp Dolor 2004; 11: 282-286.
| ||
| SUMMARY Objective: To assess the evolution of patients in our hospital with diagnosis of refractory angina treated with cervical medul-lary electrostimulation (MES) over the period 1994-2002, and to determine the costs associated to this treatment and its cost-benefit ratio. Material and methods: Retrospective study including 12 patients that were fol-lowed-up for 8 years with regular clinical exams in order to determine, both before and after the implant, the following variables: left ventricle ejection fraction (LVEF), NYHA functional stage, frequency of hospitalization, frequency of angina episodes and cafinitrina‚ administration, subjective perception of angina pain relief, exitus, hospital costs before and after the placement of EMS. Results: The MES electrode was implanted at the cervical level, being C2-C3 the most frequent location (58.3%). There were no intra-operative complications. In the early post-operative, there was only one complication due to the displacement of the electrode. Neither there were long-term complications. We found a decrease in the number of anginas per week (14 vs 4, p = 0.005) associated to a decrease in the number of fast-action nitroglycerin doses (15.7 vs 3.8, p=0.002) and a decrease in the number of hospital admissions per year (2.62 vs 0.84, p=0.003). Subjective improvement as perceived by the patient after the placement of the neuro-stimulator was 70%. The five-year hospital costs (considering only the hospitalization costs, without any other further tests) was 37,921.85 for patients with refractory angina without MES, compared to 15.150,25 e for patients with MES. © 2004 Sociedad Española del Dolor. Published by Arán Ediciones, S. L. Key words: Medullary electrostimulation. Angina. Costs. | RESUMEN Objetivo: Valorar la evolución de los pacientes, de nuestro hospital, diagnosticados de angina refractaria y tratada con estimulación eléctrica medular (EEM) cervical desde 1994-2002, además de valorar los costes asociados a dicho tratamiento y su relación coste/beneficio. Material y métodos: Estudio retrospectivo de 12 pacientes observando su evolución a lo largo de 8 años con controles clínicos periódicos, objetivándose tanto en la historia previa como posterior al implante, las siguientes variables: fracción de eyección del ventrículo izquierdo (FEVI), estadio funcional NYHA, frecuencia de ingresos hospitalarios, frecuencia de episodios anginosos e ingesta de cafinitrinas, sensación subjetiva de mejora del dolor anginoso, exitus, costes hospitalarios previos y posteriores a la colocación del EEM. Resultados: El electrodo de EEM fue implantado a nivel cervical siendo más frecuente la localización C2-C3 (58,3%). No se presentó ninguna complicación intraoperatoria. En el postoperatorio inmediato tuvimos como única complicación un desplazamiento del electrodo. No hubo ninguna complicación a largo plazo. Comprobamos que existió una disminución del número de anginas por semana (14 vs 4 p = 0,005) asociada a una disminución del número de tomas de nitroglicerina de acción rápida (15,7 vs 3,8 p = 0,002) y a una disminución en el número de ingresos hospitalarios/año (2,62 vs 0,84 p = 0,003). La mejoría subjetiva por parte del paciente tras la colocación del neuroestimulador fue del 70%. En cuanto al coste hospitalario quinquenal (conformado sólo por el coste del ingreso sin pruebas complementarias) fue de 37.921,85 e en los pacientes con angina refractaria que no portaban EEM, frente a los 15.150,25 de los pacientes portadores EEM. © 2004 Sociedad Española del Dolor. Publicado por Arán Ediciones, S. L. Palabras clave: Electroestimulación medular. Angina. Costes.
|
1 Médico Residente
2 Jefe de la Unidad Terapeútica del Dolor
3 Médico Adjunto. Unidad Terapeútica del Dolor
4 Médico Adjunto. Servicio de Cardiología
Unidad Terapeútica del Dolor. Hospital Universitario La Fe. Valencia
Recibido: 09-03-04.
Aceptado: 30-04-04.
INTRODUCCIÓN
La electroestimulación medular se ha mostrado como una técnica de gran ayuda en el tratamiento de variados síndromes de dolor crónico.
Desde 1987 la estimulación eléctrica medular (EEM) ha sido empleada para el tratamiento de la "angina refractaria" a terapia farmacológica y no subsidiaria de tratamiento quirúrgico (1).
Los efectos antianginosos de la electroestimulación siguen siendo motivo de estudio. Se cree que principalmente disminuye el consumo de oxígeno por parte del miocardio vía reducción de la actividad simpática, así mismo disminuye la frecuencia cardiaca, la tensión arterial media (2,3) y produce una acción vasodilatadora, tan beneficiosa en las arteriopatías periféricas (4-6).
Por lo tanto creemos que los efectos clínicos de la EEM se deben a su interferencia directa sobre el estímulo simpático (7) y a la supresión del dolor anginoso por su efecto antinocioceptivo; estando ampliamente demostrada la reducción de las crisis anginosas (2,8-13) y el aumento de la capacidad funcional (2,9,11). Todo ello comporta una acción beneficiosa sobre la calidad de vida del paciente.
Simultáneamente la EEM conlleva una disminución de los ingresos hospitalarios y de la solicitud de asistencia en los servicios de urgencias, produciéndose una disminución del gasto hospitalario generado por estos pacientes (14-16).
El objetivo del estudio es valorar la evolución de nuestros pacientes diagnosticados de angina refractaria tratada con EEM desde 1994-2002. Asimismo, hemos valorado los costes asociados a dicho tratamiento y su relación coste/beneficio.
MATERIAL Y MÉTODOS
Estudio retrospectivo de 12 pacientes diagnosticados de angina de grado III/ IV de la NYHA y en los cuales un tratamiento farmacológico adecuado, a dosis máximas, no había tenido el efecto esperado y fueron desestimados para un tratamiento quirúrgico de revascularización y/ o trasplante.
Observamos la evolución a 8 años, con controles clínicos periódicos, objetivándose, tanto en la historia previa como posterior al implante, las siguientes variables: FEVI, estadio funcional NYHA, frecuencia de ingresos hospitalarios, frecuencia de episodios anginosos e ingesta de nitratos de acción rápida, frecuencia de infartos agudo de miocardio, sensación subjetiva de mejora del dolor anginoso y exitus.
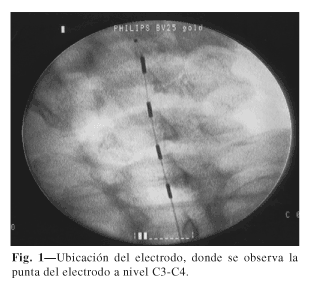
El implante del electrodo se realizó bajo sedación y anestesia local con monitorización cardiorrespiratoria. Con el paciente en decúbito prono y posición antilordosis, identificamos el espacio epidural mediante la técnica de "gota pendiente de Gutiérrez" a nivel T3. Una vez identificado, el espacio, introducimos la punta del electrodo hasta C3-C4 bajo control radiológico, siendo la posición ideal posterior y ligeramente izquierda, con respecto al tubo neural (Fig. 1). Con el electrodo en el nivel deseado, procedemos con un estimulador externo a la electroestimulación, intentando conseguir parestesias no dolorosas en la zona del dolor anginoso, modificando la posición del electrodo hasta lograrlo. A continuación, se fija el electrodo con un bucle en los cuatro puntos cardinales y se tuneliza la extensión intermedia hasta el generador (Itrel 3, Synergy), colocándose en el tejido subcutáneo del glúteo, por debajo de la cresta ilíaca.
El seguimiento clínico tras el alta es realizado sistemáticamente por los servicios de cardiología y la Unidad del Dolor.
Los datos son expresados como media ± desviación estándar. La valoración estadística se realizó mediante la prueba de los rangos con signo de Wilcoxon. Se consideró significación estadística cuando p< 0,05.
RESULTADOS
Se incluyeron en el estudio un total de 12 pacientes (11 hombres y 1 mujer), a los que se les había realizado el implante de EEM, con edades comprendidas entre los 37-83 años y estadio funcional (NYHA) (2-4). Excepto un paciente, todos tenían antecedentes personales de riesgo cardiológico (75% HTA, 16,7% diabetes y 66,7% dislipemia).
Previo a la colocación del sistema de EEM un 75% de los pacientes habían sufrido por lo menos un infarto (el 66% habían sufrido dos infartos), habiéndose intentado en el 83% técnicas de revascularización.
La zona de colocación más frecuente fue C2-C3 (58,3%). Actualmente, la zona estimulada es C3-C4 para evitar cefaleas por hiperestimulación.
Durante el seguimiento de 8 años (1994-2002), 3 pacientes no presentaron complicaciones anginosas que precisaran ingreso hospitalario y el número de ingresos por año descendió un 214%, con una media de 2,62 ± 1,09 previa a la colocación del electrodo frente a 0,84 ± 0,7 tras su colocación (p = 0,003).
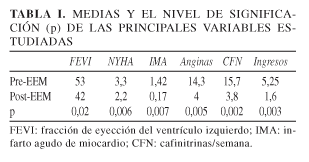
En la Tabla I se muestran las variables estudiadas y podemos destacar que se obtuvo un descenso significativo de la frecuencia de los episodios de angina por semana (14,33 pre- EEM vs 4,04 post- EEM p=0,005) acompañado de un descenso del número de cafinitrinas por semana (15,7 ± 10,19 pre- EEM vs 3,8 ± 3,8 post- EEM p = 0,002) y del número de IMA por paciente (1,42 ± 1 pre- EEM vs 0,17 ± 0,39 post- EEM p = 0,007).
Respecto los IAM posteriores al implante, dos pacientes tuvieron un infarto de miocardio documentado con sintomatología típica que no cedía con la toma de cafinitrinas, siendo ingresados en la Unidad de Cuidados Intensivos con fallecimiento de uno de los pacientes.
En lo referente a la mejoría subjetiva que tuvieron los pacientes tras la colocación del EEM fue de un 70% con respecto a la situación previa. Asimismo, disminuyó el estadio de la NYHA. Antes del implante del sistema de EEM un 50% de los pacientes eran un estadio IV. Tras su colocación eran estadio II un 50% de los pacientes (3,33 ± 0,78 pre- EEM vs 2,25 ± 0,87 post- EEM p = 0,006). Inversamente, se produjo una disminución de la fraccion de eyección del ventrículo izquierdo (53,70 ± 10,33 pre-EEM vs 42,62 ± 9,13 post-EEM p = 0,02).
En la tabla I podemos observar un resumen de la variables estudiadas pre y postimplante del EEM junto al nivel de significación.
Fueron varias las causas de alta de la terapia. Así 4 pacientes fueron trasplantados de corazón por disminución progresiva de la FEVI (tres de ellos murieron en el postoperatorio inmediato del trasplante por shock), a otros 3 les fueron explantados los sistemas de EEM (dos de ellos por ineficacia y uno por fiebre de origen desconocido (FOD) que a posteriori resultó ser de etiología odontológica, por boca séptica, empeorando de manera significativa la sintomatología del angor, tras la retirada del EEM).
En la serie sólo tuvimos un exitus por IMA no Q con sintomatología típica.
En la actualidad portan EEM cuatro pacientes con una media de 5 años de evolución y una mejoría subjetiva del 78%.
En relación con las complicaciones técnicas, reseñar por una parte, un desplazamiento del electrodo que precisó su reimplante, y por otra, el elevado número de reprogramaciones, ya fueran por la percepción de las parestesias ya por incomprensión del paciente del módulo de intensidad externo "ratón", lo que arrojó un total de 37 reprogramaciones con una media de 3,08 ± 3,92 reprogramaciones por paciente.
El cálculo de costes persigue obtener datos que no se solapen, es decir, que puedan sumarse sin que ello represente contabilizarlos dos veces. Por ejemplo, el coste de los días de estancia no debe incorporar el de cualquier procedimiento que se lleve a cabo durante los mismos y que haya sido contabilizado por separado.
Los costes diarios de la hospitalización incluyen los hoteleros básicos (lavandería, comida, limpieza, etc.), los de enfermería de planta y los de apoyo médico general. Hemos contabilizado los costes de ingreso hospitalario en la sala de cardiología durante una media de una semana, sin contabilizar las pruebas complementarias que son muy variadas dependiendo de si se han realizado anteriormente. Cuando el paciente fue ingresado en la Unidad de Cuidados Intensivos (UCI) por IMA contabilizamos además una media de una semana en la planta de cardiología para control posterior.
El coste del implante del sistema de EEM lleva implícito el coste del generador más el electrodo conjuntamente el coste de intervención quirúrgica y los de hospitalización durante 4 días posteriores al implante.
En la Tabla II podemos observar los recursos y costes de los procedimientos. Por tanto, los costes generados previos a la colocación del electrodo serían los costes de ingreso UCI tras IMA, más los de ingresos en planta tras angina prolongada.
Mientras que los costes generados durante el primer año tras la colocación del EEM serían el coste del neuroestimulador más la estancia en planta con intervención quirúrgica, costes de ingreso UCI tras IMA, más los de ingresos en planta tras angina prolongada, que se produjeran en el periodo de estimulación del EEM.
A partir del segundo año los costes que generan estos pacientes serán los del UCI tras IMA, más los de ingresos en planta tras angina prolongada además del cambio de pila (debido a que el estudio de costes lo hacemos analizando sobre un periodo de 5 años no hemos incorporado los costes del cambio de pila ya que en ningún caso se realizó antes de los 5 años).
En la Tabla III podemos observar el coste medio por paciente y por año
El coste hospitalario (reflejando solamente el coste del ingreso sin pruebas complementarias) a 5 años es de 37.921,85 , los pacientes con angina refractaria que no portan EEM frente a 15.150,25 de los pacientes que portan EEM.
DISCUSIÓN
La angina es el principal síntoma clínico de la isquemia miocárdica y esta asociado a un desequilibrio entre el aporte y la demanda de oxígeno; su tratamiento incluye terapia farmacológica junto con revascularización coronaria, intentando aumentar el suministro de oxígeno al miocardio. No obstante, existen pacientes que continúan experimentando angina a pesar del tratamiento convencional a dosis máximas.
Desde la descripción de la técnica en 1967, la EEM se ha utilizado, tradicionalmente, en el tratamiento del dolor crónico. A partir de 1987 se ha demostrado el beneficio de esta técnica para el control del dolor de características isquémicas tanto en la angina como en la isquemia de miembros inferiores (1,17).
Se han sugerido diversos mecanismos como responsables de la disminución del dolor anginoso (3,18,19):
-Reducción de la isquemia miocárdica por vasodilatación con el consiguiente aumento de aporte de sangre al miocardio.
-Disminución de la demanda miocárdica de oxígeno con redistribución del flujo sanguíneo coronario aumentando la perfusión en la zona isquémica.
-Efecto antinocioceptivo por neuromodulación.
Probablemente todas ellas en mayor o menor medida sean las responsables de los beneficios objetivados de la técnica mejorando los síntomas de los pacientes con disminución de la frecuencia e intensidad de los episodios de angina con una menor demanda de la toma de nitratos y una mayor tolerabilidad al ejercicio, proporcionando una mejor calidad de vida.
Los principales detractores de la técnica alegan que podría enmascarar el dolor isquémico de la crisis de IMA. Sin embargo diversos estudios (2,8,11,13,14) han informado de la seguridad de la técnica. Nosotros hemos observado una disminución de IMA y en caso de padecer un IMA durante el tratamiento este no enmascaró los síntomas típicos. También alegan que el coste del EEM es elevado lo cual limita su utilización; empero el beneficio proporcionado a los pacientes unido a una disminución de la demanda de atención en los servicios de urgencias y a una disminución de los ingresos hospitalarios, conlleva que la EEM signifique un sensible ahorro.
En nuestro estudio hemos obtenido una mejora de la calidad de vida en base a una mejoría subjetiva del paciente unido a disminución de la ingesta de cafinitrinas, del número de anginas y de IMA. Igualmente, obtuvimos una disminución de la presión asistencial hospitalaria disminuyendo los ingresos en planta y en la Unidad de Cuidados Intensivos. La mejora de la calidad de vida del paciente y la disminución de la presión asistencial hospitalaria unido a la disminución de coste proceso/paciente arroja un beneficio real y efectivo del uso de la EEM cervical en la angina refractaria. En conclusión, la EEM es una terapia coadyuvante eficaz y segura para los pacientes con angina refractaria mejorando la calidad de vida de los pacientes asociado a una disminución de costes hospitalarios.
| CORRESPONDENCIA: Mónica Mayo Moldes C/Mauro Guillén, 6 pta 13 46009 Valencia e-mail: mayomonica@wanadoo.es |
BIBLIOGRAFÍA
1. Murphy DF, Giles KE. Intractable angina pectoris: management with dorsal column stimulation. Med J Aust 1987; 146: 260. [ Links ]
2. Mannheimer C, Eliasson T, Augustinsson LE, et al. Electrical stimulation versus coronary artery bypass surgery in severe angina pectoris: The ESBY study. Circulation 1998; 97: 1157-63. [ Links ]
3. Benítez A, Gutiérrez-Rodríguez M, Sarasquete MC, et al. Estimulación medular en hipoxia y necrosis miocárdica. Estudio experimental con un nuevo modelo animal. Parte II. Rev Soc Esp Dolor 1994; 3: 178-87. [ Links ]
4. Broseta J, Barbera J, De Vera JA, et al. SCS in peripheral arterial disease. A cooperative study. J Neurosurg 1986; 64: 71-80. [ Links ]
5. Pallares J, Barbera J, Fenollosa P, et al. Electroestimulación medular en las insuficiencias vasculares periféricas. Protocolo e indicaciones. Dolor I C & T 1989; 4: 202-5. [ Links ]
6. Barbera J, Pallares J. Tratamiento del dolor isquémico mediante estimulación medular. Dolor I C & T 1989; 4: 205-8. [ Links ]
7. Fenollosa P, Pallares J, Llopis JE, et al. The response of the neuropatic pain to spinal cord stimulation: the predictive role of a prior sympathetic block. 7th World congress on Pain. Abstract book. IASP publications. Seatle, 1993. p. 341. [ Links ]
8. García-Moll M, Serra R, García-Moll X. Tratamiento de la angina refractaria con electroestimulación medular. Resultados del seguimiento a largo plazo. Rev Esp Cardiol 2000; 53: 321-6. [ Links ]
9. González- Darder JM, Vázquez JL, Canela P, González V. Calidad de vida del paciente con angina inestable tratado con estimulación eléctrica medular. Med Clin 1990; 95: 768-70. [ Links ]
10. González Martínez V. Estimulación medular en el tratamiento de la angina de pecho severa. Rev Soc Esp Dolor 1994; 1: 46-50. [ Links ]
11. Hautvast RW, DeJongste MJ, Staal MJ, et al. Spinal cord stimulation in chronic intractable angina pectoris: A randomized, controlled efficacy study. Am Heart J 1998; 136: 114-20. [ Links ]
12. Camba MA, Yañez A, Pita R, et al. Estimulación eléctrica medular en pacientes portadores de una angina inestable. Dolor I C& T, 1990; (Supl. Benalmádena) 122. [ Links ]
13. Ten Vaarwerk IAM, Jessurun GAJ, DeJongste MJ, et al. Clinical outcome of patients treated with spinal cord stimulation for therapeutically refractory angina pectoris. Heart 1999; 82: 82-8. [ Links ]
14. Ferrandis P, de Andrés J, Gargallo G, et al. Neuroestimulación epidural de la medula espinal en pacientes con angina refractaria. Estudio retrospectivo. Rev Soc Esp Dolor 2003; 10: 24-31. [ Links ]
15. Murray S, Carson KGS, Ewings PD, et al. Spinal cord stimulation significantly decreases the need for acute hospital admission for chest pain in patients with refractory angina pectoris. Heart 1999; 82: 89-92. [ Links ]
16. Brodison A, Chauhan A. Spinal-cord stimulation in management of angina. Lancet 1999; 354: 1748-9. [ Links ]
17. Augustinsson LE. Epidural spinal electrical stimulation in peripheral vascular disease. Pacing Clin Electrophysiol 1987; 10: 205-6. [ Links ]
18. Mannheimer C, Eliasson T, Anderson B, et al Effects of spinal cord stimulation in angina pectoris induced by pacing and possible mechanisms of action. BMJ 1993; 307: 477-80. [ Links ]
19. Rodríguez MJ, Aldaya C, Zarcos A. Estimulación de cordones posteriores en el tratamiento del dolor crónico. Rev Soc Esp Dolor 1996; 3: 202-7. [ Links ]