Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista de la Sociedad Española del Dolor
versión impresa ISSN 1134-8046
Rev. Soc. Esp. Dolor vol.12 no.5 Madrid jun./jul. 2005
ORIGINAL
Correlación de hallazgos radiológicos con los eventos adversos que posiblemente
hayan causado aracnoiditis
J. A. Aldrete1, R. F. Ghaly2, T. L. Brown3, L. A. Vascello4, F. H. Montpetit1 y S. C. Johnson1
| Aldrete JA, Ghaly RF, Brown TL, Vascello LA, Montpetit FH, Jonson SC. Correlation between radiological findings and adverse events probably causing arachnoiditis. Rev Soc Esp Dolor 2005; 12: 269-276.
| ||
| SUMMARY Clinical diagnosis of arachnoiditis is characterized by a burning, ardent pain with dysesthesia and vesical, rectal and sexual dysfunction that appear after an adverse event during a spinal surgical procedure; it can be confirmed through magnetic resonance or myelogram followed by lumbar spine tomography. In this study, a retrospective review was conducted of image studies from 436 patients referred to a pain clinic with diagnosis of arachnoiditis in order to identify specific patterns on the radiological images that could help to determine the potential etiology of this disease. The apparent cause was correlated to the appearance of neurological changes after spine injections, interventions or surgical procedures. Neurological deficits were observed in 160 patients after myelograms, rachidian or peridural anesthesia, epidural blood patches or injection of steroids or neurolytic drugs for the management of chronic pain. Eleven (6.8%) of these patients had inflammation of roots, 135 (84.3%) had roots in bunches and 12 cases (7,5%) had roots adhered to the dural sac. Two cases of syringomyelia were observed in patients with thoracal or high lumbar peridural anesthesia. Of 276 other patients in which the clinical diagnosis of arachnoiditis was established after spine surgical procedures, 259 patients (93.8%) had roots in bunches, 152 (55%) had a deformed dural sac and peridural fibrosis was observed in 241 patients (87.3%). Pseudomeningocele and intrathecal calcifications were observed in 21 (7.6%) and 4 (0.15%) of the surgical cases, respectively. It is concluded that radiological images in cases of arachnoiditis caused by injections and invasive procedures are only characterized by roots in bunches. However, surgical patients have, in addition to roots in bunches, deformation of the dural sac and healing and fibrotic tissue at the epidural space undergoing surgery. © 2005 Sociedad Española del Dolor. Published by Arán Ediciones, S. L. Key words: Arachnoiditis. Neuropathic pain. Neurological deficit. Peridural fibrosis. Dural deformation. Pseudomeningocele.
| RESUMEN El diagnóstico clínico de aracnoiditis se caracteriza por dolor ardiente, quemante con disestesia, disfunción vesical, rectal y sexual que se presentan después de un evento adverso durante una intervención en la columna vertebral; puede ser confirmado por una resonancia magnética o por un mielograma seguido de una tomografía de la columna lumbar. En este estudio se revisaron a posteriori los estudios de imaginología de 436 pacientes referidos a una clínica de dolor con el diagnóstico de aracnoiditis con el objeto de identificar patrones específicos de imágenes radiológicas que permitieran la identificación de la posible etiología de esta enfermedad. La causa aparente fue correlacionada con la aparición de cambios neurológicos presentándose después de inyecciones, intervenciones u operaciones de la columna vertebral. Fueron notados déficits neurológicos en 160 pacientes después de mielogramas, anestesia raquídea o peridural, parches epidurales de sangre, inyecciones de esteroides o neurolíticos para tratar dolor crónico. De estos enfermos, 11 (6,8%) tenían raíces inflamadas, 135 (84,3%) tenían raíces en racimo y en 12 casos (7,5%) las raíces se adherían al saco dural. Dos casos de siringomielia fueron notados en pacientes que tuvieron anestesia peridural torácica o lumbar alta. De 276 pacientes, otros en los que el diagnóstico clínico de aracnoiditis se presentó después de intervenciones quirúrgicas de la columna vertebral, 259 pacientes (93,8%) tenían raíces en racimo, 152 (55%) tenían un saco dural deformado, y fibrosis peridural se notó en 241 enfermos (87,3%). Pseudomeningoceles y calcificaciones intratecales se notaron en 21 (7,6%) y en 4 (0,15%) de los casos operados, respectivamente. Se deduce que las imágenes radiológicas en casos de aracnoiditis causados por inyecciones e intervencionismo, se caracterizan únicamente por raíces en racimo. Mientras que en los pacientes operados tienen, además de raíces en racimo, deformidades del saco dural y tejido cicatricial y fibrótico en el espacio epidural intervenido quirúrgicamente. Palabras clave: Aracnoiditis. Dolor neuropático. Déficit neurológico. Fibrosis peridural. Deformidad dural. Pseudomeningocele.
|
1Aldrete Pain Care Center and the Arachnoiditis Foundation, Inc. Birmingham, Alabama, EE.UU.
2Neurocirujano. Ghaly Neurosurgicak Associates. Aurora. Illinois, EE.UU.
3Radiólogo. Clearwater, Florida, EE.UU.
4Profesor Asociado de Anestesiología. Universidad de Kentuchy. Lexington, Kentuchy. EE.UU.
Recibido: 22-03-05.
Aceptado: 08-06-05.
INTRODUCCIÓN
El diagnostico clínico de aracnoiditis (ARC) suele ser problemático, ya que generalmente los pacientes también poseen procesos degenerativos o traumáticos de la columna vertebral. Estas circunstancias hacen que el momento de aparición y la posible causa de la aracnoiditis sean difíciles de establecer. Si además varios procedimientos son ejecutados de una manera secuencial, sin evidencia radiológica, entre uno y otro, la correlación de la aparición de los síntomas con los cambios radiológicos es casi imposible (1).
MÉTODOS
De enero de 1990 a octubre de 2004, un total de 436 pacientes, con el diagnóstico de ARC, fueron referidos a la Clínica de Aracnoiditis. El diagnóstico fue confirmado llevando a cabo una revisión retrospectiva del expediente médico, siguiendo en detalle los cambios neurológicos como la aparición de dolor quemante, disestesia y disfunción de esfínteres después de una intervención invasiva de la columna vertebral, correlacionando tal evento desfavorable con evidencia radiológica de lesiones típicas de ARC. Además se llevó a cabo un examen neurológico completo y una revisión detallada de todas las imágenes radiológicas de la región afectada. Si estaba indicado, se ordenaba otro estudio de imaginología.
Las lesiones radiológicas fueron agrupadas de acuerdo con el procedimiento que se llevó a cabo, incluyéndose en el grupo A aquellos pacientes en los que se documentó el déficit neurológico después de un procedimiento para el tratamiento del dolor crónico, anestesia raquídea o peridural o un parche epidural sanguíneo. Este grupo incluyó un total de 160 pacientes, de 26 a 67 años de edad. El grupo B incluyó 267 enfermos adultos de 36 a 71 años de edad. La revisión retrospectiva de los expedientes fue hecha por JAA con RFG o con LAV. En la totalidad, de los 436 enfermos, el criterio del diagnóstico radiológico de aracnoiditis fue tomado de la guía previamente publicada por Aldrete y Brown (2). Todos los estudios radiológicos fueron examinados personalmente por TFB y/o JAA. SCJ o FHM obtuvieron, mantuvieron y clasificaron los expedientes clínicos, los tabularon y participaron en la atención médica de los pacientes.
RESULTADOS
En los 160 pacientes incluidos en el grupo A, las imágenes radiológicas más comúnmente notadas fueron raíces nerviosas en racimo y/o inflamadas y menos frecuentemente se encontraron adheridas al saco dural o siringomielia (Tabla I).
Los pacientes en el grupo B, se separaron en cuatro subgrupos que incluyeron:
1. Postlaminectomía (72 casos) en uno o más espacios intervertebrales que además incluyeron 2 casos de granuloma y 2 casos de meningioma presentes en la punta de catéteres intratecales.
2. Postlaminectomía en los que razgamiento incidental de la dura ocurrió y fue reparada durante la intervención (39 casos).
3. Fusiones raquídeas construidas de hueso (en 54 casos).
4. Fusiones raquídeas sostenidas por tornillos pediculares y placas (111 casos), otros 12 en los que cajas intervertebrales sustituyeron los discos correspondientes y dos con escoliosis que se corrigió con los soportes de Luque.
Las lesiones radiológicas observadas en el grupo B se describen en la Tabla II, incluyendo además de raíces nerviosas inflamadas, raíces en racimos, fibrosis peridural, deformidades del saco dural, pseudomeningoceles y calcificaciones intratecales. De estos 276 pacientes, 173 (62,6%) tenían más de una de las lesiones radiológicas ya descritas.
DISCUSIÓN
Antes de tener la mielografía, los casos de aracnoiditis eran diagnosticados en la mesa de operaciones o postmortem (3,4). Las imágenes antiguas de medios de contraste en el líquido cefalorraquídeo espinal demostraban casos avanzados de paquimeningitis o aracnoiditis obliterante con raíces nerviosas emplastadas (5,6). Irónicamente los medios de contraste que permitían hacer el diagnóstico causaban un buen número de lesiones similares (7,8), siendo a veces imposible determinar si las lesiones pre-existían al mielograma, o este las había causado (9). Diagramas idealísticos (10) reproducían malamente las verdaderas proporciones y perspectiva que se encontraban en el espacio subaracnoideo (11). Desde 1944, el pantopaque fue aparentemente el agente más popular, ya que obtenía una buena reproducción de las imágenes con contraste entre los diferentes elementos intratecales; sin embargo pronto se encontró que causaba la misma enfermedad (10,12,13), pero fue mantenido en uso clínico hasta 1986 cuando la FDA finalmente prohibió su venta en los EE.UU. debido a su lenta eliminación (1 ml/año) y su alta osmolaridad (14,15). (Fig. 1).
La visualización de las estructuras intratecales fue ampliada y mejorada cuando la tomografía se hacía después de una mielografía, pero aun teniendo la posibilidad de una reacción inflamatoria que resultase después de su administracion (16). Eventualmente en las últimas dos décadas, la introducción de medios de contraste hidrosolubles ha disminuido considerablemente la posibilidad de daño secundario a estos agentes (7,10,17)
El advenimiento de la resonancia magnética ha permitido identificar lesiones intradurales sin necesidad de inyecciones invasivas en el interior del canal vertebral (18); las imágenes de este recinto pueden ser aún mejor delineadas con la administración endovenosa del medio de contraste gadolinium (19), que permite identificar, con nitidez, cada raíz nerviosa, ligamentos, líquido cefalorraquídeo, sangre, grasa, músculo, etc.
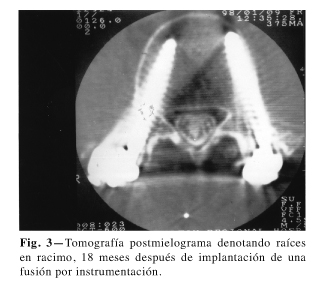
Los pacientes incluidos en este estudio tenían síntomas identificados con la presencia de ARC o una de sus variantes (1,20). Las raíces nerviosas, en la etapa inicial de inflamación del cuadro aracnoidítico, están aumentadas de diámetro por edema intersticial (21) y frecuentemente son movilizadas anteriormente, en lugar de estar localizadas en la mitad posterior del saco dural en donde se precipitan por gravedad en situaciones normales. Hay varios perfiles de localización anormal de las raíces dentro del saco dural (2,22), desde una forma de filamento, en "racimo de uvas', en "collar de perlas", etc. En los segmentos más inferiores del saco dural, las raíces se encuentran en la periferia pero no adheridas a la pared del saco dural, estando simétricamente posicionadas si no hay un proceso inflamatorio (23) (Figs. 2 y 3).
Después de tres o cuatro meses, el patrón cambia hacia un proceso proliferativo (23), en el cual las raíces están agrupadas como en racimos, pero sin edema de las mismas (19,22), teniendo generalmente un diámetro normal, pero una posición asimétricamente anormal, mejor observadas en las vistas axiales (8).
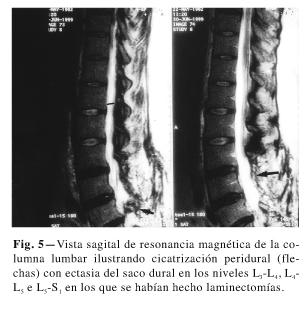
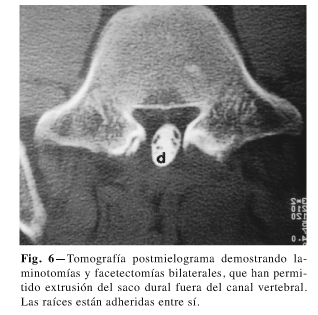
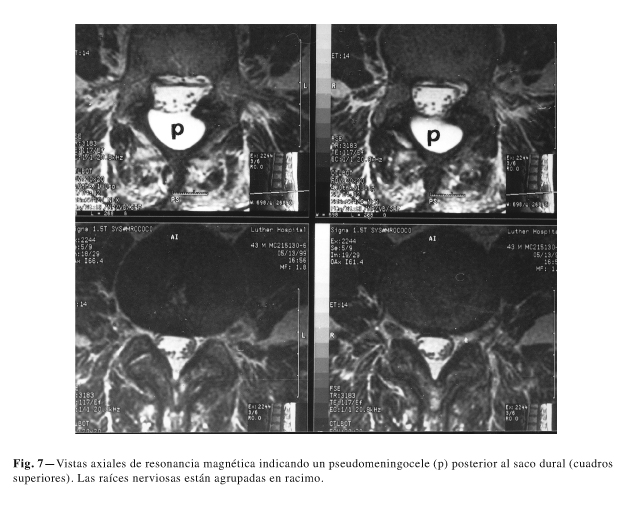
Deformidades del saco dural (2,22) (Fig. 4) y un proceso de cicatrización peridural (Fig. 5) fueron observadas en casos quirúrgicos (postlaminectomías o fusiones), ocasionalmente adhiriendo el saco dural a una de las láminas unilateralmente (19), fibrosis extensa desplazando la teca hacia una posición asimétrica así como ectasia del saco dural (Fig. 6) y después de laminectomía bilateral, extrusión del saco dural fuera del canal vertebral (Fig. 7). La durotomía incidental continúa siendo aún de cierta consecuencia aunque se reparen al momento, debido a la posibilidad de recurrencia y fuga de LCR en el periodo posquirúrgico inmediato (24,25) con la posibilidad de cefalea persistente o infección de la herida a veces terminando en psedomeningoceles (26,27) (Fig. 8). Las calcificaciones intratecales, son casi patognomónicas de ARC apareciendo después de extensas intervenciones quirúrgicas en las que ha habido abundante hemorragia. (Fig. 9).
En este estudio, se estableció una relación entre las lesiones presentes en ARC con el evento que pudo haber iniciado el proceso aracnoidítico revelado por un déficit neurológico subsiguiente a una anestesia epidural o subaracnoidea (20,28) en la que pudo ocurrir parestesia, sangrado, sobredosis, etc., o por algunos procedimientos de algiología como son inyecciones de esteroides (20), neurolíticos como la solución salina hipertónica (29,30), fenol (31), azul de metileno o medicamentos adyuvantes como la adición de bicarbonato de sodio (32) o sangre (33,34) que ingresan accidentalmente al compartimiento subaracnoideo.
Es de importancia hacer notar que los especialistas que atiendan a estos pacientes se familiarizen con las imágenes que diferencian el diagnóstico de aracnoiditis sobre todo en laminectomías con fibrosis extradural (35-37); pero la aparición súbita junto con un evento inesperado ocurriendo en alguna intervención del raquis puede anunciar un evento catastrófico requiriendo consulta neurológica, repetición del estudio de imagenología para establecer una causa y efecto y si es necesario actuar para prevenir el paso de la fase inflamatoria a la fase proliferativa de esta enfermedad.
|
BIBLIOGRAFÍA
1. Aldrete JA. Clinical diagnosis. In: Aldrete JA, ed. Arachnoiditis: the silent epidemic. Denver: Futuremed, 2000. p. 201-19. [ Links ]
2. Aldrete JA, Brown TL. Laboratory and radiological diagnosis in arachnoiditis. In: Aldrete JA, ed. Arachnoiditis: the silent epidemic. Denver: Futuremed, 2000. p. 241-52. [ Links ]
3. Vincent C, Puech P, David M. Sur le diagnostic, le traitement chirurgical le pronostic, des arachnoiditis spinales. Rev Neurol 1930; 1: 577-9. [ Links ]
4. Puusepp L. Surgical intervention in four cases of myelitis compression caused by osseous deposits in the arachnoidea of the spinal cord (arachnoiditis ossificans). J Nerv Ment Dis 1931; 74: 1-9. [ Links ]
5. Spiller WG, Musser JH, Martin E. A case of intradural spinal cyst with operation and recovery. Univ of Pennsylvania M Bull 1903; 16: 27-31 and 56-60. [ Links ]
6. Wilson SAK. Pachymeningitis spinalis hypertrophica. In: Bruce T, ed. Neurology, Baltimore: AN Williams and Wilkins 1940. p. 9-11. [ Links ]
7. Strain W. Radiocontrast agents for neuroradiology. In: Knoefel PK, ed. International Encyclopedia of Pharmacology and Therapeutics. Radiocontrast Agents. Pergamon Press, 1971; 2: 365-93. [ Links ]
8. Tarlov IM. Pantopaque meningitis disclosed at operation. JAMA 1945; 128: 1014-6. [ Links ]
9. Aldrete JA, Brown TL. Myelography. In: Aldrete JA, ed. Arachnoiditis: the silent epidemic. Denver: Futuremed, 2000. p. 49-63. [ Links ]
10. Quiles M, Marchisello PJ, Tsairis P. Lumbar adhesive arachnoiditis. Etiologic and pathologic aspects. Spine 1978; 3: 45-50. [ Links ]
11. Burton CV, Wiltse LL. Editorial and symposium on lumbar arachnoiditis. Nomenclature, etiology and pathology. Spine 1978; 3: 23-92. [ Links ]
12. Howland WJ, Curry JL, Butler AK. Pantopaque arachnoiditis. Radiology 1963; 80: 489-91. [ Links ]
13. Howland WJ, Curry JL, Butler AK. Pantopaque arachnoiditis: Experimental study of blood as potentiating agent. Radiology 1963; 80: 371-9. [ Links ]
14. Davies FL. Effect of unabsorbed radiographic contrast media in the central nervous system. Lancet 1956; 2: 747-8. [ Links ]
15. Bearing EA. Notes on the retention of pantopaque in the subarachnoid space. Am J Surg 1950; 80: 455-8. [ Links ]
16. Lee BCP, Kazam E, Newman AD. Computer tomography of the spine and the spinal cord. Radiology 1979; 128: 95-102. [ Links ]
17. Haughton VM, Ho KC, Uriger GF. Arachnoiditis following myelography with watersoluble agents. Radiology 1977; 125: 731-3. [ Links ]
18. Ross JS, Masaryk TJ, Modic MT, et al. MRI imaging of lumbar arachnoiditis. JNR 1987; 149: 1025-32. [ Links ]
19. Johnson CE, SZE G. Benign lumbar arachnoiditis: MRI imaging with gadopentate di meglumine. AJR 1990; 155: 873-80. [ Links ]
20. Aldrete JA. Neurological deficit and arachnoiditis after neuraxial anesthesia. Acta Anesthesiol Scand 2003; 93: 3-12. [ Links ]
21. Avidan A, Gomori M, Davidson E. Nerve root inflammation demonstrated by MRI in a patient with transient neurological symptoms after intrathecal injection of lidocaine. Anesthesiology 2002; 97: 257-8. [ Links ]
22. Delamarter RB, Ross JS, Masaryk TJ, Modic MT, Bohlman HH. Diagnosis of lumbar arachnoiditis by magnetic resonance imaging. Spine 1990; 15: 304-10. [ Links ]
23. Aldrete JA. Anatomopathology. In: Aldrete JA, ed. Arachnoiditis: the silent epidemic. Denver: Futuremed, 2000. p. 7-17. [ Links ]
24. Jones AM, Stambough JL, Balderstyon RA, et al. Long-term results of lumbar spine surgery complicated by incidental durotomy. Spine 1989; 14: 443-6. [ Links ]
25. Goodkin R, Laska LL. Unintended "incidental" durotomy during surgery of the lumbar spine: medicolegal implications. Surg Neurol 1995; 43: 4-14. [ Links ]
26. Lau KK, Stebnyckyj M, McKenzie A. Post-laminectomy pseudomeningocele: an unusual case of bone erosion. Australas Radiol 1992; 36: 262-4. [ Links ]
27. Aldrete JA, Ghaly RF. Post-laminectomy pseudomeningocele: an unsuspected cause of low back pain. Reg Anesth 1995; 20: 75-9. [ Links ]
28. Aldrete JA, Ferrari H. Myelopathy with syringomyelia following thoracic epidural anaesthesia. Anaesth Intens Care 2004; 32: 161-4. [ Links ]
29. Kim R, Porter RW, Chi BH, Kim SW. Myelopathy after intrathecal administration of hypertonic saline. Neurosurgery 1998; 22: 942-5. [ Links ]
30. Aldrete JA, Zapata JC, Ghaly RF. Arachnoiditis following epidural adhesiolysis with hypertonic saline. Report oftwo cases. Pain Digest 1996; 6: 368-70. [ Links ]
31. Romero-Figueroa S, Aldrete JA, Martínez-Cruz A, Castillo-Henkel C, Guizar-Sahgun G. Nerve root axon regeneration after intrathecal injection of phenol. American Society Anesthesiology Annual Meeting, San Francisco, CA, 2003. p. 280. [ Links ]
32. Otero P, Aldrete JA, Guizar G. Wet taps from NaHCO3 and lidocaine producing cauda equine syndrome and arachnoiditis. American Society of Anesthesiologists Annual Meeting. Las Vegas NV, 2004. [ Links ]
33. Reynolds AF Jr, Hameroff SR, Blitt CD. Spinal subdural epoiarachnoid hematoma: a complication of epidural patch technique. Anesth Analg 1980; 59: 702-3. [ Links ]
34. Aldrete JA, Brown TL. Intrathecal hematoma and arachnoiditis after prophylactic blood patch through a catheter. Anesth Analg 1997; 84: 233-4. [ Links ]
35. Hogland J, Freemont AJ, Denton J, Teddie M. Retained surgical swab debris in post laminectomy arachnoiditis and peridural fibrosis. J Bone Joint Surg Br 1988; 70: 659-62. [ Links ]
36. Matsui H, Tsuji H, Kanamori M, Kawaguchi Y, Yudok K. Laminectomy induced arachnoradiculitis: a postoperative serial MRI study. Neuroradiology 1995; 37: 660-6. [ Links ]
37. Nakano M, Matsui H, Miaki K. Postlaminectomy adhesion of the cauda equina. Changes of postoperative vascular permeability of the cauda equina in rats. Spine 1997; 22: 298-304. [ Links ]