Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista de la Sociedad Española del Dolor
versión impresa ISSN 1134-8046
Rev. Soc. Esp. Dolor vol.17 no.1 Madrid ene./feb. 2010
La sinergia farmacológica aplicada a la analgesia: revisión de la combinación de ibuprofeno con codeína
Pharmacological synergy applied to analgesia: review of the combination of ibuprofen with codeine
J.R. González-Escalada
Unidad del Dolor, Hospital Ramón y Cajal, Madrid, España
Dirección para correspondencia
RESUMEN
La analgesia multimodal que participa actualmente en todos los protocolos de analgesia postoperatoria también se utiliza por los especialistas en dolor crónico que manejan la combinación de fármacos como una rutina para optimizar la eficacia de la analgesia; la combinación de fármacos es una práctica bien conocida y muy extendida, gracias a su demostrada rentabilidad terapéutica, y habitualmente se utiliza tanto en anestesia como en analgesia. El concepto del balance adecuado entre efectividad y seguridad es primordial, y aunque la calidad del tratamiento aplicado se mide según el alivio conseguido, el confort se evalúa teniendo en cuenta la combinación entre eficacia analgésica y la ausencia o mínima presencia de efectos secundarios, siendo primordial en el tratamiento del paciente con dolor. En este sentido, parece claro que la búsqueda de las dosis mínimas eficaces de cada fármaco es una premisa necesaria para plantear la combinación de dosis idónea. La búsqueda de los fármacos que deben componer una combinación y las dosis a emplear debe ser fruto de la investigación, pero debe ser corroborada por la experiencia clínica, la opinión de los expertos y las evidencias publicadas. En este trabajo, se realiza una extensa revisión de la experiencia clínica existente con la combinación de ibuprofeno con codeína, haciendo un análisis de los antecedentes históricos que llevaron a su uso, los trabajos que permitieron demostrar su sinergia y compatibilidad farmacocinética y los trabajos pioneros de investigación clínica que permitieron concluir que la dosis fija idónea de esta combinación es la mezcla de 400 mg de ibuprofeno con 30 mg de codeína. Es difícil sacar conclusiones acerca de la efectividad analgésica de los diferentes antiinflamatorios no esteroideos, pero no cabe duda que según los datos acumulados hasta la actualidad, el ibuprofeno se sitúa entre los más efectivos y es una buena opción para incluirlo en cualquier producto galénico de combinación analgésica. Muchos trabajos en dolor agudo indican que el ibuprofeno sólo mejora la eficacia del paracetamol y de la unión de paracetamol con codeína. Los estudios comparativos entre ibuprofeno con codeína y codeína a altas dosis demuestran una diferencia muy significativa (p > 0,05) a favor de la combinación. Además, estas diferencias se amplían en estudios de dolor agudo con dosis múltiples y en estudios de dolor crónico. La unión de ibuprofeno y codeína en dosis fija, de aparición reciente en nuestro país, cumple con todos los criterios exigibles para ser denominada y etiquetada como terapia muldimodal y ha demostrado ser una excelente opción terapéutica para dolor agudo y dolor crónico en los múltiples estudios revisados.
Palabras clave: AINE; Ibuprofeno; Codeína; Sinergias; Opiáceos; Dolor agudo; Analgesia multimodal; Dolor crónico.
ABSTRACT
Multimodal analgesia, which is currently included in all postoperative analgesia protocols, is also used by specialists in chronic pain who routinely use drug combinations to optimize analgesic effectiveness; drug combination is a well-known and widespread practice due to its demonstrated therapeutic utility and is routinely used in both anesthesia and analgesia. The concept of an adequate balance between safety and effectiveness is essential. Although the quality of treatment is measured by the relief obtained, comfort is evaluated by taking into account the relation between analgesic efficacy and the absence, or minimal presence, of adverse effects, which is crucial in the treatment of patients with pain. The search for the minimum effective dose for each drug is crucial to achieve the optimal combination of doses. The search for drugs to form a combination and the doses to be used should be the result of research but should also be corroborated by clinical experience, expert opinion and published evidence. The present article provides an extensive review of clinical experience of the use of ibuprofen with codeine and analyzes the historical antecedents leading to the use of this combination, the studies demonstrating the synergy between these drugs and their pharmacokinetic compatibility and the pioneer clinical studies that allowed the optimal fixed dose of this combination to be defined as 400 mg of ibuprofen with 30 mg codeine. It is difficult to draw conclusions on the analgesic effectiveness of the distinct non-steroidal anti-inflammatory agents but, according to the data gathered to date, ibuprofen is undoubtedly among the most effective agents in this class and is a good option for inclusion in any galenic product combining analgesics. Numerous studies in acute pain indicate that ibuprofen only improves the efficacy of paracetamol and that of the combination of paracetamol and codeine. Studies comparing ibuprofen plus codeine with high-dose codeine show a highly significant difference (p > 0.05) in favor of the combination. Moreover, the differences are increased in studies of acute pain with multiple doses and in studies of chronic pain. The fixed-dose combination of ibuprofen plus codeine, recently introduced in Spain, fulfills all the criteria required for multimodal therapy and has been demonstrated to be an excellent therapeutic option for acute and chronic pain in the numerous studies reviewed.
Key words: NSAID; Ibuprofen; Synergies; Opioids; Acute pain; Multimodal analgesia; Chronic pain.
Introducción
El dolor participa en el sistema integral de defensa animal mediante una estructura anatómica propia, cuya función es asegurar que el estímulo nocivo se perciba con rapidez y desencadene una sensación suficientemente repulsiva y desagradable como para que el individuo desarrolle reflejos inmediatos de rechazo.
La analgesia precoz cumple esencialmente 2 funciones: en primer lugar, evita el sufrimiento innecesario y la cascada de cambios hemodinámicos y homeostáticos que provoca en el organismo la estimulación aguda, y en segundo lugar, evita la posible cronificación del proceso y previene las complicaciones derivadas de una excesiva y prolongada inhibición psicomotora que puede ser motivo de un rápido y progresivo deterioro de la función. En el dolor agudo se involucran diversos mecanismos que sensibilizan al sistema nervioso, amplifican el dolor y hacen que el síntoma se dilate en el tiempo y en el espacio; por eso, la combinación de fármacos analgésicos actuando sobre distintas dianas parecía que empíricamente debería ser una buena herramienta para mejorar el equilibrio fisiológico del organismo y optimizar la eficacia de la propia analgesia. Esto quedó plenamente demostrado en el cuidado del paciente recién operado, donde es una práctica habitual aconsejar combinaciones de analgésicos según una rutina que se denomina analgesia multimodal y que actualmente participa en todos los protocolos de analgesia postoperatoria. Esta estrategia también se utiliza por los especialistas en dolor crónico que manejan la combinación de fármacos como una rutina para optimizar la eficacia de la analgesia; por tanto, se puede afirmar que la combinación de fármacos es una práctica bien conocida y muy extendida, gracias a su demostrada rentabilidad terapéutica, y se utiliza habitualmente tanto en anestesia como en analgesia.
La elección de una determinada combinación farmacológica no es casual ni caprichosa. Según el concepto de lo adecuado, para el tratamiento del dolor bastaría con unir moléculas con mecanismos analgésicos efectivos y diferentes. Pero aunque esencialmente idóneo, esto no es suficiente. Se necesita, además, que estos productos no compitan metabólicamente, que su farmacodinamia sea compatible y que la acción analgésica de ambos se sume. Fuera del ambiente hospitalario hay un reto más: que la administración de ambos fármacos sea lo más cómoda y fácil para el paciente; con este último objetivo, se elaboran galénicas con la combinación de dosis fijas de las moléculas. Estas fórmulas exigen además una premisa accesoria: que las características físicas de ambos fármacos permitan su fusión galénica. Aun así, y elegida la formula deseada, es necesario buscar otros beneficios más sólidos, ya que la simple suma de las actividades analgésicas de las moléculas sólo justificaría la comodidad de administración.
La sinergia farmacológica tras la administración conjunta de 2 moléculas implica que el efecto resultante supera la simple suma del efecto de los 2 fármacos cuando se aplican aisladamente. Por lo tanto, la existencia de sinergia analgésica entre las moléculas justifica suficientemente cualquier esfuerzo y trabajo galénico. La sinergia potencia la efectividad de la mezcla y permite utilizar dosis menores de cada fármaco sin menoscabar la eficacia, mejorando así la seguridad.
En analgesia, el concepto del balance adecuado entre efectividad y seguridad es primordial y, aunque la calidad del tratamiento aplicado se mide según el alivio conseguido, el confort se evalúa teniendo en cuenta la combinación entre eficacia analgésica y la ausencia o mínima presencia de efectos secundarios, siendo primordial en el tratamiento del paciente con dolor agudo. En este sentido, parece claro que la búsqueda de las dosis mínimas eficaces de cada fármaco es una premisa necesaria para plantear la combinación de dosis idónea. Esta búsqueda es fruto de la investigación, pero se debe corroborar por la experiencia clínica, la opinión de los expertos y las evidencias publicadas.
Una vez sentadas las bases para considerar aceptable la combinación de 2 fármacos sinérgicos, su utilización en fórmulas galénicas con dosis fijas y óptimas ayuda a la racionalización del tratamiento y a la simplificación de su administración. Hay varios ejemplos de combinaciones de analgésicos a dosis fijas en el mercado español; todos ellos gozan de excelente aceptabilidad, tanto por parte de los profesionales como por parte de los pacientes, mejorando el cumplimiento terapéutico. En este artículo se revisa la combinación de ibuprofeno, un antiinflamatorio no esteroideo (AINE), sin duda el más utilizado en analgesia por su excelente ratio de eficacia/seguridad, y la codeína, un opiáceo menor, fármaco paradigmático del segundo escalón del ya conocido protocolo analgésico de la Organización Mundial de la Salud.
Revisión histórica de la combinación de antiinflamatorios no esteroideos con opiáceos
Ningún agente analgésico es perfecto y no puede tratar todos los tipos de dolor. Cada producto tiene algunas ventajas y también desventajas en comparación con los demás y, por lo tanto, los resultados clínicos podrían mejorarse con la combinación de algunos de ellos. Una combinación galénica es más efectiva cuando se emplean fármacos que actúan por mecanismos analgésicos diferentes y, sobre todo, si son sinérgicos1, lo que implica inhibir la nocicepción en distintos lugares de su transmisión o percepción; de esta forma, la combinación de moléculas puede proporcionar un alivio más eficaz para un espectro más amplio de dolor y, además, reducir los efectos adversos farmacológicos.
No hace muchos años que se descubrió que el mecanismo de acción de los AINE iba ligado a la inhibición de la síntesis de prostaglandinas2; desde entonces, estos fármacos se habían considerado el ejemplo del analgésico periférico. Estudios recientes han demostrado que, además de su acción periférica, también ejercen su efecto antinociceptivo actuando sobre el sistema nervioso central (SNC)3 y, especialmente, en la médula espinal4. La acción central de los AINE se achacó, en principio, a una actividad antiprostaglandínica central5 y aunque esto parece indudable, posteriormente se ha comprobado que también están involucrados otros mecanismos de neuromodulación no ligados a la inhibición de la ciclooxigenasa (COX) en el SNC6,7. A partir de estos nuevos descubrimientos, los AINE se perfilan como analgésicos de acción mixta, central y periférica, ampliando de forma notable sus indicaciones terapéuticas en dolor. Actualmente, han tomado relevancia los mecanismos analgésicos centrales mediante los que actúan los AINE, sobre todo después de haberse descrito las importantes acciones neuroprotectoras que tienen estos fármacos sobre el SNC, al neutralizar los efectos neurotóxicos que ejercen ambas isoenzimas de la COX, tanto la COX-1 como la COX-2, sobre las estructuras de la médula espinal8,9. Estos mecanismos centrales puede ser la explicación de la distinta potencia analgésica que muestran los AINE. Basándose en este hecho, McCormack7 estratifica este grupo de fármacos según su eficacia y sitúa a ibuprofeno dentro del grupo de los AINE con mayor potencia analgésica. Bien es verdad que esto no era una novedad, ya que antes de esa publicación y desde su descubrimiento hace ya muchos años10, la eficacia analgésica del ibuprofeno era bien conocida y referida en multitud de trabajos clínicos11-14.
Siguiendo el camino inverso, inicialmente los opiáceos se consideraron como analgésicos de exclusiva acción central. El mecanismo de acción analgésica de los opiáceos se debe a su unión a unos receptores específicos cuya ocupación produce una profunda analgesia. Esta hipótesis era ya antigua y ampliamente barajada por los investigadores desde hacía muchos años15, pero los receptores no se consiguieron aislar hasta 198916. De la misma forma, los ligandos naturales de estos receptores, denominados endorfinas, que eran conocidos desde hacía tiempo17, no se pudieron codificar hasta años después, en 1993. Hasta entonces, se creía que los receptores opiáceos estaban confinados al SN y, por tanto, sólo era allí donde estos fármacos deberían ejercer su acción analgésica, y aunque ya se sabía que había actividad opiácea fuera del SNC (ganglio de la raíz dorsal)18, no fue hasta 1990 cuando Stein et al19 describen receptores opiáceos en las terminaciones nerviosas de las aferentes nociceptivas, detallando la sobreexpresión de estos receptores en los tejidos inflamados, evidenciando la eficacia analgésica de los opiáceos aplicados periféricamente20 en condiciones de inflamación. De esta forma, los opiáceos también se pueden considerar fármacos de acción mixta (central y periférica) e incluso interactuar de forma beneficiosa durante el proceso inflamatorio periférico, dándose así fuertemente la mano con los otros analgésicos conocidos, los AINE.
La codeína es un opiáceo débil, cuya pobre acción analgésica es conocida desde hace muchos años21. Desde la descripción inicial, en las primeras publicaciones en que se realizaron curvas de dosis/eficacia, se observó que la codeína tenía un efecto de saturación a partir de los 60 mg por vía parenteral y, a partir de estas dosis, no se conseguía disminuir el umbral del dolor aunque se aumentara su dosis. Además, este efecto "techo" se producía cuando sólo se había conseguido un descenso del 50% del umbral del dolor, por lo que se le consideró como un analgésico opiáceo débil o de baja potencia. A pesar de estas limitaciones, la codeína mostraba un perfil idóneo para los dolores suaves moderados, ya que su seguridad era mayor que la de los opiáceos más potentes22,23. Buscando mejorar su potencia, pronto se empezaron a utilizar mezclas de codeína con otros analgésicos, y como hasta hace pocos años se consideraba a los AINE como fármacos de acción únicamente periférica y los opiáceos de acción central exclusiva, su combinación resultaba de una lógica incuestionable, suponiendo que el resultado de la unión de estos 2 mecanismos daría como resultado una sinergia analgésica muy completa24. En concreto, se empezaron a utilizar combinaciones con el ácido acetilsalicílico y el paracetamol, mezclas que incluso sirvieron posteriormente como el gold standar para estudios comparativos con otros fármacos analgésicos para el dolor leve-moderado25.
Pero la historia de la combinación de analgésicos para potenciar su acción era antigua. Prácticamente, desde que Bayer comercializó la aspirina se buscaron fusiones con otros productos para mejorar su tolerabilidad, disminuir los efectos indeseables o mejorar su eficacia. La combinación de acido acetilsalicílico y cafeína fue la pionera en la combinación de fármacos antinociceptivos, y poco después aparecieron mezclas de paracetamol con codeína y cafeína. Las primeras experiencias se publican en modelos de dolor agudo26,27 y concluyen que la mezcla de estos 2 fármacos supera los resultados antinociceptivos de los mismos productos individualmente. En los ensayos iniciales, las dosis empleadas de los fármacos eran muy bajas, 300 mg de paracetamol más 20 mg de codeína, por lo que se destacaba que la incidencia de efectos secundarios era mucho menor que la de los fármacos aislados.
Muchos años después de utilizar galénicas que contenían estas mezclas, se llegó a la conclusión de que estas combinaciones constituyen una estrategia útil que consigue varios objetivos: por un lado, la mayor comodidad para el paciente; por otro, mejorar el cumplimiento terapéutico y simplificar la prescripción, y finalmente, lo más importante, mejorar la eficacia sin incrementar los efectos adversos y minorizar los efectos adversos sin menoscabar la eficacia28.
La combinación de paracetamol y codeína, que a pesar de los años de uso y del hecho que se cuestione su efectividad29-31 sigue siendo muy utilizada, e incluso en algunos hospitales de Estados Unidos se emplea como referente y estándar para el dolor durante el período de poscirugía obstétrica, y ha evidenciado ser eficaz tanto tras cesárea y episiotomía como para otras intervenciones perineales en la mujer29. Sin embargo, muchos autores cuestionan su utilización y han demostrado fehacientemente que no proporciona más alivio que un AINE aislado del tipo del ibuprofeno o naproxeno30-32. Una situación similar ocurre cuando se compara un AINE aislado con la mezcla de paracetamol e hidrocodona, un opiáceo no comercializado en España, no apreciando diferencias en eficacia analgésica entre los 2 grupos33; e incluso hay estudios que no encuentran diferencias entre el paracetamol aislado y la mezcla de paracetamol con hidrocodona34.
Es muy posible que la escasa efectividad de estas mezclas se deba a que se utilizan fármacos con mecanismos de acción no claramente sinérgicos. En una revisión reciente, la mezcla de paracetamol con oxicodona puede mejorar la eficacia de la oxicodona aislada35, pero con un comportamiento psicofarmacológico similar entre la mezcla de paracetamol con hidrocodona y de paracetamol con oxicodona36; es decir, en estos estudios se observa una eficacia escasamente sumativa (no sinérgica) entre las 2 combinaciones. Esto hace pensar que mejor que combinar 2 fármacos de acción fundamentalmente central, parecería más adecuado la combinación de paracetamol con otros antiinflamatorios de acción periférica37,38, ocurrencia que ya se había demostrado eficaz hace mucho tiempo39, o bien buscar la combinación de un AINE con acción antiprostraglandínica periférica, como el ibuprofeno, con un opiáceo más o menos potente40, simulando la analgesia multimodal cuya eficacia es incuestionable41. La combinación de un opiáceo con ibuprofeno ya se sabe que es muy eficaz en dolor agudo42,43, aportando mayor confort a los pacientes, y es un hecho constatado que la combinación de ibuprofeno/oxicodona es mucho más eficaz que la mezcla de paracetamol/ oxicodona o de paracetamol/hidrocodona44 (fig. 1), siendo la adición del AINE, en este caso el ibuprofeno, la que marca las diferencias entre los grupos.

Figura 1 Comparación de una mezcla de oxicodona/ibuprofeno
con la de oxicodona/paracetamol e hidrocodona/paracetamol,
según estudio de Litkowski et al40. TOTPAR6: alivio total del
dolor a las 6 h; SPID6: suma de diferencias en escala del
dolor durante 6 h.
Investigación y evidencias de la efectividad analgésica de la combinación de ibuprofeno y codeína
Así pues, hay suficientes razones para afirmar que la mezcla de un fármaco opiáceo con un AINE de gran potencia analgésica, como el ibuprofeno, cumple con los criterios idóneos para conseguir una buena combinación de mejor eficacia antihiperalgésica. El sinergismo entre el ibuprofeno y un fármaco opiáceo parece evidente40,42-44. Como consecuencia de este efecto analgésico mejorado es posible utilizar dosis más bajas y, por tanto, disminuir la incidencia de los efectos adversos individuales de los fármacos45, con lo que se gana en confort analgésico.
En la década de los ochenta, varios autores experimentaron con la combinación de ibuprofeno con codeína46-49, evidenciando que la combinación era más eficaz que la codeína aislada46,47 (fig. 2) y que los pacientes que tomaron la mezcla consumían menos analgesia accesoria que los que tomaron codeína sola46. En otro estudio que comparaba distintas dosis de ibuprofeno mezcladas con distintas dosis de codeína frente a aspirina y placebo, se observó que cualquiera de las combinaciones utilizadas (ibuprofeno/codeína: 200/15, 400/30 y 800/60) era más eficaz que el placebo y que la aspirina administrada en dosis analgésica (fig. 3), sin encontrar grandes diferencias entre las distintas combinaciones probadas pero evidenciando que la que contenía las dosis de 400 mg de ibuprofeno y 30 mg de codeína era la que mostraba el mejor balance entre eficacia y seguridad48. En otro estudio, se demuestra que la combinación de ibuprofeno y codeína supera en eficacia a la de aspirina con codeína; en este estudio, en ambos grupos de tratamiento se utilizaron las mismas dosis de codeína50, y se comprueba que además de mejorar la eficacia hay una menor incidencia de efectos secundarios en el grupo de ibuprofeno. Mc-Quay et al51, en un estudio cruzado sobre un modelo clínico de dolor agudo en cirugía del tercer molar, comparan la mezcla de ibuprofeno y codeína frente a ibuprofeno solo, y encuentran que la adición de 20 mg de codeína a una dosis fija de ibuprofeno no sólo mejora la eficacia analgésica del AINE, sino que, además, la diferencia se amplía con el uso repetido y continuado del tratamiento, lo que permite predecir que esta mezcla es un producto idóneo para su uso crónico (fig. 4). En otro estudio cruzado posterior, el mismo grupo realiza un estudio que compara la combinación de ibuprofeno con codeína con otra de paracetamol con codeína, apreciándose significativas diferencias a favor del grupo de ibuprofeno52, sin que hubieran diferencias en la incidencia de efectos adversos entre los 2 grupos. Resultados similares obtienen Quiding et al53, que comparan también ibuprofeno y su combinación con codeína en un modelo de dolor crónico en pacientes con coxartrosis, observando el mismo comportamiento descrito por McQuay et al en el sentido de que la eficacia de esta combinación de fármacos mejora después de dosis repetidas.

Figura 2 Estudio doble ciego, aleatorizado y de dosis única en
113 pacientes sometidos a una episiotomía. Ibuprofeno + codeína
es más eficaz que codeína y placebo. Tomada de Norman et al46.
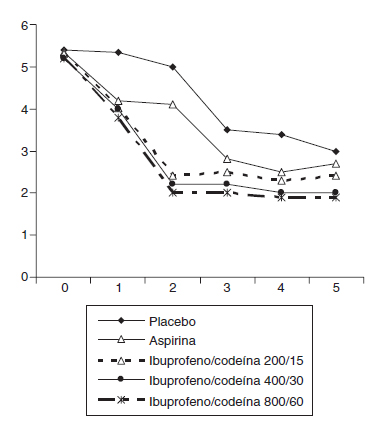
Figura 3 Estudio de eficacia de varias mezclas de ibuprofeno
+ codeína, frente a aspirina y placebo. Tomada de Frame et al48.
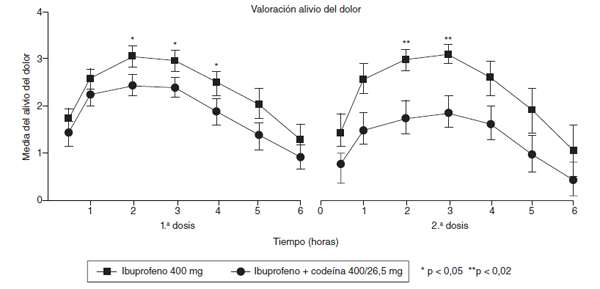
Figura 4 Estudio doble ciego, aleatorizado, cruzado y de dosis múltiple en pacientes sometidos a
cirugía dental, comparando la eficacia de ibuprofeno + codeína, ampliándose las diferencias a partir
de la segunda dosis. Tomada de McQuay et al51.
Tras estas evidencias iniciales, se realizaron investigaciones encaminadas a objetivar la previsible sinergia entre ambos productos. En 1992 Doak et al54, basándose en los resultados ya publicados en dolor agudo, diseñan un estudio aleatorizado y controlado con placebo en un modelo clínico de dolor crónico, en pacientes con artrosis, en el que comparan la combinación de ibuprofeno más codeína con cada uno de los fármacos administrados aisladamente54. En este estudio se encontraron diferencias muy significativas entre los 4 grupos, y el grupo de ibuprofeno con codeína fue el que más analgesia aportaba. Tras el análisis más detallado de los datos y buscando sinergias, se observó que la utilización de dosis bajas de codeína en el producto de combinación potenciaba la acción del ibuprofeno de forma considerable, mejorando la analgesia tanto durante el día como durante la noche y demostrando una clara acción sinérgica entre ambos productos; estos resultados permitieron observar que esta mejoría analgésica no se acompaña de un aumento de efectos secundarios a largo plazo, concluyendo que se trata de una combinación muy adecuada para el tratamiento del dolor crónico. Los resultados iniciales se confirmaron poco después en un estudio doble ciego en un modelo similar de dolor crónico55, y aunque estos autores encontraron más efectos adversos gastrointestinales en los pacientes a los que se administró la combinación que en los que recibieron sólo ibuprofeno, ellos mismos reflexionaron que no les parecía que estos efectos estuvieran ligados a la codeína, al no haber diferencia en la incidencia de efectos centrales; actualmente, ya se conoce que esta posibilidad existe tras la demostración de la sinergia de los efectos centrales entre los AINE y los agonistas mu56, aunque afortunadamente en los estudios posteriores no se ha vuelto a repetir este dato.
También se hicieron estudios farmacocinéticos en voluntarios sanos para observar si había variabilidad en los parámetros farmacocinéticos y, por supuesto, en los resultados clínicos y en la respuesta analgésica cuando los fármacos se utilizaban combinadamente, o bien en el mismo preparado galénico o bien de forma conjunta pero en preparaciones independientes57. En el estudio al que hacemos referencia, se establece por primera vez que no hay interacciones farmacocinéticas ni físicas, tanto si se utilizan las 2 moléculas de forma combinada, y sólo se observa que la combinación de 400 mg de ibuprofeno y 60 mg de codeína puede llegar a producir una absorción más rápida en el tubo digestivo con aparición más precoz de los picos sanguíneos máximos, aunque bien es verdad que a este hallazgo los propios autores le confieren poca relevancia y repercusión clínica por su expresa variabilidad, sugiriendo estudios más amplios y más concluyentes al respecto.
A nosotros nos ha parecido muy interesante la hipótesis que se establece en un trabajo de revisión reciente, que deduce que la combinación de un AINE y un opiáceo puede revertir parcialmente los efectos adversos ligados a la acción central de aquellos, gracias a la demostrada acción sinérgica de ambos productos en la sustancia gris periacueductal, una región cerebral crítica en analgesia y donde, curiosamente, convergen las acciones centrales de ambos productos58-60 y que podría permitir bajar las dosis del opiáceo progresivamente sin menoscabar la analgesia.
Ya hay suficiente experiencia clínica con la combinación de ibuprofeno con codeína en preparados galénicos en dosis fija, y parece suficientemente demostrada la seguridad y eficacia de esta combinación según los resultados publicados en varios estudios clínicos de ésta46-55. Todos los autores coinciden en señalar que no sólo la combinación es más eficaz que los fármacos empleados de forma aislada, sino que además la sinergia analgésica entre ellos permite emplear dosis más bajas y minorizar la incidencia de efectos adversos. Aun a pesar de que casi todos los autores coinciden en afirmar que la mezcla de 400 mg de ibuprofeno con 30 mg de codeína es la que mejor perfil de seguridad aporta y que no se consiguen grandes diferencias en eficacia empleando dosis mayores, Sunshine et al61 publican un trabajo en dolor agudo en el que demuestran mejorar el beneficio que se obtiene con la combinación clásica (400/30) al emplear la combinación de 400 mg de ibuprofeno y 60 de codeína. Resultados similares publican Hellman et al62, aunque ambos no comparan la eficacia de la dosis habitual (400/30) frente a la que ellos proponen (400/60), por lo que no es posible sacar conclusiones de esta propuesta. Con los datos de que se dispone en la actualidad, preferimos alinearnos con la gran generalidad de autores consultados, que siguen recomendando y optando por las dosis de 400/30 como la combinación óptima entre estas 2 moléculas.
Conclusión
Las combinaciones de analgésicos se utilizan muy frecuentemente en clínica. Sin embargo, una de las más utilizadas en la práctica clínica en el mundo occidental, la combinación de paracetamol con codeína, ha sido cuestionada desde hace tiempo, e incluso recientemente se demuestra que es menos potente que la utilización de un AINE, el ibuprofeno, administrado de forma aislada, e incluso que la acción de esta opción analgésica además de ser más efectiva produce un efecto más prolongado63. Muchos autores refrendan estos resultados29-31, aunque advierten que la combinación de un AINE con un opiáceo no es mala táctica. De hecho, un metaanálisis reciente64 demuestra que la adición de una dosis fija de codeína a paracetamol mejora la eficacia del paracetamol administrado en las mismas dosis de forma aislada en el dolor postoperatorio del adulto, estimando un número estimado de pacientes a tratar (NNT) de 2,2 para dosis de 1.000 mg de paracetamol con 60 mg de codeína, con NNT mucho menos efectivos3,9 e inefectivos6,9 para dosis menores. Estos resultados permiten afirmar que la utilización conjunta de paracetamol con codeína no es mala como "concepto de estrategia analgésica", aunque sí puede ser un error la elección de los productos o las dosis empleadas en la combinación. De hecho, según los resultados del citado metaanálisis, bajar desde la dosis de 1 g de paracetamol y 60 mg de codeína proporciona un buen descalabro al NNT; la razón de su pobre eficacia en dolor agudo se debe a su escasa sinergia analgésica, pero también a la falta de indicación para esta patología.
El dolor agudo es el resultado de un proceso multifactorial con la participación de mecanismos centrales y periféricos que transmiten y modulan la respuesta al dolor. Una de las principales causas que subyacen en el dolor agudo es la inflamación, que se inicia siempre "periféricamente" en el foco del proceso lesivo y que invoca el aumento de la sensibilidad de las terminaciones nerviosas periféricas y/o de los nociceptores que, a la fin y a la postre, producen una amplificación de la sensación del dolor producida por la propia lesión. Si la analgesia combinada ha sido utilizada ampliamente y con éxito en dolor agudo, se debe a este concepto etiopatogénico "multifactorial" que justificaba la incorporación de analgésicos múltiples en una sola terapia de combinación, la denominada "analgesia multimodal", que proporcionaba ganancias claras en el alivio del dolor. Pero no cualquier combinación de fármacos es adecuada para cualquier tipo de dolor. Esa simplificación podría llevarnos sin duda al fracaso terapéutico. Para que una terapia combinada para el dolor agudo sea considerada multimodal, debería cumplir los criterios de abordar las diferentes vías del dolor de forma simultánea y asociada. La inclusión de un fármaco AINE, prototipo de los productos que gozan de la capacidad de neutralizar el proceso inflamatorio al actuar como inhibidores de la síntesis de prostaglandinas periféricas y, sobre todo, al ser fármacos que interfieren con la primera etapa de la transmisión del dolor, asegura que la primera parte del argumento quedaría cubierta. También brinda la posibilidad de justificar los resultados clínicos publicados en dolor agudo y explicaría que una simple dosis de ibuprofeno supere la efectividad de la combinación de paracetamol con codeína e incluso que su acción sea más duradera.
El ibuprofeno es el AINE más conocido y utilizado en el mundo occidental; mantiene las propiedades antipiréticas y antiinflamatorias que le confieren su pertenencia a este grupo farmacológico, pero esencialmente disfruta de un potente perfil analgésico que se estima en 3,5 veces superior al de la aspirina en modelos de dolor agudo. Hace años, tras su magistral revisión, McCormack7 aproximó un distinto perfil de potencial analgésico a los distintos AINE, adjudicando al ibuprofeno un dignísimo tercer puesto entre los 9 AINE considerados, justo detrás del ketoprofeno y el ketorolaco. No hemos conseguido encontrar otra referencia bibliográfica posterior a McCormack que siga esta línea y permita jerarquizar las moléculas pertenecientes a este grupo de fármacos según su potencia analgésica. Todos los autores que revisan trabajos con AINE, tratan en sus revisiones a estos productos como un bloque, sin fisuras y los comparan en su conjunto con otros productos pero no entre sí, asumiendo una efectividad común, unos efectos secundarios similares y una actividad terapéutica superponible; de este proceder sólo eximen a los COX-2 sin tener en cuenta que se trata de una gran miscelánea de moléculas de diferente origen y con muy distinta actividad terapéutica. De esta forma, es difícil sacar conclusiones acerca de la efectividad analgésica de los diferentes AINE, pero no cabe duda que según los datos acumulados hasta la actualidad, el ibuprofeno se sitúa entre los más efectivos y es una buena opción para incluirlo en cualquier producto galénico de combinación analgésica.
De la misma forma que la adición de codeína al paracetamol amplía la pobre efectividad analgésica de aquel, su unión al ibuprofeno implementa la reconocida y poderosa analgesia del ibuprofeno, pero de forma más acusada por el referido sinergismo que hay entre estas 2 moléculas. Esto se hacía muy evidente tras los primeros años de utilización de la combinación y, desde luego, ha quedado ampliamente demostrado tras los estudios de investigación de Norman et al46 y Frame et al48. Debemos destacar de las primeras experiencias con esta combinación, la referencia constante de todos los autores en señalar algo verdaderamente inesperado: la disminución de los efectos adversos. Tras los resultados del estudio de Frame et al, parece incuestionable que la mezcla fija de 400 mg de ibuprofeno con 30 mg de codeína es la idónea, ya que su eficacia muestra una gráfica "suficiente" y prácticamente superponible a la dosis superior, manteniendo sin embargo una destacable seguridad. Estas dosis, que están por debajo de las máximas toleradas, además de ser más seguras y manifestar ese descenso de efectos secundarios que todos los autores reseñan, permiten además abrir la ventana terapéutica, algo que siempre preocupa cuando hablamos de tratamientos con AINE, donde el techo terapéutico y analgésico condiciona nuestra proyección ante el paciente y su enfermedad. Así pues, sin menoscabar la eficacia analgésica, partimos de dosis inferiores a las habituales de ibuprofeno y esto permite mantener un margen accesorio de maniobra para agudizaciones o exacerbaciones del dolor.
Hay suficientes datos que permiten afirmar que la sinergia entre un inhibidor de la COX y un opiáceo se produce por varios mecanismos, conjugando mecanismos periféricos con centrales (la hiperalgesia primaria del proceso inflamatorio con la hiperalgesia secundaria por sensibilización central), mecanismos periféricos con periféricos (la inflamación secundaria al proceso lesivo con la inflamación neurógena) y mecanismos centrales con centrales (la referida conjugación de efectos en la sustancia gris periacueductal). La unión de ibuprofeno y codeína en dosis fija, de aparición reciente en nuestro país, cumple con todos los criterios exigibles para ser denominada y etiquetada como terapia muldimodal y ha demostrado ser una excelente opción terapéutica para dolor agudo en los múltiples estudios realizados.
Pero sería injusto relegar la combinación de ibuprofeno con codeína en dosis fija a esa única indicación. Realmente, tanto los resultados del estudio de McQuay et al51, realizado en un modelo de dolor agudo con dosis repetidas, como los del estudio de Quiding et al53, realizado en un modelo de dolor crónico, demuestran que la utilización repetida del fármaco mejora su perfil analgésico. Esto sí es novedoso en analgesia y esto sí le confiere un valor añadido a la combinación. Este comportamiento farmacológico puede explicarse por la potenciación de la sinergia tras las primeras dosis, ya que una vez neutralizados los factores moleculares periféricos por el AINE, puede haber un mejor acoplamiento del trabajo de ambos fármacos y como consecuencia un descenso del estímulo nocivo periférico que llega al segmento medular donde trabajará con más eficacia un opiáceo poco potente como es la codeína, mostrando así su mejor nivel de eficacia. Sea por este motivo o por otro que se nos escapa, clínicamente se ha observado que las administraciones consecutivas de la combinación se manifiestan progresivamente más eficaces y esto le confiere un perfil extraordinariamente útil para su recomendación en dolor crónico; precisamente en los estudios realizados en dolor crónico, la evidencia de efectividad muestra que hay mayores diferencias con respecto a placebo que en dolor agudo. Más aún si tenemos en cuenta los últimos descubrimientos acerca de la gran convergencia en los mecanismos centrales cerebrales de potenciación y persistencia del dolor, y la recientemente demostrada sinergia central entre los AINE y los opiáceos, que colocan las combinaciones entre ambos en un primer plano en el tratamiento del paciente con dolor crónico, sobre todo teniendo en cuenta la hipótesis de que la combinación de un AINE y un opiáceo puede revertir parcialmente los efectos adversos ligados a la acción central de los segundos gracias a la convergencia de las acciones centrales de ambos productos58-60.
El tratamiento multimodal, o terapia analgésica balanceada, ha servido de excusa para la aparición reciente de nuevas combinaciones analgésicas65 y no se puede argumentar nada que pueda cuestionarlo. La búsqueda de los mejores fármacos, las mejores sinergias y, finalmente, el mejor confort del paciente, hace tener esperanza en el crecimiento en eficacia de nuestro armamentario analgésico. El tratamiento multimodal no es un concepto que deba quedar relegado al tratamiento del dolor agudo, como es lógico; este concepto puede y debe extenderse a cualquier estrategia analgésica, y se debe incluir en cualquier plan preestablecido o en la guía clínica de cualquier proceso doloroso, ya que hoy día nadie duda en señalar la eficacia de estos tratamientos en el manejo del proceso doloroso.
Conflicto de intereses
El autor declara no tener ningún conflicto de intereses.
Bibliografía
1. Sveen K, Gilhuus-Moe O. Paracetamol/codeine in relieving pain following removal of impacted mandibular third molars. Int J Oral Surg. 1975;4:258-66. [ Links ]
2. Vane JR. Inhibition of prostaglandin synthesis as a mechanism of action for aspirin-like drugs. Nat New Biol. 1971;231:237-9. [ Links ]
3. Carlsson KH, Helmreich J, Jurna I. Activation of inhibition from the periaqueductal grey matter mediates central analgesic effect of metamizol (dipyrone). Pain. 1986;27:373-90. [ Links ]
4. Jurna I, Spohrer B, Bock R. Intrathecal injection of acetylsalicylic acid, salicylic acid and indomethacin depresses C fibreevoked activity in the rat thalamus and spinal cord. Pain. 1992; 49:249-56. [ Links ]
5. Willingale HL, Gardiner NJ, McLymont N, Giblett S, Grubb BD. Prostanoids synthesized by cyclo-oxygenase isoforms in rat spinal cord and their contribution to the development of neuronal hyperexcitability. Br J Pharmacol. 1997;122:1593-604. [ Links ]
6. Cherng CH, Wong CS, Ho ST. Spinal actions of nonsteroidal anti-inflammatory drugs. Acta Anaesthesiol Sin. 1996;34:81-8. [ Links ]
7. McCormack K. Non-steroidal anti-inflammatory drugs and spinal nociceptive processing. Pain. 1994;59:9-43. [ Links ]
8. Kaufmann WE, Andreasson KI, Isakson PC, Worley PF. Cyclooxygenases and the central nervous system. Prostaglandins. 1997; 54:601-24. [ Links ]
9. Vanegas H, Schaible HG. Prostaglandins and cycloxygenases in the spinal cord. Prog Neurobiol. 2001;64:327-63. [ Links ]
10. Chalmers TM. Clinical trials of a new drug, ibufenac, in the treatment of rheumatoid arthritis: a preliminary report. Ann Rheum Dis. 1963;22:358-62. [ Links ]
11. Boardman PL, Nuki G, Hart FD. Ibuprofen in the treatment of rheumatoid arthritis and osteo-arthritis. Ann Rheum Dis. 1967;26: 560-1. [ Links ]
12. Jasani MK, Downie WW, Samuels BM, Buchanan WW. Ibuprofen in rheumatoid arthritis. Clinical study of analgesic and anti-inflammatory activity. Ann Rheum Dis. 1968;27:457-62. [ Links ]
13. Adams SS, McCullough KF, Nicholson JS. The pharmacological properties of ibuprofen, an anti-inflammatory analgesic and antipyretic agent. Arch Int Pharmacodyn Ther. 1969;178:115-29. [ Links ]
14. Brown DL, Mackey DC. Management of postoperative pain: influence of anesthetic and analgesic choice. Mayo Clin Proc. 1993;68:768-77. [ Links ]
15. Spector S. Opiate receptors and their clinical implications. Circ Res. 1980;46:I-138-41. [ Links ]
16. Goldstein A, Naidu A. Multiple opioid receptors: ligand selectivity profiles and binding site signatures. Mol Pharmacol. 1989; 36:265-72. [ Links ]
17. Tregear GW, Coghlan JP. Enkephalin, endorphin, and the opiate receptor. Circ Res. 1980;46:I-142-8. [ Links ]
18. Lamotte C, Pert CB, Snyder SH. Opiate receptor binding in primate spinal cord: distribution and changes after dorsal root section. Brain Res. 1976;112:407-12. [ Links ]
19. Stein C, Hassan AH, Przewlocki R, Gramsch C, Peter K, Herz A. Opioids from immunocytes interact with receptors on sensory nerves to inhibit nociception in inflammation. Proc Natl Acad Sci USA. 1990;87:5935-9. [ Links ]
20. Khoury GF, Stein C, Garland DE. Intra-articular morphine for pain after knee arthroscopy. Lancet. 1990;336:874. [ Links ]
21. Eddy NB. Studies of morphine, codeine and their derivatives; general methods. J Pharm Exper Therap. 1932;45:339. [ Links ]
22. Davis FA. Poppy politics. The codeine (methylmorphine) connection. Clin Toxicol. 1978;12:505-6. [ Links ]
23. Wolff HG, Hardy JD, Goodell H. Studies on pain. Measurement of the effect of morphine, codeine, and other opiates on the pain threshold and an analysis of their relation to the pain experience. J Clin Invest. 1940;19:659-80. [ Links ]
24. Grotto M, Dikstein S, Sulman FG. Additive and augmentative synergism between analgesic drugs. Arch Int Pharmacodyn Ther. 1965;155:365-72. [ Links ]
25. Iles JD. Relief of postoperative pain by ibuprofen: a report of two studies. Can J Surg. 1980;23:288-90. [ Links ]
26. Analgesic combinations of paracetamol and codeine. Practitioner. 1968;200:584-9. [ Links ]
27. Levin HM, Bare WW, Berry FN, Miller JM. Acetaminophen with codeine for the relief of severe pain in postpartum patients. Curr Ther Res Clin Exp. 1974;16:921-7. [ Links ]
28. Raffa RB. Pharmacology of oral combination analgesics: rational therapy for pain. J Clin Pharm Ther. 2001;26:257-64. [ Links ]
29. Nauta M, Landsmeer ML, Koren G. Codeine-acetaminophen versus nonsteroidal anti-inflammatory drugs in the treatment of post-abdominal surgery pain: a systematic review of randomized trials. Am J Surg. 2009;198:256-61. [ Links ]
30. Drendel AL, Gorelick MH, Weisman SJ, Lyon R, Brousseau DC, Kim MK. A randomized clinical trial of ibuprofen versus acetaminophen with codeine for acute pediatric arm fracture pain. Ann Emerg Med. 2009;54:553-60. [ Links ]
31. Chen T, Adamson PA. Comparison of ibuprofen and acetaminophen with codeine following cosmetic facial surgery. J Otolaryngol Head Neck Surg. 2009;38:580-6. [ Links ]
32. Malmstrom K, Kotey P, Coughlin H, Desjardins PJ. A randomized, double-blind, parallel-group study comparing the analgesic effect of etoricoxib to placebo, naproxen sodium, and acetaminophen with codeine using the dental impaction pain model. Clin J Pain. 2004;20:147-55. [ Links ]
33. Reed KL, Smith JR, Lie T, Adams DF. A pilot study comparing ketoprofen and acetaminophen with hydrocodone for the relief of postoperative periodontal discomfort. Anesth Prog. 1997;44: 49-54. [ Links ]
34. Miner JR. Randomized double-blind placebo controlled crossover study of acetaminophen, ibuprofen, acetaminophen/hydro-codone, and placebo for the relief of pain from a standard painful stimulus. Acad Emerg Med. 2009;16:911-4. [ Links ]
35. Gaskell H, Derry S, Moore RA, McQuay HJ. Single dose oral oxycodone and oxycodone plus paracetamol (acetaminophen) for acute postoperative pain in adults. Cochrane Database Syst Rev. 2009;(3):CD002763. [ Links ]
36. Zacny JP, Gutiérrez S. Within-subject comparison of the psychopharmacological profiles of oral hydrocodone and oxycodone combination products in non-drug-abusing volunteers. Drug Alcohol Depend. 2009;101:107-14. [ Links ]
37. Qiu HX, Liu J, Kong H, Liu Y, Mei XG. Isobolographic analysis of the antinociceptive interactions between ketoprofen and paracetamol. Eur J Pharmacol. 2007;557:141-6. [ Links ]
38. Mitchell A, Van Zanten SV, Inglis K, Porter G. A randomized controlled trial comparing acetaminophen plus ibuprofen versus acetaminophen plus codeine plus caffeine after outpatient general surgery. J Am Coll Surg. 2008;206:472-9. [ Links ]
39. Murphy JE, Donald JF, Layes Molla A. Analgesic efficacy and acceptability of fenoprofen combined with paracetamol and compared with dihydrocodeine tartrate in general practice. J Int Med Res. 1978;6:375-80. [ Links ]
40. Oldfield V, Perry CM. Oxycodone/Ibuprofen combination tablet: a review of its use in the management of acute pain. Drugs. 2005;65:2337-54. [ Links ]
41. Duellman TJ, Gaffigan C, Milbrandt JC, Allan DG. Multi-modal, pre-emptive analgesia decreases the length of hospital stay following total joint arthroplasty. Orthopedics. 2009;32:167. [ Links ]
42. Van Dyke T, Litkowski LJ, Kiersch TA, Zarringhalam NM, Zheng H, Newman K. Combination oxycodone 5 mg/ibuprofen 400 mg for the treatment of postoperative pain: a double-blind, placebo-and active-controlled parallel-group study. Clin Ther. 2004;26: 2003-14. [ Links ]
43. Singla N, Pong A, Newman K; MD-10 Study Group. Combination oxycodone 5 mg/ibuprofen 400 mg for the treatment of pain after abdominal or pelvic surgery in women: a randomized, double-blind, placebo- and active-controlled parallel-group study. Clin Ther. 2005;27:45-57. [ Links ]
44. Litkowski LJ, Christensen SE, Adamson DN, Van Dyke T, Han SH, Newman KB. Analgesic efficacy and tolerability of oxycodone 5 mg/ibuprofen 400 mg compared with those of oxycodone 5 mg/acetaminophen 325 mg and hydrocodone 7.5 mg/acetaminophen 500 mg in patients with moderate to severe postoperative pain: a randomized, double-blind, placebo-controlled, single-dose, parallel-group study in a dental pain model. Clin Ther. 2005;27:418-29. [ Links ]
45. Beaver WT. Combination analgesics. Am J Med. 1984;77:38-53. [ Links ]
46. Norman SL, Jeavons BI, O´Brien PM, Johnson IR, Hitchcock A, Noyelle RM, et al. A double-blind comparison of a new ibuprofen-codeine phosphate combination, codeine phosphate, and placebo in the relief of postepisiotomy pain. Clin Ther. 1985; 7:549-54. [ Links ]
47. Hill CM, Carroll MJ, Giles AD, Pickvance N. Ibuprofen given preand post-operatively for the relief of pain. Int J Oral Maxillofac Surg. 1987;16:420-4. [ Links ]
48. Frame JW, Fisher SE, Pickvance NJ, Skene AM. A double-blind placebo-controlled comparison of three ibuprofen/codeine combinations and aspirin. Br J Oral Maxillofac Surg. 1986;24: 122-9. [ Links ]
49. Giles AD, Hill CM, Shepherd JP, Stewart DJ, Pickvance NJ. A single dose assessment of an ibuprofen/codeine combination in postoperative dental pain. Int J Oral Maxillofac Surg. 1986;15: 727-32. [ Links ]
50. Cooper SA, Engel J, Ladov M, Precheur H, Rosenheck A, Rauch D. Analgesic efficacy of an ibuprofen-codeine combination. Pharmacotherapy. 1982;2:162-7. [ Links ]
51. McQuay HJ, Carroll D, Watts PG, Juniper RP, Moore RA. Codeine 20 mg increases pain relief from ibuprofen 400 mg after third molar surgery. A repeat-dosing comparison of ibuprofen and an ibuprofen-codeine combination. Pain. 1989;37:7-13. [ Links ]
52. McQuay HJ, Carroll D, Guest P, Juniper RP, Moore RA. A multiple dose comparison of combinations of ibuprofen and codeine and paracetamol, codeine and caffeine after third molar surgery. Anaesthesia. 1992;47:672-7. [ Links ]
53. Quiding H, Grimstad J, Rusten K, Stubhaug A, Bremnes J, Breivik H. Ibuprofen plus codeine, ibuprofen, and placebo in a single- and multidose cross-over comparison for coxarthrosis pain. Pain. 1992;50:303-7. [ Links ]
54. Doak W, Hosie J, Hossain M, James IGV, Reid I, Miller AJ. A novel combination of ibuprofen and codeine phosphate in the treatment of osteoarthritis: A double-blind placebo controlled study. J Drug Dev. 1992;4:179-87. [ Links ]
55. James IGV, Miller AJ. A combination of ibuprofen and codeine phosphate in the management of osteoarthritis: A double-blind comparison with ibuprofen. Br J Clin Res. 1993;4:199-210. [ Links ]
56. Williams JT. The painless synergism of aspirin and opium. Nature. 1997;390:557-9. [ Links ]
57. Kaltenbach ML, Mohammed SS, Mullersman G, Perrin JH, Derendorf H. Pharmacokinetic evaluation of two ibuprofen-codeine combinations. Int J Clin Pharmacol Ther. 1994;32:210-4. [ Links ]
58. Christie MJ, Connor M, Vaughan CW, Ingram SL, Bagley EE. Cellular actions of opioids and other analgesics: implications for synergism in pain relief. Clin Exp Pharmacol Physiol. 2000;27: 520-3. [ Links ]
59. Christie MJ, Vaughan CW, Ingram SL. Opioids, NSAIDs and 5-lipoxygenase inhibitors act synergistically in brain via arachidonic acid metabolism. Inflamm Res. 1999;48:1-4. [ Links ]
60. Vaughan CW, Ingram SL, Connor MA, Christie MJ. How opioids inhibit GABA-mediated neurotransmission. Nature. 1997;390: 611-4. [ Links ]
61. Sunshine A, Roure C, Olson N, Laska EM, Zorrilla C, Rivera J. Analgesic efficacy of two ibuprofen-codeine combinations for the treatment of postepisiotomy and postoperative pain. Clin Pharmacol Ther. 1987;42:374-80. [ Links ]
62. Hellman M, Ahlström U, Andersson L, Strid S. Analgesic efficacy of an ibuprofen-codeine combination in patients with pain after removal of lower third molars. Eur J Clin Pharmacol. 1992; 43:347-50. [ Links ]
63. Heidrich G, Slavic-Svircev V, Kaiko R. Efficacy and quality of ibuprofen and acetaminophen plus codeine analgesia. Pain. 1985;22:385-97. [ Links ]
64. Toms L, Derry S, Moore RA, McQuay HJ. Single dose oral paracetamol (acetaminophen) with codeine for postoperative pain in adults. Cochrane Database Syst Rev. 2009 Jan 21;(1): CD001547. [ Links ]
65. Schug SA. Combination analgesia in 2005 - a rational approach: focus on paracetamol-tramadol. Clin Rheumatol. 2006;25 S1: S16-21. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Correo electrónico: jr.escalada@telefonica.net
Recibido el 1 de septiembre de 2009;
Aceptado el 1 de diciembre de 2009














