Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista de la Sociedad Española del Dolor
versão impressa ISSN 1134-8046
Rev. Soc. Esp. Dolor vol.20 no.3 Madrid Mai./Jun. 2013
https://dx.doi.org/10.4321/S1134-80462013000300006
Fentanilo en el dolor irruptivo oncológico
Fentanyl for breakthrough cancer pain
J. Moya Riera1, M. Murillo González2, D. Rodríguez Mesa3 e Y. Escobar Álvarez4
1Unidad del Dolor. Hospital Mateu Orfila. Menorca
2Servicio de Oncología Radioterápica. Hospital 12 de Octubre. Madrid
3Unidad de Cuidados Paliativos. Hospital Sant Joan de Reus. Tarragona
4Servicio de Oncología Médica. Hospital General Universitario Gregorio Marañón. Madrid
Dirección para correspondencia
RESUMEN
El control del dolor en el paciente oncológico es un aspecto importante en la calidad de la asistencia a las personas.
El fármaco de elección en el tratamiento del DIO requiere una potencia adecuada y una muy rápida velocidad de absorción. Esta velocidad es un aspecto crítico.
Las preparaciones de fentanilo, debido a su gran potencia, son probablemente los fármacos que el clínico debe emplear en el DIO, pero no todas las preparaciones de fentanilo presentan una cinética similar.
Las propiedades farmacocinéticas del comprimido bucal de fentanilo (CBF) con tecnología OraVescent®, han mostrado una gran velocidad de absorción, mucho más rápida que otras preparaciones de opiáceos.
Se dispone de evidencia suficiente que indica que la preparación de CBF es eficaz en los episodios de DIO.
El CBF ha mostrado eficacia también en dolor irruptivo no relacionado con el cáncer.
Palabras clave: Fentanilo. Dolor irruptivo. Cáncer.
ABSTRACT
Pain control is an important aspect in the quality of the healthcare.
The drug of choice in breakthrough pain control requires potency and a very fast rate of absorption. This speed is a critical aspect.
The preparations of fentanyl, because of its great potency, probably are drugs that the clinician should use in patients with breakthrough pain, but not all fentanyl preparations have similar kinetics.
The pharmacokinetic properties of fentanyl buccal tablets (FBT) powered by OraVescent® drug delivery technology have shown great speed of absorption, much faster than other preparations of opiates.
There is evidence indicating that the preparation of FBT fentanyl is effective in episodes of cancer breakthrough pain.
Fentanyl FTB has also shown efficacy in breakthrough pain not related to cancer.
Key words: Fentanyl. Breakthrough pain. Cancer.
Introducción
El dolor irruptivo oncológico (DIO) puede definirse como una exacerbación transitoria de dolor intenso en un paciente con dolor crónico relativamente estable y adecuadamente controlado (1). Los estudios en pacientes con dolor oncológico han mostrado una prevalencia alta de estos episodios (2,3) que son un problema no resuelto en su totalidad. Muchos autores aceptan que, actualmente, el dolor oncológico no está suficientemente controlado (4-7) pese a ser un aspecto muy importante en la calidad de la atención sanitaria de las personas.
Un aspecto relevante del DIO es que su aparición no es previsible y que la mayoría de episodios (87%) tienen una duración menor a una hora (8). Así mismo su etiopatogenia no es completamente conocida, siendo un fenómeno complejo y heterogéneo.
El tratamiento del dolor en oncología suele ser insuficiente por falta de conocimientos sobre la fisiopatología del dolor, los fármacos disponibles, su utilización no adecuada o a dosis insuficientes y, sobre todo, porque no se valora correctamente la intensidad, ya que el dolor es un síntoma difícil de valorar y cuantificar. El control del dolor en el paciente oncológico incluye aspectos farmacológicos, emocionales y socio-familiares, pero los primeros son probablemente los más importantes.
Fentanilo: una aproximación a un fármaco ideal en dio
El tratamiento del DIO requiere un fármaco de rápido inicio de acción, corta duración y potencia adecuada. Actualmente tan solo un 9% de los episodios de DIO se tratan con opioides de rápida acción (9).
Una práctica común en el tratamiento del DIO es añadir opioides de acción corta, como morfina, hidrocodona u oxicodona de liberación inmediata. Sin embargo estos fármacos requieren un mínimo de 30 minutos para producir efecto analgésico y en consecuencia muchas veces su utilización no es efectiva.
A mediados de la década de los 50 la morfina era el analgésico estándar para el control del dolor. En esta década se inició la investigación con opioides de mayor potencia, inicio de acción más rápido y menores efectos adversos. Fentanilo fue sintetizado por Paul Janssen en Janssen Pharmaceutical en 1959 (10). Janssen había trabajado con un fármaco antiespasmódico, petidina (meperidina), que tenía propiedades analgésicas potentes y observó que en su estructura química tenía, al igual que la morfina, un anillo de piperidina al que él y sus colaboradores atribuyeron los efectos analgésicos. Sin embargo era menos potente que la morfina, debido a que sus propiedades hidrofílicas dificultaban su penetración en el sistema nervioso. A partir de la petidina, Janssen sintetizó moléculas más solubles en lípidos, entre ellas el fentanilo que es 80 veces más potente que la morfina (10).
En la década de 1960, el fentanilo fue introducido como un anestésico intravenoso y todavía hoy se usa por su corta duración de acción en el periodo perioperatorio y en premedicación, inducción y mantenimiento de la anestesia, así como para el control del dolor postoperatorio (11). El fentanilo es también usado como suplemento analgésico en la anestesia general o regional (11). Posteriormente en los años 90 se introdujo fentanilo por vía transdérmica y más recientemente por vía transmucosa para el tratamiento del dolor irruptivo.
Fentanilo: propiedades farmacocinéticas y farmacodinámicas
Fentanilo es un analgésico opioide que actúa sobre los receptores opioides μ localizados en el sistema nervioso, produciendo analgesia y sedación, aunque determinados análogos pueden producir efectos también a través de los receptores delta y kappa (12). Se caracteriza por su potencia muy alta, siendo su administración intravenosa 80 veces más potente que la administración intravenosa de morfina (13). Los efectos del fentanilo, así como su toxicidad, están relacionados con su concentración plasmática, aunque con el tiempo, los pacientes desarrollan tolerancia.
Administrado por vía intravenosa el fentanilo atraviesa fácilmente la barrera hematoencefálica debido a su liposolubilidad y entra con rapidez en el sistema nervioso central (14). Administrado por vía oral se absorbe por el tracto gastrointestinal y sufre un metabolismo intestinal y hepático (metabolismo hepático de primer paso), por lo que su biodisponibilidad es baja, aproximadamente del 30% (15). Debido a estas limitaciones se desarrollaron otras formulaciones de fentanilo para uso ambulatorio, incluyendo preparaciones para administración nasal, transdérmica y transmucosa.
La administración transdérmica de fentanilo ha sido ampliamente estudiada y pese a la dificultad de atravesar el estrato córneo de la piel, la elevada liposolubilidad del fentanilo permite la absorción por esta vía (16). La vía transdérmica es adecuada para el control del dolor basal, pero no para tratar el DIO.
Tras la administración de fentanilo por vía nasal a través de un pulverizador, las gotas forman un gel fino en la mucosa nasal y el fármaco se difunde desde el gel, absorbiéndose a través de la mucosa nasal, esta absorción modulada por el gel restringe el valor máximo en la concentración plasmática (Cmax), mientras que permite que se alcance pronto ese valor máximo (Tmax). En un estudio farmacocinético llevado a cabo por Fisher (17) mostró que el fentanilo se absorbe rápidamente después de la administración de una dosis única por vía intranasal, con una mediana de Tmax de 15 a 21 minutos.
El fentanilo es metabolizado principalmente por el citocromo P450, tiene una vida media corta y se elimina por vía renal.
El tratamiento del dolor irruptivo con fentalino parenteral puede satisfacer los requisitos de rapidez y corta duración de acción, pero este enfoque no es factible para el manejo del DIO. Como hemos mencionado, en el tratamiento del DIO se utilizan también otras vías de administración del fármaco, como es la vía transmucosa y sublingual que describiremos a continuación.
Fentanilo: administración a través de la mucosa oral
La mucosa bucal es una vía adecuada para la liberación de fármacos, ya que es fácilmente accesible, carece del estrato córneo que dificulta la penetración del fármaco y evita el metabolismo hepático de primer paso (18).
Esta vía de absorción tiene ventajas sobre la vía oral, principalmente su rapidez de inicio de acción, pero también la minimización del metabolismo hepático de primer paso del fentanilo, así como su mejor tolerancia en pacientes con disfagia, náuseas o vómitos (19).
La formulación de citrato de fentanilo transmucosa oral (CFOT), fue el primer opiode de acción rápida que se utilizó para el control del DIO. Se utiliza con un aplicador, desplazándolo por la mucosa bucal sin masticar. Posteriormente aparecieron comprimidos sublinguales y comprimidos bucales con tecnología OraVescent
Actualmente existen tres tipos de formulación transmucosa disponibles: citrato de fentanilo oral transmucoso (CFOT), comprimido bucal de fentanilo (CBF) y citrato de fentanilo sublingual (CFS). En la tabla I se exponen las características de biodisponibilidad e inicio de acción.
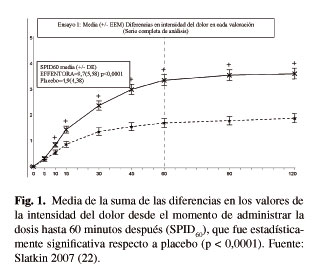
La seguridad y eficacia del comprimido bucal de fentanilo (CBF) se ha evaluado en pacientes que recibieron el medicamento al inicio de un episodio de dolor irruptivo. En la fig. 1 se observan los resultados del ensayo clínico pivotal (22), en el que el criterio de valoración principal fue la media de la suma de las diferencias en la intensidad del dolor desde el momento de administrar la dosis hasta 60 minutos después (SPID60), que fue estadísticamente significativo con respecto a placebo (p < 0,0001).
En un segundo ensayo clínico (23), el criterio de valoración principal fue SPID30. Este fue estadísticamente significativo con respecto a placebo (p < 0,0001) y registrando una mejora significativa en la diferencia de intensidad del dolor a los 15 minutos (primer punto temporal medido).
El programa de desarrollo clínico del CBF ha incluido también tres estudios de eficacia, con diseño doble ciego y controlado con placebo, en pacientes con buena tolerancia a los opioides que presentaban dolor irruptivo asociado a dolor crónico no oncológico (24-26). La variable principal de valoración de eficacia, SPID60, fue significativamente superior con CBF comparado con placebo (p < 0,005).
Todos los ensayos se basan en la percepción del dolor por parte del paciente tras administrar CBF o placebo al inicio del episodio de dolor irruptivo. No se ha estudiado la utilidad del CBF como preventivo de los episodios.
El sistema oravescent®: La velocidad de absorción es importante
La tecnología OraVescent® permite optimizar la absorción de los comprimidos al incorporar un efecto efervescente, que produce cambios en el pH. Los comprimidos efervescentes de fentanilo contienen ácido cítrico, bicarbonato sódico y citrato de fentanilo.
Al entrar en contacto con la saliva, la combinación de ácido cítrico y bicarbonato forma ácido carbónico que disminuye el pH, favoreciendo la disolución del fentanilo ionizado. Paralelamente este ácido carbónico se disocia en CO2 y H2O y la liberación de este CO2 aumenta el pH, favoreciendo la absorción del fentanilo no ionizado (Fig. 2).
Es probable que este aumento de pH forme una bomba fisiológica, causada por el gradiente de concentración local de fentanilo no ionizado, que impulsa el paso del fármaco a través de la barrera lipídica de la mucosa bucal. El aumento del pH da lugar a una forma no ionizada y absorbible de fentanilo a través de la mucosa.
En la fig. 3 (Pather y cols.) (28) se observa la concentración sérica de fentanilo después de la administración de 200 µg de fentanilo en comprimidos efervescentes (CBF OraVescent®), 200 µg de fentanilo en comprimidos no efervescentes y 200 µg en forma de citrato de fentanilo transmucosa oral (CFOT). La absorción fue más eficiente y más rápida con los comprimidos efervescentes, comparado con los otros dos sistemas (tmax p < 0,003, Cmax p < 0,001). Otro estudio mostró resultados similares (29).
Otros factores en la farmacocinética del CBF: proporcionalidad de la dosis, bioequivalencia, influencia de la edad, presencia de mucositis
El dolor oncológico es un problema que afecta muchas veces a personas mayores. Los estudios con citrato de fentanilo transmucosa en este grupo de edad han mostrado que no se observan diferencias en los parámetros farmacocinéticos comparados con personas jóvenes (30) y en consecuencia no se considera necesario modificar la dosis en personas de edad avanzada (30).
A fin de evaluar la proporcionalidad de la dosis de fentanilo bucal, un estudio en cuatro etapas mostró relaciones aproximadamente lineales entre las dosis y los parámetros farmacocinéticos dependientes de la dosis (31). Además, recientemente se ha informado de la proporcionalidad de la dosis administrando 1.300 µg (32). En consecuencia un aumento de la dosis ocasiona incrementos predecibles en la exposición sistémica al fentanilo.
Otro aspecto importante es el hecho de que la administración bucal y sublingual de fentanilo CBF son bioequivalentes (33). De esta manera, la administración por vía sublingual de un comprimido bucal de fentanilo (CBF) puede proporcionar una alternativa a la administración bucal si las condiciones del paciente lo requieren.
Los pacientes con cáncer, particularmente los tratados con radioterapia, desarrollan frecuentemente mucositis. En estos pacientes, Darwish (34) realizó un estudio de farmacocinética, comparando la absorción de una dosis de fentanilo en comprimidos efervescentes en pacientes con y sin mucositis. Los resultados mostraron que la absorción fue similar en ambos grupos y que el fármaco fue bien tolerado. No se registraron efectos adversos en la mucosa oral en los pacientes con mucositis.
Seguridad y tolerabilidad
La mayoría de los efectos adversos registrados con CBF fueron de intensidad leve o moderada, y comparables a los observados con otros opioides, y los efectos graves se relacionaron predominantemente con la enfermedad subyacente. Principalmente se han notificado efectos adversos gastrointestinales (náuseas, vómitos, estreñimiento) y sobre el sistema nervioso central (mareo, vértigo, cefalea).
Se ha realizado también un estudio abierto a largo plazo (35) cuyos resultados mostraron un perfil de acontecimientos adversos comparable al observado en pacientes con cáncer tratados con opioides. La mayoría de pacientes no requirió cambios en la dosis en el transcurso del tiempo.
Los estudios de seguridad se han realizado con pacientes tratados previamente con opiáceos, por lo que cabe suponer que estos pacientes presentaban un cierto grado de tolerancia. Cabe destacar que el tratamiento con opioides de acción prolongada, utilizados para tratar el dolor basal, debe estabilizarse antes de iniciar el tratamiento con CBF y el paciente debe proseguir el tratamiento con el opioide de larga duración mientras esté tomando CBF. Es aconsejable monitorizar al paciente durante el proceso de ajuste de dosis y considerar el riesgo potencial de depresión respiratoria. El CBF ha sido clasificado como categoría C durante el embarazo (el riesgo no puede ser excluido).
La mayoría de los pacientes valoraron positivamente el tratamiento con CBF: 93% valoraron como excelente o buena la rapidez de inicio de acción, 82% la comodidad de uso y el 88% mostraron preferencia por este tratamiento frente a la medicación previa (35).
Bibliografía
1. Portenoy RK, Forbes K, Lussier D, et al. Difficult pain problems: an integrated approach. In: Doyle D, Hanks G, Cherny N, et al (editors). Oxford Texbook of Palliative Medicine 3rd ed. Oxford: Oxford University Press; 2004. p. 438-58. [ Links ]
2. Breivik H, Cherny N, Collett B, et al. Cancer related pain: a pan-European survey of prevalence, treatment, and patient attitudes. Ann Oncol. 2009;20(8):1420-33. [ Links ]
3. Greco MT, Corli O, Montanari M, et al; Writing Protocol Committee; Cancer Pain Outcome Research Study Group (CPOR SG) Investigators. Epidemiology and pattern of care of breakthrough cancer pain in a longitudinal sample of cancer patients: results from the Cancer Pain Outcome Research Study Group. Clin J Pain. 2011;27(1):9-18. [ Links ]
4. Delgado-Guay MO, Bruera E. Management of pain in the older person with cancer. Part 2: treatment options. Oncology (Williston Park). 2008;22(2):148-52. [ Links ]
5. Yennurajalingam S, Braiteh F, Bruera E. Pain and terminal delirium research in the elderly. Clin Geriatr Med. 2005; 21(1):93-119. [ Links ]
6. Basso U, Monfardini S. Multidimensional geriatric evaluation in elderly cancer patients: a practical approach. Eur J Cancer Care. 2004;13:424-33. [ Links ]
7. Bernabei R, Gambassi G, Lapane K, et al. Management of pain in elderly patients with cancer. SAGE Study Group. Systematic Assessment of Geriatric Drug Use via Epidemiology. JAMA. 1998;279(23):1877-82. [ Links ]
8. Gomez-Batiste X, Madrid F, Moreno F, et al. Breakthrough cancer pain: prevalence and characteristics in patients in Catalonia, Spain. J Pain Symptom Manage. 2002;24:45-52. [ Links ]
9. Datos IMS QIII 2010. [ Links ]
10. Stanley TH, Egan TD, Van Aken H. A tribute to Dr. Paul A. J. Janssen: entrepreneur extraordinaire, innovative scientist, and significant contributor to anesthesiology. Anesth Analg. 2008;106(2):451-62. [ Links ]
11. Peng PW, Sandler AN. A review of the use of fentanyl analgesia in the management of acute pain in adults.Anesthesiology 1999;90:576-99. [ Links ]
12. Maguire P, Tsai N, Kamal J, et al. Pharmacological profiles of fentanyl analogs at mu, delta and kappa opiate receptors. Eur J Pharmacol. 1992;213(2):219-25. [ Links ]
13. Resine T, Pasternak G. Opioid analgesics and antagonist. In: Hardman JG et al (editors). Goodman and Gilman's Pharmacologic Basis of Therapeutics. 9th ed. New York. McGraw-Hill, 1996. p. 521-55. [ Links ]
14. Fine PG, Portenoy RK. A Clinical Guide to Opioid Analgesia. 2o Ed. New York, NY: Vendome Group Health Care Division. 2007. [ Links ]
15. Streisand JB, Varvel JR, Stanski DR, et al. Absortion and bioavalability of oral transmucosal fentanyl. Anesthesiology. 1991;75:223-9. [ Links ]
16. Hill HF. Clinical pharmacology of transdermal fentanyl. Eur J Pain 1990;11:81-91. [ Links ]
17. Fisher A, Watling M, Smith A, et al. Pharmacokinetics and relative bioavailability of fentanyl pectin nasal spray 100-800 µg in healthy volunteers. Int J Clin Pharmacol Therap, 2010;48:860-7. [ Links ]
18. Nicolazzo JA, Reed BL, Finnin BC, et al. Buccal penetration enhancers-how do they really work? J Control Release.2005;105:1-15101(3):738-43. [ Links ]
19. Zhang H, Zhang J, Streisand JB, et al. Oral mucosal drug delivery: clinical pharamacokinetics and therapeutic applications. Clin Pharmacokinet. 2002;41:661-80. [ Links ]
20. Darwish M, Tempero K, Kirby M, et al. Absolute and relative bioavailability of fentanyl buccal tablet and oral transmucosal fentanyl citrate. J Clin Pharmacol. 2007;47:343-50. [ Links ]
21. Ficha técnica Abstral® [ Links ].
22. Slatkin NE et al. Fentanyl buccal tablet for relief of breakthrough pain in opioid-tolerant patients with cancer-related chronic pain. J Support Oncol. 2007; 5:327-34. [ Links ]
23. Portenoy RK, Taylor D, Messina J, et al. A randomized, placebo-controlled study of fentanyl buccal tablet for breakthrough pain in opioid-treated patients with cancer. Clin J Pain. 2006; 22:805-11. [ Links ]
24. Farrar JT, Messina J, Xie F, et al. A novel 12-week study, with three randomized, doublé blind, placebo-controlled periods to evaluate fentanyl buccal tablets for the relief of breakthrough pain in opioid-tolerant patients with noncancer-related chronic pain. Pain Med. 2010;11(9):1313-27 [ Links ]
25. Simpson DM, Messina J, Xie F, et al. Fentanyl buccal tablet for the relief of breakthrough pain in opioid-tolerant adult patients with chronic neuropathic pain: a multicenter, randomized, double-blind, placebo-controlled study. Clin Ther. 2007;29:588-601. [ Links ]
26. Portenoy RK, Messina J, Xie F, et al. Fentanyl buccal tablet (FBT) for relief of breakthrough pain in opioid-treated patients with chronic low back pain: a randomized, placebo-controlled study. Curr Med Res Opin. 2007;23:223-33. [ Links ]
27. Durfee S, Messina J, Khankari R. Fentanyl Effervescent Buccal Tablets. Am J Drug Delv. 2006;4(1):1-5. [ Links ]
28. Pather SI, Siebert JM, Hontz J, et al. Enhanced buccal delivery of fentanyl using the OraVescent drug delivery system. Drug Deliv Technol. 2001;1:54-7. [ Links ]
29. Darwish M, Tempero K, Kirby M, et al. Pharmacokinetics and dose proportionality of fentanyl effervescent buccal tablets in healthy volunteers. Clin Pharmacokinet. 2005;44(12):1279-86. [ Links ]
30. Kharasch ED, Hoffer C, Whittington D. Influence of age on the pharmacokinetics and pharmacodynamics of oral transmucosal fentanyl citrate. Anesthesiology. 2004;101(3):738-43. [ Links ]
31. Darwish M, Kirby M, Robertson P Jr et al. Pharmacokinetic properties of fentanyl effervescent buccal tablets: a phase I, open label, crossover study of single-dose 100,200,400 and 800 microg in healthy adult volunteers. Clin Ther 2006; 28(5):707-14. [ Links ]
32. Darwish M, Tempero K, Kirby M, et al. Relative bioavailability of the fentanyl effervescent buccal tablet (FEBT) 1,080 pg versus oral transmucosal fentanyl citrate 1,600 pg and dose proportionality of FEBT 270 to 1,300 microg: a single-dose, randomized, open-label, three-period study in healthy adult volunteers. Clin Ther. 2006 May;28(5):715-24. [ Links ]
33. Darwish M, Kirby M, Jiang JG, et al. Bioequivalence following buccal and sublingual placement of fentanyl buccal tablet 400 microg in healthy subjects. Clin Drug Invest. 2008; 28:1-7 [ Links ]
34. Darwish M, Kirby M, Robertson P, et al. Absorption of fentanyl from fentanyl buccal tablet in cancer patients with or without oral mucositis: a pilot study. Clin Drug Investig. 2007; 27(9):605-11. [ Links ]
35. Weinstein SM, Messina J, Xie F. Fentanyl buccal tablet for the treatment of breakthrough pain in opioid-tolerant patients with chronic cancer pain: a long term, open label safety study. Cancer. 2009;11:2571-9. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Jordi Moya Riera
e-mail: jordimoyariera@gmail.com
Recibido: 12-09-12
Aceptado: 24-12-12