INTRODUCCIÓN
El SANP es una entidad descrita por Amarenco hacia 1987 1, resultando fundamental su conocimiento por parte del cirujano.
El nervio pudendo presenta tres ramas terminales: el nervio rectal inferior, perineal y dorsal del pene/clítoris 2,3,4, existiendo puntos críticos de atrapamiento: el ligamento sacroespinoso y sacrotuberoso, el proceso falciforme y el canal de Alcock. En la etiología del atrapamiento aparecen actividades profesionales/deportivas que implican posición de sedestación 5,6, traumatismos perineales 7), causas ginecológicas 8,9,10, radioterapia pélvica, etc. 11,12,13.
La clínica fundamental es el dolor en el territorio de distribución del nervio, uni o bilateral, que empeora a lo largo del día y al sentarse, y mejora al acostarse. Puede asociar síntomas proctológicos (estreñimento, sensación de cuerpo extraño rectal), urinarios o sexuales 14,15,16. A la exploración destaca el signo de Tinel (dolor desencadenado al comprimir el nervio contra la espina isquiática) y el Rolling Test (desplazamiento de la piel y subcutáneo del ano hacia pubis, reproduciendo el dolor) 17.
El test de latencia motora distal (St. Mark´s) tiene gran importancia 18,19,20,21,22. Existen criterios diagnósticos conocidos como criterios de Nantes 23 (Tabla 1). El diagnóstico diferencial se establece con endometriosis, tumores, metástasis, etc. 23,24.
El tratamiento incluye manejo sintomático del dolor con fármacos 25,26,27, infiltraciones corticoideoanestésicas 28,29,30, fisioterapia pélvica 31, toxina botulínica 32, etc. En el tratamiento quirúrgico destaca la técnica transglútea, transperineal o transvaginal 33,34,35,36 con el objetivo de liberar el nervio.
Se está investigando con células madres, radioterapia pulsada, laparoscopia, etc., con resultados todavía poco concluyentes 37.
MATERIAL Y MÉTODOS
Presentamos un estudio observacional prospectivo de 53 pacientes con proctalgia que cumplen criterios de Nantes 33, diagnosticados de SANP, en los que se puncionó el nervio según técnica descrita posteriormente.
Objetivos:
Establecer la relación de la proctalgia con SANP.
Comprobar la respuesta inmediata a la infiltración anestésica.
Valorar los resultados clínicos postinfiltración y la eficacia del tratamiento a medio plazo (seis meses).
Para evaluar los resultados utilizamos la Escala Visual Analógica del dolor (EVA) en tres momentos:
La técnica utilizada es la punción-hidrodistensión con corticoides-ropivacaína al 0,2 % a nivel del tronco y ramas terminales del nervio. En posición de litotomía, vía transdérmica, guiándonos por ecografía transanal y utilizando neuroestimulador. La punción se repite a la semana de la primera y pasadas dos semanas de la segunda punción hasta un total de tres infiltraciones (Figura 1). En pacientes sin mejoría significativa se plantea una segunda "tanda" de punciones.
Hemos considerado dos grupos de trabajo, cuyo punto de corte se estableció de forma aleatoria según nuestros resultados:
No respondedores: pacientes cuya reducción de puntuación de escala EVA a partir de los seis meses de la primera punción ha sido menor del 30 %.
Respondedores: pacientes cuya reducción de puntuación de escala EVA a partir de los 6 meses de la primera punción ha sido mayor o igual del 30 %.
Análisis estadístico
Se ha aplicado el test de Chi-cuadrado, V de Cramer y Wilcoxon a las variables sexo, antecedentes personales, ramas afectas, signos clínicos, positividad o negatividad en el test de St. Mark´s y puntuación en escala EVA pre y postinfiltración en relación con ser respondedor o no respondedor.
RESULTADOS
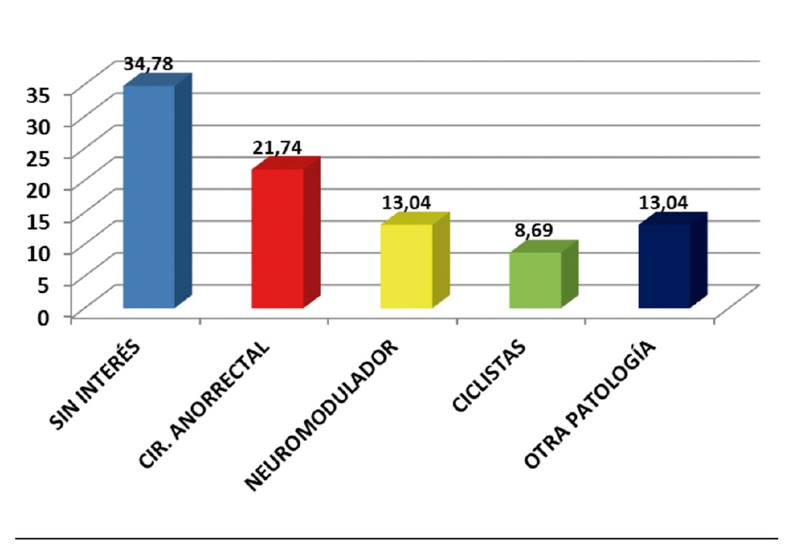
De los 53 pacientes estudiados, el 43,39 % son varones y el 56,61% mujeres. Han sido respondedores el 34,78 % de los varones y el 43,33 % de las mujeres. En relación con las ramas nerviosas afectas (según presenten sintomalogía sexual-rama anterior, urológica-rama media, proctológica-rama posterior), el 64,15 % tenían afectación de tres ramas, el 30,18 % afectación de dos ramas y afectación única de rama posterior en el 5,67 % de los casos. Observamos que en el grupo de afectación de tres ramas existe mayor porcentaje de no respondedores con respecto al de dos ramas. La edad media de los pacientes estudiados ha sido de 56,8 años (24-85 años). En cuanto a los antecedentes personales, en el grupo de varones destacan antecedentes de cirugía anorrectal (21,74 %) y sin interés (34,78 %), y en el de mujeres a estos dos grandes grupos se añade el de antecedentes ginecológicos (33,33 %) (Figura 2 y Figura 3). El signo de Tinel fue positivo en el 98,1% de los casos, y el Rolling Test únicamente resultó afirmativo en el 37,73 % de los casos sin diferencias entre respondedores y no respondedores. El test de latencia motora distal del nervio resultó patológico en el 88,46 % de los casos y observamos que en el grupo de respondedores existe casi el doble de pacientes (19,05 %) con un test normal.
La puntuación media prepunción en la escala EVA es de 7,74 (7,08 de media en el grupo de respondedores y 7,83 en el de no respondedores). La puntuación EVA referida inmediatamente tras la punción obtiene una media de 1,19 encontrando el 79,25 % de los pacientes con puntuación 0 y se observa una media de 0,4 en los respondedores y de 1,72 en los no respondedores.
A partir de los 6 meses observamos 32 pacientes no respondedores (60,38 %) y 21 respondedores (39,62 %) (Figura 4). El 24,52 % de los pacientes refieren EVA 0. La puntuación media global de EVA en este periodo es de 5,39, observando en el grupo de respondedores una media de 1,14 y en el de no respondedores de 8,18 (Figura 5).
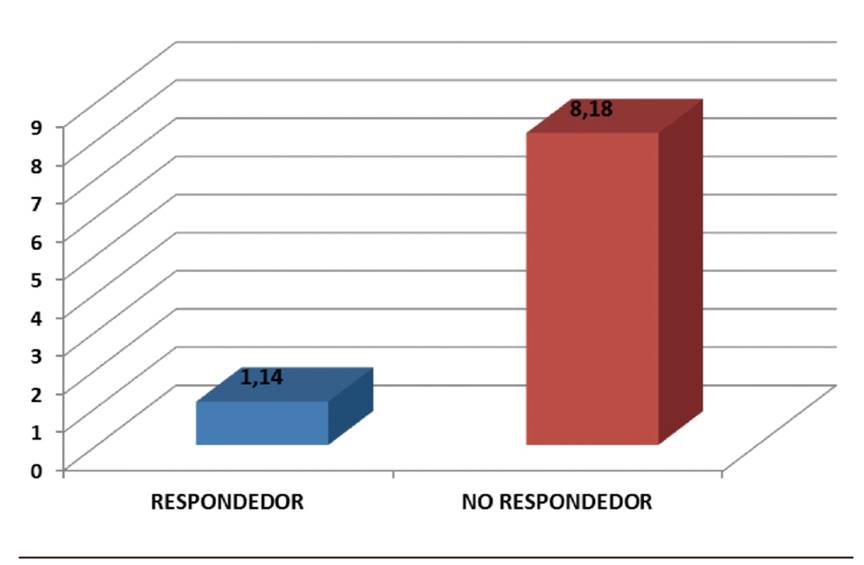
Fig. 5 Puntuación EVA media en el grupo de respondedores y no respondedores a partir de los seis meses.
En las 159 punciones practicadas, únicamente hemos constatado 4 complicaciones (2,51 %): dos amenorreas, un sangrado vaginal y un síncope vasovagal. Actualmente, 16 pacientes están recibiendo una segunda -tanda- de infiltraciones.
Aplicando la estadística a la variable sexo, antecedentes, ramas afectas, signos clínicos, St. Mark´s en relación con la respuesta al tratamiento, no hemos observado significación estadística. Por el contrario, al relacionar la puntuación en la escala EVA preinfiltración con la puntuación postinfiltración a partir de los seis meses, tanto para la muestra global como distinguiendo entre sexos, sí hemos observado significación estadística utilizando el test de Wilcoxon (p 0,00003).
DISCUSIÓN
El SANP es una entidad descrita por primera vez en 1987 por el Dr. Amarenco, dándole el nombre de Síndrome de Parálisis Perineal del Ciclista 1. Desde entonces, Shafik, Bautrant, Robert, Beco, Benson, etc., han arrojado luz en distintos puntos relacionados con el síndrome, pese a lo cual quedan muchos aspectos por esclarecer 2.
Las series publicadas señalan que la incidencia y la prevalencia son desconocidas, probablemente debido a que esta patología resulta infradiagnosticada, siendo el tiempo medio de diagnóstico de 4 años (rango de 1 a 15 años). Durante este tiempo, los pacientes son valorados por varios especialistas (cirujanos, ginecólogos, urólogos, etc.) los cuales muchas veces, por desconocimiento de este síndrome, no emiten un diagnóstico certero ofreciendo soluciones inefectivas, con lo que se prolonga el tiempo de diagnóstico con el consiguiente empeoramiento de la calidad de vida de los pacientes y el gasto innecesario de recursos sanitarios mal dirigidos.
En cuanto a la distribución por sexos, Lema 38 señala que el SANP se presenta más frecuentemente en el sexo femenino afirmando que en los próximos años en Europa y América, una de cada siete mujeres desarrollarán un SANP, probablemente debido a que gran parte de los factores etiológicos son propios del sexo femenino como la larga lista de causas ginecológicas 39. Los resultados de nuestro estudio concuerdan con lo publicado, ya que el 56,6 % de nuestros pacientes son mujeres y observamos que en el grupo de varones responden a las infiltraciones el 34,78 %, mientras que en el grupo de mujeres responden el 43,33 %, por lo que deducimos que las mujeres responden mejor a las infiltraciones anestésicas aunque sin significación estadística.
Las series publicadas señalan que en el SANP no existe una predilección por ningún grupo de edad, aspecto que confirmamos en nuestra muestra 40.
En relación con la etiología, se implicaron actividades profesionales o deportivas que impliquen tiempo prolongado en posición de sedestación como hípica, ciclismo, etc. 1,6. En nuestra muestra hay cuatro ciclistas profesionales, lo que supone el 7,5 % de los casos. Existen causas ginecológicas-obstétricas como el parto vaginal, episiotomía, cirugía pelviana y vaginal 8,9,10 en las que se ha observado mayor incidencia de SANP. En nuestra serie hemos constatado un 33,3 % de mujeres con antecedentes ginecológicos. En relación con la cirugía anorrectal, pocos estudios analizan su relación con el SANP, aunque Bautrant 41 señala la cirugía pélvica como una de las causas más frecuentes del síndrome. En nuestra serie, el 18,86 % de los pacientes presentan antecedentes de cirugía anorrectal.
Otros procesos relacionados con el síndrome son los traumatismos perineales 7, radioterapia pelviana, prolapso rectal, etc., de los cuales no hemos objetivado representación en nuestra muestra.
Existen muchos casos en los que no se identifica una causa destacable. Así, en nuestra muestra, el 33,33 % de las mujeres y el 34,78 % de los varones no presentaban antecedentes de interés.
En nuestro estudio, la proctalgia es la constante fundamental a la que puede añadirse sintomatogía de otras ramas nerviosas 14,15,16,17. Beco, en 2004 18, analizó la asociación entre incontinencia fecal, urinaria y dolor perineal, observando que el 71 % de los pacientes presentaban dos de estos síntomas mientras que el 13 % presentaban los tres. Por el contrario, en nuestra muestra, el 64,15 % de los casos presentan sintomatología de tres ramas, el 30,18 % de afectación de dos ramas y el 5,67 % con afectación única de rama posterior. Observamos que en el grupo de pacientes que presentan sintomatología de las tres ramas se incluye un mayor porcentaje de pacientes no respondedores (65,71 %) frente a aquellos que presentan afectación de dos ramas (50 %), con lo cual observamos peor respuesta en los pacientes con afectación de tres ramas.
El signo de Tinel lo consideramos un signo valioso, muy sensible, ya que en el 98,1 % de nuestros pacientes resultó positivo, siendo un único paciente, no respondedor, el que mostró este signo negativo, con lo cual demuestra además ser un signo específico. En cuanto al Rolling Test 17, fue positivo únicamente en el 37,73 % de nuestra muestra, no observando diferencias significativas entre respondedores y no respondedores, por lo que consideramos este signo como poco sensible y poco específico.
El estudio neurofisiológico más importante es el Test de Latencia Motora Distal del nervio (St. Mark´s) que se basa en medir la velocidad de conducción motora del nervio, no siendo útil para valorar la extensión de la lesión 19,20. En nuestra muestra, en el 88,46 % de los casos resultó patológico. Si distinguimos entre respondedores y no respondedores, en los primeros resultó patológico en el 80,95 % de los casos, mientras que en los segundos mostró valores patológicos en el 90,625 %, confirmando que es un test sensible y específico. A la vista de nuestros datos, deducimos que cuando los pacientes presentan un test de St. Mark´s normal responden mejor.
Resulta fundamental para el diagnóstico de exclusión realizar pruebas de imagen. En nuestra muestra se realizó TAC en 14 casos, RMN en todos y ecografía endorrectal en 49 pacientes.
También es necesario hacer diagnóstico diferencial con el síndrome de atrapamiento del nervio cutáneo posterior de la pierna, ya que en este último el dolor puede afectar a periné pero exclusivamente al escroto o labios mayores sin implicar, a diferencia de la neuralgia del pudendo, al ano, el pene o el clítoris 42. M. Mollo 21) aplicó el doppler color en la arteria pudenda interna como apoyo al diagnóstico.
El tratamiento del SANP se fundamenta en tres pilares, el tratamiento sintomático, punciones corticoideo anestésicas y la intervención quirúrgica.
En nuestra serie, todos los pacientes han recibido tratamiento médico, a base de amitriptilina y antiepilépticos, como la pregabalina o la gabapentina ampliamente utilizadas en la literatura 26,27.
El fundamento de nuestro estudio es analizar el tratamiento con punciones corticoideo-anestésicas 28,29,30,40,43. Es una técnica segura, ya que solo hemos objetivado cuatro complicaciones menores. Con respecto al tratamiento quirúrgico, en España no está desarrollado, aunque el Hospital de Vigo está comenzando con la técnica de descompresión del nervio por vía transglútea.
Hemos utilizado la escala EVA aplicada a la proctalgia porque consideramos que es un método fácil y que refleja fielmente la realidad. Así hemos obtenido una puntuación media prepunción de 7,74. En los respondedores, la puntuación media en la escala EVA ha sido de 7,08 y en los no respondedores de 7,83, con lo que ya en el periodo prepunción observamos una ligera tendencia a presentar puntuación más alta en el grupo de no respondedores.
La puntuación EVA media en el periodo inmediato tras la punción ha sido de 1,19 y es de destacar que en 42 de los 53 pacientes estudiados, la puntuación referida ha sido 0, de lo que puede deducirse que la técnica es efectiva a corto plazo. Sin embargo, al analizar la evolución observamos que muchos pacientes de los que han mostrado respuesta favorable, con el paso del tiempo se vuelven sintomáticos y alcanzan una puntuación igual o superior a la referida prepunción, con lo cual la puntuación EVA inmediata postpunción no es un buen indicador de respuesta a largo plazo.
A partir de los seis meses, tras la primera punción se obtuvo una puntuación media en escala EVA de 5,39. En 13 pacientes la puntuación ha sido 0, lo que supone el 24,52 % de los casos. Hemos obtenido 32 pacientes no respondedores (60,38 %) y 21 pacientes respondedores (39,62 %). De estas cifras deducimos que, aunque la respuesta no sea completa a largo plazo, los respondedores mantienen mejoría no despreciable a lo largo del tiempo tras la primera punción. Este hecho es trascendental, ya que muchos de nuestros pacientes llevan años con sintomatología invalidante, refractaria a todo tipo de tratamiento convencional, formando parte de un periplo de especialistas que no son capaces de ofrecer una solución a sus problemas, por lo que una mejoría en su nivel del dolor de más del 30 % en su puntuación en la escala EVA prepunción, les supone tanto alivio, satisfacción y agradecimiento que lo consideramos un gran avance y una solución que aunque muchas veces no sea total, mejora mucho la calidad de vida.
Aplicando la prueba de Wilcoxon y comparando los valores en la puntuación EVA prepunción con respecto a la puntuación EVA postpunción a partir de los seis meses, se observa que los valores de EVA han descendido significativamente, lo cual nos reafirma en que la punción-hidrodistensión corticoideo-anestésica es una técnica eficaz que ofrece mejoría completa, y en otros casos parcial, a un importante porcentaje de pacientes.
En la literatura apenas hay registradas series que evalúen como la nuestra el seguimiento más allá del periodo inmediato tras la primera punción. Así, Ricci 40 analiza la infiltración del nervio pudendo guiada por TC en una serie de cinco pacientes, afirmando que todos disminuyeron el dolor tras la infiltración, pero añadiendo que solo el seguimiento permitirá evidenciar el mantenimiento de buenos resultados. Similares hallazgos obtuvieron Mcdonald y Spigos 44 sin obtener datos a largo plazo. Fannucci 45 coincide con nosotros en que las punciones resultan un tratamiento seguro, obteniendo una eficacia clínica superior a nosotros (92 % a los 12 meses). Dehkharghani 46 demostró una elevada tasa de éxito, pero basándose en el resultado inmediato postinfiltración sin tener datos a largo plazo. Filler, en 2009 47, apuesta por el uso de la RMN para obtener imágenes precisas del nervio y dirigir mejor las infiltraciones. Como comentamos anteriormente, nuestra técnica es guiada por ecografía. Rofael en 2008 34 demostró que la ecografía permite visualizar puntos anatómicos, así como observar la difusión del anestésico local y mejorar la precisión de la técnica, reduciendo al mínimo las complicaciones. Choi 48 aplicó la fluoroscopia para mejorar la visión refiriendo una tasa de éxito del 100 % basado en la reducción en dos puntos en la escala EVA medido a los 12 meses tras la punción. A nuestro juicio cabe señalar que una reducción de dos puntos en la escala EVA no la hemos considerado como exitosa, ya que nos hemos basado en reducción de porcentaje sobre la puntuación basal en la escala EVA, considerándolo mejor reflejo de la realidad. Le Tallec de Certaines 49 analizó el tiempo de evolución del dolor y la respuesta a la infiltración, observando mejores resultados en los casos de neuralgia con un inicio del dolor inferior a un año. Analizando este dato, tal vez se debe a que el dolor de corta evolución, "agudo", obedece a causas solucionables, transitorias, mientras que el dolor "crónico" puede deberse a causas "permanentes" de difícil resolución.
Actualmente existen dos tendencias tras el fracaso de la primera punción. Estas son, nueva "tanda" de punciones o derivar hacia cirugía descompresiva.
En nuestro medio, optamos por una segunda "tanda" de punciones, por ser menos agresiva insistiendo en el tratamiento conservador.
Popeney, Ansell y Renney 50 apuestan por la cirugía descompresiva exponiendo los buenos resultados presentados por medio centenar de pacientes. En 2007, Robert 51 demuestra mejores resultados con tratamiento quirúrgico vs. tratamiento médico.
En algunas unidades especializadas en el dolor, se está investigando el uso de la radiofrecuencia pulsada o la utilización de neuromoduladores sacros, lo cual plantea nuevas líneas de investigación.
En conclusión, el SANP es una entidad dolorosa e invalidante, de incidencia y prevalencia desconocida, infradiagnosticada y más frecuente en el sexo femenino sin rango de edad predilecto para su aparición. Existe un alto porcentaje de pacientes con antecedentes ginecológicos, de cirugía anorrectal y sin interés. Según nuestros datos, la afectación de tres ramas es la más frecuente y el grupo que peor responde. El signo de Tinel es sensible y específico al contrario que el Rolling Test y consideramos que el test de St. Mark`s es un buen test diagnóstico. En nuestra experiencia, el tratamiento con punción-hidrodistensión corticoideo-anestésica logra rescatar/mejorar a un importante porcentaje de pacientes, con buenos resultados a medio plazo (seis meses) aliviando el dolor al 39,62 % de los casos y de forma estadísticamente significativa con relación al dolor prepunción.











 texto en
texto en