Meu SciELO
Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO  Similares em Google
Similares em Google
Compartilhar
Revista Española de Salud Pública
versão On-line ISSN 2173-9110versão impressa ISSN 1135-5727
Rev. Esp. Salud Publica vol.72 no.5 Madrid Set. 1998
EFECTOS DE VACUNA DE LA ENFERMEDAD MENINGOCOCICA EN CANTABRIA
Álvaro González de Aledo Linos y Jesús García Merino
Programa de vacunación antimeningocócica. Consejería de Sanidad de Cantabria.
Correspondencia:
Álvaro González de Aledo
Dirección General de Sanidad y Consumo
C/ Marqués de la Hermida, 8
39009 Santander
INTRODUCCIÓN
A principios de 1997 la Consejería de Sanidad detectó en Cantabria un incremento en la incidencia de enfermedad meningocócica, con un mayor predominio del serogrupo C y una mayor letalidad de las formas clínicas. La tasa de incidencia de enfermedad meningocócica en 1996 había sido de 10.81100.000, y el porcentaje del serogrupo C del 53.8%. La "tasa primaria de ataque" por el serogrupo C, en el grupo de riesgo de 18 meses a 19 años, aumentó preocupantemente a principios de febrero de 1997: mientras que a finales de 1996 era de 311.00.000, en la semana 4 de 1997 se elevaba a 711.00.000, en la semana 5 a 131.100.000 y en la semana 7 a 141.100.000. En las 8 primeras semanas del año se produjo un incremento en el número de meningitis meningocócicas del 190% respecto al mismo periodo de 1996, y un incremento del 260% en los casos por serogrupo C. Además, éstos revistieron mayor gravedad, con una letalidad del 13.79% para el total de las meningitis meningocócicas y del 1l.11% para las del serogrupo C. Por otra parte, se detectó la difusión de la misma cepa epidémica que estaba circulando en España (la C: 2b: Pl. 2, 5) en los casos en que se serotipó.
Ante esta situación, se tomó la decisión de iniciar una campaña de vacunación de la población de riesgo (18 meses a 19 años), a realizar en el menor tiempo posible, para atajar el brote y dejar a la población protegida, con la intención de disminuir los niveles endémicos en los próximos años. El grupo de riesgo fue establecido en las edades especificadas debido a que en 1996 más del 95% de los casos de enfermedad meningocócica en Cantabria se habían producido en menores de 20 años. Se calculó evitar por lo menos 150 casos de meningitis C, y 16 muertes en los próximos 5 años, que se elevarían a casi el doble si la eficacia clínica de la vacuna se cifrara en 10 años, como está descrito para los niños más mayores y los adultos1. Se utilizó la vacuna con polisacárido bivalente antimeningocócica A+C. Aunque en el mundo se han administrado más de 250 millones de dosis de esta vacuna desde hace más de 20 años, su utilización no tenía precedentes en esta Comunidad Autónoma, y en el resto del país sólo se había utilizado en campañas masivas de ámbito regional ese mismo invierno, en Galicia y en la Rioja.
DESARROLLO DE LA CAMPAÑA DE VACUNACIÓN
La decisión de vacunar se tomó el 14 de febrero de 1997. Se consiguió tramitar la adquisición y disponer de las dosis vacunales en una semana, a pesar de que en aquella época aún no se había autorizado su comercialización en España, por lo que hubo que importarla. La campaña se dividió en dos fases. La primera (vacunación escolar) se dirigió a vacunar a la población escolarizada, y se desarrolló entre los días 24 y 28 de febrero (por la tarde). Se dio prioridad a este colectivo por ser fácilmente accesible, al ser la escolarización obligatoria, y suponer más del 85% del total del grupo de riesgo. Con los equipos de atención primaria dependientes de la Consejería de Sanidad y del Insalud, así como con otros equipos de las Direcciones Generales de Sanidad y de Bienestar Social -es decir, sin contrataciones especiales de personal- se vacunaron 88.207 escolares (el 94.32% del censo escolar y el 81,83% de la totalidad de¡ grupo de riesgo) en 4 días y medio, y ello a pesar de la huelga del transporte que dificultó todas las operaciones de reparto de las vacunas, que debió realizarse con medios y personal propios, y con la ayuda de la Policía Local y Guardia Civil. La segunda fase, vacunación de los niños no escolarizados en los puntos habituales de vacunación, se desarrolló entre los días 3 y 12 de marzo. En las dos semanas de campaña se consiguió vacunar a 100.732 niños, es decir, el 93,45% de la población diana. En los meses siguientes se mantuvo abierta la vacunación para quienes no se habían vacunado en su momento y para los lactantes que fueran alcanzando la edad de 18 meses. Este criterio viene motivado porque en Cantabria la endemia meningocócica, al menos en los años más recientes, no tiene carácter estacional, produciéndose tantos casos en el periodo primavera- verano como en el de otoño-invierno. Con esta pauta, hasta el 31-12- 97 se mantuvo una cobertura vacunal del 95,17%, sólo en el sector público, teniendo en cuenta que la vacuna ya está libremente disponible en las farmacias y muchos niños se están vacunando en centros privados.
Los únicos efectos adversos de la vacuna durante la campaña de vacunación, sobre más de 100.000 dosis administradas, fueron una reacción urticarial inmediata, 2 reacciones urticariales tardías, y una convulsión febril postvacunal coincidente con proceso infeccioso, recuperándose todas ellas sin secuelas.
RESULTADOS DE LA CAMPAÑA EN CUANTO A EFICACIA CLINICA
Después de la campaña de vacunación transcurrió un año sin producirse ningún caso de meningitis C entre los vacunados (eficacia del 100%). En la semana 7 de 1998 se produjo el primer caso en una niña de 5 años que había sido vacunada, con un curso clínico benigno (eficacia vacunal actualmente del 95.68% en todas las edades), no habiéndose declarado más casos hasta la semana 10 de 1998, en que se hace este análisis (figura l). Este hecho no puede ser atribuido a la estacionalidad que se atribuye al meningococo, pues entre los no vacunados la incidencia no ha disminuido significativamente, con lo que también parece deducirse que la vacuna no induce inmunidad de rebaño (tabla l)2. Por otra parte la letalidad global de la enfermedad (tanto en vacunados como en no vacunados) ha sido de cero.
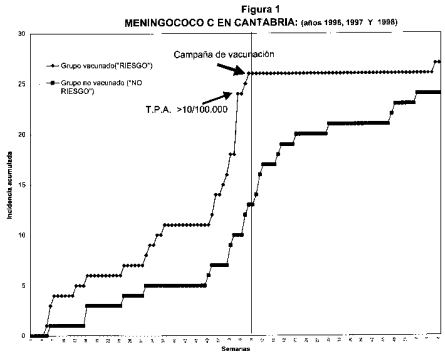
Tabla l
Efecto de la vacunación
| GRUPO DE EDAD | INCIDENCIA 3/96 A 2197 | INCIDENCIA 3197 A 2/98 | p |
| < 18 meses | 105,261100.000 | 122,801100.000 | NS |
| 18 m.-19 a. Vacunados | 21,33/100.000 | 0,921100.000 | < 0.05 |
| 18 m.-19 a. No vacunados (*) | 21,33/100.00 | 0/100.000 (**) | NS |
| >= 20 años | 1,39/100.000 | 0,931100.000 | NS |
| (*) Incidencia en el grupo de riesgo antes de la campaña de vacunación. (**) Sobre 4.311 niños del grupo de riesgo que quedaron sin vacunar. | |||
ESTUDIO DE SEROPROTECClÓN. DESARROLLO Y RESULTADOS.
A pesar del buen resultado inicial de la campaña de vacunación, se realizó en Cantabria un estudio de seroprotección para ayudarnos a decidir la revacunación si la evolución epidemiológica fuera desfavorable al acercarnos al límite de eficacia de la vacuna en los más pequeños, que los expertos sitúan entre 1 y 3 años3,4. Para ello, durante tres semanas de diciembre de 1997 (10 meses tras la campaña, para tener los resultados en febrero de 1998) se obtuvieron muestras de sangre de 423 niños vacunados de los que finalmente 414 fueron válidos para el estudio. Esta muestra se obtuvo de extracciones oportunistas realizadas en los hospitales y Centros de Atención Primaria, así como de niños escolarizados en las guarderías dependientes de la Dirección General de Bienestar Social. Los 9 niños excluidos del análisis lo fueron por estar recibiendo tratamiento inmunosupresor o corticoterapia, por referir historia de meningitis bacteriana previa, o por problemas técnicos en la prueba. Se midió la tasa de anticuerpos bactericidas5 en el laboratorio de neisserias del Centro Nacional de Microbiología de Majadahonda, estableciéndose el nivel de "efecto vacunal' en la dilución >=118. Este título es el sugerido por el Instituto de Salud Carlos III para unificar la evaluación de los estudios que se realicen en diferentes Comunidades Autónomas, aunque algunos trabajos de la bibliografía lo sitúan en 1/46,7. De un primer análisis provisional de los resultados se deduce una relación directa entre la edad al vacunarse y el porcentaje de niños con nivel bactericida >= 118, siendo en el grupo de 18-24 meses del 0%, en los del grupo de 25-36 meses alrededor del 8%, en los del grupo de 37-48 meses alrededor del 1 % y los mayores de 49 meses alrededor del 48%. No obstante, es preciso estratificar más este último grupo por su heterogeneidad de edades, y al haber comprobado que en los mayores de 14 años la positividad supera el 80%.
CONCLUSIONES DE LA EXPERIENCIA EN CANTABRIA
De esta experiencia en nuestra Comunidad Autónoma podemos extraer las siguientes conclusiones:
1º) La indicación de realizar una campaña de vacunación debe basarse únicamente en la epidemiología local, debido a las grandes diferencias interprovinciales.
2º) Si se decide vacunar, debe darse gran importancia a la información pública, pues puede ocurrir que las diferentes autoridades sanitarias o profesionales estén enviando mensajes contradictorios a la población.
3º) El éxito de la campaña, en cuanto a rapidez y cobertura, depende de una coordinación entre todas las instituciones sanitarias y de la prioridad que se le conceda, debiéndose posponer otras actividades durante la misma. En nuestro caso, opinamos que el resultado positivo durante el primer año de seguimiento obedece a la rapidez con que se consiguió vacunar al grupo de riesgo.
4º) Debe darse prioridad a la vacunación en los colegios o grupos organizados.
5º) Debe seguirse estrictamente un protocolo, pues la presión social, una vez iniciada la campaña, es enorme en el sentido de extender la vacunación más allá de la edad considerada de riesgo.
6º) La eficacia inmediata de la vacuna para el control del brote es excelente, ofreciendo una gran seguridad (mínimos efectos secundarios y muy pocas contraindicaciones).
7º) La tasa de anticuerpos bactericidas decae pronto, sobre todo en las edades inferiores. Las dos últimas circunstancias nos obligan a ser muy cautos con el uso indiscriminado de la vacuna, y a utilizarla exclusivamente, como recoge la bibliografía, en situaciones epidémicas.
8º) Es urgente llegar a un acuerdo entre todas las Comunidades Autónomas en cuanto a definir qué se entenderá por "persistencia del riesgo epidémico" de cara a la revacunación de los más pequeños, pues este extremo no queda claro en los trabajos publicados (para la primovacunación se define una "tasa primaria de ataque" fácil de calcular, pero no así para la revacunación).
BIBLIOGRAFÍA
1. González Enríquez J, García Comas L, Alcaide Jiménez JF, Sáenz Calvo A y Conde Olasaregui J. Eficacia de la vacuna meningocócica de polisacárido capsular del grupo C. Rev Esp Salud Pública 1997; 71(2): 103-126. [ Links ]
2. De Wals P, Dionne M, Douville-Fradet M, Boulianne N, Drapeau J and De Serres G. Impact of a mass immunization campaign against serogroup C meningococcus in the province of Quebec, Canada. Bull 1996; 74: 407-411. [ Links ]
3. Centers For Disease Control And Prevention. Control and prevention of meningococcal disease and Control and prevention of serogroup C meningococcal disease: evaluation and management of suspected outbreaks: recommendations of the Advisory Committee on Inmunization Practices (ACIP). MMWR 1997; 46 (No. RR-5): 1-21. [ Links ]
4. American Academy of Pediatrics. Meningococcal disease prevention and control strategies for practice-based physicians. Pediatrics 1996; 97: 404-411 . [ Links ]
5. Maslanka SE, Gheesling LL, Libutti DE, Donaldson K, Harakeh HS, Dykes JK et al. Standardization and Multilaboratory comparison of Neisseria Meningitidis serogroup A and C serum bactericidal assays. Clin Diag Labor Inmunol 1997; 4: 156-167. [ Links ]
6. Peltola H, Safari A, Kayhty H, Karanko V, y André FE. Valoración de dos vacunas meningocócicas tetravalentes (ACYW135) en lactantes y niños pequeños. Estudio clínico comparando el efecto inmunógeno de los polisacáridos 0-acetil negativo y 0-acetil positivo del grupo C. Pediatrics (ed.esp.) 1985; 20: 54-58 . [ Links ]
7. Mitchell LA, Ochnio JJ, Glover C, Lee AY, Ho M and Bell A. Analysis of meningococcal serogroup C-specific antibody levels in British Columbia children and adolescents. J Infect Dis 1996; 173: 1009-13 . [ Links ]














