Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Salud Pública
versión On-line ISSN 2173-9110versión impresa ISSN 1135-5727
Rev. Esp. Salud Publica vol.87 no.5 Madrid sep./oct. 2013
https://dx.doi.org/10.4321/S1135-57272013000500003
Inmunología de la poliomielitis: vacunas, problemas para la prevención/erradicación e intervenciones de futuro
Poliovirus Immunology: Vaccines, Problems for the Prevention/Eradication and Future Interventions
Eduardo Fernández-Cruz Pérez (1) y Carmen Rodríguez-Sainz (2)
(1) Servicio de Inmunología Clínica. Hospital General Universitario Gregorio Marañón. Madrid.
(2) Laboratorio Inmunovirología e Inmunogenética Molecular del Servicio de Inmunología Clínica. Hospital General Universitario Gregorio Marañón. Madrid.
Dirección para correspondencia
RESUMEN
La poliomielitis es una enfermedad infecto-contagiosa que afecta preferentemente a los niños menores de 5 años y está causada por el poliovirus, un enterovirus perteneciente a la familia Picornaviridae. El virus entra a través de la mucosa oral y se multiplica en las células del epitelio tanto de la orofaringe como del tracto gastrointestinal, liberando virus a nivel de las secreciones orofaríngeas y a través de la materia fecal. La vía de transmisión es fecal-oral y/o oral-oral. La mayoría de los casos de infección son asintomáticos y autolimitados al tracto gastrointestinal. Eventualmente puede diseminarse al sistema nervioso central y afectar a las motoneuronas del asta anterior de la médula espinal ocasionando parálisis e incluso la muerte.
El curso natural de la infección depende de múltiples factores, como el tipo de inóculo viral (serotipos VP1, 2 y 3) y factores del huésped/sistema inmunológico, que incluye el estado nutricional, las infecciones concurrentes y la capacidad de inducir respuestas inmunológicas protectoras sistémicas de tipo humoral, con anticuerpos anti-víricos circulantes neutralizantes, y respuestas de la inmunidad de mucosas y adaptativa.
Discutiremos los aspectos actuales de la inmunopatogénesis de la infección por el poliovirus, la interacción huésped-virus y la eficacia y los problemas en el desarrollo de las estrategias con las diferentes vacunas anti-poliovirus, para que la inmunización sea más efectiva en relación a la inducción de los mecanismos protectores que evitan el desarrollo de la enfermedad, la transmisión del virus, los rebrotes de infección y eventualmente facilitan la consecución de su erradicación.
Palabras clave: Poliovirus. Poliomielitis. Vacuna Antipolio de Virus Inactivados. Vacuna antipolio oral. Respuesta inmune de la mucosa. Inmunidad adaptativa. Prevención y control. Erradicación de la enfermedad.
ABSTRACT
Polio is a contagious disease that is caused by the poliovirus, an enterovirus in the family Picornaviridae. The virus enters through the oral mucosa and multiplies in epithelial cells of both the oropharynx as the gastrointestinal tract, releasing virus in oropharyngeal secretions and through the stool. The mode of transmission is fecal-oral and/or oral-oral. The virus preferentially infects children under 5 years. Most infections are asymptomatic and self-limiting gastrointestinal tract. Eventually it spreads to the central nervous system and affects the anterior horn motor neurons of the spinal cord causing paralysis and even death. We will describe host-virus interaction and the natural history of infection which depends on many factors, including the type of viral inoculum (serotypes VP1, 2 and 3) and host factors, such as nutritional status, concurrent infections and the ability to induce protective immune responses, such as, humoral anti-viral antibody responses with neutralizing antibodies, mucosal immunity and systemic adaptative immune responses. We will discuss the relevant aspects of the immuno-pathogenesis of the infection by poliovirus and the problems related to the host-virus interactions in the subjects vaccinated, with the latest advances in the strategies to develop optimal protection with the different poliovirus vaccines that could allow the development of a more effective immunization with induction of the effect or mechanisms that would prevent development of the disease, transmission of the virus, out-breaks and eventually the poliovirus eradication.
Key words: Poliovirus. Poliomyelitis. Poliovirus vaccine, inactivated. Poliovirus vaccine, oral. Mucosal immunity. Adaptative immunity. Prevention and control. Disease eradication.
Poliovirus: estructura, sitios antigénicos y serotipos
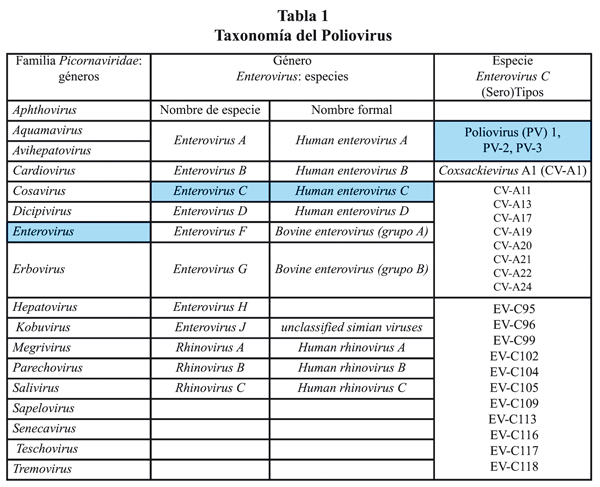
El Poliovirus es un enterovirus de la familia Picornaviridae1,2. Su nombre (pico: pequeño; RNA: ribonucleic acid) se introdujo en 1963 para denominar a esta familia que comprende a un grupo de virus de pequeño tamaño que contienen ácido ribonucléico (RNA) como material genético. La familia Picornaviridae incluye 37 especies agrupadas en 17 géneros3,4. El Poliovirus pertenece al género Enterovirus C (tabla 1).
La estructura del virión del poliovirus se muestra en la figura 1. Su genoma es una cadena simple de RNA (+) y está recubierto por una nucleocápside (Capside Virion Protein; VP) con cuatro subunidades (VP1, VP2, VP3 y VP4). Las proteínas de la cápside VP1, VP2 y VP3 están localizadas en la superficie del virión y constituyen los antígenos (Ag) importantes para la inducción de anticuerpos neutralizantes.
Existen tres sitios principales de neutralización antigénica (N-Ag) en las VP: N-Ag I, II y III. El sitio antigénico más frecuente es N-Ag I (el 90% de los anticuerpos neutralizantes tipo 2 y tipo 3 están dirigidos frente a N-Ag I (figura 1).
El poliovirus existe como 3 tipos antigénicos o serotipos PV-1, PV-2, y PV-3 (tabla 2). Para todos los serotipos virales la mayoría de los epítopos de los sitios N-Ag se encuentran en clusters en VP1. Ha habido poca evolución antigénica en los sitios N-Ag y los aislados virales no relacionados del tipo-salvaje del poliovirus [wild-type poliovirus (WTP)] varían en uno o más sitios N-Ag5 (figura 1). La proteolisis con proteasas de N-Ag I le hace perder las propiedades antigénicas y previene el desarrollo de los anticuerpos neutralizantes de mucosa.
El poliovirus entra en las células infectadas a través del receptor CD155 y comienza su ciclo biológico replicativo (figura 2). En el interior de la célula infectada el RNA del virus se traduce para dar lugar a una poliproteína cuyo procesamiento conduce a las diferentes proteínas codificadas por el virus. La replicación de su material genético permite la síntesis de más material proteíco o su encapsidación para liberar nueva progenie viral6.
Poliovirus: vías de entrada, receptores y diseminación de la infección
El poliovirus es un enterovirus que tiene tropismo por la mucosa orofaríngea y del tracto gastrointestinal. Entra por la cavidad oral y a nivel celular se une al receptor del poliovirus (PVR), la molécula CD155 en las superficies de las células epiteliales7. CD155 es un péptido glicosilado con tres ectodominios Ig-like (NH2-V-C2-C2). El RNA mensajero de CD155 se ha detectado en cerebro, médula espinal, íleon, leucocitos, pulmón, placenta, corazón, músculo esquelético e hígado. Sin embargo, la mayoría de las infecciones ocurren en el tracto gastrointestinal (GI) y sistema nervioso central (SNC) (figura 3). Con respecto a la diseminación del poliovirus tanto a nivel de las mucosas como sistémica, infecta las células del epitelio de la mucosa orofaríngea e intestinal8. Trabajos recientes sugieren que la respuesta de interferón tipo I (específicamente la de interferón alfa y beta) es un factor importante que define qué tipos de células son diana de la replicación del virus de la polio.
Se han propuesto tres hipótesis no excluyentes para explicar su entrada al sistema nervioso central (SNC). Todas las teorías requieren viremia primaria. La primera hipótesis predice que los viriones pasan directamente de la sangre al SNC a través de la barrera hematoencefálica9. Una segunda hipótesis sugiere que los viriones son transportados desde los tejidos periféricos a los que llega a través de la sangre, por ejemplo el tejido muscular, a la médula espinal, a través de las vías nerviosas por transporte axonal retrógrado10. Una tercera hipótesis es que el virus es transportado hasta el SNC a través de los monocitos o macrófagos infectados6.
Evolución clínica
En el 90-95% de los sujetos infectados la infección por poliovirus es asintomática. El 4-5% de los individuos pueden presentar infección abortiva similar a otras infecciones virales entéricas o meningitis viral aséptica. En aproximadamente el 5% de los casos el virus se propaga y se replica en otros sitios, tales como la grasa marrón, el tejido reticuloendotelial (SRE) y el músculo (figura 3). Aproximadamente, el 0,5% pueden presentar infección activa con enfermedad. La replicación viral sostenida causa viremia secundaria y conduce al desarrollo de síntomas leves, como fiebre, cefalea y odinofagia. La poliomielitis paralítica implicando al bulbo se presenta en menos del 1% de las infecciones y se produce cuando el virus entra en el SNC y se replica en las neuronas motoras de la médula espinal, tronco cerebral o corteza motora, lo que resulta en la destrucción selectiva de las neuronas motoras que conducen a la parálisis temporal o permanente. En casos raros la poliomielitis paralítica implica al aparato respiratorio , lo que conduce a un paro respiratorio y, eventualmente, a la muerte.
Los individuos inmunocomprometidos excretan poliovirus durante períodos de tiempo más prolongados, ocasionalmente tres años o más11.
Tras un período largo silente o asintomático, la infección por poliovirus puede asociarse a una enfermedad secundaria que recuerda la enfermedad neuronal motora.
Prevención de la poliomielitis: vacunas
La poliomielitis no tiene cura pero es prevenible. En 1955, el científico Jonas Salk desarrolló la Vacuna Inactivada de la Polio (inactivated polio vaccine: IPV)12. Años mas tarde, entre 1961y 1963 el Dr. Albert Sabin desarrolló las Vacunas Orales de la Polio monovalente y trivalente (oral polio vaccine: OPV)13-15.
Vacuna inactivada de la polio
La vacuna de poliovirus inactivados trivalente (IPV) diseñada por Jonas Salk fue la primera que consiguió una licencia en 1955. El constructo de la vacuna deriva de cepas seleccionadas de WTP inactivadas con formalina, cuya potencia inmunogénica fue aumentada en 197012,15. La figura 4 muestra a Jonas Salk en una Conferencia sobre VIH celebrada en San Francisco (6th International AIDS Conference, San Francisco, United States, 1990) donde presentó una vacuna frente al SIDA con un constructo de similar diseño, con un virión completo inactivado, derivado de cepas de un paciente con virus de la inmunodeficiencia humana (VIH-1). En la figura aparece también el ponente Dr. Eduardo Fernández-Cruz que colaboró activamente con el Dr. Salk y realizó una investigación en España durante el período 1998-2007 para el desarrolló clínico de la vacuna Salk con el inmunógeno VIH-1, obteniendo resultados sobre su potencial eficacia para inducir respuestas potentes de la inmunidad celular específica anti-VIH en pacientes con infección crónica por el VIH-116,17.
La IPV puede estar formulada como una combinación de vacunas con otros antígenos (DTP, Hib y Hepatitis B)15. Actualmente en aproximadamente 60 países industrializados usan solo IPV para la inmunización rutinaria en niños o una estrategia secuencial de la vacuna oral trivalente con virus atenuados (OPV) y subsiguientemente inmunización con IPV (OPV/IPV).
Ambas vacunas, IPV y OPV, inducen de forma efectiva inmunidad humoral, con producción de anticuerpos neutralizantes específicos frente a poliovirus en el suero. La estrategia de inmunización con 3 dosis de IPV en las semanas 6, 10 y 14 fue altamente efectiva (83%-100%) en estimular la respuesta de anticuerpos circulantes específicos frente a los 3 serotipos (1, 2 y 3) de poliovirus18. Sin embargo, la vacuna IPV es menos efectiva que la OPV en estimular las respuestas inmunológicas en las mucosas, tiene un coste mayor por dosis que la OPV y requiere ser inyectada con agujas estériles por personal sanitario entrenado.
OPV: Vacuna oral de la polio
Es la vacuna antipolio más ampliamente utilizada, de bajo coste y que de forma rápida bloquea la transmisión viral. Al ser su ruta de administración la vía oral, se asemeja a la infección natural.
Contiene cepas de poliovirus vivos atenuados de Sabin [tras pases repetidos de las cepas del vírus-tipo salvaje (WTV) en cultivos de tejidos]. Estas cepas tienen mutaciones atenuantes y sustituciones en varios sitios antigénicos N-Ag que las hacen menos neurovirulentas y están bajo una presión de selección negativa durante su replicación en el intestino. Así pues, la atenuación disminuye mucho su neurovirulencia y su capacidad de ser transmitido.
La OPV se presenta en forma de vacuna trivalente. Otras formulaciones son la monovalente (ya sea tipo 1, 2 o 3) y la bivalente (tipos 1 y 3). Las formas monovalentes y bivalentes son más inmunogénicas que la trivalente, descartando la interferencia de la tipo 2 de Sabin. Un estudio reciente demuestra que la OPV de los tipos 1 y 3 es superior a la OPV trivalente en la inducción de inmunidad sérica de tipo específica después de dos dosis de vacunas19.
La Organización Mundial de la Salud (OMS) recomienda que el programa de inmunización de rutina [Expanded Programme for Immunization (EPI)] incluya la administración de una dosis de OPV al nacimiento más tres dosis espaciadas al menos cuatro semanas.
El virus de la OPV se secreta en las secreciones nasofaríngeas y en las heces, por lo que indirectamente podrían vacunar a los contactos próximos de los receptores de la vacuna.
La evidencia empírica apoya la efectividad de la vacuna OPV. Ha quedado demostrada su eficacia en la interrupción de la circulación del poliovirus. Así mismo, la OPV es eficaz en la prevención de la enfermedad paralítica en un 90%15.
La forma trivalente de la OPV es altamente eficaz estimulando la respuesta inmune sistémica con anticuerpos circulantes específicos a todos los serotipos en los países industrializados. Sin embargo, en los países en vías de desarrollo la eficacia es sólo del 73% y del 70% de los individuos vacunados en cuanto a la generación de anticuerpos frente a los serotipos 1 y 3, respectivamente20, 21.
La OPV induce también inmunidad de mucosas (inmunidad intestinal) tras repetidas inmunizaciones, aunque su efecto es de corta duración. La inmunidad de mucosas se puede evaluar directamente midiendo la sIgA en las secreciones nasofaringeas y en el intestino. La detección de sIgA específica frente al poliovirus en intestino se ha correlacionado con una reducción de virus excretado22,23. La OPV induce anticuerpos neutralizantes en la nasofaringe en más de un 70% de receptores de la vacuna24.
Efectos adversos de la vacunación con OPV
Se ha descrito la aparición de cepas de poliovirus derivadas de la vacunación (VDPVs). Son cepas virales que ganan capacidad replicativa y/o neurovirulencia debido a cambios antigénicos o recombinaciones espontáneas de los serotipos virales25. Ello ha dado lugar a la poliomielitis paralítica asociada a la vacunación (VAPP). En los países con vacunación OPV se han descrito 2-4 casos/106 nacimientos y por año. El riesgo es mayor tras la primera dosis y disminuye con las vacunaciones ulteriores26.
Los VDPVs que se replican en el intestino pueden tener las características de neurovirulencia y transmisión de los WPV. Los VDPVs se han subdividido en 2 grupos:
1) VDPVs inmunodeficientes (iVDPVs), aislados en sujetos con inmunodeficiencias primarias (IDP) y 2) VDPVs circulantes (cVDPVs: circulating vaccine-derived poliovirus) aislados tras prolongada replicación del virus de la vacuna. Tales virus circulantes cVDPV tienen el potencial de causar rebrotes de polio. Durante el período 2000-2009 se reportaron globalmente 12 brotes epidémicos de cVDPV27.
Prevenir la emergencia de los cVDPVs requiere mantener altos niveles de vacunación en todos los países antes de que la polio sea erradicada globalmente. Por otra parte, los inmunodeficientes con IDP (con inmunodeficiencia variable común, CVID) pueden excretar de forma crónica el poliovirus, lo cual constituiría un reservorio. Aunque la prevalencia de iVDPVs es baja, la existencia de estos casos plantea también un potencial riesgo para la erradicación.
En términos generales, OPV es una vacuna segura aunque la caída de las defensas inmunológicas en las personas vacunadas (Immunity Gap) puede ser un factor de riesgo de rebrotes de infección importante. El riesgo de VAPP, cVDPV y de iVDPV ha llevado a muchos países a cambiar la relativamente barata y sencilla OPV por la de mayor coste administrada por vía parenteral, la vacuna SALK inactivada contra la polio (IPV).
Para hacer frente a cVDPVs, el Grupo de Expertos en Asesoramiento Estratégico (SAGE), principal órgano de orientación política en el mundo para la inmunización, en 2012 recomendó la retirada del componente de tipo 2 de la vacuna antipoliomielítica oral de la inmunización sistemática en todos los países, introduciendo la nueva vacuna oral bivalente (bOPV), reforzado además por la introducción de al menos una dosis de IPV. Entre los avances más significativos de esta estrategia, en febrero de 2012, la India celebró un año sin polio por poliovirus salvaje autóctono. El principal éxito de esta estrategia se debió al uso de la nueva bOPV28,29.
Potenciación de las respuestas inmunológicas sistémicas y de mucosas frente al poliovirus
Inmunidad Sistémica: inducción de anticuerpos neutralizantes circulantes
La vacunación secuencial (países industrializados) o la administración simultanea (países en desarrollo) usando IPV y OPV (una dosis de OPV al nacimiento, más ya OPV en las semanas 6, 10 y 14, ó la administración simultánea de OPV e IPV en las semanas 6, 10 y 14) demostró una potenciación en la inducción de la inmunidad sistémica incrementando la respuesta de anticuerpos neutralizantes circulantes, siendo la media de los niveles de anticuerpos sistémicos para los 3 serotipos virales más alta en el grupo que recibió las vacunas OPV-IPV simultáneamente30,31.
Se observó también que una dosis de potenciación (booster) de IPV tras 3 dosis de OPV era capaz de cerrar efectivamente el immunity gap.
Inmunidad de mucosas (sIgA):
Tanto en países industrializados como en desarrollo, la administración secuencial de IPV y OPV resultó eficaz para producir respuesta de inmunidad de mucosas (sIgA nasofaríngea) frente a los tipos 1, 2 y 3:
Tres-dosis de OPV mostraron la máxima eficacia de niveles de sIgA en las secreciones nasofaríngeas, frente a 3-dosis de IPV ó la combinación IPV-IPV-OPV que presentaron niveles significativamente más bajos de sIgA32. En estos estudios, la IPV se mostró menos efectiva que la OPV en estimular las respuestas inmunes de anticuerpos de mucosas (sIgA en la nasofaringe e intestino).
Una inmunización Booster con IPV en individuos previamente inoculados con OPV (OPV-primed) o expuestos a WPV es capaz de estimular fuertemente los niveles de anticuerpos circulantes y de mucosa (sIgA)33. En los individuos vacunados-IPV y tras el boost con OPV, se observó un incremento de la cantidad de sIgA específica de poliovirus secretada en el intestino34.
Efecto en el Shedding viral: tiempo de excreción del Poliovirus
Los anticuerpos de mucosa (sIgA) inducidos por las vacunas pueden neutralizar el poliovirus en el intestino resultando una reducción del tiempo de excreción del poliovirus tipo 1 y 3 en la faringe, en el intestino y las heces.
En los estudios realizados en Oman, Gambia y Thailandia cuando se hizo el challenge se observó una reducción del mucosal shedding (excreción del poliovirus tipo 1 y 3) tanto en el grupo OPV como (OPV/IPV: IPV más 2-dosis OPV) indicando que en ambos se había inducido inmunidad de mucosas35.
Estudios en los sujetos seronegativos como en los “no-immunes” el número de días que excretan virus por las heces es de una media de 20 frente a los vacunados con OPV como en los vacunados con OPV/IPV (IPV más 2-dosis OPV) que han mostrado que se ha inducido inmunidad de mucosas con una reducción del tiempo de excreción del virus (viral shedding) de 5-7 días y del título viral (>0,5 log)36.
Problemas a superar con las vacunas de la polio e intervenciones de futuro
Basándose en la información anterior, se deberían considerar nuevas estrategias de intervención para superar los fallos de vacunación que incluirían re-evaluar y modificar el uso de las vacunas existentes.
Son muchos los retos que el desarrollo de vacunas eficaces plantea de cara al futuro. Se sabe que las vacunas orales incluyendo la del poliovirus, rotavirus y cólera han demostrado una capacidad limitada para inducir inmunidad de mucosa e inmunidad sistémica, posiblemente debido a algún mecanismo común todavía por esclarecer.
Uno de los objetivos principales a alcanzar con la vacunación sería la activación y trigger de la inmunidad de mucosas y específica que está mediada a través de la inmunidad innata y de la inmunidad adaptativa (figura 5). La figura muestra la respuesta inmunológica ante la presencia de un antígeno bacteriano o vírico en el tejido linfoide asociado al intestino (GALT: gut-associated lymphoid tissue), tanto organizado como difuso (linfocitos intraepiteliales (LIE). Las Placas de Peyer son agregados organizados de tejido linfoide que se encuentran predominantemente en la mucosa del íleo terminal y contienen numerosos folículos linfoides. Los antígenos y microbios son transportados a través de las células M (células epiteliales diferenciadas para esta función) y seguidamente son captados por las células dendríticas (CD), lo cual constituye un paso crítico en la inducción de la inmunidad adaptativa. Los antígenos captados por las CD dentro de la placa de Peyer son transportados por estas células a los ganglios linfáticos mesentéricos (GLM), donde se producen las interacciones entre las CD y los linfocitos T y B a través de la secreción de citocinas, integrinas y quimiocinas, los cuales eventualmente migran a los ganglios linfáticos de drenaje con posterior retorno a las mucosas intestinal y sistémica (oral, bronquial y genital), donde ejercen su función protectora. Esta función se realiza a través de una inmunidad de mucosas defensiva con producción de IgA secretora (sIgA), el mayor contribuyente a la inmunidad adaptativa de la mucosa frente a microorganismos, o mediante tolerancia mucosa, con inmunosupresión selectiva de respuestas inflamatorias37-39. Las propias células epiteliales de la mucosa intestinal suponen una barrera frente a la translocación de antígenos y participan como sensores del contenido de la luz intestinal a través de receptores tipo Toll (TLR) expresados en su superficie.
Se han descrito alteraciones en ambos tipos de respuesta inmunológica, innata y adquirida, en el período neonatal y en la temprana infancia40-42. En cuanto a la inmunidad innata se han descrito alteraciones de la función del macrófago y una reducción significativa de factores celulares y factores solubles que participan como mecanismos de la inmunidad local de las mucosas, tales como, la lisozima, amilasa y la lactoferrina40-42. Además, el tracto gastrointestinal no contiene “microbióta” al nacimiento, con lo cual el lumen intestinal se desarrolla con los componentes que forman el microbioma en los primeros meses de la vida, de lo que dependerá que el sistema inmunitario de las mucosas responda de una manera u otra, es decir, mediante inmunidad productiva o con tolerancia mucosa. Se desconoce el papel de los TLRs, patrones moleculares de reconocimiento asociado a patógenos, en la inmunidad inducida por la vacunación frente a poliovirus40-42.
En lo que respecta a la inmunidad adaptativa, la respuesta celular T está sesgada u orientada hacia una respuesta tipo Th1 en lugar de Th2, Th17 o Treg, debido a la inmadurez de las células dendríticas (DC) y a su incapacidad para secretar citocinas tipo IL-12. Hay estudios que sugieren que la vacunación OPV en la infancia no es capaz de inducir una respuesta sistémica Th2 dominante15. Existe información limitada disponible sobre el desarrollo o función de las respuestas inmunes mediada por células T frente al poliovirus tras la inmunización o tras la infección. A este respecto se requiere más información para determinar si este es un posible mecanismo por el cual OPV puede no funcionar adecuadamente en niños con un desarrollo insuficiente de la respuesta Th2.
Modelos matemáticos de funcionamiento de las vacunas podrán ayudar al diseño de estrategias para la protección óptima con OPV. Así mismo, son necesarios más estudios para establecer la estrategia y el papel de IPV en el boosting de la respuesta inmune específica frente al poliovirus.
En conclusión, es necesario el desarrollo de preparaciones de vacunas de mucosas más efectivas mediante innovación en las rutas de administración, por ejemplo vacunas por vía sublingual, los sistemas de delivery, adyuvantes y de inmunomodulación, para estimular de forma efectiva la producción de anticuerpos circulantes y de mucosa y la re-dirección del tráfico de DCs y otras células inmunológicas efectoras a la superficie de las mucosas37-39,43.
Bibliografía
1. Adams MJ, King AMQ and Carstens EB. Ratification vote on taxonomic proposals to the International Committee on Taxonomy of Viruses. Arch Virol. 2013; 158: 2023-2030. [ Links ]
2. Knowles NJ, Hovi T, Hyypi T, King AMQ, Lindberg AM, Pallansch MA, et al. Picornaviridae. En: Virus Taxonomy: Classification and Nomenclature of Viruses: Ninth Report of the International Committee on Taxonomy of Viruses. Ed: King AMQ, Adams MJ, Carstens EB, Lefkowitz EJ. San Diego: Elsevier; 2012. p. 855-880. [ Links ]
3. The Picornaviridae. Londres: The Pirbright Institute; 2013. Disponible en: http://www.picornaviridae.com/ [ Links ]
4. International Committee on Taxonomy of Viruses (ICTV). Picornaviridae Study Group. Disponible en: http://talk.ictvonline.org/files/ictv_documents/m/msl/4440.aspx [ Links ]
5. Martín J, Minor PD. Picornaviridae Study Group. Characterization of CHAT and Cox type 1 live-attenuated poliovirus vaccine strains. J Virol. 2002; 76: 5339-49. [ Links ]
6. De Jesus NH. Epidemics to eradication: the modern history of poliomyelitis. Virol J. 2007; 4(1): 70. [ Links ]
7. Racaniello VR. One hundred years of poliovirus pathogenesis. Virol. 2006; 344: 9-16. [ Links ]
8. Mueller S, Wimmer E, Cello J. Poliovirus and poliomyelitis: A tale of guts, brains, and an accidental event. Virus Res. 2005; 111: 175-193. [ Links ]
9. Yang W, Terasaki T, Shiroki K, et al. Efficient delivery of circulating poliovirus to the central nervous system independently of poliovirus receptor. Virol. 1997; 229 (2): 421-8. [ Links ]
10. Ohka S. Yang WX, Terada E, Iwasaki K, Nomot A. Retrograde transport of intact poliovirus through the axon via the first transport system. Virol. 1998; 250 (1): 67-75. [ Links ]
11. Kimpen JL, Ogra PL. Poliovirus vaccines: a continuing challenge. Pediatr Clin N Am. 1990; 37: 627-49. http://www.pubmed.gov/2161507 [ Links ]
12. Salk JE. Studies in human subjects on active immunization against poliomyelitis. 1. A preliminary report. J Amer Med Assoc. 1953; 151: 1081-98. [ Links ]
13. Sabin AB. Characteristics and genetic potentialities of experimentally produced and naturally occurring variants of poliomyelitis virus. Ann NY Acad Sci. 1955; 61: 924-38. [ Links ]
14. Sabin AB. Characteristics and genetic potentialities of experimentally produced and naturally occurring variants of poliomyelitis virus. Ann NY Acad Sci. 1955; 61: 924-38. [ Links ]
15. World Health Organization. Polio vaccines and polio immunization in the pre-eradication era: WHO position paper. Wkly Epidemiol Rec. 2010 Jun 4; 85(23): 213-28. Disponible en: http://www.who.int/wer/2010/wer8523/en/index.html. [ Links ]
16. Fernandez-Cruz E, Moreno S, Navarro J, Clotet B, Bouza E, Carbone J, et al. Therapeutic immunization with an inactivated HIV-1 Immunogen plus antiretrovirals versus antiretroviral therapy alone in asymptomatic HIV-infected subjects. Vaccine. 2004; 22 (23-24): 2966-73. [ Links ]
17. Valor L, Navarro J, Carbone J, Rodríguez-Sáinz C, Gil J, López F, et al. Immunization with an HIV-1 immunogen induces CD4+ and CD8+ HIV-1-specific polyfunctional responses in patients with chronic HIV-1 infection receiving antiretroviral therapy. Vaccine. 2008; 26(22): 2738-2745. [ Links ]
18. Cuba IPV Study Collaborative Group. Randomized, placebo-controlled trial of inactivated poliovirus in Cuba. N Engl J Med. 2007; 356: 1536-44. [ Links ]
19. Sutter RW, John TJ, Jain H, Agarkhedkar S, Ramanan PV, Verma H, et al. Immunogenicity of bivalent types 1 and 3 oral poliovirus vaccine: a randomised, double-blind, controlled trial. Lancet. 2010; 376: 1682-8. [ Links ]
20. Faden H, Modlin JF, Thoms ML, McBean AM, Ferdon MB, Ogra PL. Comparative evaluation of immunization with live attenuated and enhanced-potency inactivated trivalent poliovirus vaccines in childhood: systemic and local immune responses. J Infect Dis. 1990; 162: 1291-7. [ Links ]
21. Dayan GH, Thorley M, Yamamura Y, Rodríguez N, McLaughlin S, Torres LM, et al. Serologic response to inactivated poliovirus vaccine; a randomized clinical trial comparing 2 vaccination schedules in Puerto Rico. J Infect Dis. 2007; 195: 12-20. [ Links ]
22. Plotkin SA, Vidor E. Poliovirus vaccine - inactivated. En: Plotkin SA, Orenstein WA, Offit PA, editors. Vaccines. Philadelphia: Elsevier; 2008. p. 605-30. [ Links ]
23. Sutter RW, Patriarca PA. Inactivated and live, attenuated poliovirus vaccines: mucosal immunity. In: Edouard Kurstak, editor. Measles and poliomyelitis -vaccines and immunization. New York: Springer; 1993. p. 279-94. [ Links ]
24. Zhaori G, Sun M, Ogra PL. Characteristics of the immune response to poliovirus virion peptides after immunization with live or inactivated polio vaccines. J Infect Dis. 1988; 158: 160-5. [ Links ]
25. Kew OM, Sutter RW, de Gourville EM, Dowdle WR, Pallansch MA. Vaccine-derived polioviruses and the endgame strategy for global polio eradication. Annu Rev Microbiol. 2005; 59: 587-635. [ Links ]
26. World Health Organization. Risk assessment: frequency and burden of VAPP, cVDPV and iVDPV. In: Report of the interim meeting of the Technical Consultative Group (TCG) on the Global Eradication of Poliomyelitis. Geneva: World Health Organization; 2002. [ Links ]
27. Global Polio Eradication Initiative. Circulating vaccine-derived poliovirus1 (cVDPV) 2000-2011. Available from: http://www.polioeradication.org/Dataandmonitoring/Poliothisweek/Circulatingvaccinederivedpoliovirus.aspx [ Links ]
28. Sutter RW, John TJ, Jain H, Agarkhedkar S, Ramanan PV, Verma H, et al. Immunogenicity of bivalent types 1 and 3 oral poliovirus vaccine: a randomised, double-blind, controlled trial. Lancet 2010; 376: 1682-8. [ Links ]
29. John TJ, Vashishtha VM. Eradicating poliomyelitis: India's journey from hyperendemic to polio-free status. Indian J Med Res. 2013 May; 137(5): 881-94. [ Links ]
30. WHO Collaborative Study Group on Oral and Inactivated Poliovirus Vaccines. Combined immunization of infants with oral and inactivated poliovirus vaccines: results of a randomized trial in The Gambia, Oman, and Thailand. Bull World Health Organ. 1996; 74: 253-68. [ Links ]
31. du Chatelet IP, Merchant AT, Fisher-Hoch S, Luby SP, Plotkin SA, Moatter T, et al. Serological response and poliovirus excretion following different combined oral and inactivated poliovirus vaccines immunization schedules. Vaccine. 2003; 21: 1710-8. [ Links ]
32. Faden H, Modlin JF, Thoms ML, McBean AM, Ferdon MB, Ogra PL. Comparative evaluation of immunization with live attenuated and enhanced-potency inactivated trivalent poliovirus vaccines in childhood: systemic and local immune responses. J Infect Dis. 1990; 162: 1291-7. [ Links ]
33. Herremans TM, Reimerink JH, Buisman AM, Kimman TG, Koopmans MP. Induction of mucosal immunity by inactivated poliovirus vaccine is dependent on previous mucosal contact with live virus. J Immunol. 1999; 162: 5011-8. [ Links ]
34. Hovi T. Inactivated poliovirus vaccine and the final stages of poliovirus eradication. Vaccine. 2001; 19: 2268-72. [ Links ]
35. Modlin JF, Halsey NA, Thoms ML, Meschievitz CK, Patriarca PA, Baltimore Area Polio Vaccine Study Group. Humoral and mucosal immunity in infants induced by three sequential IPV-OPV immunization schedules. J Infect Dis. 1997; 75: S228-34. [ Links ]
36. Cuba IPV Study Collaborative Group. Randomized, placebo-controlled trial of inactivated poliovirus in Cuba. N Engl J Med. 2007; 356: 1536-44. [ Links ]
37. Eduardo Fernández-Cruz, Diana Alecsandru, Carmen Rodríguez-Sainz y José Luis Subiza. Nuevas bases científicas para la utilización de vacunas de mucosas en la clínica. En: Progresos en terapias inmunomoduladoras con inmunoglobulinas y con vacunas de mucosas en patologías infecciosas. Editor: Prof. Eduardo Fernández Cruz; Madrid: SICAM; 2013. p. 41-58. [ Links ]
38. Cecil Czerkinsky. Mecanismos inmunológicos básicos para el desarrollo de vacunas de mucosas contra infecciones, enfermedades autoinmunes y alergias. En: Progresos en terapias inmunomoduladoras con inmunoglobulinas y con vacunas de mucosas en patologías infecciosas. Editor: Prof. Eduardo Fernández Cruz; Madrid: SICAM; 2013. p. 59-70. [ Links ]
39. Liam O´Mahony. Activación de células dendríticas por componentes bacterianos a través de receptores para patrones moleculares. Papel inmunorregulador a nivel de la mucosa intestinal. En: Progresos en terapias inmunomoduladoras con inmunoglobulinas y con vacunas de mucosas en patologías infecciosas. Editor: Eduardo Fernández Cruz editor. Madrid: SICAM; 2013. p. 71-88. [ Links ]
40. Holmgren J, Czerkinsky C. Mucosal immunity and vaccines. Nat Med. 2005; 11: S45-53. [ Links ]
41. Iwasaki A, Medzhitov R. Regulation of adaptive immunity by the innate immune system. Science. 2010; 327: 291-5. [ Links ]
42. Levy O. Innate immunity of the newborn: basic mechanisms and clinical correlates. Nat Rev Immunol. 2007; 7: 379. [ Links ]
43. Fernández-Cruz E, editor. Progresos en terapias inmunomoduladoras con inmunoglobulinas y con vacunas de mucosas en patologías infecciosas. 1ª ed. Barcelona: Letra Médica SCP; 2013. Disponible en: http://www.inmunologiamadrid.com/pdfs/75_progresos_en_terapias_inmunomoduladoras....pdf [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Eduardo Fernández-Cruz
Servicio de Inmunología Clínica
Hospital General Universitario Gregorio Marañón
Doctor Esquerdo, 46
28007 Madrid
eduardo.fernandezcruz@salud.madrid.org