Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Española de Salud Pública
versión On-line ISSN 2173-9110versión impresa ISSN 1135-5727
Rev. Esp. Salud Publica vol.89 no.5 Madrid sep./oct. 2015
https://dx.doi.org/10.4321/S1135-57272015000500002
El tráfico inverso de medicamentos. Experiencia en Galicia
The Reverse Traffic of Drugs Phenomenon. Experience in Galicia, Spain
Raquel Vázquez-Mourelle (1), Elia Rodriguez Costa (2), José Manuel Pose Reino (2) y Luis Cadórniga Valiño (3)
(1) Gerencia de Gestión Integrada. Servizo Galego de Saúde. Xunta de Galicia. Santiago de Compostela. España.
(2) Subdirección General de Inspección, Auditoría y Acreditación de Servicios Sanitarios. Consellería de Sanidade. Xunta de Galicia. Santiago de Compostela. España.
(3) Jefatura Territorial de Sanidade. Servicio de Inspección de Servicios Sanitarios. Pontevedra. España.
Dirección para correspondencia
RESUMEN
La circulación intracomunitaria de medicamentos entre países de la Unión Europea realizada por laboratorios farmacéuticos y almacenes mayoristas es una actividad permitida denominada comercio paralelo. Como España se encuentra entre los Estados con menor precio de estos productos, su actividad principal es el envío a otros países. Sin embargo, en la adquisición de fármacos con este objeto ha emergido un fenómeno denominado "tráfico inverso de medicamentos", que se desarrolla sin observar la normativa sanitaria en el canal legal de distribución en nuestro país. Consiste en que los almacenes mayoristas obtienen los medicamentos de las oficinas de farmacia, en lugar de obtenerlos de otros almacenes o de laboratorios farmacéuticos conforme a la legislación vigente, invirtiendo de esta forma el circuito legal de suministro, ya que las oficinas de farmacia no los dispensan al público.
Este trabajo profundiza en los riesgos que para la salud pública ocasionan estas prácticas, detalla los resultados de la inspección de servicios sanitarios en Galicia que, en relación al total de procedimientos sancionadores a establecimientos farmacéuticos del período 2011-2014, fueron saniconados por esta causa 15 oficinas de farmacia y 5 almacenes, correspondiendo las máximas multas a la red formada por un almacén farmacéutico (1.000.000€ y cierre por 3 años) y 4 oficinas de farmacia (2.400.000€). Así mismo, se especifica la metodología de actuación y se identifica el escenario de adquisición ilegal para realizar este comercio exterior con mayores beneficios económicos, y se destacan los puntos fuertes de éxito y nuevas acciones para mejorar su abordaje.
Palabras clave: Tráfico de medicamentos, Desvío de medicamentos sujetos a prescripción, medicamentos falsificados, suministro y distribución, comercio, oficinas de farmacia, regulación de gobierno, legislación farmacéutica, industria farmacéutica, legislación de medicamentos, sanción.
ABSTRACT
IInter-state movement of drugs between EU countries by pharmaceutical companies and distribution warehouses is a permitted activity called parallel trade. As Spain is among the states with lower price of these products, its main activity is shipping to other countries; however, a phenomenon has emerged in acquiring drugs for this purpose, called "reverse traffic" that develops without observing the health regulations in the legal distribution channel in our country; in which, the pharmaceutical distribution warehouses, rather than getting drugs from other pharmaceutical companies or pharmaceutical distribution warehouses under the current legislation, obtain them from community pharmacies, thus reversing the legal supply circuit, as this drugs do not end dispensed to the public.
This paper studies the risks to public health caused by these practices, detailing the results of health inspections in Galicia, where in relation to the total pharmaceutical establishments sanctioning procedures in the period 2011-2014, were sanctioned for this reason 15 community pharmacies and 5 distribution warehouses, the maximum fines belonging to a network consisting of a pharmaceutical distribution warehouse, with a 1,000,000 € fine and closure for 3 years, and 4 community pharmacies, with 2,400,000 € total fine; It also specifies the methodology of action, identifies the scene of illegal acquisition to make this trade with the greatest economic benefits, highlights the strengths of the success and further action to improve its approach.
Key words: Drug Trafficking; Prescription drug diversión; Counterfeit Drugs; Supply and Distribution; Commerce; Pharmacies; Government Regulation; Legislation Pharmacy; Drug Industry; legislation drug, punishment.
Introducción
El comercio exterior de medicamentos es una operación legal y permitida en España para los laboratorios farmacéuticos titulares de la autorización de comercialización, para los laboratorios fabricantes y/o importadores así como para las tres figuras legalmente reconocidas como entidades de distribución de medicamentos (almacenes mayoristas de distribución, almacenes por contrato y los almacenes de medicamentos bajo control o vigilancia aduanera) habida cuenta de la premisa de la libre circulación de mercancías dentro de la Unión Europea (UE)1 como la primera de las cuatro libertades fundamentales del mercado interior, aunque el mercado farmacéutico tenga la especial peculiaridad de que la fijación del precio del producto lo regulan, en muchos casos, las autoridades sanitarias, como ocurre en España.
A la circulación intracomunitaria de medicamentos se le denomina distribución o comercio paralelo2. Se le apoda paralela en la medida en que la venta tiene lugar en otro Estado dentro de la UE fuera de la red de comercio local que los laboratorios fabricantes o comercializadores han establecido inicialmente como destino, siempre que se haya autorizado su comercialización en el país de origen. Lo que hace que esta actividad sea un modelo de negocio es la diferencia de precios de los medicamentos en el espacio europeo (generalmente de los financiados en aquellos países donde el precio está intervenido por la Administración Pública) y las fluctuaciones en los valores de moneda para los Estados Miembros que no utilizan el euro, siendo materia objeto de revisión3 y de debate internacional4, ya que produce grandes ganancias al comerciante paralelo, aunque de ello se deriven problemas en la accesibilidad al medicamento en el país que lo exporta5.
Para el envío a otros Estados miembros desde España se deben cumplir unos requisitos básicos recogidos en el artículo 54 del Real Decreto 824/2010, de 25 de junio6, con la única limitación de notificación previa de cada envío que desde el año 2012 determinó la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) para los medicamentos identificados como críticos, con el fin de proteger la Salud Pública7. No se dispone de ninguna otra normativa específica, ni nacional ni europea, que regule estas remisiones de medicamentos con origen en España.
En España la actividad de comercio paralelo principal son los envíos intracomunitarios7,8, en la cual medicamentos que inicialmente son puestos en el mercado español son enviados a otros países de la UE. Sin embargo, como en la mayoría de las actividades comerciales con gran volumen de negocio, se ha constatado una actividad sumergida ilegal por parte de algunos almacenes mayoristas de distribución, sin conocimiento de la Administración competente y sin observar las garantías sanitarias, a la que se denomina "tráfico, comercio o distribución inversa", que básicamente consisten en que los mayoristas en lugar de obtener los medicamentos de otros almacenes o de laboratorios farmacéuticos, conforme establece la legislación vigente, los adquieren de las oficinas de farmacia, invirtiendo de esta forma el sentido del suministro, ya que estas no los dispensan al público sino que los revierten al canal comercial revendiéndolos a los distribuidores. El principal motivo de su auge es la diferencia de precios señalada entre países, ya que España se encuentra entre los de precios más bajos junto con Grecia, Portugal y Reino Unido. Entre los de mayor precio tenemos a Alemania, Dinamarca y Suecia9.
Para un mejor entendimiento de este fenómeno conviene añadir que los envíos a otros países por parte de los mayoristas se intentan llevar a cabo también al margen del laboratorio farmacéutico fabricante y comercializador, ya que la mayoría de los estudios existentes concluyen que reduce sus ganancias10. La industria farmacéutica ha intentado poner veto estableciendo a los mayoristas un precio más alto para estas operaciones (llamado "doble precio o precio dual", es decir, un precio libre para las exportaciones y otro precio inferior, el intervenido de financiación pública en España, para comercializar en el Sistema Nacional de Salud) pero ha sido recurrido por entender que se trata de un acuerdo anticompetitivo y que niega la premisa principal de la UE de existencia de un mercado único11. Es ahí donde cobran protagonismo las farmacias comunitarias, utilizadas ilegalmente para la adquisición de medicamentos y que tienen como destino final otro país, evitando así el control que la industria realiza sobre los mayoristas.
No fue hasta el 26 de julio de 2013, con la incorporación efectiva al ordenamiento jurídico español de la Directiva 2011/62/UE12 del Parlamento Europeo y del Consejo de 15 de diciembre de 8 de junio sobre prevención de la entrada de medicamentos falsificados en la cadena de suministros legal, cuando los fármacos que son comercializados a través de este tráfico inverso podrían, en algún caso, estar considerados como falsificados si su presentación se razona falsa en cuanto a su historial, incluidos los registros y documentos relativos a los canales de distribución empleados. No obstante, la inspección de servicios sanitarios de la Consejería de Sanidad de la Xunta de Galicia lleva desde el año 2010 abordando la lucha contra estas conductas ilícitas, donde se han desarrollado efectivas estrategias específicas para minimizarlas.
Existe un artículo científico publicado en España en relación a estas prácticas ilegales13, pero debido a su actualidad y a sus repercusiones sanitarias, asistenciales y mediáticas, se considera de interés abordar en mayor profundidad, destacar aspectos de especial trascendencia no recogidos en él y actualizar los resultados obtenidos en su abordaje.
El presente trabajo muestra cómo repercute en la población desde el punto de vista de la salud pública la adquisición ilegal de medicamentos en España por parte de algunos almacenes mayoristas de distribución para realizar envíos intracomunitarios con mayores beneficios económicos, y refleja las actuaciones, metodología y los resultados de la Inspección de Servicios Sanitarios para combatir estas prácticas en los últimos años.
El fenómeno del tráfico inverso de medicamentos en España
A lo largo del año 2014 la prensa especializada en información farmacéutica en España14,15 se hizo eco de las operaciones nacionales de la Guardia Civil contra un nuevo fenómeno de tráfico ilícito de fármacos bautizado como distribución o comercio "inverso" de medicamentos. Nos referimos a las operaciones Pharmacon, Caduceo16, operación Convector17 y Noisa18, esta última desarticulada en Galicia en noviembre de 2014, con núcleo central de la red en esta Comunidad Autónoma que tuvo una repercusión mediática en la prensa local19 y nacional20 y que también fue objeto de publicación médica especializada a nivel internacional21,22.
Una de las principales causas que se enjuician en el marco de estas actuaciones es un posible delito contra la salud pública, acompañado de otro tipo de delitos (blanqueo de capitales, estafa...), que implica a administradores de almacenes mayoristas de distribución de estos productos y a profesionales sanitarios, como son los farmacéuticos titulares de oficinas de farmacia que, como agentes más próximos al ciudadano, deben ser garantes de una correcta atención farmacéutica. Ambos establecimientos son los actores principales en la cadena de suministro de medicamentos en España23,24 para garantizar su correcta y necesaria disposición a la población que abastecen.
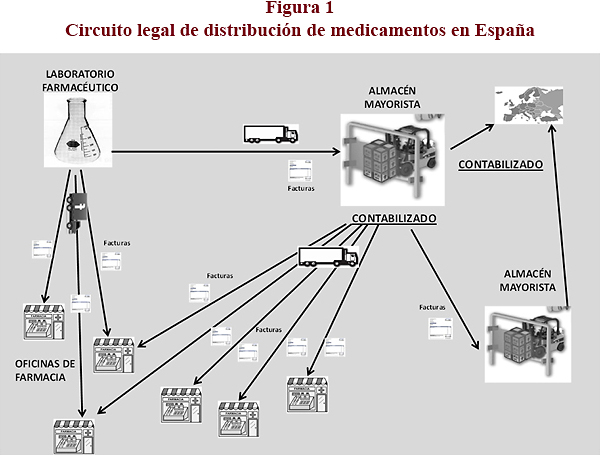
La razón esencial de que a este fenómeno se le denomine comercio, distribución o tráfico inverso de medicamentos radica en que invierte el circuito legal de distribución doméstico, es decir, la actividad que desarrollan los establecimientos farmacéuticos en estas redes es justo la contraria para la que han sido autorizados: los almacenes mayoristas, uno de los tres tipos de entidades de distribución reconocidas legalmente en las que se ha constatado las conductas ilícitas descritas, cuya función prioritaria y esencial es el abastecimiento a las oficinas de farmacia y a los servicios de farmacia legalmente autorizados en el territorio nacional, pasan a obtener los medicamentos a través de oficinas de farmacias en lugar de ponerlos a su disposición, y las oficinas de farmacia pasan a hacer, adicionalmente, actividades propias de la distribución suministrando a estos mayoristas los medicamentos que han adquirido previamente a otros almacenes o a laboratorios farmacéuticos, cuando el destino final de los mismos debe ser, en todo caso, la persona que los demanda en su territorio. El objetivo de esta práctica de adquisición ilegal emergente es el envío de estos medicamentos a otros países de la UE para obtener un mayor beneficio económico en sus ventas, al margen de los laboratorios farmacéuticos y fuera del control y supervisión de las autoridades sanitarias.
En la figura 1 se expone el circuito normal legal de cómo se debe realizar la distribución de medicamentos entre almacenes mayoristas y oficinas de farmacia como agentes principales de la cadena legal de suministro en España.
De las operaciones de comercio inverso ni el Ministerio de Sanidad, Servicios Sociales e Igualdad, ni la AEMPS ni las Consejerías de Sanidad de las Comunidades Autónomas disponen de información alguna en cuanto a su volumen. Se desarrollan incumpliendo los requisitos sanitarios legalmente establecidos, habida cuenta de la cualidad inherente de clandestinidad de una actuación ilegal, lo que hace que este asunto esté siendo objeto de debate monográfico en foros especializados25 y se encuentre en la actual agenda política farmacéutica.
Lo que realmente interesa a este artículo es acreditar la pérdida de garantías sanitarias y el riesgo que para la salud pública ocasiona este hecho ya que la distribución dentro de territorio español por los incumplidores se lleva a cabo sin observar la normativa específica nacional ni las autonómicas de ordenación y atención farmacéutica, lo que hace que se comprometa la seguridad asistencial al paciente en el acceso, consumo y administración del fármaco en circulación. Por eso se trata de una prioridad en los programas de la inspección de servicios sanitarios de las Consejerías de Sanidad, en concreto de la Inspección Farmacéutica como cuerpo especializado en garantizar la seguridad de la cadena de suministro de productos farmacéuticos al ciudadano.
Se hace imprescindible pues, detallar los riesgos que generan estas prácticas ilícitas:
a) Suministro discontinuo o irregular en el abastecimiento de medicamentos26.
Está demostrado que no asegurar un suministro adecuado y continuado del fármaco prescrito puede producir efectos adversos o errores en la medicación administrada, siendo los más frecuentes los errores de dosis o de elección equivocada de fármaco al tener que seleccionar una alternativa terapéutica, evidenciándose casos de éxitus27. Similares repercusiones tendría el caso de que la molécula afectada corresponda a las que no pueden ser sustituibles por el farmacéutico28,29 y ni que decir tiene si la sustancia farmacológica en falta no dispone de alternativa.
Además, son frecuentes en la práctica asistencial diaria la falta de adherencia al tratamiento o errores en la toma de medicamentos cuando los pacientes están sometidos a cambios en la marca30 por la falta en el suministro del fármaco prescrito, ya que implica cambios de color y presentación en el envase, acondicionamiento primario o formulación. La falta total de suministro en el caso de laguna terapéutica puede también suponer un coste añadido al sistema sanitario si se tiene que recurrir a la importación del medicamento como extranjero o si el paciente necesita ingreso hospitalario debido a su empeoramiento por retraso en su farmacoterapia.
Las principales causas descritas en la literatura científica achacan este problema de suministro al precio y al marco legal existente26, totalmente relacionado con estos comportamientos de comercio y distribución señaladas. Prueba de ello ha sido la red de tráfico ilegal de la Operación NOISA, cuyo detonante fue la denuncia interpuesta31 por el desabastecimiento de ciertos medicamentos32 por parte de la Asociación Infantil Oncológica de padres y madres con hijos enfermos de cáncer (ASION), nombre que deriva de las siglas de dicha Asociación leídas en sentido contrario. El principal medicamento afectado era la mercaptopurina, indicada para tratar la leucemia linfocítica aguda, recogido en la relación de la AEMPS como crítico por los problemas de suministro desde el 30 de abril del año 201433.
b) Pérdida de la trazabilidad del lote de fabricación del medicamento y de las transacciones realizadas con los mismos.
La trazabilidad en este caso concreto puede definirse como la capacidad de controlar, de forma preestablecida, el rastro de los envases de un determinado lote a lo largo de todo el proceso de fabricación hasta su disposición para uso y consumo, que nos permite conocer su histórico, ubicación y trayectoria a lo largo de toda la cadena de suministro en un momento dado a través del balance de entradas y salidas en cada agente donde debe registrarse la información mínima establecida para cada transacción. El artículo 90 del vigente Texto Refundido de la Ley de garantías y uso racional de medicamentos y productos sanitarios23 establece esta precisa obligación a los almacenes farmacéuticos y oficinas de farmacia con la justificación expresa de lograr un adecuado abastecimiento del mercado para establecer garantías de seguridad para los ciudadanos. En el embalaje exterior y en el acondicionamiento primario los fabricantes deben incorporar los elementos necesarios para determinar esta trazabilidad de lote34 y los mayoristas deben tener en todo momento esta información a disposición de la autoridad sanitaria24 (unidades suministradas, devueltas, lote al que pertenece y destinatario).
Esta obligación se justifica como una medida que coadyuva no sólo a evitar un eventual desabastecimiento sino a suministrar una precisa información sobre el último destino de los medicamentos comercializados, en consonancia con lo establecido por la directiva 2004/27/CE35. Conviene añadir que se considera importante y necesario para una correcta y más segura práctica asistencial36 así como para atender adecuadamente el deber de farmacovigilancia37,38.
Es de resaltar que estas garantías de trazabilidad de lote y transacciones facilitan considerablemente la retirada efectiva del mercado de productos defectuosos y permite luchar de forma más eficaz contra las falsificaciones en las fronteras de la UE39,40. Por tanto, es indiscutible que se trata de una herramienta imprescindible de gestión para reaccionar con rapidez ante cualquier problema detectado de calidad en la fabricación o de alteración de las propiedades farmacológicas a través de la red de alertas farmacéuticas de la AEMPS.
c) Falta de conservación adecuada durante el almacenamiento y transporte.
Estas conductas de tráfico ilícito ponen en riesgo la correcta conservación de los medicamentos, fundamental para que puedan mantener su actividad farmacológica de forma óptima. Las directrices europeas vigentes41 recogen estas premisas para garantizar la confianza de que el producto suministrado mantiene su calidad e integridad, siendo necesario llevar un control de la temperatura y asegurar la cadena de frío para los que sean termolábiles.
Una mala conservación puede convertir tanto al principio activo como a la forma farmacéutica en ineficaz, a la vez que añade el riesgo de manifestarse un efecto indeseado impredecible (reacciones de oxidación, reducción, desnaturalización de proteínas, modificación del efecto terapéutico, aparición de metabolitos tóxicos en la formulación...42), en definitiva compromete la estabilidad del fármaco.
d) Riesgo de desvío al mercado clandestino.
Habida cuenta de que se trata de un comercio encubierto donde se pierde la trazabilidad del lote de fabricación y el control por parte de la Administración Pública Sanitaria, existe mayor probabilidad de desvío de estos medicamentos para utilización sin fines terapéuticos o con fines ajenos a cualquier prescripción médica y uso racional. Riesgo de especial relevancia sería en aquellas sustancias adictivas o de posible utilización en dopaje deportivo43, que son frecuentemente utilizadas ilegalmente con un objetivo que no es ni el tratamiento ni curación ni alivio de enfermedades, y fuera de las condiciones autorizadas para las que el medicamento ha sido probado que es seguro.
La inspección de servicios sanitarios frente al tráfico inverso de medicamentos
La Inspección de Servicios Sanitarios es un Cuerpo especial facultativo superior44-45 de las Administraciones Públicas Sanitarias con condición de autoridad46 cuya función principal es el control de calidad en todos los niveles asistenciales para garantizar la seguridad. El ejercicio de autoridad sanitaria se considera un servicio básico de salud pública que ha sido acuñado como "policía médica"47. Todos los establecimientos, servicios o centros que desarrollen alguna actividad relacionada con la prestación farmacéutica están sometidos a su supervisión, inspección y control48 y encuentran el amparo normativo básico de su actuación en el artículo 108.3 del actual Texto Refundido de la Ley de garantías y uso racional de los medicamentos y productos sanitarios23.
La Comunidad Autónoma Gallega contaba en 2014 con 1.346 oficinas de farmacias y 24 almacenes farmacéuticos de distribución autorizados para atender a una población de 2.772.92849 habitantes, y con 10 Inspectores Farmacéuticos de la Consellería de Sanidade para la ejecución de las competencias encomendadas en la normativa sanitaria50 y en los programas y planes de inspección establecidos51.
La Inspección Farmacéutica se enfrenta al tráfico inverso de medicamentos con acciones directas sobre los agentes que actúan en la cadena legal de suministro instaurando una metodología en el año 2013 que no precisa de la colaboración del establecimiento inspeccionado, aunque sí de la colaboración de las empresas logísticas de transporte utilizados por ellas. Los primeros casos investigados en Galicia datan de 2010, y fueron consecuencia de la denuncia de un laboratorio farmacéutico que alertó de elevadas compras de una oficina de farmacia.
El material, método y procedimientos utilizados para combatir estas prácticas se detalla en la tabla 1, en la que se sigue el orden cronológico normal de las actuaciones inspectoras, que tiene como punto de partida la selección inicial de medicamentos testigo, es decir, la muestra sobre la que se centrarán las investigaciones para acreditar la trazabilidad de sus transacciones y probar la inversión del circuito de comercialización. Los medicamentos testigo seleccionados son aquellos para los que existen indicios, sospechas o pruebas de problemas de suministro o que se encuentran en la relación de medicamentos para los que es conocida su posible salida intracomunitaria a través del comercio paralelo.
Resultados de la inspección de servicios sanitarios
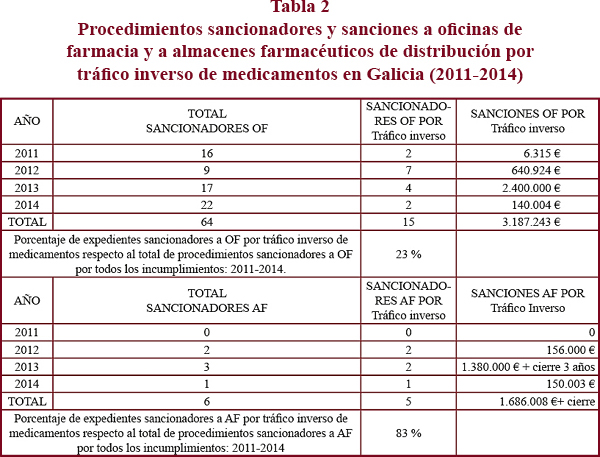
Los resultados de la inspección de servicios sanitarios con la metodología descrita reflejan que, en relación al total de procedimientos sancionadores incoados a establecimientos farmacéuticos por todos los incumplimientos durante el período 2011-2014, fueron sancionados por esta exclusiva causa de tráfico inverso el 23% las oficinas de farmacia y el 83% los almacenes farmacéuticos (tabla 2).
El año 2013 fue el de mayores sanciones económicas impuestas gracias al cambio normativo realizado en Galicia59 para combatir estas prácticas al incluir dos tipos específicos en el cuadro de infracciones muy graves para estas actuaciones ilegales en la Ley 5/1999, de 21 de mayo, de ordenación farmacéutica de Galicia56 (56.c)9.bis, para la oficina de farmacia y 56.c)9.ter para el almacén farmacéutico). Las máximas sanciones corresponden a la gran organización empresarial detectada en mayo del año 2012 formada por un almacén farmacéutico, núcleo central de las operaciones, con 1.000.000 € y cierre por 3 años de sanción (cuya motivación de la graduación máxima fue el agravante de coexistir un riesgo para la salud pública con intencionalidad), y 4 oficinas de farmacia afincadas una en cada provincia gallega, con 600.000 € de multa impuestos por oficina. Todas las actuaciones realizadas que fueron recurridas por esta gran red fueron confirmadas por los Tribunales Contencioso Administrativos de Galicia en el mes de julio del año 201553,57,58,60-66, habiendo sido determinante la intervención, como testigo-perito, de los inspectores farmacéuticos, instructores de los expedientes sancionadores, ya que además de testigos de los hechos objeto de las actuaciones realizadas poseen los conocimientos científicos, prácticos y técnicos sobre esta materia, colaborando de esta forma con la Administración de Justicia (figura reconocida en la actual Ley de Enjuiciamiento Civil, artículo 370.467).
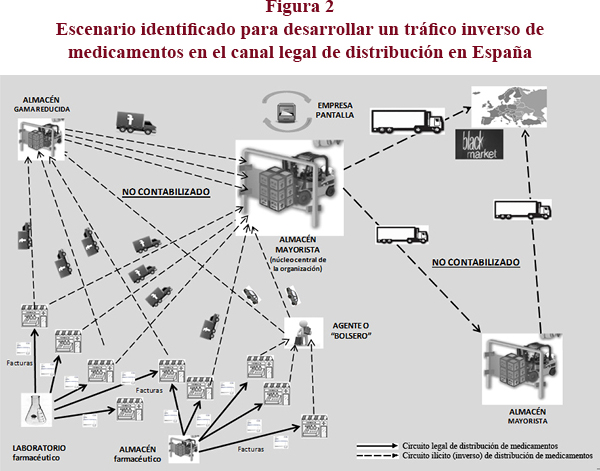
Resultado de agregar y analizar toda la información derivada de los procesos señalados se consiguió identificar el escenario de este entramado empresarial en el tráfico inverso en medicamentos (figura 1) donde la adquisición ilegal por parte del almacén mayorista núcleo central de la red se consigue por dos vías:
a) A través de la oficina de farmacia que realiza el pedido directamente al laboratorio farmacéutico que emite la factura, sin embargo la entrega se hace al almacén mayorista central de la red o a otro mayorista intermediario más pequeño con quien está en connivencia (efecto denominado "triangulación" con el fin de evitar la conexión directa con la farmacia suministradora). Los medicamentos nunca llegan a la oficina de farmacia que emitió el pedido y esta lleva una contabilidad paralela de estos suministros.
Las oficinas de farmacia suministradoras tienen dos perfiles claros diferenciados: unas cuentan con un farmacéutico testaferro como titular, sometido a administrador de la organización, y otras son farmacias comunitarias que se prestan a esta actividad a cambio del 5% de beneficio neto de estas ventas.
b) A través de agentes o "bolseros", personas físicas que recorren las oficinas de farmacia para adquirir, sin receta médica, normalmente formulaciones farmacéuticas innovadoras que presentan un importante diferencial de precio respecto a otros países. Estos agentes hacen acopio y entregan "su mercancía" al almacén núcleo central o a su intermediario.
La organización principal realiza la posterior gestión de estas adquisiciones ilegales a través de "empresas pantalla o fantasma" (que la organización utiliza como vehículo para realizar una administración, contabilidad y/o facturación paralela clandestina) con el fin de camuflar estas transacciones, simulando, incluso, devoluciones o compras en forma de productos sanitarios (no medicamentos). El destino final de los fármacos es otro país a través del comercio paralelo directamente o a través de otros almacenes mayoristas de distribución con los que está en connivencia.
Comentarios
El abordaje de un acontecimiento emergente de tráfico ilícito de medicamentos como es la distribución inversa ha llevado a actualizar el marco legal a la realidad existente, tanto en el cuadro de infracciones administrativas56,59, para recoger de forma expresa estas posibles prácticas y poder sancionar acorde a los riesgos que ocasionan, como en relación al desarrollo de la función inspectora, con el fin de reforzar y garantizar la seguridad jurídica necesaria para los inspectores sanitarios en el ámbito de su actuación48. Ha llevado también a innovar y priorizar las acciones que han conseguido sancionar de forma efectiva estos actos que comprometen seriamente la salud pública.
El mayor reto ha sido conseguir implantar una metodología de investigación que no necesitaba de la colaboración del establecimiento inspeccionado, habida cuenta del premeditado y sistemático impedimento a la labor inspectora y a la interposición de 3 querellas criminales contra los funcionarios públicos en el ejercicio de sus funciones. Otro de los principales problemas encontrados ha sido la opacidad contable de los agentes implicados, así como la gran dispersión geográfica de los movimientos comerciales, no solo dentro de la comunidad sino también fuera de ella.
Existen todavía aspectos importantes a resolver como son la ampliación del plazo legal de custodia de recetas médicas por las oficinas de farmacia, especialmente relevante para las del ámbito privado y una mejor identificación del medicamento fabricado para conseguir una trazabilidad más precisa.
Es necesario seguir desarrollando e innovando actuaciones inspectoras proactivas para combatir estas prácticas, priorizarlas en los planes y programas de inspección sanitaria y potenciar la colaboración entre administraciones públicas, sanitarias y no sanitarias, con una estrategia nacional conjunta que, sin lugar a dudas, exigen un gran esfuerzo, dedicación y compromiso de todos los profesionales implicados.
Desde el punto de vista de la persecución penal, a pesar del avance normativo del vigente Código con entrada en vigor el 1 de julio de 201568, la experiencia nos indica que para conseguir el encaje como delito contra la salud pública debe quedar constatado que a consecuencia de esta distribución inversa se ha producido, es decir, se ha materializado, un peligro para la vida o la salud de las personas que viene conectada directamente por esta actuación. Por ello parece que, actualmente, es la Inspección Farmacéutica de las Consejerías de Sanidad de las Comunidades Autónomas, en coordinación con otras Administraciones Públicas, el primer y principal ejecutor en la lucha contra esta actividad ilícita recurriendo a la vía penal a situaciones muy concretas en las que el peligro se haya consumado o el daño se hubiese producido.
Finalmente cabe realizar una reflexión del futuro del actual modelo de farmacia comunitaria en nuestro país, considerado ejemplar, de seguir prestándose a realizar estas prácticas determinados farmacéuticos titulares de oficina de farmacia con el único fin de conseguir un beneficio económico adicional.
Agradecimientos
A Pilar Álvaro Esteban, por sus aportaciones, interés e implicación. A Inocencia Pazos Díaz, Begoña Rocha Blanco, Cristina Torres Martín. A Eduardo Carracedo Martínez. En especial a Ana Vázquez Estepa por su apoyo y a Pilar Farjas Abadía, ex Consejera de Sanidad de la Xunta de Galicia que impulsó en esta Comunidad el cambio normativo del año 2012 para combatir estas conductas ilícitas.
Bibliografía
1. Diario Oficial de las Comunidades Europeas. Tratado de Funcionamiento de la Unión Europea. DOUE núm 83 de 30/03/2010. [ Links ]
2. Real Decreto 1785/2000, de 27 de octubre, sobre la circulación intracomunitaria de medicamentos de uso humano. BOE núm 259 de 28/10/2000. [ Links ]
3. Darba J, Rovira J. Parallel Imports of Pharmaceuticals in the Euroepan Union. Pharmacoeconomics. 2008. 14 (Suplly 1): 129-136. [ Links ]
4. EU: An introduction to pharmaceutical parallel trade In Europe. Life Sciencia Leadre. Abril, 2014. [ Links ]
5. Killick J, Schulz A. Parallel Trade in Europe-the Tide is Turning. 2006. Disponible en: http://jp.whitecase.com/files/Publication/f6ff768c-0cca-4182-991f-10e1f369bd1f/Presentation/PublicationAttachment/80d9592b-a347-4979-bf5e-19d6319c523a/article_Parallel_trade_in_Europe.pdf. [ Links ]
6. Boletin Oficial del Estado. Real Decreto 824/2010, de 25 de junio, por el que se regulan los laboratorios farmacéuticos, los fabricantes de principios activos de uso farmacéutico y el comercio exterior de medicamentos y medicamentos en investigación. BOE núm. 165 de 8/07/2010. [ Links ]
7. Agencia Española de Medicamentos y Productos Sanitarios. Circular n.o 2/2012, Notificación previa de envíos de medicamentos a otros Estados miembros. Disponible en: http://www.aemps.gob.es/informa/circulares/industria/2012/docs/circular_2-2012.pdf. [ Links ]
8. Agencia Estatal de Medicamentos y Productos Sanitarios. Memoria de actividades 2014, Disponible en: http://www.aemps.gob.es/laAEMPS/memoria/docs/memoria-2014.pdf. [ Links ]
9. Vogler S, Kilpatrick K, Zaheer-Ud-Din Babar. Analysis of Medicines Prices in New Zeland and 16 Euroepan Countries. Value in health. 2015. 18: 434-492. [ Links ]
10. Shen Guo, Bin Hu, Hai Zhong. Impact of parallel trade on pharmaceutical firm's profits: rise or fall?. Eur J Health Econ. 2013. 14: 345-355. [ Links ]
11. Maria Cedó. A vueltas con el doble precio en los medicamentos. Situación actual. Pharmatech. 2015. Núm 14. [ Links ]
12. Boletín Oficial del Estado. Ley 10/2013, de 24 de julio, por la que se incorporan al ordenamiento jurídico español las Directivas 2010/84/UE del Parlamento Europeo y del Consejo, de 15 de diciembre de 2010, sobre farmacovigilancia, y 2011/62/UE del Parlamento Europeo y del Consejo, de 8 de junio de 2011, sobre prevención de la entrada de medicamentos falsificados en la cadena de suministro legal, y se modifica la Ley 29/2006, de 26 de julio, de garantías y uso racional de los medicamentos y productos sanitarios. BOE núm 177 de 25/07/2013. [ Links ]
13. Vazquez Mourelle R, Cadórniga Valiño L, Torres Martín C, Rodríguez Costa E, Pose Reino JM, Álvaro Esteban P. Tráfico inverso: una actividad ilícita emergente en la cadena de suministro de medicamentos en España. Arsh Pharm. 2014. 55 (Supp 4): 01-07. [ Links ]
14. La "Operación Noisa" prolonga el mes horribilis de la distribución. Disponible en: http://www.elglobal.net/noticias-medicamento/2014-11-14/farmacia/la-operacion-noisa-prolonga-el-mes-horribilis-de-la-distribucion/pagina.aspx?idart=873258. [ Links ]
15. La nueva trama de comercio ilegal de fármacos podría estar relacionada con "Campeón". Disponible en: http://www.correofarmaceutico.com/comercio-ilegal-medicamentos/nueva-trama-podria-estar-relacionada-con-campeon. [ Links ]
16. Desarticulada una organización que distribuía medicamentos a países de Europa fuera de los canales legales de distribución. Disponible en: https://www.guardiacivil.es/ga/prensa/noticias/4968.html. [ Links ]
17. La Guardia Civil desmantela el mayor entramado de tráfico ilícito de medicamentos para su exportación. Disponible en: https://www.guardiacivil.es/es/prensa/noticias/5130.html. [ Links ]
18. Desmantelada una red dedicada al tráfico ilegal de medicamentos a través del "comercio inverso". Disponible en: http://www.guardiacivil.es/va/prensa/noticias/5205.html. [ Links ]
19. La jueza envía a la cárcel al líder de la trama farmacéutica y a dos hijos suyos. Disponible en: http://www.lavozdegalicia.es/noticia/galicia/2014/11/14/jueza-envia-carcel-lider-trama-farmaceutica-dos-hijos-suyos/0003_201411G14P10996.htm. [ Links ]
20. Cae la mayor trama de tráfico ilícito de medicamentos. Disponible en: http://politica.elpais.com/politica/2015/01/09/actualidad/1420803433_344389.html. [ Links ]
21. Spanish special forces dismantle parallel trade network that caused drug shortages BMJ 2015;350:h490 doi: 10.1136/bmj.h490 de 5/02/2015. [ Links ]
22. Study on Corruption in the Healthcare Sector. Publications Office of the European Union, October 2013. doi:10.2837/58154. [ Links ]
23. Real Decreto Legislativo 1/2015, de 24 de julio , por el que se aprueba el texto refundido de la Ley de garantías y uso racional de los medicamentos y productos sanitarios. Boletín Oficial del Estado núm. 177, de 25 de julio de 2015. [ Links ]
24. Real Decreto sobre distribución de medicamentos de uso humano. Real Decreto 782/2013, de 11. Boletín oficial del Estado núm 251 de 19/10/2013. [ Links ]
25. Vázquez Mourelle R. El Camino hacia un nuevo marco. X Jornadas de Inspección Farmacéutica. Disponible en: http://www.aemps.gob.es/laAEMPS/eventos/inspeccion-control/2013/docs/X-jornada-IF_Santiago-Compostela/programa_X-jornada-galicia.pdf. [ Links ]
26. De Weerdt E, Simoens S, Hombroeckx , Casteels M, Huys I. Causes of drug shortages in the legal pharmaceutical framework. Regul Toxicol Pharmacol. 2015 Mar; 71 (2):251-8. [ Links ]
27. McLaughlin M, Kotis D, Thomson K, Harrison M, Fenessy G, Postelnick M, et al. Effects on patient care caused by drug shortages: A survey. JMCP, 2013; 19: 783-788. [ Links ]
28. Boletín Oficial del Estado. Orden SCO/2874/2007, de 28 de septiembre por la que se establecen los medicamentos que constituyen excepción a la posible sustitución por el farmacéutico con arreglo al artículo 86.4 de la Ley 29/2006, de 26 de julio, de garantías y uso racional de los medicamentos y productos sanitarios. BOE núm 239 de 5/10/2007. [ Links ]
29. Boletín Oficial del Estado. Resolución de 4 de abril de 2014, de la Agencia Española de Medicamentos y Productos Sanitarios, por la que se actualiza el anexo I de la Orden SCO/2874/2007, de 28 de septiembre, por la que se establecen los medicamentos que constituyen excepción a la posibilidad de sustitución por el farmacéutico con arreglo al artículo 86.4 de la Ley 29/2006, de 26 de julio, de garantías y uso racional de medicamentos y productos sanitarios sanitarios. BOE núm. 113 de 9/05/2014. [ Links ]
30. Aaron S. Kesselheim, Alexander S. Misono, William H. Shrank, Jeremy A. Greene; Michael Doherty, Jerry Avorn, Niteesh K. Choudhry. Variations in Pill Appearance of Antiepileptic Drugs and the Risk of Nonadherence. JAMA INTERN MED. 2013. 173 (3):202-208. [ Links ]
31. Asociación de padres de niños con cáncer. Disponible en: http://www.asion.org/medios.html. [ Links ]
32. Suministro como medicamentos en situaciones especiales de varios citostáticos de Aspen Pharma Trading LTD. Disponible en: http://www.aemps.gob.es/informa/notasInformativas/medicamentosUsoHumano/problemasSuministro/2014/NI-MUH_13-2014-citostaticos-aspen.htm. [ Links ]
33. Listado de medicamentos con problemas de suministro a fecha 13/08/2015. Disponible en: http://www.aemps.gob.es/cima/fichasTecnicas.do?d-1338201-p=7&d-1338201-o=2&metodo=buscarDesabastecidos&metodo=buscarDesabastecidos&metodo=buscarDesabastecidos&metodo=buscarDesabastecidos&d-1338201-s=0. [ Links ]
34. Boletín Oficial del Estado. Real Decreto 1345/2007, de 11 de octubre, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso humano fabricados industrialmente. BOE núm 267 de 7/11/2007. [ Links ]
35. Diario Oficial de la Unión Europea. Directiva 2004/27/CE que modifica la Directiva 2001/83/CE por la que se establece un código comunitario sobre medicamentos de uso humano. DOUE L 136/34 de 30/04/2004. [ Links ]
36. Santulli P, Marcellin L, Touboul C, Ballester M, Darai E, Rouzier R. Experience with TachoSil in obstetric and ginecologic surgery. International Journal of Gynecology and obstetrics. 2011.Vol 113:112-115. [ Links ]
37. Casadevall N, EdwarsIR, Felix T, Graze PR, Litten JB, Strober BE, Wamock DG. Pharmacovigilance and biologics: considerations, needs and challenges. Expert Opin Bilo Ther. 2013 Jul. 13(7):1039-47. [ Links ]
38. Boletín Oficial del Estado. Real Decreto 577/2013, de 26 de julio, por el que se regula la farmacovigilancia de medicamentos de uso humano. BOE núm 179 de 27/07/2013. [ Links ]
39. Diario Oficial de la Unión Europea. Directiva 2011/62/UE que modifica la Directiva 2001/83/CE por lo que se establece un código comunitario sobre medicamentos de uso humano en lo relativo a la prevención de la entrada de medicamentos falsificados en la cadena de suministro legal. DOUE L 1 74/74 de 1/07/2011. [ Links ]
40. Estrategia frente a Medicamentos Falsificados 2012_2015. Disponible en: http://www.aemps.gob.es/publicaciones/publica/docs/Estrategia_falsificados_2012-2015.pdf. [ Links ]
41. Diario Oficial de la Unión Europea. Directrices de 5 de noviembre de 2013 sobre prácticas de correcta distribución de medicamentos para uso humano. DOUE de 23/11/2013. [ Links ]
42. Bovaira Garcia MJ, Lorente Fernández L, De la Rubia Nieto N, San Miguel Zamora MT. Conservación de medicamentos termolábiles. Año 2004. Disponible en: http://www.sefh.es/pdfs/ConservacionDeMedicamentos.pdf. [ Links ]
43. Vázquez Mourelle R, Carracedo Martínez E, Eugenio Ces Gens, Cadórniga Valiño L, Álbaro Esteban P, Pose Reino JM. Control de la dispensación de esteroides anabolizantes androgénicos. Gac Sanit. 2015;29(4):304-307. [ Links ]
44. Boletín Oficial del Estado. Ley 17/1989, de 23 octubre de Creación de escalas de personal sanitario de Galicia. BOE núm. 36 de 10 de febrero de 1990. [ Links ]
45. Diario Oficial de Galicia. Decreto núm. 5/1992, de 16 de enero, de Integración del personal sanitario transferido del Insalud en los cuerpos, escalas y clases del personal sanitario de la Comunidad. DOG núm. 16 de 24 enero 1992. [ Links ]
46. Boletín Ofical del Estado. Ley 8/2008, de 10 de julio, de Salud de Galicia. BOE núm 202 de 21/08/2008. [ Links ]
47. Villalbí JR, Meritxell Cusí, Caylà Joan A, Duràn J, Guix J. El ejercicio de autoridad sanitaria: los principios, lo reglamentado y la incertidumbre. Gac Sanit 21 (2); 2007: 172-75. [ Links ]
48. Diario Oficial de Galicia. Decreto 53/2014, de 16 de abril, de ordenación de la Inspección de Servicios Sanitarios de la Comunidad Autónoma de Galicia. DOG núm. 88 de 9/05/2014. [ Links ]
49. Instituto Galego de Estatística. Poboación segundo sexo e grupo quinquenais de idade. Ano 2011. Disponible en: http://www.ige.eu/igebdt/esqv.jsp?ruta=verPpalesResultados.jspOP=1 & B=1 & M= & COD=5261 & R=1[all] & C=2[all] & F=0:0;3:2011;9912:12 & S & TI=1. [ Links ]
50. Boletín Oficial del Estado. Ley 14/1986, de 25 de abril, General de Sanidad. BOE núm 102 de 29/04/1986. [ Links ]
51. Diario Oficial de Galicia. ORDEN de 12 de febrero de 2014 por la que se aprueba el Plan de inspección sobre centros, servicios, establecimientos y prestaciones sanitarias para el período 2014-2017. DOG núm 35 de 20/02/2014. [ Links ]
52. González Pérez J. y González Navarro F. Comentarios a la ley del régimen jurídico de las Administraciones Públicas y Procedimiento Administrativo Común (Ley 30/1992, de 26 de noviembre). Revista de Administración Pública. Año 2004. N.o 164: 1876. [ Links ]
53. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. Procedimiento Ordinario núm 4748/2013. Sentencia de 30/10/2014. [ Links ]
54. Boletín Oficial del Estado. Ley 30/1992, de 26 de noviembre, de Régimen Jurídico de las Administraciones Públicas y del Procedimiento Administrativo Común. BOE núm 285 de 27/11/1992. [ Links ]
55. Boletín Oficial del Estado. Real Decreto 1398/1993, de 4 de agosto, por el que se aprueba el Reglamento del Procedimiento para el Ejercicio de la Potestad Sancionadora. BOE núm 189 de 09/08/1993. [ Links ]
56. Boletín Oficial del Estado. Ley 5/1999, de 21 de mayo, de Ordenación Farmacéutica de Galicia. BOE núm 144 de 17/06/1999. [ Links ]
57. Juzgado Contencioso-Administrativo n.o 1 de Lugo. Procedimiento Ordinario 358/2012R. Sentencia de 19/11/2014. [ Links ]
58. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. Procedimiento Ordinario núm 4410/2013. Sentencia de 2/07/2015. [ Links ]
59. Diario Oficial de Galicia. Ley 12/2011, 26 diciembre, de medidas fiscales y administrativas. DOG núm 248 de 30/12/2011. [ Links ]
60. Tribunal Superior de Justicia de Galicia. Contencioso Administrativo Sección 2. Procedimiento Ordinario núm 4376/2013. Sentencia de 2/07/2015. [ Links ]
61. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. Procedimiento Ordinario núm 4696/2013. Sentencia de 2/07/2015. [ Links ]
62. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. Procedimiento Ordinario núm 4793/2012. Sentencia núm 466/2015 de 27/2015. [ Links ]
63. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. Procedimiento Ordinario núm 4078/2014. Sentencia núm 471/2015 de 9/07/2015. [ Links ]
64. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. PO 4175/2014 Sentencia de 23/07/2015. [ Links ]
65. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. Sentencia núm PO 4326/2014 de 30/07/2015. [ Links ]
66. Tribunal Superior de Justicia de Galicia. Sala Contencioso Administrativa Sección 2. PO 4153/2014 Sentencia de 30/07/2015. [ Links ]
67. Boletín Oficial del Estado. Ley 1/2000, de 7 de enero, de Enjuiciamiento Civil. BOE núm 7 de 8/01/2000. [ Links ]
68. Boletín Oficial del Estado. Ley Orgánica 1/2015, de 30 de marzo, por la que se modifica la Ley Orgánica 10/1995, de 23 de noviembre, del Código Penal. BOE núm 77 del 31/03/2015. Microbiol Clin. 2013; 31:643-8. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Raquel Vázquez Mourelle
Dirección-Gerencia
Complejo Hospitalario Clínico Universitario
de Santiago de Compostela
Travesía A Choupana s/n
15706 Santiago de Compostela
A Coruña
raquel.vazquez.mourelle@sergas.es