Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Anales del Sistema Sanitario de Navarra
versión impresa ISSN 1137-6627
Anales Sis San Navarra vol.39 no.1 Pamplona ene./abr. 2016
Hepatitis tóxica colestástica por clopidogrel en un paciente pluripatológico
Cholestasic toxic hepatitis due to clopidogrel in a patient with multiple conditions
D. Etxeberria-Lekuona1, I. Méndez-López1, M. R. Mercado2, J. Oteiza3, M. Arteaga1, V. Jarne1
1. Servicio de Medicina Interna, Hospital García Orcoyen. Estella. Navarra.
2. Servicio de Anatomía Patológica, Complejo Hospitalario de Navarra. Pamplona, Navarra.
3. Servicio de Medicina Interna, Complejo Hospitalario de Navarra. Pamplona, Navarra.
Dirección para correspondencia
RESUMEN
El clopidogrel es un fármaco antiagregante de la familia de la tienopiridinas muy utilizado en pacientes con cardiopatía isquémica, ictus y arteriopatía periférica. La toxicidad hepática por este fármaco es muy infrecuente. En la bibliografía únicamente se han descrito 16 casos, y solo en dos de ellos se practicó una biopsia hepática. Se presenta el caso de un paciente de 78 años pluripatológico que presentó una hepatitis tóxica colestásica severa por este fármaco y los hallazgos de la biopsia hepática que se le realizó. El cuadro se resolvió tras la retirada del fármaco.
En base a los hallazgos de nuestro caso y los de los casos previamente publicados se revisan las características de la hepatitis tóxica por clopidogrel y su manejo diagnóstico y terapéutico.
Palabras clave: Clopidogrel. Toxicidad. Hepatotoxicidad. Biopsia.
ABSTRACT
Clopidogrel is a thienopyridine-class antiplatelet drug commonly used in ischemic heart disease, cerebrovascular disease and peripheral artery disease. Liver toxicity due to this drug is very infrequent. We found 16 cases in the literature, and in only two of them liver biopsy was carried out. We report the case of a 78 year old patient with multiple conditions affected by severe toxic cholestatic hepatitis due to clopidogrel and the results of the liver biopsy performed. Hepatitis was resolved after discontinuing the drug.
Based on the characteristics of this case and other previously published cases, we review the characteristics of toxic hepatitis due to clopidogrel and its diagnosis and treatment.
Key words: Clopidogrel. Toxicity. Hepatotoxicity. Biopsy.
Introducción
El clopidogrel es un fármaco antiagregante muy utilizado en pacientes con cardiopatía isquémica, ictus y arteriopatía periférica. Sus efectos secundarios más frecuentes son: dispepsia, náuseas, diarrea, trastornos hemorrágicos, erupciones cutáneas, cefalea, mareo, trombopenia y neutropenia. La toxicidad hepática por clopidogrel es muy infrecuente, habiéndose descrito únicamente 16 casos en la bibliografía, y solo dos de ellos con biopsia hepática1,2. Se describe el caso de un paciente pluripatológico que presentó una hepatitis tóxica colestásica severa por este fármaco y los hallazgos de la biopsia hepática que se realizó3.
Caso clínico
Se trata de un paciente varón de 78 años que ingresó en el servicio de Medicina Interna en febrero del 2014 por un cuadro de anorexia, disnea, edemas en extremidades inferiores y deposiciones diarreicas de una semana de evolución. Entre sus antecedentes destacaban: diabetes mellitus tipo 2, hipertensión arterial, hipercolesterolemia, insuficiencia renal crónica estadio 4, cardiopatía isquémica, hipotiroidismo primario y arteriopatía periférica. No bebía alcohol y había dejado de fumar cinco años antes. En los estudios analíticos iniciales destacaba una acidosis metabólica con pH 7,27, pO2 117 mmHg, pCO2 18,6 mmHg y HCO3 12 mmol/L, un empeoramiento de su insuficiencia renal crónica con creatinina de 5,8 mg/dl y urea de 214 mg/dL, y un patrón de colestasis hepática, con bilirrubina total 2,1 mg/dL, bilirrubina directa 1,6 mg/dL, aspartato aminotransferasa (AST) 136 U/L, alanina aminotransferasa (ALT) 106 U/L, gamma-glutamiltransferasa (GGT) 736 U/L y fosfatasa alcalina (FA) 1.441 U/L. El hemograma no mostraba alteraciones significativas. En la anamnesis el paciente negó el consumo de setas o de productos de herboristería o medicina alternativa, y no recordó haber introducido tratamientos nuevos durante los últimos meses. Sin embargo, reconoció que había abandonado por su cuenta el tratamiento que llevaba de forma crónica con bicarbonato 500 mg oral. Los análisis microbiológicos de heces resultaron positivos para toxina y antígenos de Clostridium difficile.
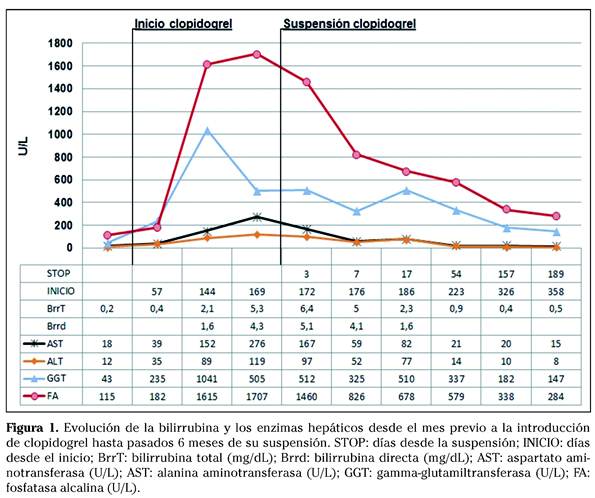
El cuadro clínico y la función renal mejoraron con la reintroducción de bicarbonato, hidratación parenteral y tratamiento antibiótico con metronidazol, pero los controles analíticos sucesivos evidenciaron un leve aumento de las enzimas hepáticas (Fig. 1). Se solicitó un estudio analítico con hormonas tiroideas, ceruloplasmina, ferritina, saturación de transferrina, α-fetoproteína, antígeno carcinoembrionario, antígeno tumoral 19-9, inmunoglobulinas, factor reumatoide, anticuerpos anti-nucleares, anti-músculo liso, anti-mitocondriales, anti-LKM (Liver Kidney Microsomal) y anti-citoplasma de neutrófilos citoplasmáticos, y serología infecciosa para hepatitis A, B y C, HIV, mononucleosis infecciosa y citomegalovirus, siendo todos los resultados negativos. Se volvió a revisar el tratamiento habitual del paciente. La medicación que el paciente tomaba de forma crónica era: atorvastatina 20 mg, furosemida 40 mg, ezetimiba 10 mg, levotiroxina 75 µg, nitroglicerina en parches de 5 mg, clopidogrel 75 mg, insulina, ranitidina 300 mg, amlodipino 10 mg y bicarbonato 500 mg. De estos fármacos, la atorvastatina es la que con más frecuencia aparece publicada como agente causante de hepatitis4. A pesar de ello, se consideró que la sospecha para este fármaco era muy baja porque el paciente llevaba 4 años tomándolo sin problemas. Con respecto al resto de medicaciones, el paciente estaba tomando todas ellas desde hacía más de un año, a excepción de clopidogrel, que había sido introducido por el servicio de Cirugía Vascular tras la realización de un bypass fémoro-peroneo 4 meses antes del primer ingreso en nuestro servicio. Debido a la baja frecuencia de hepatotoxicidad por este fármaco inicialmente se optó por mantenerlo y vigilar la evolución del paciente1,2.
El primer día de ingreso se había realizado una ecografía abdominal que no había mostrado obstrucción en la vía biliar. Ante la persistencia de las alteraciones analíticas se realizó una colangio-resonancia magnética (RM) hepática que mostró un hígado de tamaño normal, con intensidad de señal homogénea y sin lesiones focales. Las vías biliares no estaban dilatadas y no se objetivaban imágenes obstructivas. Tras la realización de esta prueba, el paciente llevaba varios días sin diarreas y se encontraba subjetivamente mucho mejor, por lo que se decidió darle el alta y continuar los estudios de forma ambulatoria. Sin embargo, a los pocos días de ser dado de alta comenzó de nuevo a perder el apetito y tuvo que reingresar 2 semanas después por clínica de anorexia, astenia, prurito generalizado y distensión abdominal. Sus constantes eran normales, aunque con tendencia a la hipertensión sistólica, y en la exploración física destacaba la presencia de ictericia conjuntival, un abdomen globuloso, no doloroso a la palpación y sin hepatomegalia, y edemas maleolares con fóvea. En los estudios analíticos se constataba un empeoramiento de la función hepática con bilirrubina total, 5,3 mg/dL, bilirrubina directa, 4,3 mg/ dL, AST 276 U/L, ALT 119 U/L, GGT 505 U/L y FA 1727 U/L. En una nueva ecografía abdominal se halló la presencia de ascitis que se distribuía por todos los espacios intraperitoneales. El hígado seguía presentando un tamaño y morfología normal, con ecoestructura conservada y con la vía biliar de calibre normal.
Teniendo en cuenta la evolución clínica se reconsideró la posibilidad de que la hepatitis fuera de causa farmacológica y se suspendió el clopidogrel. Se realizó una biopsia hepática en que la que se observó un patrón mixto de daño hepatocelular y colestasis. Los espacios porta aparecían aumentados de tamaño a expensas fundamentalmente de linfocitos, con tendencia a la formación de puentes. En los lobulillos se apreciaba una esteatosis mixta periportal, fundamentalmente microgotular, imágenes de satelitosis alrededor de los hepatocitos con balonización y marcada colestasis, tanto intracelular como extracelular. La biopsia era compatible con esteatohepatitis no alcohólica de etiología tóxico-medicamentosa (Fig.2). Se sustituyó el tratamiento con clopidogrel por triflusal. En los controles analíticos sucesivos se constató una progresiva mejoría de los marcadores de función hepática que se evidenció desde la primera semana tras la suspensión del fármaco (Fig. 1) y continuó durante las siguientes. Para valorar la relación de causalidad entre cropidogrel y la lesión hepática se aplicaron la escala diagnóstica de daño hepático inducido por fármacos de María y Victorino5, obteniéndose un resultado de "posible" reacción adversa al fármaco (11 puntos), y la escala de RUCAM (Roussel Uclaf Causality Assessment Method), obteniéndose un resultado de "altamente probable" (más de 8 puntos)5,6. En ambas escalas se valora la respuesta a una prueba de reintroducción del fármaco, que en nuestro caso se desestimó por razones éticas.
El paciente evolucionó de forma favorable los primeros meses después del último ingreso en nuestro servicio, pero 6 meses después del alta presentó un empeoramiento de la función renal y tuvo que ser incluido en el programa de diálisis. Dos meses después presentó un episodio de isquemia aguda del pie izquierdo que requirió intervención quirúrgica revascularizadora. Tras la intervención el paciente evolucionó desfavorablemente y falleció tres días más tarde. En el control evolutivo los niveles de bilirrubina y enzimas de citolisis habían vuelto a la normalidad, pero la FA y la GGT no lo habían hecho del todo (Fig. 1).
Discusión
El clopidogrel, al igual que la ticlopidina, es un fármaco tienopiridínico cuya actividad se basa en la inhibición de la agregación plaquetaria inducida por adenosina difosfato (ADP). Es un profármaco que es activado a nivel hepático por varios isoenzimas del citocromo P450, incluido el CYP3A4, transformándose en un metabolito tiol activo que pasa a unirse de forma específica e irreversible al quimiorreceptor P2Y12, presente en la superficie de las plaquetas, impidiendo su unión al ADP1,7. En la década de los 90 y a comienzos del presente siglo diferentes estudios demostraron su aplicabilidad para el tratamiento de la cardiopatía isquémica, los ictus isquémicos y la arteriopatía periférica, con una menor incidencia de efectos secundarios en comparación con la ticlopidina, especialmente en lo que se refiere a la toxicidad hematológica, que es el principal factor limitante para la utilización de este último fármaco7,8. Por otra parte, aunque también se han publicado bastantes casos de toxicidad hepática por ticlopidina, este tampoco es un efecto secundario habitual del clopidogrel9.
La edad de los pacientes en los casos de hepatitis tóxica por clopidogrel comunicados hasta ahora va de los 50 a los 89 años1,2. La forma más frecuente de presentación de esta hepatitis es un patrón mixto con daño hepatocelular y colestasis, pero también se han comunicado casos en los que predominaba el daño hepatocelular o la colestasis2,3,10. En dos casos el paciente presentó un síndrome de respuesta inflamatoria sistémica que incluía fiebre2,11. El grado de daño hepático varía desde una elevación moderada de enzimas hepáticas hasta una hepatitis aguda severa, y puede tardar en manifestarse entre 2 días y 6 meses después de la introducción del fármaco2. El tratamiento fundamental es la retirada del fármaco, y de forma característica la función hepática mejora al hacerlo, con un periodo de recuperación que oscila de 1 semana a 6 meses, aunque en alguno de los casos publicados el deterioro hepático en el momento de retirar el fármaco era tal que el paciente no mejoró y falleció al poco tiempo12. No están claros los mecanismos implicados en la hepatotoxicidad por clopidogrel. En los casos en los que se conoce la dosis administrada la dosis de mantenimiento siempre era de 75 mg/día, por lo que no parece deberse a un mecanismo de toxicidad dosis dependiente, sino más bien a un mecanismo idiosincrático. Este mecanismo a veces se engloba dentro de una reacción de hipersensibilidad, si bien son pocos los casos de hepatitis por clopidogrel en los que el paciente ha presentado manifestaciones sugestivas de hipersensibilidad (rapidez de instauración, fiebre, rash, eosinofilia)1,2,13.
El diagnóstico se basa fundamentalmente en la existencia de una cronología compatible entre el consumo del fármaco y la aparición de las alteraciones hepáticas, lo cual parece claro en el presente caso, además de la exclusión de causas alternativas3. El consumo simultáneo de otros fármacos potencialmente hepatotóxicos dificulta el diagnóstico. En nuestro caso el más sospechoso era la atorvastatina, pero aunque este fármaco puede producir toxicidad hepática similar a la observada en nuestro paciente, la frecuencia es menor del 1% con la dosis que llevaba, la alteración suele ser más leve, se suele producir en los primeros meses de tratamiento y el patrón analítico descrito en población española suele ser hepatocelular o mixto, no colestásico4,14. Por último, hay que destacar que la mejoría de la función hepática que se produjo tras suspender clopidogrel tuvo lugar a pesar de mantener el tratamiento con este fármaco. Con respecto al resto de fármacos que tomaba el paciente, estos se asocian a una muy baja incidencia de alteraciones hepáticas, frecuentemente leves, y el paciente los estaba tomando desde hacía más de un año.
La biopsia hepática no es esencial para el diagnóstico de hepatotoxicidad por fármacos, aunque ayuda a reforzarlo y excluir diagnósticos alternativos. En los dos únicos casos de la bibliografía en los que se realizaron biopsias hepáticas, coincide en describir un patrón mixto de daño hepatocelular y colestasis, similar al que encontramos en nuestro caso2,15. Al igual que en otros tipos de hepatitis por fármacos, el patrón observado en la biopsia hepática puede no corresponderse exactamente con el patrón bioquímico, que es el que se utiliza para clasificar daño hepático inducido por fármacos3.
En este artículo se presenta un caso infrecuente, pero no excepcional, de hepatitis secundaria al consumo de clopidogrel, que muestra cómo la revisión exhaustiva de la medicación que se ha consumido es fundamental en todo paciente que presente alteraciones de la función hepática. Consideramos que la toxicidad por clopidogrel debe incluirse en el diagnóstico diferencial de las hepatitis en aquellos pacientes que toman este fármaco. Y a pesar de que debido a la baja incidencia de las alteraciones hepáticas no está indicada la monitorización rutinaria de la función hepática en los pacientes en tratamiento con clopidogrel, creemos que sí deben realizarse estos estudios en caso de que aparezca cualquier dato clínico compatible con toxicidad hepática.
Bibliografía
1. Kapila A, Chhabra L, Locke Ad, Patel P, Khanna A, Reddy Cm, et al. An idiosyncratic reaction to clopidogrel. Perm J 2015 ; 19: 74-76. [ Links ]
2. Pisapia R, Abdeddaim A, Mariano A, Rianda A, Vincenzi L, Taibi C, et al. Acute hepatitis associated with clopidogrel: a case report and review of the literature Am J Ther 2015; 22: e8-e13. [ Links ]
3. Aithal GP, Watkins PB, Andrade RJ, Larrey D, Molokhia M, Takikawa H, et al. Case definition and phenotype standardization in drug-induced liver injury. Clin Pharmacol Ther 2011; 89: 806-815. [ Links ]
4. Arca M. Atorvastatin: a safety and tolerability profile. Drugs 2007; 67 Suppl 1: 63-69. [ Links ]
5. Maria Va, Victorino Rm. Development and validation of a clinical scale for thediagnosis of drug-induced hepatitis. Hepatology 1997: 26: 664-669. [ Links ]
6. Danan G, Benichou C. Causality assessment of adverse reactions to drugs-I. A novel method based on the conclusions of international consensus meetings: application to drug-induced liver injuries. J Clin Epidemiol 1993; 46: 1323-1330. [ Links ]
7. Wiper A, Schmitt M, Roberts Dh. Clopidogrel-induced hepatotoxicity. J Postgrad Med. 2008; 54: 152. [ Links ]
8. Savi P, Herbert JM. Clopidogrel and ticlopidine: P2Y12 adenosine diphosphate-receptor antagonists for the prevention of atherothrombosis. Semin Thromb Hemost 2005; 31: 174-183. [ Links ]
9. Pizarro AE, Andrade RJ, García-Cortés M, Lucena MI, Pérez-Moreno JM, Puertas M, et al. Hepatitis aguda por ticlopidina. Presentación de 12 casos y revisión de la literatura. Rev Neurol 2001; 33: 1014-1020. [ Links ]
10. Goyal RK, Srivastava D, Lessnau KD. Clopidogrel-induced hepatocellular injury and cholestatic jaundice in an elderly patient: case report and review of the literature. Pharmacotherapy 2009; 29: 608-612. [ Links ]
11. López-Vicente J, Garfia C, López-Medrano F, Yela C. Toxicidad hepática y síndrome de respuesta inflamatoria sistémica por clopidogrel. Rev Esp Cardiol 2007; 60: 323-324. [ Links ]
12. Kastalli S, El Aïdli S, Zaïem A, ben Abdallah H, Daghfous R. Fatal liver injury associated with clopidogrel. Fundam Clin Pharmacol 2010; 24: 433-435. [ Links ]
13. Ng JA, Goldberg N, Tafreshi MJ. Clopidogrel-induced hepatotoxicity and fever. Pharmacotherapy 2006; 26: 1023-1026. [ Links ]
14. Perdices EV, Medina-Cáliz I, Hernando S, Ortega A, Martín-Ocaña F, Navarro JM, et al. Hepatotoxicidad asociada con el uso de estatinas: análisis de los casos incluidos en el registro de hepatotoxicidad español. Rev Esp Enferm Dig 2014; 106: 246-254. [ Links ]
15. Hollmuller I, Stadlman S, Graziadei I, Vogel W. Clinicohistopathological characteristics of clopidogrel-induced hepatic injury: case report and review of literature. Eur J Gastroenterol Hepatol 2006; 18: 931-934. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Ivan Méndez-López
C/ Santa Soria s/n
31200 Estella. Navarra
E-mail: ivan.mendez.lopez@navarra.es
Recepción: 17-9-2015
Aceptación provisional: 5-10-2015
Aceptación definitiva: 3-11-2015