Introducción
Las duplicaciones intestinales son anomalías con una incidencia de 1:4.500-12.500 recién nacidos vivos, que se localizan a lo largo de todo el tubo digestivo, desde la boca hasta el ano. Para determinar su diagnóstico debe cumplir los siguientes criterios: presencia de una capa de músculo liso bien desarrollada, revestimiento epitelial representativo del tracto digestivo e íntima relación con alguna parte del tubo digestivo1. En menos del 20% de los casos esta lesión puede presentarse en comunicación con el intestino sano con el cual tiene relación2.
La ubicación más común de estas lesiones es a nivel ileal, seguido por el yeyuno y el esófago; solo entre un 5 y un 7% de las duplicaciones se presentan a nivel duodenal3. Generalmente se encuentran en la primera o segunda porción del duodeno, siendo excepcional su localización a nivel piloroduodenal, con menos de 10 casos publicados en la literatura4-12.
Se presenta el caso de una recién nacida con clínica de obstrucción del tracto digestivo superior secundario a un quiste de duplicación piloroduodenal, excepcional por la localización y la edad, a fin de describir el proceso diagnóstico y el manejo terapéutico realizado.
Caso clínico
Presentamos el caso de una niña, hija de madre de 31 años, sana. El embarazo fue bien controlado, con ecografías prenatales secuenciales en las que se visualizó, en el segundo trimestre, una imagen quística de 14 x 11 mm a nivel central del abdomen sobre vejiga, sin evidencia de continuación con ningún órgano. El parto fue por cesárea urgente en la semana 40+1.
Al nacimiento se le realizó una exploración física en la que destacó la presencia de una gran masa palpable en hemiabdomen derecho, por lo que la niña fue trasladada a nuestro centro.
En la ecografía abdominal realizada a su llegada se observó una lesión de 6x4x4 cm compatible con duplicación duodenal. La sospecha se basó en la presencia de una imagen ovoidea aneicoica, con ecos en su interior, compatible con detritus, que presentaba una periferia bien definida con doble pared: una zona interna ecogénica y una externa hiperecogénica. La lesión estaba ubicada en hipocondrio derecho, adyacente al duodeno, produciendo un moderado efecto masa sobre la vesícula biliar y el parénquima hepático (Fig. 1).
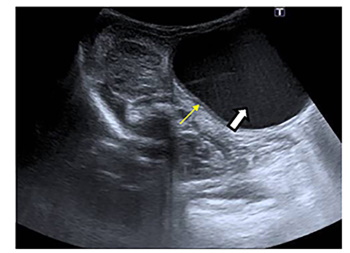
Figura 1. Ecografía abdominal. Imagen ovoidea aneicoica, con ecos en su interior, detritus (flecha blanca), periferia bien definida con doble pared (flecha amarilla) compuesta por una zona interna ecogénica y una externa hiperecogénica.
Ante estos hallazgos y dado el buen estado general de la paciente, sin presencia de náuseas, vómitos o distensión abdominal, se decidió iniciar tolerancia con lactancia materna y realizar un estudio diferido de la lesión, a fin de descartar dependencia de la vía biliar y filiar la porción duodenal relacionada con la duplicación.
A las 24 horas de vida la paciente comenzó con rechazo de la ingesta y episodios de vómitos no biliosos, por lo que se decidió restablecer la dieta absoluta y se colocó una sonda nasogástrica. Durante las 12 horas siguientes presentó empeoramiento del estado general, con aumento del débito por la sonda nasogástrica y de los episodios eméticos, que continuaron siendo no biliosos. Ante la presencia de este cuadro, compatible con obstrucción intestinal alta, se decidió intervención quirúrgica urgente.
Para valorar la lesión se realizó una tomografía axial computarizada (TAC) abdominal, previa a la cirugía, que confirmó la presencia de una imagen quística en hipocondrio derecho de aproximadamente 6,7 x 5 x 6 cm en íntimo contacto con hígado, vesícula biliar y riñón derecho, así como con asas intestinales y cámara gástrica medialmente, afianzando la sospecha de quiste piloroduodenal (Fig. 2).
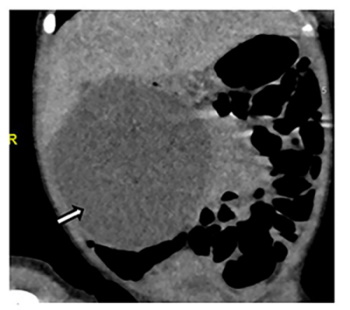
Figura 2. TAC abdominopélvica. Imagen quística (flecha blanca) en hipocondrio derecho de aproximadamente 6,7 x 5 x 6 cm.
Se realizó un abordaje mediante laparotomía transversa supraumbilical. Durante la cirugía se observó un quiste dependiente del borde antimesentérico de la primera porción duodenal y píloro, que producía una compresión a dicho nivel que explicaba la clínica obstructiva que presentaba la paciente (Fig. 3). Se llevó a cabo una resección de la pared libre del quiste, previa introducción de una sonda transpilórica, observándose que lesión e intestino sano compartían vascularización común y pared muscular, únicamente estaban separados por un tabique de mucosa.
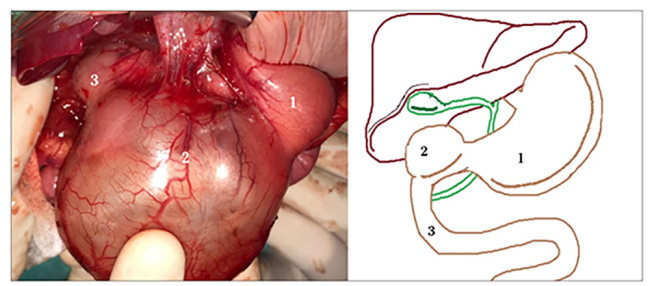
Figura 3. El gran tamaño de la lesión producía compresión de las estructuras adyacentes, ocasionando un cuadro de obstrucción. 1: estomágo; 2: quiste de duplicación dependiente del borde antimesentérico del duodeno sano; 3: duodeno sano.
Debido al compromiso pilórico, en un inicio se planteó realizar resección parcial y mucosectomía que no resultó viable debido a la hipovascularización de la pared muscular compartida entre el quiste y el intestino sano. Por lo tanto, se realizó una sección a ambos lados de la lesión quística, que abarcó píloro y primera porción duodenal. Posteriormente se realizó una anastomosis sobre la sonda transpilórica que tutorizaba la unión siguiendo el principio de Billroth I (anastomosis termino-terminal entre el estómago y el remanente duodenal). Se realizó la maniobra de Kocher para favorecer la movilización del quiste y así facilitar una anastomosis libre de tensión.
Previamente a la resección se localizó la desembocadura del conducto pancreático biliar, situado aproximadamente a 1,5 cm de la terminación del quiste, lo que permitió una resección segura sin afectar a la vía biliar.
La paciente fue dada de alta a la semana de la cirugía, presentando una ingesta y ganancia ponderal adecuadas. El examen histopatológico confirmó que se trataba de un quiste piloroduodenal con mucosa de tipo intestinal.
Discusión
Las duplicaciones duodenales son entidades raras, con una presentación clínica variable, dependiendo de su localización y su relación con estructuras vecinas. Principalmente se manifiestan como dolor abdominal, seguido de náuseas, vómitos y colestasis hepática;el 79% suelen presentar clínica antes de la primera década de la vida3. La pancreatitis es la complicación más común debido a obstrucción del conducto pancreático secundaria a la compresión debido al tamaño del quiste o a la obstrucción de la vía biliar por secreciones, lodo biliar o micropiedras3-5. En nuestra paciente neonatal debutó con distensión abdominal y vómitos no biliosos, signos típicos de obstrucción previa a la desembocadura de los conductos pancreático y biliar en duodeno.
La duplicación duodenal puede presentarse como un hallazgo prenatal13, siendo importante realizar el diagnóstico diferencial con quiste ovárico, quiste mesentérico, malformación linfática, quiste de colédoco o quiste renal/hepático/pancreático6,7. Por tanto, al nacimiento siempre será necesaria su confirmación mediante prueba de imagen. El diagnóstico de nuestra paciente fue prenatal, en el segundo trimestre, sin conseguir determinar la organodependencia de la lesión.
Actualmente no existe un método gold standard para filiar estas lesiones; entre las alternativas están la ecografía, la TAC o la resonancia magnética nuclear (RMN).
La ecografía debe ser siempre la prueba de imagen inicial, que mostrará una imagen de quiste complejo con ecos internos y doble pared13 mientras que, como en el caso presentado, la TAC y la RMN proporcionan información complementaria sobre las relaciones de la lesión9. Idealmente la prueba a realizar es la RNM, especialmente la colangio-RMN, a fin de descartar la existencia de comunicación con la vía biliar principal y diferenciar esta patología del quiste de colédoco. La TAC se reserva generalmente para los casos urgentes, en los que la RMN no está disponible, puesto que sus beneficios en esta patología son más limitados. En nuestro caso, inicialmente planificamos realizar un estudio diferido mediante RNM, pero ante el empeoramiento clínico de la paciente se optó por realizar una TAC urgente, la cual no logró determinar organodependencia. Probablemente debido a la corta edad de la paciente, las pruebas de imagen tipo TAC no logran determinar con precisión la dependencia orgánica de la lesión, ya que en estos pacientes hay menos grasa abdominal que separe las vísceras, dificultando la interpretación14. En determinados casos podría ser útil la colangiopancreatografía retrograda endoscópica, técnica relativamente novedosa que se ha descrito fundamentalmente en la literatura para el diagnóstico y el tratamiento de los quistes ubicados en la segunda porción duodenal de niños mayores y adultos15-17, probablemente porque la dificultad técnica se incrementa en pacientes neonatos. En cualquier caso, el diagnóstico final siempre será anatomopatológico.
El tratamiento se elegirá en función del tamaño del quiste, su ubicación y relación con las estructuras vecinas7. La técnica de elección es la resección completa de la lesión debido al riesgo de malignización de la mucosa de la duplicación a largo plazo, como se deduce de la revisión llevada a cabo por Ma y col18, quienes recopilaron 67 casos de tumores secundarios a la malignización de duplicaciones del tracto digestivo, tres de ellas localizadas a nivel duodenal.
Si la exéresis completa con anastomosis no es posible debido al compromiso de estructuras vecinas, se plantea la escisión de la pared libre del quiste mediante mucosectomía del resto de la pared en contacto con el intestino adyacente; se recomienda resecar la mayor cantidad de quiste posible a fin de eliminar la totalidad de la mucosa ectópica. Esta marsupialización tiene la ventaja de ser un procedimiento menos invasivo, con recuperaciones postoperatorias más rápidas; sin embargo, no exime de posibles complicaciones a largo plazo y, además, no siempre es factible debido al compromiso de la vascularización que se produce al resecar parte de las paredes libres del quiste6-8, como en este caso. Debido a la afectación pilórica, la resección parcial con mucosectomía inicialmente planteada se sustituyó por una resección completa debido al compromiso de la vascularización al resecar la pared libre de la lesión. Se han descrito mucosectomías endoscópicas en quistes localizados a nivel de la segunda porción duodenal; son procesos menos invasivos pero solo pueden realizarse en casos muy concretos, y no existen datos publicados en neonatos15-17. Parece prudente realizar una quistografía intraoperatoria cuando la posible comunicación del quiste con la vía biliar no está clara8, ya que en caso de compromiso de la vía biliar podría ser necesario realizar una pancreatoduodenectomía cefálica o procedimiento de Whipple19.
En pacientes asintomáticos no está estipulada la edad óptima para realizar esta cirugía. Mientras algunos autores recomiendan realizarla en los primeros seis meses de vida debido al elevado número de complicaciones presentadas durante el primer año13, el resto abogan por esperar a que el paciente alcance una mayor edad con el fin de facilitar la técnica quirúrgica y disminuir los riesgos anestésicos.
No es posible analizar el seguimiento a largo plazo de los pacientes con quiste piloroduodenal porque la mayoría de trabajos publicados presentan casos clínicos con un corto seguimiento, limitados al diagnóstico y al acto quirúrgico. Sin embargo, cuando se consigue una resección completa, o una escisión total de la mucosa secretora, el pronóstico a largo plazo parece ser excelente, ya que no hay complicaciones descritas en la literatura.
En conclusión, el quiste piloroduodenal es una entidad congénita cuyos síntomas y signos son un desafío, siendo imprescindibles las pruebas de imagen complementarias para establecer el diagnóstico y plan terapéutico a seguir. El objetivo quirúrgico será la exéresis de la lesión; aunque se han descrito otras alternativas con el fin de evitar complicaciones, muchas de ellas no son factibles en la etapa neonatal por las dificultades terapéuticas que conllevan.














