Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Avances en Periodoncia e Implantología Oral
versión On-line ISSN 2340-3209versión impresa ISSN 1699-6585
Avances en Periodoncia vol.24 no.1 Madrid abr. 2012
Antiinflamatorios no esteroides como terapia adjunta al raspado y alisado radicular en periodontitis
Non-steroidal anti-inflammatory as an adjunct to scaling and root planning in periodontitis
Ardila Medina C.M.*
* Profesor Asistente. Facultad de Odontología. Universidad de Antioquía. Miembro de la Junta Directiva de la Asociación Colombiana de Periodoncia y Oseointegración
Dirección para correspondencia
RESUMEN
La destrucción periodontal resulta de la interacción entre la placa bacteriana y la respuesta inflamatoria inducida por mediadores que incluyen enzimas del huésped, citoquinas, y metabolitos del ácido araquidónico (AA) tales como las prostaglandinas (PGs). Las PGs participan en la regulación de diversas funciones celulares bajo condiciones fisiológicas y patológicas. La ciclooxigenasa (COX) proporciona la conversión de AA a PGs en tres formas funcionalmente distintas: COX-1, COX-2 y COX-3. COX-2, se induce después de estimular una variedad de citoquinas inflamatorias, factores de crecimiento y lipopolisacáridos. Expresiones elevadas de COX-2 en periodontitis incrementan los niveles de PGs E2, considerados como los mayores mediadores de la destrucción tisular periodontal. Los antiinflamatorios no esteroides (AINES) inhiben la elaboración de productos COX y pueden atenuar el avance de la pérdida ósea, convirtiéndose en una alternativa terapéutica para el manejo de la periodontitis.
Palabras clave: Agentes antiinflamatorios, no esteroideos, ciclooxigenasa, periodontitis.
SUMMARY
Periodontal tissue destruction occurs as a result of the interaction between dental plaque bacteria and the immunoinflamatory response induced by mediators like host enzymes, cytokines, and arachidonic acid metabolites such as prostaglandins (PGs). PGs play a role in the regulation of diverse cellular functions under physiological and pathological conditions. The ciclooxigenase (COX) enzyme providing the conversion of AA to PGs exists in two functionally distinct COX isoforms: COX-1 and COX-2. COX-2. The COX-2, is induced after stimulation by a variety of inflammatory cytokines, growth factors, and lipopolysaccarides. Higher expressions of COX-2 in periodontitis results in increases of the levels of prostaglandin E2 which are major mediators of periodontal tissue destruction. Non-steroidal anti-inflammatory drugs inhibit the production of COX products and can attenuate the progression of periodontal bone loss, become a therapeutic alternative for the management of periodontitis.
Key words: Anti-inflammatory agents, non-steroidal, ciclooxigenase, periodontitis.
Introducción
Estudios inmunológicos y moleculares relacionados con la patogénesis de la enfermedad periodontal han demostrado que, aun cuando la biopelícula es el factor etiológico primario, la enfermedad se presenta debido al resultado de las interacciones entre patógenos bacterianos específicos y la respuesta inflamatoria e inmunológica del huésped (1, 2). Diferentes estudios realizados en animales y humanos (3, 4) indican que los metabolitos del ácido araquidónico (AA), principalmente las prostaglandinas (PGs), son mediadores fundamentales de la reabsorción ósea alveolar. La ciclooxigenasa (COX) proporciona la conversión de AA a PGs en tres formas funcionalmente distintas: COX-1, COX-2 y COX-3. Parece que COX-2 es la enzima primordialmente responsable de la producción de PGs E2 (PGE2) durante las infecciones periodontales (5).
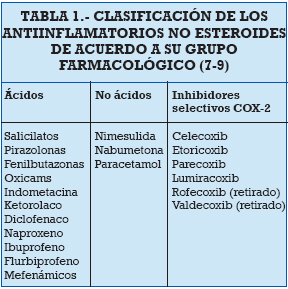
El tratamiento periodontal incluye la desorganización mecánica de los microorganismos de la biopelícula asociados con la superficie del diente que presenta bolsa periodontal (6). Teniendo presente la naturaleza inmunoinflamatoria inherente a la periodontitis, la modulación de factores humorales y celulares específicos puede ampliar potencialmente el efecto de la terapia mecánica, resultado que puede lograrse con medicamentos inhibitorios de la biosíntesis de PGs (7). Los antiinflamatorios no esteroideos (AINES) inhiben la elaboración de productos COX y pueden atenuar el avance de la pérdida ósea, convirtiéndose en una alternativa terapéutica adjunta para el manejo de la periodontitis. Empleando diferentes formas de administración, los AINES evaluados en diversas investigaciones incluyen según su grupo farmacológico ácidos, no ácidos e inhibidores selectivos de COX-2 (7-9) (Tabla 1). El objetivo de este artículo es presentar las opciones terapéuticas que ofrecen los AINES como alternativa de tratamiento adjunta al raspado y alisado radicular, teniendo presente su potencial en la modulación de la respuesta inmunoinflamatoria del huésped en pacientes con periodontitis.
Inhibidores de la ciclooxigenasa
Investigaciones en patofisiología inflamatoria han reconocido que existen al menos tres formas de COX responsables de la formación de productos del AA (10). COX-1, se encuentra en casi todas las células y es importante en funciones fisiológicas normales como el mantenimiento de la integridad de la mucosa gástrica y la homeostasis vascular y renal. COX-2, se expresa durante la reacción inflamatoria e interviene en la diferenciación celular, mitogénesis y señales de transducción especializadas (11). COX-3, se ha descrito recientemente como una variante de COX-1, siendo más abundante en la corteza cerebral y corazón (10).
Se ha sugerido que las actividades terapéuticas de los AINES derivan del bloqueo de COX-2, mientras que los efectos colaterales como ulceración gastrointestinal y hemorragia, daño renal y disfunción plaquetaria se deben a la inhibición de COX-1 (12). De esta forma, un bloqueo selectivo de COX-2 conduce a la inhibición del dolor y la inflamación sin ocasionar los efectos adversos producidos por COX-1 en los tejidos gástricos y renales (13). Sin embargo, es importante enfatizar que los inhibidores COX-2 deben emplearse con precaución, especialmente en pacientes con riesgo de enfermedad cardíaca isquémica e infarto (14).
Estudios en animales
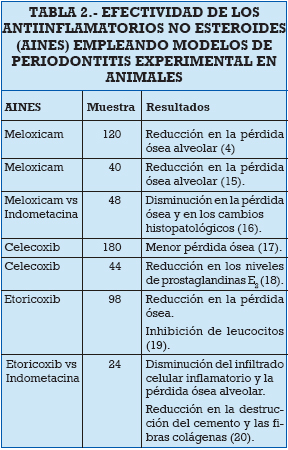
Los estudios realizados en animales para evaluar inhibidores no selectivos y selectivos de la ciclooxigenasa han empleado modelos de periodontitis experimental en ratas Wistar (4, 15-20) (Tabla 2). Oliveira y cols (4), investigaron el efecto del meloxicam sobre la pérdida ósea en periodontitis inducida experimentalmente. Un total de 120 ratas fueron distribuidas aleatoriamente en un grupo control, y un grupo experimental al que se le administró meloxicam 3 mg/kg/día, intraperitonealmente, por 3, 7, 14 o 30 días. En el grupo tratado con meloxicam se observó una reducción en la pérdida ósea alveolar en todos los períodos de tiempo estudiados. Estos resultados fueron corroborados por Nassar y cols (15), suministrando meloxicam en 40 ratas distribuidas en ocho grupos experimentales. Se colocaron ligaduras de algodón en el margen gingival de los primeros molares inferiores derechos de algunas ratas. Cuatro grupos fueron tratados por 5 o 15 días con una dosis oral y los grupos restantes fueron usados como controles. Después de cinco días, los grupos dosificados con meloxicam presentaron significativamente menor pérdida ósea (p<0,05) cuando se compararon con los grupos control, sin embargo, después de 15 días de tratamiento no se observaron diferencias significativas en la pérdida ósea. Además, no se presentaron manifestaciones sistémicas visibles. Empleando también un modelo experimental, Bezerra y cols (16), compararon dos AINES (meloxicam e indometacina) con el fin de investigar su capacidad para prevenir la pérdida ósea. Estos investigadores evaluaron la pérdida ósea alveolar en 48 ratas midiendo directamente la distancia entre la unión cemento esmalte y el hueso alveolar, a diferencia de los estudios de Oliveira y cols (4), y Nassar y cols (15), quienes emplearon radiografías para medirla. Los grupos experimentales fueron tratados subcutáneamente durante siete días mediante indometacina (0,5, 1 o 2 mg/kg) o meloxicam (0,75, 1,5 o 3 mg/kg), mientras que el grupo control no recibió ningún tipo de tratamiento. En el grupo no tratado, se observó una pérdida ósea significativa e incremento en el número de osteoclastos. En los grupos experimentales se disminuyó tanto la pérdida ósea como los cambios histopatológicos. En las ratas tratadas con indometacina se observaron hemorragias y úlceras estomacales, y las dosificadas con meloxicam presentaron petequias en el grupo tratado con 3 mg/kg.
El celecoxib, inhibidor selectivo COX-2, también se ha evaluado en diferentes estudios (17, 18). Holzhausen y cols (17), investigaron el efecto del celecoxib en el progreso de la pérdida ósea en un modelo de periodontitis en ratas. Ciento ochenta ratas fueron distribuidas aleatoriamente en tres grupos experimentales: celecoxib 10 mg/kg/día (Ce1), celecoxib 20 mg/kg/día (Ce2), o 10 ml/kg de solución salina. Se tomaron radiografías digitalizadas estandarizadas después del sacrificio (3, 5, 10, 18 y 30 días) para medir la cantidad de pérdida ósea alrededor de la superficie mesial del primer molar de cada rata. Los grupos tratados con celecoxib presentaron significativamente menor pérdida ósea al compararse con los controles (p<0,0001). Además, se observó una interacción significativa entre el tratamiento con celecoxib y el tiempo (p<0,03). Las diferencias en el promedio de la pérdida ósea entre el control y Ce1 fueron significativas solamente a los 18 días y, entre el control y Ce2 a los cinco y 18 días. Al final del periodo experimental no hubo diferencias significativas entre los grupos experimentales. Vardar y cols (18), también evaluaron los efectos de celecoxib sobre el nivel de prostaglandinas E2 en los tejidos gingivales, induciendo periodontitis experimental mediante inyecciones repetidas de endotoxina Escherichia coli. Un total de 44 ratas adultas fueron divididas en cinco grupos. Al final de la segunda semana, las ratas fueron sacrificadas, los tejidos gingivales fueron disecados y extraídos para analizarse. Como conclusión, los autores recomendaron celecoxib en el tratamiento de la periodontitis, debido a que su administración reveló reducción significativa en los niveles de prostaglandinas E2 gingivales.
Holzhausen y cols (19), estudiaron otro inhibidor selectivo COX-2: etoricoxib. Estos investigadores evaluaron 98 ratas asignadas aleatoriamente en tres grupos experimentales. Se les colocaron ligaduras de algodón en el margen gingival de los primeros molares inferiores derechos y se asignaron a uno de los siguientes grupos: un grupo control que recibió una dosis oral de 1 ml/kg de solución salina; un segundo grupo que recibió 6 mg/kg de etoricoxib (Etol1); un tercer grupo que recibió 12 mg/kg de etoricoxib (Etol2). Después del sacrificio se tomaron radiografías digitales estandarizadas para medir la cantidad de pérdida ósea. Los grupos tratados con etoricoxib presentaron menor pérdida ósea cuando se compararon con los controles (p<0,05), inhibiendo además, los leucocitos observados después del tercer día, a partir de la inducción de periodontitis. Azoubel y cols (20), investigaron el efecto de etoricoxib e indometacina en periodontitis experimental y compararon sus efectos gastrointestinales. Seis ratas por grupo fueron tratadas con dosis orales de 3 o 9 mg/kg de etoricoxib, 5 mg/kg de indometacina o 0,2 ml de solución salina. Los tratamientos iniciaron cinco días después de la inducción de la periodontitis, cuando se detectó la reabsorción ósea, y continuaron hasta el sacrificio (día 11). La pérdida ósea alveolar se midió a partir de la suma de las distancias entre los vértices de las cúspides y el hueso alveolar. Se examinó macroscópicamente la mucosa gástrica, e histopatológicamente el periodonto y la mucosa gástrica/intestinal. La pérdida ósea se inhibió significativamente (p<0,05) mediante 3 y 9 mg/kg de etoricoxib e indometacina: control = 4,08 ± 0,47 mm; etoricoxib (3 mg/kg) = 1,89 ± 0,26 mm; etoricoxib (9 mg/kg) = 1,02 ± 0,14 mm; indometacina = 0,64 ± 0,15 mm. La evaluación histopatológica del periodonto demostró que el etoricoxib y la indometacina disminuyeron el infiltrado celular inflamatorio, la pérdida ósea alveolar, la destrucción del cemento y las fibras colágenas. El análisis macroscópico e histológico de la mucosa gástrica e intestinal demostró que etoricoxib promovió menor daño que la indometacina.
Estudios en humanos
Diferentes estudios se han llevado a cabo con el fin de evaluar el efecto de la administración adjunta de AINES sobre los parámetros periodontales, bioquímicos, clínicos y radiográficos (3, 7, 8, 21-23). Tipton y cols (21), estudiaron fibroblastos gingivales humanos con el fin de determinar el efecto de inhibidores COX sobre la PGE2. Para ello, se cultivaron fibroblastos gingivales de sujetos saludables o con periodontitis avanzadas en medios libres de suero por 24 horas, empleando indometacina, celecoxib o rofecoxib. Todos los inhibidores COX ocasionaron disminución de PGE2 estimulada por la interleuquina 1β y sólo los inhibidores selectivos COX-2 produjeron parcial disminución de la interleuquina-6 en pacientes con periodontitis agresivas. Los resultados de este estudio fueron corroborados recientemente, empleando el mismo modelo experimental (22).
Algunos ensayos clínicos han investigado la efectividad de los AINES como terapia adjunta al raspado y alisado radicular (RAR) en pacientes con periodontitis crónica y agresiva (3, 7, 8, 23, 24) (Tabla 3). Flemmig y cols (23), investigaron si la terapia periodontal convencional y ácido acetilsalicílico (AAS) administrado sistémicamente, presentaban sinergismo cuando se combinaban para el tratamiento de la periodontitis. En el ensayo se incluyeron 30 pacientes con diagnóstico de periodontitis crónica, entre moderada y avanzada, asignados aleatoriamente a cada uno de los grupos de estudio. El diseño de la investigación abarcó cuatro terapias: RAR mas AAS de 500 mg 4 veces/día, RAR mas placebo 4 veces/día, AAS de 500 mg 4 veces/día sin RAR, y placebo 4 veces/día sin RAR. Se observó sinergismo de ASA y RAR, resultando en una eficacia terapéutica equivalente a la suma individual, en cuanto a la reducción de la inflamación gingival y la profundidad de la bolsa, durante las seis semanas de observación (interacción: p>0,05). Aras y cols (7) determinaron el posible efecto del naproxeno sobre el estado clínico y el perfil enzimático del fluido crevicular, como terapia adjunta al RAR en pacientes con periodontitis crónica. Un total de 34 sujetos fueron divididos en dos grupos con el fin de recibir naproxeno o placebo. Al inicio y al final del estudio se obtuvieron muestras de fluido gingival y evaluación de índices clínicos. El grupo experimental fue tratado con un protocolo que consistió en RAR y administración de naproxeno (275 mg/día durante siete días). En el grupo placebo, los pacientes fueron tratados igualmente pero se dosificó placebo a cambio de naproxeno. Todos los parámetros clínicos, exceptuando el promedio de sangrado fueron significativamente inferiores en el grupo experimental (p<0,05). Además, en el grupo que recibió AINES se presentó disminución significativa de la concentración de la actividad de la enzima elastasa en el fluido crevicular. Los autores concluyeron que su utilización como terapia adjunta al tratamiento periodontal podría traer beneficios. Vardar y cols (24), evaluaron el efecto de nimesulida y naproxeno como terapia adjunta al RAR, en pacientes con periodontitis crónica, sobre los niveles de prostaglandina E2 y F2α en los tejidos gingivales. Treinta pacientes fueron divididos en tres grupos de 10 cada uno. El primer grupo recibió 100 mg de nimesulida, el segundo 275 mg de naproxeno y el tercero placebo, todos en un régimen de 2 dosis/día por 10 días. Todos los grupos mostraron reducción estadísticamente significativa en el índice de placa bacteriana (25) y en el sangrado al sondaje (al tercer día y a los tres meses), y presentaron disminución en la profundidad de sondaje y ganancia en el nivel de inserción clínica (a los tres meses). En el grupo naproxeno, se observó una disminución significativa de los niveles de PGE2, reducción que fue insignificante en el grupo nimesulida; el grupo placebo presentó un incremento significativo de PGE2 en el décimo día. Los grupos nimesulida y naproxeno mostraron disminución significativa de la prostaglandina F2α, mientras el placebo mostró un incremento significativo. Yen y cols (3), evaluaron la eficacia de celecoxib en conjunto con RAR en sujetos con periodontitis crónica. Un total de 131 sujetos fueron asignados aleatoriamente para recibir RAR y celecoxib (200 mg) o placebo diariamente durante seis meses. Los índices clínicos fueron evaluados cada tres meses durante un año. En el grupo celecoxib, fueron superiores los promedios de reducción en la profundidad de sondaje y ganancia de inserción clínica, principalmente en sitios con profundidad moderada y avanzada. Este grupo también presentó un mayor porcentaje de sitios con ganancia de inserción > 2 mm y pocos sitios con pérdida > 2 mm. Los dos grupos mostraron mejoría en el control de placa (25) y en el sangrado al sondaje. Los resultados de esta investigación demostraron que el celecoxib puede ser efectivo como tratamiento adjunto al RAR, al reducir la pérdida de inserción progresiva en pacientes con periodontitis crónica.
Muy pocos estudios clínicos controlados se han realizado para evaluar el efecto de los AINES adjunto a la terapia no quirúrgica en pacientes con periodontitis agresiva (8, 26, 27). Reddy y cols (26), realizaron un ensayo clínico controlado doble ciego con el fin de determinar la eficacia del meclofenamato en pacientes con periodontitis agresiva. Se incluyeron en el estudio 22 sujetos con sitios activos de enfermedad periodontal determinados por evaluación ósea mediante radiografías estandarizadas, realizadas al inicio del tratamiento y a los seis meses, y mediante índices clínicos registrados en la línea de base, y a los tres y seis meses. Después de realizado el RAR, los sujetos fueron asignados aleatoriamente a placebo, y 50 o 100 mg de meclofenamato dos veces al día. Se empleó un software especializado para aislar la lesión de la imagen de sustracción y medir el cambio óseo a lo largo de la raíz. El grupo placebo presentó una pérdida ósea promedio de 0,42 ± 0,06 mm, y los grupos dosificados con meclofenamato en dosis bajas y altas presentaron un promedio de ganancia ósea de 0,07 ± 0,05 y 0,20 ± 0,07 mm, respectivamente. Jeffcoat y cols (27), estudiaron el efecto del naproxeno en la reducción de la actividad de la enfermedad periodontal en 15 pacientes con periodontitis agresiva. En este estudio doble ciego todos los pacientes fueron tratados con RAR. De este modo, siete pacientes recibieron 500 mg de naproxeno 2 veces diarias por tres meses y ocho sujetos recibieron placebo. La actividad de la enfermedad fue evaluada de tres formas. En primer lugar, se determinó la altura ósea alveolar mediante radiografías estandarizadas. En segundo lugar, se evaluaron las alteraciones en el metabolismo óseo alveolar administrando difosfonato metileno, previo a la dosificación y tres meses después. Por último, se evaluó la pérdida o ganancia ósea empleando radiografías de sustracción digital. Se presentó una menor pérdida ósea en los pacientes tratados con naproxeno (p<0,001), determinada por el análisis de la altura ósea durante los tres meses de estudio. Radiográficamente, en el grupo tratado con naproxeno, se observó un incremento significativo en la proporción de dientes que presentaron ganancia ósea. Finalmente, Azoubel y cols (8), en un estudio piloto realizado recientemente, evaluaron el efecto del tratamiento con etoricoxib de corta duración, como terapia ajunta al RAR, sobre parámetros clínicos y radiográficos, y niveles de PGE2 en periodontitis agresiva. Los sujetos fueron asignados aleatoriamente al grupo experimental o control (10 personas por grupo) para ser tratados con RAR y etoricoxib, 120 mg/día, o placebo por siete días. Los índices clínicos se registraron antes y un mes después de la terapia. Así mismo, los niveles de PGE2 se midieron en el fluido crevicular mediante radioinmunoensayos al inicio del estudio, y 7 y 30 días después del tratamiento. Al final del periodo experimental, no se observaron diferencias estadísticamente significativas en los parámetros clínicos entre los grupos, aun cuando ambos presentaron mejoría significativa en todas las variables examinadas. Se presentó una disminución en los niveles de inserción clínica desde 5,54 ± 0,47 mm a 3,59 ± 0,53 mm en el grupo experimental y desde 5,92 ± 1,10 mm a 3,69 ± 0,8 mm en el grupo control. Además, se encontró una disminución de la PGE2 después de siete días de tratamiento. Los autores concluyeron que el etoricoxib no promueve una mejoría adicional de los parámetros clínicos pero produce una reducción inicial en los niveles de PGE2 en el fluido crevicular, que podría relacionarse con una mejoría de la condición ósea.
Conclusiones
La importancia reconocida de la respuesta inflamatoria del huésped en la patogénesis de la enfermedad periodontal establece la posibilidad de explorar nuevas estrategias de tratamiento. Cuando se utilizan AINES en estudios realizados en animales, teniendo presentes sus limitaciones, se observa una reducción significativa en la pérdida ósea y en los niveles de prostaglandinas E2 gingivales, sugiriendo su aplicación clínica en el tratamiento de la periodontitis. A pesar de los múltiples diseños experimentales, las variaciones en el tamaño de la muestra y las características de las poblaciones, diferentes ensayos clínicos demuestran que la inhibición de los metabolitos del ácido araquidónico mediante AINES adjuntos al tratamiento mecánico, reducen la inflamación gingival y el progreso de la enfermedad periodontal. Sin embargo, los efectos adversos que presentan algunos inhibidores COX, implica utilizarlos con precaución cuando se manejan en el tratamiento conjunto de la periodontitis.
Bibliografía
1. Beklen A, Hukkanen M, Richardson R, Konttinen YT. Immunohistochemical localization of Toll-like receptors 1-10 in periodontitis. Oral Microbiol Immunol 2008;23: 425-31. [ Links ]
2. Inaba H, Tagashira M, Honma D, Kanda T, Kou Y, Ohtake Y, et al. Identification of hop polyphenolic components which inhibit prostaglandin E2 production by gingival epithelial cells stimulated with periodontal pathogen. Biol Pharm Bull 2008;31:527-30. [ Links ]
3. Yen CA, Damoulis PD, Stark PC, Hibberd PL, Singh M, et al. The effect of a selective cyclooxygenase-2 inhibitor (celecoxib) on chronic periodontitis. J Periodontol 2008;79:104-13. [ Links ]
4. Oliveira TM, Sakai VT, Machado MA, Dionísio TJ, Cestari TM, Taga R, et al. COX-2 inhibition decreases VEGF expression and alveolar bone loss during the progression of experimental periodontitis in rats. J Periodontol. 2008; 79:1062-9. [ Links ]
5. Noguchi K, Yanai M, Shitashige M, Nishihara T, Ishikawa I. Cyclooxygenase-2-dependent prostaglandin production by peripheral blood monocytes stimulated with lipopolysaccharides isolated from periodontopathogenic bacteria. J Periodontol 2000;71:1575-82. [ Links ]
6. American Academy of Periodontology. Parameter on chronic periodontitis with advanced loss of periodontal support. J Periodontol 2000;71(5 Suppl):856-8. [ Links ]
7. Aras H, Caðlayan F, Güncü GN, Berberoðlu A, Kilinç K. Effect of systemically administered naproxen sodium on clinical parameters and myeloperoxidase and elastase-like activity levels in gingival crevicular fluid. J Periodontol 2007;78:868-73. [ Links ]
8. Azoubel MC, Sarmento VA, Cangussú V, Azoubel E, Bittencourt S, Cunha FQ, et al. Adjunctive benefits of systemic etoricoxib in non-surgical treatment of aggressive periodontitis: short-term evaluation. J Periodontol 2008;79:1719-25. [ Links ]
9. Aagaard L, Hansen EH. Information about ADRs explored by pharmacovigilance approaches: a qualitative review of studies on antibiotics, SSRIs and NSAIDs. BMC Clin Pharmacol 2009;9:4-18. [ Links ]
10. Chandrasekharan NV, Dai H, Roos KL, Evanson NK, Tomsik J, Elton TS, et al. COX-3, a cyclooxygenase-1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: cloning, structure, and expression. Proc Natl Acad Sci USA 2002;99:13926-31. [ Links ]
11. Paquette DW, Williams RC. Modulation of host inflammatory mediators as a treatment strategy for periodontal diseases. Periodontology 2000;24:239-52. [ Links ]
12. Lohinai Z, Stachlewitz R, Szekely AD, Feher E, Dezsi L, Szabo C. Evidence for the expression of cyclooxygenase-2 enzyme in periodontitis. Life Sci 2001; 70:279-90. [ Links ]
13. Engelhardt G. Pharmacology of meloxicam, a new non-steroidal anti-inflammatory drug with an improved safety profile through preferential inhibition of COX-2. Br J Rheumatol 1996;35(Suppl 1):4-12. [ Links ]
14. McGettigan P, Henry D. Cardiovascular Risk and Inhibition of Cyclooxygenase. A systematic review of the observational studies of selective and nonselective Inhibitors of cyclooxygenase 2. JAMA 2006;296:1633-44. [ Links ]
15. Nassar CA, Nassar PO, Nassar PM, Spolidorio LC. Selective cyclooxygenase-2 inhibition prevents bone resorption. Braz Oral Res 2005;19:36-40. [ Links ]
16. Bezerra MM, de Lima V, Alencar VB, Vieira IB, Brito GA, Ribeiro RA, et al. Selective cyclooxygenase-2 inhibition prevents alveolar bone loss in experimental periodontitis in rats. J Periodontol 2000;71:1009-14. [ Links ]
17. Holzhausen M, Rossa Júnior C, Marcantonio Júnior E, Nassar PO, Spolidório DM, Spolidório LC. Effect of selective cyclooxygenase-2 inhibition on the development of ligature-induced periodontitis in rats. J Periodontol 2002;73:1030-6. [ Links ]
18. Vardar S, Buduneli E, Baylas H, Berdeli AH, Buduneli N, Atilla G. Individual and combined effects of selective cyclooxygenase-2 inhibitor and omega-3 fatty acid on endotoxin-induced periodontitis in rats. J Periodontol 2005;76:99-106. [ Links ]
19. Holzhausen M, Spolidorio DM, Muscará MN, Hebling J, Spolidorio LC. Protective effects of etoricoxib, a selective inhibitor of cyclooxygenase-2, in experimental periodontitis in rats. J Periodontal Res 2005;40 (3):208-11. [ Links ]
20. Azoubel MC, Menezes AM, Bezerra D, Oriá RB, Ribeiro RA, Brito GA. Comparison of etoricoxib and indomethacin for the treatment of experimental periodontitis in rats. Braz J Med Biol Res 2007;40:117-25. [ Links ]
21. Tipton DA, Flynn JC, Stein SH, Dabbous MKh. Cyclooxygenase-2 inhibitors decrease interleukin-1beta-stimulated prostaglandin E2 and IL-6 production by human gingival fibroblasts. J Periodontol 2003;74: 1754-63. [ Links ]
22. Tipton DA, Gay DC, DeCoster VA. Effect of a cyclooxygenase-2 inhibitor on interleukin-1beta-stimulated activation of the transcription factor nuclear factor-kappa B in human gingival fibroblasts. J Periodontol 2007;78:542-9. [ Links ]
23. Flemmig TF, Rumetsch M, Klaiber B. Efficacy of systemically administered acetylsalicylic acid plus scaling on periodontal health and elastase-alpha 1-proteinase inhibitor in gingival crevicular fluid. J Clin Periodontol 1996;23:153-9. [ Links ]
24. Vardar S, Baylas H, Huseyinov A. Effects of selective cyclooxygenase-2 inhibition on gingival tissue levels of prostaglandin E2 and prostaglandin F2alpha and clinical parameters of chronic periodontitis. J Periodontol 2003 ;74:57-63. [ Links ]
25. OLeary TJ, Drake RB, Naylor JE. The plaque control record. J Periodontol 1972;43:38. [ Links ]
26. Reddy MS, Palcanis KG, Barnett ML, Haigh S, Charles CH, Jeffcoat MK. Efficacy of meclofenamate sodium (Meclomen) in the treatment of rapidly progressive periodontitis. J Clin Periodontol 1993;20:635-40. [ Links ]
27. Jeffcoat MK, Page R, Reddy M, Wannawisute A, Waite P, Palcanis K, et al. Use of digital radiography to demonstrate the potential of naproxen as an adjunct in the treatment of rapidly progressive periodontitis. J Periodontal Res 1991;26:415-21. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Carlos Martín Ardila Medina
Carrera 47 No. 20 sur 46
Envigado Antioquía Colombia
57(4) 3348122
E-mail: martinrdila@gmail.com
Fecha de recepción: 13 de abril 2009.
Fecha de aceptación: 21 de abril 2009.