Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Clínica de Medicina de Familia
versión On-line ISSN 2386-8201versión impresa ISSN 1699-695X
Rev Clin Med Fam vol.5 no.2 Barcelona jun. 2012
https://dx.doi.org/10.4321/S1699-695X2012000200007
Síndrome Doloroso Regional Complejo
The Complex Regional Pain Synndrome
Concepción Cuenca Gonzáleza, María Isabel Flores Torresb, Karla Vanesa Méndez Saavedrac, Idoya Barca Fernándeza, Alejandro Alcina Navarroa, Alejandro Villena Ferrerd
aMédico de Familia, Especialista en Rehabilitación. Servicio de Medicina Física y Rehabilitación. Hospital Universitario Clínico San Carlos. Madrid
bServicio de Medicina Física y Rehabilitación. Hospital La Inmaculada Huercal-Overa. Almería
cServicio de Medicina Física y Rehabilitación. Complejo Hospitalario Universitario, Albacete
dMédico de Familia. Consultorio de La Alberca de Záncara. CS de San Clemente. Cuenca
Dirección para correspondencia
RESUMEN
El síndrome doloroso regional complejo es una enfermedad crónica y compleja cuyo diagnóstico precoz es esencial para una evolución favorable así como para evitar complicaciones. Esta entidad pasa habitualmente desapercibida, realizándose su diagnóstico principalmente por la exploración clínica del paciente y siendo por tanto de fácil identificación si conocemos sus síntomas y formas de presentación. Podemos comenzar el tratamiento farmacológico desde Atención Primaria, realizando posteriormente una correcta derivación al médico rehabilitador para la prescripción de tratamiento fisioterápico y seguimiento evolutivo.
Palabras clave: Síndromes de Dolor Regional Complejo, Distrofia Simpática Refleja, Causalgia.
ABSTRACT
Complex regional pain syndrome is a chronic, complex illness whose early diagnosis is essential for favourable progress and in order to avoid complications. This entity usually goes unnoticed, with diagnosis taking place mainly through medical examination of the patient, and thus resulting easy to identify if its symptoms and signs are known. Drug treatment can be commenced at primary health care with subsequent referral to a rehabilitator for the prescription of physiotherapeutic treatment and monitoring.
Key words: Complex Regional Pain Syndromes, Reflex Sympathetic Dystrophy, Causalgia.
Introducción
El Síndrome Doloroso Regional Complejo (SDRC) es clásicamente conocido como distrofia simpático refleja (DSR) o Síndrome de Südeck. Esta enfermedad es explicada por primera vez por Paget en 1862 y Wolf en 1877, siendo Mitchel (1864) el primero en utilizar el término de causalgia1. La Asociación Internacional para el estudio del Dolor (IAPS) determinó en 1993 adoptar la denominación de SDRC y a partir de 1994 lo clasifica en 2 tipos, según la existencia o no de lesión nerviosa.
El SDRC engloba un conjunto de entidades nosológicas que se manifiestan tras una lesión o daño y cuya clínica se caracteriza por la presencia de dolor regional, predominantemente distal, acompañado de alteraciones sensitivas, cambios cutáneos, cambios de temperatura, disfunción vasomotora, presencia de edema y retraso en la recuperación funcional2. La duración y magnitud de la clínica es más duradera de la esperada y, en ocasiones, conlleva manifestaciones psicológicas, siendo la evolución en el tiempo variable. Es importante realizar diagnóstico diferencial con otras entidades que presenten síntomas y signos similares.
La IAPS define dos tipos de SDRC: el tipo I (Distrofia Simpática Refleja o Síndrome de Südeck), en el que no se identifica ninguna lesión nerviosa y representa el 90% de los casos clínicos y el tipo II (Causalgia), en la que sí objetivamos lesión nerviosa.
El SDRC con frecuencia aparece tras un episodio nocivo desencadenante, principalmente cirugías o traumatismos menores y se manifiesta con dolor espontáneo o hiperalgesia, no limitado a dermatomas ni a la distribución territorial de un nervio periférico. Suelen ser cuadros desproporcionados al episodio previo (de poca intensidad) y en el territorio de la lesión puede o no haber aparecido edema, anormalidad en flujo sanguíneo cutáneo o actividad sudomotora3.
La incidencia presenta grandes variaciones: 0,05-35% en función de la población analizada y de los criterios diagnósticos establecidos.Las edades varían en los distintos estudios consultados, siendo la edad media de presentación de 45 años. Existe una predominancia por el sexo femenino (60-80%) y no parece existir predilección de razas4,5.Se ha observado la afectación, con mayor frecuencia, de un único miembro, con predominancia del hemicuerpo izquierdo respecto al derecho y puede afectarse cualquier localización, incluidos órganos intraabdominales o pélvicos.Se estima que el 20-35% de los pacientes presenta algún grado de incapacidad como consecuencia del proceso.
La etiología del SDRC se puede clasificar en causas potenciales, posibles y estadísticamente significativas (tabla 1). La etiología iatrogénica es un diagnóstico fácilmente identificable en pacientes intervenidos quirúrgicamente de Síndrome del Túnel Carpiano (STC) o Síndrome de Dupuytren.

Tabla 1. Clasificación de las causas del SDRC.
La patogénesis del SDRC es todavía dudosa y entre las series estudiadas se demuestra que en el 35% de los casos no se ha observado un factor desencadenante. Se ha atribuido al Sistema Nervioso Central (SNC) un papel en la patogénesis del SDRC a partir de determinadas observaciones, como el hecho de que el bloqueo del Nervio Simpático unilateral mejora los casos con afectación bilateral o que la actividad del Sistema Nervioso Simpático regulada por el hipotálamo (temperatura corporal) aumenta en el área dañada6, por ejemplo.
La fisiopatología del SDRC no se ha definido con exactitud. Se han observado como mecanismos fisiopatológicos: un factor desencadenante, la neurotransmisión del impulso nervioso a centros simpáticos regionales, la percepción distorsionada del mensaje y una exagerada respuesta neurovegetativa en intensidad y extensión que desencadena una alteración regional y mantenida de la microcirculación7.
Clínica
Son varios los síntomas y signos que podemos observar en estos pacientes. Entre ellos destacamos, por su frecuencia: dolor intenso, hiperestesia, hiperalgesia, alodinia, déficit sensorial, trastorno hemisensorial, hipoestesia, tumefacción, sudoración anormal, cambios cutáneos (palidez, fibrosis, hiperqueratosis, piel brillante y fina, cambios de temperatura y coloración, etc.), atrofia muscular y ósea y alteraciones tróficas8.
También pueden presentar disfunción motriz como temblores, distonía, mioclonías, limitación de movilidad articular y alteración muscular9.
Bonica describió tres etapas en el SDRC:
- Estadio I: sin causa aparente o seguido de un evento. Presentan dolor difuso, tipo quemazón, en un miembro, de predominio nocturno que se intensifica con los movimientos. Se acompaña de edema, hiperhidrosis, trastornos de la sensibilidad y crecimiento rápido de vello y uñas. La piel está eritematosa con aumento de la temperatura. La duración aproximada de esta fase es de varios días a tres meses (figura 1).
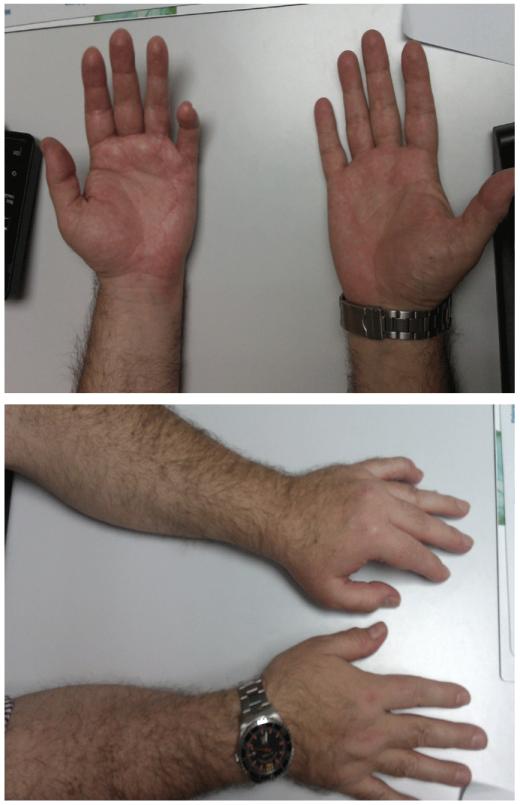
Figura 1. Varón con SDRC tipo I en fase aguda inflamatoria en extremidad
superior izquierda distal tras cirugía por enfermedad de Dupuytren.
- Estadio II: hay una tendencia a la disminución del dolor y de los signos pseudoinflamatorios, con tendencia a la impotencia funcional. La piel se presenta fina y cianótica y existen cambios en las faneras: el crecimiento del vello se enlentece y las uñas aparecen agrietadas y friables. Pueden aparecer retracciones tendinosas y cápsulo-ligamentosas que limitan el balance articular. Duración aproximada de tres a seis meses (figura 2).

Figura 2. Mujer con SDRC tipo I en fase distrófica en extremidad superior izquierda distal.
- Estadio III: es el más severo, caracterizado por limitación de la movilidad. Los pacientes pueden presentar un síndrome hombro-mano, contractura de dedos, cambios tróficos cutáneos y ungueales y pueden aparecer movimientos involuntarios, espasmo muscular y pseudoparálisis. En la radiografía ósea se observa importante desmineralización. La aparición de trastornos psiquiátricos de tipo depresivo es relativamente frecuente. Duración más de seis meses o un año10,11,12.
Diagnóstico
No existen signos ni síntomas patognomónicos y no hay una prueba de diagnóstico definitiva del SDRC. El diagnóstico se basa en la elaboración de una completa historia clínica que incluye la severidad y duración de los síntomas y signos, tipo de fractura y gravedad de la lesión y en la exploración física del miembro afecto13.
Se ha intentado elaborar criterios diagnósticos estandarizados que faciliten el diagnóstico y tratamiento dada la dificultad que entraña el manejo de esta entidad, siendo actualmente los más aceptados los de Kozín (tabla 2) y los de la IASP (tabla 3)14. Estos últimos fueron revisados por la propia IASP en 2007 (criterios de Budapest) encontrando una sensibilidad del 85% y una especificidad del 69%12,15.

Tabla 2. Criterios diagnósticos de Kozin

Tabla 3. Criterios diagnósticos de la Asociación internacional para el estudio del dolor (IASP)
Son varias las pruebas complementarias que se emplean en el manejo de este cuadro clínico y que nos sirven como ayuda para el diagnóstico diferencial con otros síndromes de dolor crónico3. Sin embargo, la utilidad de las mismas no siempre justifica su petición.
Entre las pruebas complementarias utilizadas16,17 podemos encontrar:
- Pruebas de laboratorio (analítica): no se observan alteraciones significativas. Los reactantes de fase aguda pueden ser normales.
- Radiografía: es de utilidad en fases tardías, pudiéndose observar desmineralización ósea tras inmovilización. Presenta una sensibilidad y especificidad de 73% y 57%. Genant et al. establecieron 5 parámetros radiológicos (tabla 4)5. Otros autores describen un proceso regional que muestra una imagen unilateral de desmineralización de las metaepífisis de predominio subcondral, lesiones heterogéneas de tipo geódico y osteoporosis de intensidad variable, pudiendo afectarse articulaciones vecinas y del resto de la extremidad.

Tabla 4. Parámetros radiográficos de Genant.
- Tomodensitometría: aporta resultados similares a los obtenidos con la radiografía, con la ventaja de poder disponer de dicha información en un estadio más precoz para un tratamiento adecuado y seguimiento de la remineralización ósea.
- TAC: una asimetría de flujo en la fase 1, 2 y/o 3 es sugerente de SDRC. Aporta información relevante en diagnósticos complejos (coexistencia de alteraciones vasomotoras, afectación de tendones, ligamentos, cápsula articular y partes blandas)18. En la TAC observamos un área focal de osteoporosis asemejándose la imagen al queso suizo cuando la entidad se encuentra en estadio III. No es más sensible ni específica que la escintigrafía, con los inconvenientes de su mayor coste y la exposición del paciente a una dosis de radiación. No se aconseja como prueba diagnóstica.
- RMN: es de utilidad para realizar un diagnóstico precoz y establecer diagnóstico diferencial con otras patologías (osteonecrosis de cadera)2. Las imágenes obtenidas son de interés especialmente en los estadios clínicos I y III.
- Gammagrafía: recomendada en estadios I y II, desaconsejada en estadio III, con una sensibilidad y especificidad de 97% y 86%. Su principal indicación es para el diagnóstico precoz del SDRC. En fases iniciales se observa hipercaptación ósea intensa y precoz a nivel regional que sobrepasa los límites de la articulación afectada. Ocasionalmente, en fase tardía se puede observar hipocaptación del isótopo14.
- Otras pruebas: flebografía intraósea, Q-SART19 (se emplea como índice indirecto de la actividad simpática y registra para ello la producción del sudor), termografía (sólo indicada en fase I), fluximetría cutánea por técnica doppler láser, bloqueo neural diferencial y electromiograma (indicado para diagnóstico de SDRC tipo II). La realización conjunta de termografía y Q-SART nos aporta una excelente información predictora de respuesta al bloqueo simpático, presentando un 94% de sensibilidad y 98% de especificidad.
El diagnóstico diferencial va a depender de la fase evolutiva. En fase inicial habrá que considerar artritis infecciosas, artritis reumáticas, artropatía inflamatoria, arteriopatía periférica y trombosis venosa profunda. En fase crónica (con secuelas) con la enfermedad de Dupuytren, esclerodermia y fascitis plantar. En afectaciones de la cadera conviene descartar coxitis y osteonecrosis. Si existe desmineralización ósea será recomendable descartar fracturas de estrés, osteoporosis y tumores óseos benignos y malignos (tabla 5).

Tabla 5. Diagnóstico diferencial del SDRC
Tratamiento
Para una completa recuperación y evitar secuelas es aconsejable instaurar un tratamiento precoz, individualizado y multidisciplinar, basado en el control del dolor, tratamiento rehabilitador y terapias psicológicas20,12. La finalidad es conseguir la funcionalidad previa con las medidas analgésicas adecuadas en cada caso. Un tratamiento precoz e intensivo del SDRC podría disminuir las posibilidades de cronificación.
TRATAMIENTO FARMACOLÓGICO
El paracetamol y los antiinflamatorios no esteroideos suelen utilizarse como primera línea de tratamiento en la fase aguda y los últimos pueden estar indicados para tratar la inflamación, aunque la evidencia es insuficiente para recomendarlos como tratamiento eficaz del dolor.
Aunque los corticoides han demostrado, en varios ensayos, un efecto beneficioso sobre el dolor, el edema y la movilidad en la fase aguda, su utilización es controvertida por sus efectos negativos sobre la masa ósea. Las pautas utilizadas pueden ser variables y podemos encontrar, según autores, desde prednisona 30 mg/día con reducción progresiva durante 12 semanas hasta dosis más potentes de 30-60 mg repartidos a lo largo del día con reducción progresiva en 2-4 semanas.
La gabapentina a dosis de 600-1800 mg/día durante las primeras 8 semanas puede mejorar significativamente el dolor en el SDRC, aunque no parece controlar otros síntomas como la hiperalgesia o la alodinia.
La calcitonina se ha utilizado a dosis de 100 U/día s.c. o 200 U/día por vía nasal aunque la evidencia de efectos beneficiosos es controvertida según autores. Su utilización requiere suplementos de calcio 4 horas después de su aplicación.
Los bifosfonatos han demostrado mejorar los signos inflamatorios y la movilidad aunque la dosis, tiempo de tratamiento y vía de administración son variables en los diferentes estudios.
La tabla 6 recoge diferentes opciones de tratamiento farmacológico para el control del dolor4,14,21,22.

Tabla 6. Tratamiento farmacológico del SDRC. Nivel de la recomendación:
A (revisiones sistemáticas y meta-análisis de ensayos clínicos
y ensayos clínicos individuales con intervalos de confianza estrechos),
B (revisiones sistemáticas de estudios de cohortes y de casos y controles,
estudios de cohortes y de casos y controles individuales y ensayos clínicos de menor calidad),
C (series de casos y estudios de cohortes y de casos y controles de mala calidad),
D (opiniones de expertos).
BLOQUEOS
En la tabla 7 recogemos los principales tipos de bloqueo. Un metaanálisis publicado en 2010 hace referencia a los grados de recomendación según la vía de administración: intravenoso (no recomendado) y percutáneo (indicado si fallan los vasodilatadores en la fase fría II)16,21.

Tabla 7. Bloqueos nerviosos en el SDRC. Nivel de la recomendación:
A (revisiones sistemáticas y meta-análisis de ensayos clínicos y ensayos
clínicos individuales con intervalos de confianza estrechos),
B (revisiones sistemáticas de estudios de cohortes y de casos y controles,
estudios de cohortes y de casos y controles individuales y ensayos clínicos de menor calidad),
C (series de casos y estudios de cohortes y de casos y controles de mala calidad),
D (opiniones de expertos).
ESTIMULACIÓN ELÉCTRICA MEDULAR
La aplicaremos en aquellos casos en que tras 6 meses de tratamiento rehabilitador y/o bloqueo simpático no se observa mejoría. Su principal indicación es en la disminución de la intensidad del dolor, sobre todo en pacientes muy deteriorados para mejorar su calidad de vida23,24. Se considera efectiva en SDRC tipo I (con fuerza de la recomendación elevada) y en el SDRC tipo II (recomendación débil). A partir de los 12 meses de tratamiento, los costes son menores que en el tratamiento estándar del SDRC.
ESTIMULACIÓN MAGNÉTICA TRANSCRANEAL REPETITIVA DE LA CORTEZA MOTORA (rTMS)
Es una terapia con resultados prometedores, aunque no conocemos la duración de su efecto analgésico ni efectos secundarios.
TRATAMIENTO REHABILITADOR
Como consecuencia de la posible evolución tórpida de esta patología, el diagnóstico precoz es fundamental para el inicio temprano del tratamiento rehabilitador, proponiéndose terapia de forma individualizada. El objetivo principal es evitar la discapacidad asociada al dolor y la limitación de la movilidad (tabla 8).

Tabla 8. Tratamiento rehabilitador del SDRC. Nivel de la recomendación:
A (revisiones sistemáticas y meta-análisis de ensayos clínicos
y ensayos clínicos individuales con intervalos de confianza estrechos),
B (revisiones sistemáticas de estudios de cohortes y de casos y controles,
estudios de cohortes y de casos y controles individuales y ensayos clínicos de menor calidad),
C (series de casos y estudios de cohortes y de casos y controles de mala calidad),
D (opiniones de expertos)
En el campo de la rehabilitación tenemos distintos abordajes que se deben emplear de forma conjunta en aquellos casos en los que sea necesario25,26:
- Cinesiterapia activa y pasiva, que consistirá en la realización de movimientos suaves graduales e incremento progresivo de estímulos sensoriales (objetos de distinta textura/ baños de contraste calor-frío), si bien son más recomendables los movimientos activos, ya que los pasivos pueden actuar como estímulos dolorosos. Es recomendable realizar fisioterapia asociada a tratamientos analgésicos, bloqueos simpáticos, periféricos y electroanalgesia con TENS. Un ensayo clínico aleatorizado (n=135) ha demostrado que la cinesiterapia aplicada junto a tratamiento farmacológico tiene un efecto clínicamente relevante sobre la severidad de los síntomas y la funcionalidad del paciente27,28.
- Terapia ocupacional: tiene efectos positivos sobre la severidad de las limitaciones funcionales y sobre el nivel de actividad en pacientes con SDRC I27,28. El tratamiento se basa en el uso del miembro afectado sin dolor y en promover la integración del miembro en los usos diarios del paciente, pudiendo ser empleadas férulas como apoyo funcional para disminuir los síntomas29,30,31.
- Electroterapia: Los TENS (estimulación eléctrica nerviosa transcutánea) han sido empleados para calmar el dolor en pacientes con SDRC I. Existen estudios de limitada calidad metodológica que señalan beneficios en estos pacientes con el uso de TENS32,33. Una vez comprobado si son efectivos en el control del dolor, es recomendable su uso.
- Otros: crioterapia, masoterapia, baños de contraste, magnetoterapia. Ante la presencia de edemas en los miembros inferiores podemos utilizar el drenaje linfático manual (DLM), ejercicios activos con pesas y la deambulación controlada. El ejercicio físico más recomendables para este síndrome es la natación, la hidrocinesiterapia y el taichí. La evidencia sobre los beneficios de la acupuntura es escasa34.
TERAPIA PSICOLÓGICA
Es recomendable la aplicación de tratamiento psicológico, sobre todo en casos más severos, recibiendo tanto el paciente como sus familiares información adecuada sobre los síntomas de la enfermedad, fisiopatología, evolución y las posibles interacciones con los factores psicológicos. En tiempos inferiores a 6-8 semanas de duración no estaría indicado realizarla. Será necesario valorar el tipo de tratamiento específico en cada caso como terapia de grupo o psicoterapia cognitiva-conductual34.
Pronóstico
El pronóstico del SDRC generalmente es favorable. El 74% de los pacientes presenta una resolución espontánea de los síntomas. Un diagnóstico erróneo prolongado y retrasar el inicio de un tratamiento correcto pueden dar lugar a una importante discapacidad crónica, presentando hasta un 50% de pacientes que no han recibido tratamiento sintomático antes del año secuelas irrecuperables35.
La aplicación de un tratamiento precoz, en los primeros tres meses desde el inicio de los síntomas, mejorará la evolución del cuadro. El 80% de pacientes que reciben tratamiento sintomático en el primer año mejora significativamente.
Si bien el pronóstico a largo plazo es favorable, se estima que solo un 20% de los afectados puede recuperar su nivel previo de funcionalidad33. Observamos secuelas leves (dolor, edema) en 20-40% de los casos. La presencia de secuelas más graves puede precisar intervención quirúrgica e incluso amputaciones.
Prevención
La prevención es el mejor tratamiento del SDRC. Como prevención primaria podemos utilizar la vitamina C. En varios estudios se demuestra que el uso de 500-1000 mg de vitamina C durante 45-55 días reduce el riesgo de presentar SDRC I tras fractura de muñeca comparado con placebo16.
Respecto al empleo de la calcitonina, no existe evidencia suficiente para sustentar su uso en prevención primaria, aunque la administración de 100 U/día s.c. durante 4 semanas podría prevenir las recaídas21.
En la mayoría de los casos la mejor prevención es la detección y tratamiento precoces. Se recomienda actuar en el primer estadio, cuando aun no se observan cambios radiológicos, con movilización precoz del miembro afectado.
Es importante una correcta educación del paciente en las diferentes terapias prescritas y su participación activa en aquellas que lo permitan, así como una adecuada orientación a nivel laboral.
Bibliografía
1. Gler BS, Schwartz L, Alien R. Síndromes de dolor regional complejo: tipo I (distrofia simpático refleja) y tipo II (causalgia). En: Loeser JD, Butler SH, Chap-man CR, et al. Bonica Terapéutica del Dolor. Vol I. McGraw-Hill Interamericana, Tercera edición, México; 2003. p. 467-967. [ Links ]
2. Fornos-Vieitez B, López-Díez FE, Ciriza-Lasheras A, López-López D. Síndrome de Sudeck (distrofia simpático refleja). Semergen. 2008; 34: 455-8. [ Links ]
3. Ribera MV. Síndrome de dolor regional complejo tipo I y II. Dolor. 2003; 18:83-4. [ Links ]
4. Neira F, Ortega JL. El Síndrome doloroso regional complejo y medicina basada en la evidencia. Rev Soc Esp Dolor. 2007; 2:133-46. [ Links ]
5. Satishchandra K. Reflex Sympathetic Dystrophy Surgery. Emedicine [Internet]. 2011 [citado 16 Ene 2012]; Disponible en: http://emedicine.medscape.com/article/1269453-overview. [ Links ]
6. Abdi S, Sheon RP. Etiology, clinical manifestations and diagnosis of complex regional pain syndrome in adults. Uptodate [Internet] 2011 [citado 16 Ene 2012]; http://www.uptodate.com/contents/etiology-clinical-manifestations-and-diagnosis-of-complex-regional-pain-syndrome-in-adults. [ Links ]
7. Schwartzman RJ, Alexander GM, Grothusen J. Pathophysiology of complex regional pain syndrome. Expert Rev Neurother 2006; 6(5): 669-81. [ Links ]
8. Rho RH, Brewer RP, Lamer TJ, Wilson PR. Complex regional pain syndrome. Mayo Clin Proc 2002; 77:174-80. [ Links ]
9. Wheeler AH. Complex Regional Pain Syndromes. Emedicine [Internet]. 2011 [citado 19 Ene 2012]; Disponible en: http://emedicine.medscape.com/article/1145318-overview. [ Links ]
10. Alvarez López JC. Distrofia simpático refleja o síndrome de dolor regional complejo tipo I. Rev Soc Esp Dolor. 2003;10:294-302. [ Links ]
11. Veldman PHJM, Reynen HM, Arntz IE, Geris RS. Signs and symptoms of reflex sympathetic distrophy, prospective study of 829 patients. Lancet. 1993; 342:1012-6. [ Links ]
12. Márquez Martínez E, Ribera Canudas MV, Mesas Idáñez A, et al. Síndrome de dolor regional complejo. Semin Fund Esp Reumatol. 2011. doi: 10.1016/j.semreu.2011.10.005. [ Links ]
13. Quisel A, Gilí JM, Witherell R. Complex regional pain syndrome under-diagnosed. J Fam Pract. 2005; 54 (6):524-32. [ Links ]
14. Holgado Catalán S, González Sibila C. Distrofía simpático-refleja. FMC 2007; 14:458-64. [ Links ]
15. Harden RN, Bruehl S, Pérez RS, Birklein F, Marinus J, et al. Validation of proposed diagnostic criteria (The Budapest Criteria) for Complex Regional Pain Syndrome. Pain. 2010; 150:268-74. [ Links ]
16. Domingo Regany E, Rodríguez Bacardit N. Síndrome de dolor regional complejo. Fisterra.com [Internet]. 2011 [citado 19 Ene 2012]; Disponible en: http://www.fisterra.com/guias-clinicas/sindrome-dolor-regional-complejo/. [ Links ]
17. Pichot C. Distrofia simpático refleja / síndrome de dolor regional complejo tipo I: exploraciones complementarias. Rev Esp Reumatol. 1998; 25:270-75. [ Links ]
18. Rodrigo MD, Perena MJ, Serrano P, et al. Síndrome de dolor regional complejo. Rev Soc Dolor. 2000; 7: Supl. II, 78-97. [ Links ]
19. Matases MS. Síndrome del dolor regional complejo. Dolor neuropàtico periférico. Dolor 2002; 17:78-86. [ Links ]
20. Calvo-García C, Escudero-Socorro M, Gómez-García A. Síndrome de dolor regional complejo sin causa aparente. A propósito de un caso. Rehabilitación (Madr). 2009; 43:187-90. [ Links ]
21. Perez RS, Zollinger PE, Dijkstra PU, et al. CRPS I task force. Evidence based guidelines for complex regional pain syndrome type 1. BMC Neurology 2010; 10:20. [ Links ]
22. Otero-Alvaro A, Pérez Caballer A, Gómez-Castresana F. Tratamiento farmacológico del síndrome doloroso regional complejo de las extremidades como cusa de dolor neuropático. Rev Clin Esp 2004; 204: 486-94. [ Links ]
23. Taylor RS. Spinal cord stimulation in complex regional pain síndrome and refractory neuropathic back ang leg pain / failed back surgery syndrome: results of a systematic review and meta-analysis. J Pain Symptom Manage. 2006; 31 Suppl 4: 13-9. [ Links ]
24. Kemler MA, Barendse GA, Van der Wildemberg FA, et al. The effect of spinal cord stimulation in patients with chronic reflex sympathetic dystrophy: two years follow-up of the randomized control trial. Ann Neurol. 2004; 55:13-8. [ Links ]
25. Maihófner C, Seifert F, Markovic K. Complex regional pain syndromes: New parathophysiological concepts and therapies. Eur J Neurol. 2010: 17:649-60. [ Links ]
26. Tran de QH, Doung S, Bertini P, Finlayson R.J. Treatment of complex regional pain syndrome: a review of the evidence. Can J Anaesth. 2010; 57:149-66. [ Links ]
27. Oerlemans HM, Oostendorp RA, de Boo T, Goris RJ. Pain and reduced mobility in complex regional pain syndrome I: outcome of a prospective randomised controlled clinical trial of adjuvant physical therapy versus occupational therapy. Pain 1999, 83:77-83. [ Links ]
28. Oerlemans HM, Oostendorp RA, de Boo T, van der Laan L, Severens JL, Goris JA. Adjuvant physical therapy versus occupational therapy in patients with reflex sympathetic dystrophy/complex regional pain syndrome type I. Arch Phys Med Rehabil 2000; 81:49-56. [ Links ]
29. Stanton-Hicks M, Baron R, Boas R, Gordh T, Harden N, Hendler N, et al. Complex regional pain syndromes: Guidelines for therapy. Clin J Pain 1998; 14:155-166. [ Links ]
30. Vacariu G. Complex regional pain syndrome. Disabil Rehabil 2002; 24:435-42. [ Links ]
31. Hareau J. What makes treatment for reflex sympathetic dystrophy successful? J Hand Ther 1996; 9:367-70. [ Links ]
32. Kesler RW, Saulsbury FT, Miller LT, Rowlingson JC. Reflex sympathetic dystrophy in children: treatment with transcutaneous electric nerve stimulation. Pediatrics 1988; 82:728-32. [ Links ]
33. Robaina FJ, Dominguez M, Diaz M, Rodriguez JL, de Vera JA. Spinal cord stimulation for relief of chronic pain in vasospastic disorders of the upper limbs. Neurosurgery 1989; 24:63-67. [ Links ]
34. Albaraz R, Toh Wong Y, Homer-Vanniasinkam S. Síndrome del dolor regional complejo: revision. Ann Vasc Surg. 2008; 22:322-32. [ Links ]
35. Brunner F, Nauer M, Bachmann LM. Poor prognostic factors in complex regional pain syndrome 1: A Delphi survey. J Rehabil Med. 2011; 43: 783-6. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Concepción Cuenca González
Hospital Universitario Clínico de Madrid
Profesor Marín Lagos s/n 28040, Madrid
Tel: 913303603
Correo electrónico: cuchacuenca@terra.com
Recibido el 21 de febrero de 2012
Aceptado para su publicación el 12 de abril de 2012














