Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista Clínica de Medicina de Familia
versión On-line ISSN 2386-8201versión impresa ISSN 1699-695X
Rev Clin Med Fam vol.8 no.2 Barcelona jun. 2015
https://dx.doi.org/10.4321/S1699-695X2015000200005
¿Qué inyectables pueden ser administrados por vía oral o enteral?
Which injectable medication can be administered orally or enterally?
Gregorio Romero Candela y Francisco Tejada Cifuentesb
a Residente de Farmacia Hospitalaria. Complejo Hospitalario Universitario de Albacete. Albacete (España).
b Farmacéutico de Atención Primaria. Complejo Hospitalario Universitario de Albacete. Albacete (España).
Dirección para correspondencia
RESUMEN
En este artículo recogemos los principios éticos y legales cuando hemos de decidir sobre el uso de un medicamento en condiciones distintas a las de su ficha técnica. Los medicamentos no siempre están disponibles en formulaciones adecuadas para pacientes con dificultades para tragar o pacientes con sondas de alimentación enteral. Por lo tanto, la modificación de las formas farmacéuticas puede ser necesaria. Se proporciona una lista de inyectables que pueden ser administrados por vía enteral mediante sondas de alimentación o por vía oral cuando no hay alternativas disponibles. Sin embargo, la idoneidad para la administración oral o enteral puede variar ampliamente. En este trabajo no consideramos la vía rectal, como una vía enteral adecuada para la administración de inyectables.
Palabras clave: Inyecciones. Administración Oral. Vías de Administración de Medicamentos.
ABSTRACT
In this article we collect the ethical and legal principles when we have to decide on the use of a drug in conditions other than those on its data sheet. Medicines are not always available in formulations which are suitable for patients with swallowing difficulties or patients with enteral feeding tubes. The alteration of medication formulations may therefore be necessary. This text provides a list of injectables that can be administered orally or via enteral feeding tubes when there are no available alternatives. However, they vary widely in their suitability for oral or enteral feeding administration. In this paper we do not consider the rectal route, as an adequate enteral route for administration of injectables.
Key words: Injections. Administration, Oral. Drug Administration Routes.
La forma farmacéutica es la disposición individualizada del principio activo y sus excipientes. Estas formas farmacéuticas pueden ser sólidas, semisólidas, líquidas y gaseosas. A su vez los medicamentos tienen diferentes vías de administración, siendo la tecnología farmacéutica la encargada de adecuar la forma farmacéutica y la vía de administración. Pueden existir varias vías de administración para algunas formas farmacéuticas, aunque siempre será la ficha técnica del medicamento donde se recoge la forma farmacéutica y su vía de administración idónea.
En la práctica clínica nos surgen problemas en aquellos pacientes que tiene dificultad para tragar o que son portadores de una sonda nasogástrica, ya que la formulación sólida no es idónea para este tipo de pacientes y la líquida pudiera no estar aprobada para administrar por vía oral. En estos casos, la utilización de otra vía de administración diferente a la aprobada pudiera ser necesaria.
Cuando decidimos administrar una forma farmacéutica por una vía diferente a la de su aprobación, ésta queda fuera de la indicación recogida en la ficha técnica del medicamento. Desde este momento, el fabricante ya no es responsable de cualquier evento adverso o fracaso terapéutico que pudiera aparecer durante el tratamiento.
Esta modificación trae consigo implicaciones para los profesionales responsables de la prescripción, dispensación y administración de los medicamentos, ya que esta utilización del medicamento no está avalada, y por tanto será el profesional y no el laboratorio el responsable de cualquier evento adverso que el paciente pudiera experimentar1.
Aun cuando esté justificada la administración de un fármaco por una vía diferente a la que está autorizada en la ficha técnica, hay que respetar unos principios legales y éticos que van desde la autonomía, la justicia, el principio de beneficencia, el derecho a la intimidad y la vulnerabilidad y el nivel de dependencia que presentan los pacientes con dificultad para tragar2.
Además, debemos ser conscientes de que, por muy seguros que estemos de nuestra decisión, es posible que aparezcan reacciones inesperadas potencialmente graves, por lo que se requiere una vigilancia más estrecha por parte del personal sanitario.
Solo se podrá administrar un fármaco por una vía diferente a la autorizada cuando lo indique el médico responsable. No obstante, dicho procedimiento puede llevarse a cabo por el personal de enfermería, siempre que la orden sea transmitida de manera escrita.
El Real Decreto 1015/2009, de 19 de junio3, por el que se regula la disponibilidad de medicamentos en situaciones especiales recoge el acceso a medicamentos en condiciones diferentes a las autorizadas. En el artículo 13 se indica que esta utilización de medicamentos en condiciones diferentes a las autorizadas tendrá carácter excepcional y se limitará a las situaciones en las que se carezca de alternativas terapéuticas autorizadas para un determinado paciente, respetando en todo caso las restricciones que se hayan establecido ligadas a la prescripción o dispensación del medicamento y el protocolo terapéutico asistencial del centro sanitario. En el artículo 15 se recogen las obligaciones del médico responsable del tratamiento. Estas obligaciones son:
• Informar al paciente, en términos comprensibles, de la naturaleza del tratamiento, su importancia, implicaciones y riesgos, y obtener su consentimiento conforme a la Ley 41/2002, de 14 de noviembre.
• Notificar las sospechas de reacciones adversas de acuerdo a lo previsto en el Real Decreto 1344/2007, de 11 de octubre.
• Respetar en su caso las restricciones que se hayan establecido ligadas a la prescripción o dispensación y el protocolo terapéutico asistencial del centro sanitario.
Uno de los objetivos de la bioética4, en lo que respecta a la relación asistencial con el enfermo, cualquiera que sea su patología, será la búsqueda de soluciones concretas a casos clínicos concretos, siempre que se originen conflictos, lo cual ocurre con mucha frecuencia en la situación de enfermedad incapacitante o terminal. La bioética entrará en acción cuando aparezca la posibilidad de elegir entre varias opciones, que a veces podrán ser completamente contradictorias. Ante la falta de una certeza absoluta, el dilema consistirá en buscar la forma más adecuada para tomar la mejor decisión, es decir, cómo diferenciar lo correcto de lo incorrecto, lo que es bueno de lo que es malo o incluso cómo escoger la mejor opción entre varias opciones correctas.
La bioética entra en juego en situaciones especialmente delicadas como la sedación terminal, y aunque la administración de un medicamento por una vía diferente a la autorizada no es ni de lejos comparable, es positivo el hecho de que cada vez que un profesional se plantee la cuestión de cómo actuar en estos casos, reflexione, a ser posible en colaboración con el enfermo, su familia y el resto del equipo asistencial, sobre la actitud a tomar y se trate el problema de manera individualizada. Lo habitual es tener dudas en la toma de decisiones ante esta situación, por lo que la prudencia será la mejor consejera, y resultaría pretencioso creerse en posesión de la certeza absoluta.
Siempre deberemos tener en cuenta las condiciones del principio ético del doble efecto5,6. En este caso es difícil de llevar a la práctica, de modo que se puede utilizar de forma reducida e incorrecta, valorando únicamente la intención de la persona que realiza la acción. Se tiende a resolver la cuestión de la siguiente forma: "como la intención es buena, se puede realizar la acción" o "como la intención declarada es buena, se considera que la acción es correcta".
Existen unos preceptos legales y actuaciones reguladas relacionadas con estas intervenciones que los profesionales sanitarios debemos conocer:
• Ley 41/2002, de 14 de noviembre, reguladora de la autonomía del paciente y de derechos y obligaciones en materia de información y documentación clínica. Arts. 4, 5, 8 y 9.
• Información sobre la adopción de la medida: La autorización de la medida excepcional y urgente deberá ser comunicada al paciente de modo adecuado a sus posibilidades de comprensión y a las circunstancias existentes en el momento. También debe informarse a las personas que, vinculadas a él por razones familiares o de hecho, se encuentren acompañando al paciente. La información debe darse con carácter previo, durante el mantenimiento y posteriormente.
• Historia clínica y documentos del protocolo: Debe quedar constancia en la historia clínica de las circunstancias que han justificado tanto la adopción de esta medida como su mantenimiento en el tiempo
Para cada medicamento debemos elegir la forma farmacéutica adecuada y realizar una preparación y administración correcta para no obstruir la sonda, conseguir su efectividad, y evitar efectos adversos e interacciones.
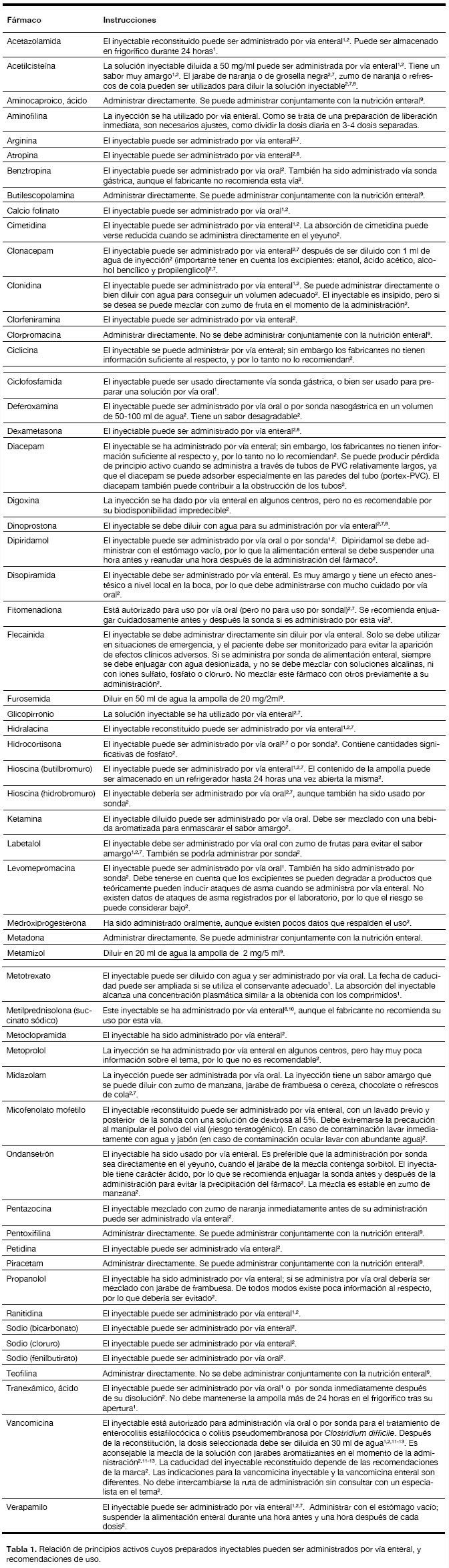
En la tabla 1 se recogen diferentes principios activos cuyos preparados inyectables se pueden administrar por vía oral o sonda gástrica, y las recomendaciones para su uso. Aunque la rectal es una vía de administración enteral y que proporciona una rápida absorción de los principios activos, no la hemos considerado en este texto debido a la complejidad que tiene la administración de fármacos que no han sido específicamente diseñados para esta vía.
Aspectos a tener en cuenta:
• Este texto no proporciona una lista completa de los inyectables que se puede administrar por vía enteral.
• La administración de inyectables por vía enteral por lo general da lugar a una práctica no autorizada. La responsabilidad legal de los profesionales de la salud no se considera en este documento.
• Este documento solo tiene en cuenta la administración enteral de los inyectables en los pacientes con dificultades para tragar o pacientes con sondas de alimentación enteral. Otras preparaciones, que pudieran ser más adecuadas, no se han considerado.
• Este documento proporciona información general sobre principios activos y por lo tanto, las diferencias entre las marcas no son consideradas.
• Este documento no tiene en cuenta las interacciones entre los fármacos y el material plástico de los tubos de nutrición enteral.
• La posible alteración de los perfiles farmacocinéticos cuando los medicamentos se administran en una forma no autorizada no ha sido considerada.
Por lo tanto, es importante tener en cuenta que cuando tengamos un paciente que requiere medicación oral y es portador de una sonda de alimentación gástrica o bien presenta dificultades para tragar, podemos considerar utilizar vías diferentes de las que el medicamento tiene autorizadas2. Únicamente, cuando no dispongamos de alternativas por vía oral, se administrarán estos medicamentos por una vía no autorizada en la ficha técnica.
Previamente a administrar los inyectables a través de las sondas de alimentación enteral o por vía oral debemos valorar su idoneidad, ya que la administración enteral presenta una amplia variabilidad inter e intraindividual1.
Para disminuir en lo posible esta variabilidad, debemos tener en cuenta distintos factores que pueden modificar la eficacia y seguridad del fármaco, como son: situación de la sonda, forma farmacéutica empleada o interacciones con la nutrición enteral y con el material de la sonda.
Bibliografía
1. White R, Bradnam V. Drug Administration via Enteral Feeding Tubes (Internet). Londres: Royal Pharmaceutical Society; 2011 (acceso 04/05/2011). Disponible en: http://www.medicinescomplete.com. [ Links ]
2. Smyth J. The NEWT Guidelines (Internet). North Wales: Betsi Cadwaladr University Local Health Board (East): 2013 (acceso 02/08/2013). Disponible en: http://www.newtguidelines.com/. [ Links ]
3. Real Decreto 1015/2009, de 19 de junio, por el que se regula la disponibilidad de medicamentos en situaciones especiales. Boletín Oficial del Estado, núm 174 (20/07/2009). [ Links ]
4. Azulay A. La sedación terminal. Aspectos éticos. An Med Interna 2003; 20 (12): 645-9. [ Links ]
5. Quill TE, Dresser R, Brock DW. The rule of double effect - a critique of its role in end-of-life decision making. N Eng J Med 1997; 337 (24): 1768-71. [ Links ]
6. Sulmasy DP, Pellegrino ED. The rule of double effect: clearing up the double talk. Arch Intern Med. 1999; 159 (6): 545-50. [ Links ]
7. Paediatric Formulary Committee. BNF for Children (Internet). Londres: BMJ Group, Pharmaceutical Press, and RCPCH Publications; 2013 (acceso 07/08/2013). Disponible en: http://www.medicinescomplete.com. [ Links ]
8. Martin J, editor. BNF for Children 2011-12 (Internet). Londres: British Medical Association, the Royal Pharmaceutical Society of Great Britain, the Royal College of Paediatrics and Child Health, and the Neonatal and Paediatric Pharmacists Group (acceso 16/09/2013). Disponible en: http://bnfc.org/bnfc/. [ Links ]
9. Guía de administración de fármacos por sonda. Versión 1.0, junio 2008. Servicio de Atención Farmacéutica Especializada de Badajoz. Gerencia del Área de Salud de Badajoz. [ Links ]
10. Antal EJ, Wright CE 3rd, Gillespie WR, Albert KS. Influence of route of administration on the pharmacokinetics of methylprednisolone. J Pharmacokinet Biopharm. 1983; 11 (6): 561-76. [ Links ]
11. Electronic Medicine Compendium (eMC). Summary of Product Characteristics - Vancomycin (Internet). Wockhardt UK Ltd. Date of last authorisation 20/05/2008 (acceso 13/05/2014). Disponible en: http://www.emc.medicines.org.uk. [ Links ]
12. Electronic Medicine Compendium (eMC). Summary of Product Characteristics - Vancomycin (Internet). Hospira UK Ltd. Date of revision of the text 30/01/2009 (acceso 13/05/2011). Disponible en: http://www.emc.medicines.org.uk. [ Links ]
13. Electronic Medicine Compendium (eMC). Summary of Product Characteristics - Vancocin (Internet). Flynn Pharma Ltd. Date of revision of the text 10/11/2008 (acceso 13/05/2011). Disponible en: http://www.emc.medicines.org.uk. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Francisco Tejada Cifuentes.
Farmacia de Atención Primaria.
Complejo Hospitalario Universitario de Albacete.
C/ Hermanos Falcó, 37.
C.P. 02006 - Albacete (España).
Correo electrónico: ftejada@sescam.jccm.es
Recibido el 26 de marzo de 2015.
Aceptado para su publicación el 2 de junio de 2015.