INTRODUCCIÓN
Las nutriciones parenterales (NPs) son mezclas estériles administradas por vía venosa central o periférica, indicada a prematuros, niños y adultos desnutridos o con riesgo de desnutrición secundaria a una patología1. Son consideradas como preparaciones magistrales y con un período de vigencia definido2.
El proceso de elaboración de estos productos es operador dependiente, realizándose de manera semi automatizada o manual, en ambos casos se realizan adiciones sucesivas de nutrientes con instrumentos no volumétricos como jeringas, por lo que la existencia de errores por exceso o defecto puede estar presente. Por otro lado posee una compleja composición química, ya que pueden contener más de 50 nutrientes (entre ellos agua, glucosa, aminoácidos, lípidos, vitaminas, electrolitos, minerales y elementos trazas)3, por lo tanto está presente el factor de inestabilidad dependiente de las interacciones químicas propias de los analitos que la componen. Uno de los eventos más relevante es la formación de precipitados calcio-fosfato4,5, también puede presentarse una variación de pH3, inestabilidad de los lípidos, generación de lipoperóxidos3,6,7,8,9, pérdida de la viscosidad de la glucosa5, perdida de actividad tampón de aminoácidos7. No debemos perder de vista que la calidad de la NP depende, además en gran medida del envase en el cual está contenida, es así como las bolsas multicapa disminuye alrededor de 100 veces el paso de oxígeno en relación a las bolsas de etilvinilacetato (EVA), disminuyendo de este modo los mecanismos de oxidación, asimismo el uso de una segunda bolsa fotoprotectora (color granate o anaranjado), así como set de infusión de estas características minimizan la degradación de los componentes por acción de la luz8,10,11. Otro factor externo que puede contribuir a la variabilidad de composición e inestabilidad química es el aporte de los diferentes excipientes de los productos farmacéuticos individualmente utilizados en la elaboración de NP12,13, así como la temperatura y tiempo de almacenamiento14.
La vigencia de cada NP también es un tema controversial, es así como la Sociedad Española de Nutrición Parenteral y Enteral (SENPE) y la Sociedad Española de Farmacia Hospitalaria (SEFH) otorgan una vigencia de hasta 4 días a la NP5 y la Sociedad Americana de Nutrición Enteral y Parenteral, ASPEN hasta 9 días15. Nosotros otorgamos una caducidad de 5 días contados desde el día de elaboración.
Los controles de calidad que actualmente se realizan a las NP son los siguientes:
Gravimétrico: control de pesada, se calcula por diferencia de peso esperado de NP total versus peso real de la mezcla. Se considera aceptable una diferencia de ± 3 a 5%. Este control refleja errores en la adición o defecto de grandes volúmenes5.
Visual: consiste en observar la bolsa de NP por el operador, donde es posible detectar alteraciones de la coloración, separación de fases, formación de precipitados, presencia de partículas o filtración del envase5.
Control microbiológico: cultivo de una muestra representativa de NP, mediante el cual es posible detectar contaminación microbiológica solo al momento de la preparación16.
Debido a la importancia e implicancia que tiene para el paciente poder contar con un producto con altos estándares de calidad y seguridad, asimismo tomando en consideración las falencias que pueden existir en relación a los controles de preparación y almacenamiento de la NP, consideramos que los controles realizados actualmente son insuficientes para asegurar que el contenido de la NP es el que corresponde a la prescripción médica, además es necesario asegurar la esterilidad microbiológica al momento de la preparación así como en el período de vigencia asignado al preparado, por lo cual nos propusimos implementar y estandarizar un control de calidad químico cuantitativo y microbiológico de la NP, realizado al momento de la elaboración (control de proceso) y el último día de establecida la caducidad de la NP (control de estabilidad química), adicional a los sugeridos por la actual legislación vigente, los cuales no dan cuenta del comportamiento químico de la mezcla durante los días de vigencia, esterilidad de la mezcla, comportamiento de los nutrientes o su degradación en el tiempo.
MATERIALES Y MÉTODOS
Selección de la muestra
Se realizó una selección aleatoria de muestras de NP durante un período comprendido entre agosto del 2015 a enero del 2016. Se analizaron 40 muestras de NP, en día 0 (día de la elaboración) y a los 5 días, para evaluar proceso de elaboración y estabilidad respectivamente.
Preparación de NP
El proceso de elaboración de NP se inicia con la prescripción de la receta médica. Para elaborar las NP se utiliza equipo Dosibag® que adiciona automáticamente glucosa, lípidos, agua y aminoácidos, posteriormente se adicionan de manera manual los componentes de menor volumen como electrolitos, vitaminas, minerales y elementos trazas. Una vez terminada la NP se realiza un control gravimétrico y visual.
Cálculo de error gravimétrico
Se calculó el promedio del error gravimétrico de cada una de las NP incluidas en el estudio a través de la siguiente fórmula:
Dónde: Peso medido = Peso real de la NP luego de su preparación; Peso esperado = Peso teórico de la NP, calculado en base a las densidades de cada nutriente que compone la NP.
Implementación de control de calidad químico
La muestra inmediatamente posterior a la preparación (control químico de preparación) y por 5 días (control químico de estabilidad). La primera y segunda muestra se analizó el día cero y cinco, respectivamente, de los analitos o nutrientes magnesio (Mg), calcio (Ca), fósforo (P), glucosa (Glu), sodio (Na), potasio (K) y cloro (Cl) en equipo Vitros® 4600 de Johnson & Johnson y Cobas® B221 de Roche. Previo a la medición se calculó la concentración teórica de cada uno de ellos (calculado en base a la indicación médica), esto para realizar las diluciones correspondientes en relación a la sensibilidad de los equipos.
Para establecer las concentraciones de cada uno de los analitos, se estableció la concentración teórica como referencia comparándose ésta con el valor obtenido en el día de la preparación (día 0) y día 5 post preparación.
La metodología utilizada para detección de contaminación microbiológica de NP ya ha sido utilizada16, consiste en filtrar 50 ml de la NP a través de un filtro de nitrato de celulosa (tamaño de poro 0,45 um), el cual es cultivado en medio agar sangre en estufa de cultivo a 37°C por 48 horas, posteriormente el cultivo completa los 7 días a 20°C en una atmósfera aeróbica durante 5 días, el resultado final del cultivo se expresa a los 7 días, como positivo o negativo expresado en unidad de formadora de colonia (ufc), el resultado es negativo si el valor es cero y positivo en caso de mayor a 1ufc, en caso de posibilidad de la muestra se realiza identificación del microorganismo encontrado. Posterior a la preparación de la NP se selecciona una alícuota para realizar el control microbiológico día cero, una segunda muestra refrigerada entre 4 y 8ºC la cual se cultiva el día 5 y una tercera muestra que se almacena de contramuestra, la cual se cultiva solo en caso de positividad de la muestra día cero.
Análisis de los datos
Control de calidad químico
Se cuantificó la concentración de 7 nutrientes (Mg, Ca, P, Glu, Na, K, Cl) en 40 muestras diferentes durante el día de elaboración (día 0) y 5 días después (día 5). A los datos obtenidos, se aplicó el Test de Grubbs para eliminar valores aberrantes (outliers). Se utilizó el método de regresión de Passing y Bablok para comparar la concentración de referencia versus el control.
Para analizar la influencia de los componentes entre sí, se utilizó una prueba de comparación de medias relacionadas, considerando un 5% de error y un 95% de nivel de confianza. Un p<0,05 determinó si hay influencia de un analito sobre otro.
RESULTADOS
Error gravimétrico
Para las 40 NP incluidas en el estudio se obtuvo un promedio de error gravimétrico de 2,3%, todas dentro del rango de aceptabilidad.
Control de calidad analítico
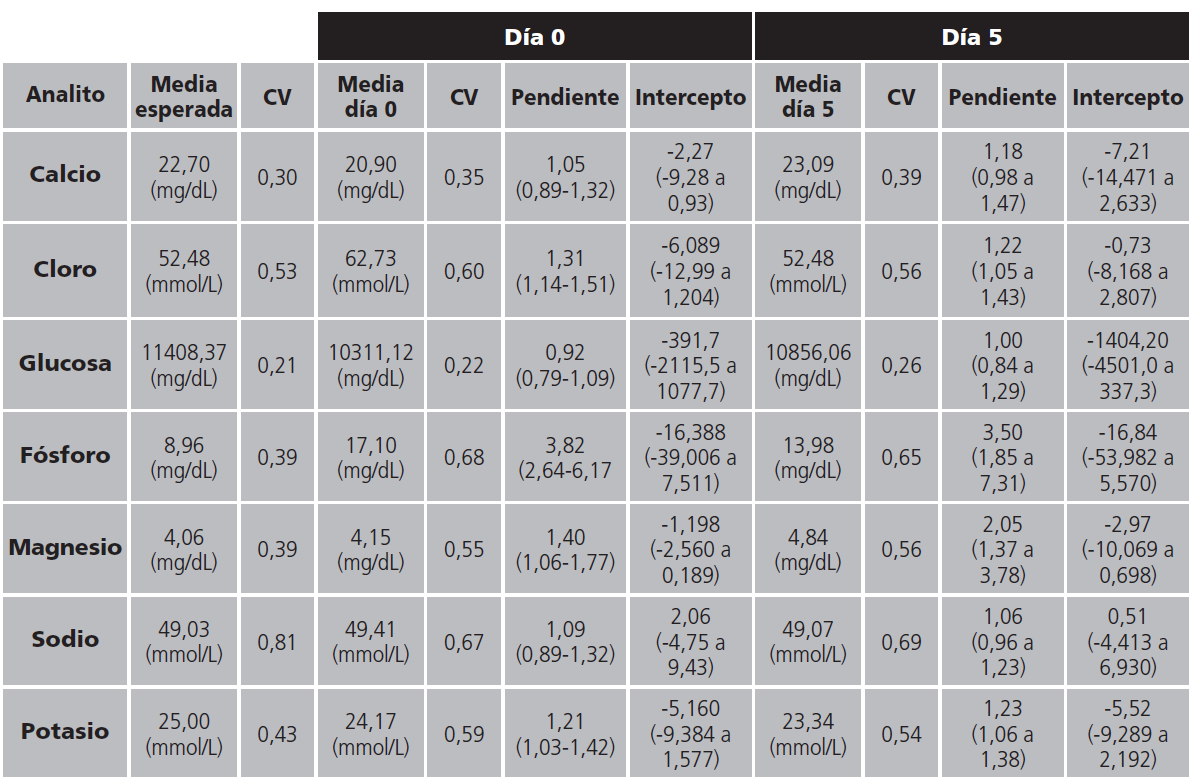
La tabla 1 muestra las medias de concentración esperada y concentración medida para cada analito durante día 0 y día 5, según regresión Passing-Bablok.
De acuerdo a las regresiones de Passing-Bablok, existe concordancia, el intervalo de confianza (IC) de la pendiente debe contener el valor 1 y el IC del intercepto el valor 0. De acuerdo a lo mostrado en la tabla 1, para las concentraciones medidas y esperadas para días 0 y 5, se observa lo siguiente:
Tabla 1. Medias de concentraciones esperadas y medidas para cada analito durante día 0 y día 5, según regresión Passing-Bablok
- K, Cl, P, Mg: no hay concordancia para mediciones en día 0 y 5 entre los valores del control versus la referencia.
- Ca, Glu: solo existe concordancia para mediciones de día 0 entre los valores del control versus la referencia y no para el día 5. Estos resultados nos indican que estos analitos cumplen las características para ser marcadores de elaboración pero no de estabilidad.
- Na: existe concordancia para mediciones de día 0 y 5 entre el valor del control versus la referencia, cumpliendo de este modo con la características de ser un buen marcador de elaboración y de estabilidad.
Al observar los valores p en las tablas 2 y 3, se puede ver que la única asociación que se repite en ambos días, es la de Ca y P, información relevante cuando se analiza la calidad de estas mezclas nutricionales, ya que la formación de precipitados Ca-P es uno de los puntos críticos y potencial factor de inestabilidad dentro de la NP.
Control de calidad microbiológico
Las 40 muestras analizadas en donde fue realizado control microbiológico no se observó crecimiento microbiano a tiempo cero, ni a los 5 días de almacenadas. Según procedimiento interno no fue necesario cultivar la contramuestra, ya que solo se cultivan en caso de posibilidad de la muestra.
Discusión
La utilización de controles de calidad cuantitativos, como los propuestos en el presente trabajo, realizados al producto terminado son una herramienta complementaria a los controles convencionales tales como medición de pH y control visual cuya información no es utilizada al momento de tomar la decisión de no aceptación de la NP para ser administrada en el paciente, esto debido a la subjetividad del resultado, a su vez el control gravimétrico, si bien es un control cuantitativo en sí, solo es posible detectar cambios solo al haber errores sobre la adición de macronutrientes tales como glucosa, aminoácidos, lípidos y agua, esto es un riesgo debido a que una NP se elabora por adición de diferentes volúmenes. Nuestros resultados indican que nuestra muestra se encuentra dentro del rango de aceptabilidad (promedio de 2,3%), sin embargo este control posee la debilidad de no poder detectar la adición de micronutrientes (agregados en pequeños volúmenes), que tienen la característica además de poseer estrecho margen terapéutico, que pueden ser potencialmente dañinos para el paciente si se adicionan en exceso o definitivamente no se adicionan como el potasio17. Teniendo en cuenta que la NP es un preparado magistral, la facultad de poder cuantificar estos micronutrientes es poder detectar si se encuentra dentro del rango de aceptabilidad, de manera de poder aceptar o desechar la NP previo a la infusión al paciente, independiente del origen del error sea este por exceso, por defecto o por omisión en la adición de ellos durante la etapa de elaboración, independiente de cual sea.
Algunos autores señalan la importancia de realizar mediciones cuantitativas de los componentes, con el objeto de establecerlo como un control de calidad, tal es el caso como la cuantificación de vitaminas como la tiamina, realizada por cromatografía de gases18. A pesar de la importancia de sugerir la realización de estos controles de calidad no se señala la metodología recomendada para medir los diferentes componentes, esto debido a que en la aplicación práctica el hecho de medir la totalidad de los componentes es inaplicable, además las metodología analíticas para medir cada una de ellos son muy diversas, lo cual encarecería el costo de cada NP, de ahí la importancia de poder seleccionar algunos que sean utilizados como marcadores seleccionados tomando en cuenta la implicancia para el paciente.
Considerando que el objetivo de este trabajo es implementar controles de calidad complementarios a los descritos en la literatura, utilizando las plataformas analíticas disponibles en la mayoría de los centros asistenciales como son los equipos de laboratorio, se debe realizar a través de la comparación de las concentraciones de cada uno de los analitos seleccionados, con la concentración referencial. En relación a los electrolitos, nuestro estudio incluyó la cuantificación de electrolitos y nutrientes tales como Ca, Na y glucosa, para los cuales se obtuvieron concentraciones concordantes con la referencia para la medición del día cero, cumpliendo con las características para ser considerados como controles de calidad de elaboración, lo cual coincide además con lo reportado por otros autores, los cuales indican la importancia de medir estos nutrientes (analitos) que se encuentran en estrecho margen terapéutico en la NP con fines de control de calidad3. Previamente es necesario hacer un análisis del tipo de analito y concentración esperada, además de considerar los coeficientes de variación (CV) esperados para cada uno de ellos. Una de las limitaciones de este estudio fue no estimar el efecto matriz previo a las mediciones de estos analitos a fin de comprobar empíricamente la influencia de las preparaciones y sus componentes en la determinación de cada analito, cosa que podría plantearse a futuro con un estudio de mayor envergadura con un mayor número de muestras. Nuestros resultados entregan datos preliminares, concretos y objetivos que permiten implementar un sistema de control químico de las NP, utilizando la metodología disponible en laboratorio clínico, cuyo uso está obviamente destinado a análisis de muestras biológicas, sin embargo considerando técnicamente es posible extrapolar a estos casos, logrando medir la concentración de analitos marcadores de control de proceso de elaboración, lo cual constituye un aporte que permite, entre otras cosas, asegurar la calidad de la elaboración de la NP, transformándose en una práctica innovadora asegurando de esta manera la calidad de estos preparados magistrales estériles que se deben administrar al paciente, similares resultados han sido descritos últimamente19.
Además de las pruebas analíticas, se realizó un control de calidad microbiológico, para evaluar y documentar la esterilidad de los procesos implicados en la elaboración de las NP y la ausencia de crecimiento bacteriano o de hongos en estas muestras. En ninguna de ellas hubo crecimiento microbiológico al cultivar las muestras según la técnica descrita, tanto en los cultivos realizados a tiempo cero y 5 días post almacenamiento. Es necesario aclarar que no existe ningún tipo de control microbiológico que podamos conocer su resultado previo a la administración del paciente, ya que el cultivo tarda 7 días, por lo tanto necesariamente los resultados deberán evaluarse en forma conjunta con el comportamiento clínico del paciente.
CONCLUSIÓN
Se logró demostrar empíricamente que se pueden realizar mediciones cuantitativas de algunos analitos que componen una NP utilizando plataformas analíticas de uso rutinario en el laboratorio clínico, lo que representa una ventaja significativa al actual sistema de control de calidad de elaboración.
Fue posible definir sodio, calcio y glucosa como marcadores de elaboración de las NP y los analitos medidos en las mezclas se mantienen estables en el tiempo sin una mayor degradación, ya que son sales estables y se pudieron cuantificar. Se determinó que luego de 5 días de almacenadas las NP, refrigeradas entre 2 y 5°C y sin exposición directa a la luz solar se mantienen estables desde el punto de vista físico químico.
Sin duda, creemos que este estudio representa un avance en pro de poder mejorar la calidad y seguridad de las NP administradas a nuestros niños.
Desde el punto de vista microbiológico la caducidad está dada por la esterilidad del preparado a los 5 días, sumado a que los contenedores e infusores que utilizamos (bolsas multicapa que disminuye el paso de oxígeno y colores anaranjados) en la elaboración de la NP.
Financiamiento: La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Agradecimientos: Al Hospital Doctor Luis Calvo Mackenna por permitir la realización del presente trabajo.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.