INTRODUCCIÓN
El estatus epiléptico (EE) es una emergencia médica que se define como una crisis epiléptica prolongada, de 5-30 minutos de duración, o una serie de crisis entre las que se no recobra plenamente el nivel de conciencia1. Su desarrollo característico consta de una primera fase con un incremento de la actividad simpática, seguida de una segunda fase de descompensación que cursa con lactacidemia, diminución del flujo cerebral, hipoglucemia, hipoxia y necrosis neuronal2.
El tratamiento de primera línea se realiza con una benzodiacepina intravenosa (IV) a la que se añaden uno o varios anticomiciales como levetiracetam, ácido valproico o fenitoína, administrados vía IV y con una primera dosis de impregnación para alcanzar el estado estacionario lo antes posible1,3. En casos donde la clínica persiste más de 60 minutos pese a recibir tratamiento anticomicial adecuado, el EE se clasifica como refractario y está indicada la inducción de un coma barbitúrico con tiopental o pentobarbital en bomba de infusión continua (BIC)1. El objetivo es parar las crisis a nivel clínico y conseguir un electroencefalograma sin actividad para disminuir el daño neuronal1,3. Si el EE persiste más de 24h o recurre en caso de disminución de la anestesia, se clasifica como EE superrefractario, cuyo manejo terapéutico consiste en mantener el coma barbitúrico y utilizar antiepilépticos de segunda línea como lacosamida, topiramato o perampanel.
DESCRIPCIÓN DEL CASO
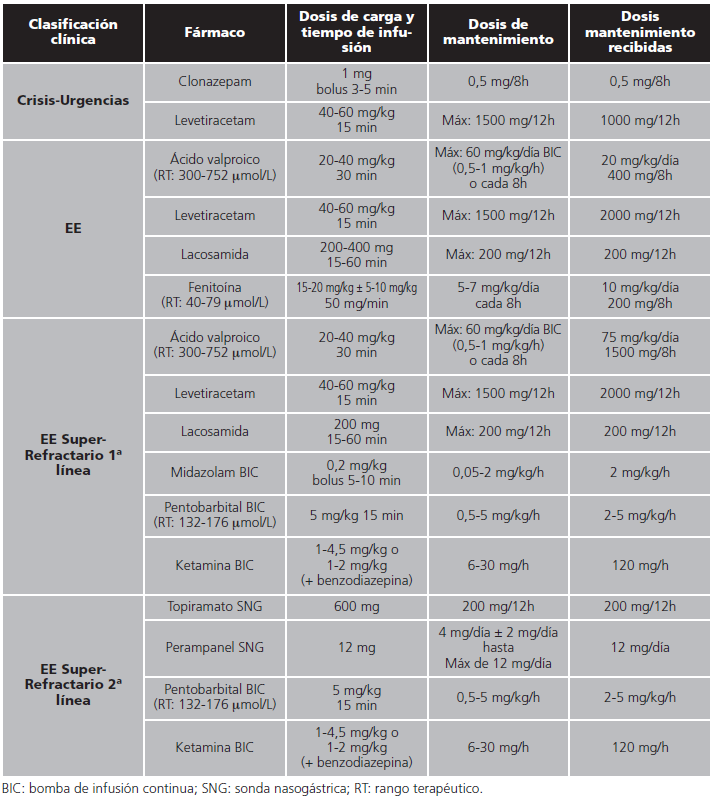
El caso trata de un varón de 28 años natural de Arabia Saudí que fue traído a urgencias por una crisis comicial, siendo tratada con clonazepam y levetiracetam IV. No constaban crisis epilépticas claras entre los antecedentes pero sí cuadros encefalopáticos en contexto de síndromes febriles. Dada la falta de respuesta al tratamiento, se valoró como EE y se trasladó a la UCI, iniciándose ácido valproico, levetiracetam, lacosamida y fenitoína IV. Las pautas de estos fármacos y los que a continuación se comentan se detallan en la tabla 1.
Desde el Servicio de Farmacia seguimos y monitorizamos el valproico y la fenitoína, realizando las recomendaciones necesarias para mantener sus concentraciones plasmáticas dentro del rango terapéutico, 300-752 μmol/L para el ácido valproico4 y 40-79 μmol/L para la fenitoína5. También valoramos interacciones farmacológicas, observando una disminución de las concentraciones de valproico debido al efecto inductor de la fenitoína y a posibles interacciones por desplazamiento, atribuible a que ambos fármacos presentan una elevada unión a proteínas plasmáticas.
Dada la persistencia clínica se clasificó como EE superrefractario, se mantuvo tratamiento con valproato, levetiracetam y lacosamida, se inició midazolam en BIC y se indujo un coma barbitúrico con pentobarbital en BIC. Finalmente se añadió también una BIC de ketamina para suprimir la actividad eléctrica. Se realizaron niveles de ácido valproico y pentobarbital, con niveles objetivo para el segundo de 132-176 μmol/L6, observándose una disminución de las concentraciones de valproico debido a la inducción farmacológica del barbitúrico.
Por indicación de Neurología, se sustituyeron los antiepilépticos clásicos por unos de segunda línea, iniciándose topiramato y perampanel por sonda nasogástrica (SNG), y se mantuvo el coma barbitúrico con pentobarbital y ketamina. Desde el Servicio de Farmacia se revisó la información disponible sobre la administración por SNG de ambos fármacos7.
Tanto las crisis como la actividad eléctrica reaparecían al disminuir las perfusiones. Los intensivistas valoraron la posibilidad de que se tratase de un paciente metabolizador rápido y plantearon la opción de realizar un estudio genético. El Servicio de Farmacia revisó el metabolismo y eliminación de todos los fármacos utilizados y tras constatar que las enzimas metabolizadoras involucradas eran variadas y que varios antiepilépticos se eliminaban mayoritariamente por vía urinaria, se descartó que la superrefractariedad del paciente se debiera a un metabolismo acelerado.
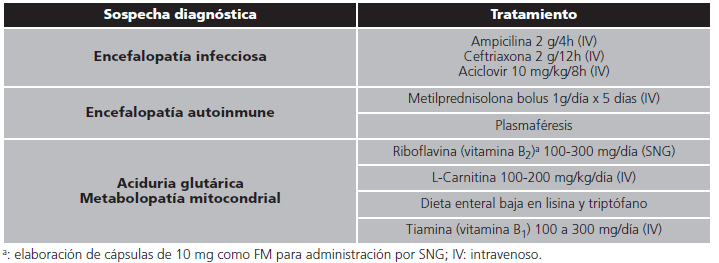
Paralelamente al control de las crisis, se realizaron varias pruebas para intentar filiar el origen del EE, valorándose como posibles etiologías una encefalopatía infecciosa o autoinmune, una aciduria glutárica o una metabolopatía con afectación mitocondrial. A la espera de los resultados de dichas pruebas, y dada la persistencia del cuadro clínico, se iniciaron los correspondientes tratamientos empíricos (tabla 2). El paciente no respondió a ningún tratamiento y los resultados de las pruebas diagnósticas no fueron concluyentes.
Ante la superrefractariedad del cuadro y el desconocimiento etiológico, se hizo una búsqueda bibliográfica que condujo a una sospecha diagnóstica de Síndrome de ganglios basales con respuesta a biotina y tiamina. Esta enfermedad, de herencia autosómica recesiva, se debe a una mutación del gen SLC19A3, que codifica para un transportador de tiamina. La mutación genera un cambio de aminoácido, dando lugar a una alteración en la funcionalidad del transportador. La mayoría de casos se han descrito en población saudí, con consanguineidad y que debutaron durante la infancia con algún episodio febril8.
El tratamiento consiste en suplementar, a dosis altas, con tiamina 20 mg/kg/día, por el déficit existente debido a la disfuncionalidad del transportador, y biotina 10 mg/kg/día, por estudios que muestran que niveles bajos ocasionan una menor expresión del transportador8,9. Por ello, se decidió añadir biotina a dosis de 10 mg/kg/día (600 mg/día) y contactar con el Servicio de Genética para realizar el estudio de la mutación. Dado que las referencias bibliográficas no especificaban vías ni formas de administración, se consensuó la elaboración de cápsulas de biotina de 600 mg para administración por SNG. El paciente tampoco respondió al tratamiento, los resultados del estudio genético fueron negativos y finalmente fue trasladado a su país, en situación de EE, por petición familiar.
DISCUSIÓN
El tratamiento del EE es complejo y requiere el uso de varios fármacos. La individualización del tratamiento y la adecuación de formas farmacéuticas según las necesidades y características del paciente son parte importante de la labor del farmacéutico. Además, nuestra figura también contribuye al abordaje global del paciente con el seguimiento y monitorización farmacocinética de tratamientos anticomiciales, para garantizar la efectividad y disminuir la aparición de efectos adversos. El estudio de interacciones entre los fármacos implicados también es de gran interés clínico.
Por otro lado, la colaboración entre profesionales de la salud de distintas especialidades siempre es enriquecedora, y la realización de estudios genéticos puede ser de gran utilidad tanto como herramienta diagnóstica como en la optimización del tratamiento.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses.