INTRODUCCIÓN
El dolor se define como una experiencia sensitiva y emocional desagradable ocasionada por una lesión tisular real o potencial según la International Asociation for Study of Pain (IASP)1,2.
Los neonatos tienen un umbral de percepción bajo y una capacidad de nocicepción intensa y difusa en el espacio derivada del desequilibrio entre el desarrollo de los receptores y vías de transmisión y procesamiento del dolor y la inmadurez de los mecanismos inhibitorios. Este desequilibrio genera que el neonato puede presentar respuestas fisiológicas y hormonales exageradas frente a un estímulo doloroso aunque sean de baja intensidad, en comparación con niños de mayor edad o adultos3-5. Experimenta a corto plazo inestabilidad clínica, caracterizada por aumento de la frecuencia cardiaca, frecuencia respiratoria y presión arterial y descenso de la saturación de oxígeno, así como con una respuesta endocrina alterada (aumento del catabolismo y de la secreción de cortisol, glucagón y catecolaminas) y complicaciones como la hemorragia intraventricular. Además varios estudios demostraron que el dolor en edades tan tempranas pueden conllevar cambios permanentes en el procesamiento del dolor, muerte neuronal y alteraciones neuroendocrinas, y fundamentalmente del neurodesarrollo generando dificultades en el aprendizaje y cambios de comportamiento tanto sociales como emotivos, como consecuencias a largo plazo del dolor en neonatos6,7. Además, los procedimientos dolorosos tienen una influencia negativa en el sueño, disminuyendo los periodos de sueño y aumentando los estados de vigilia y estrés1,5.
Los recién nacidos que precisan hospitalización, especialmente aquellos hospitalizados en la Unidad de Cuidados Intensivos de Neonatos (UCINN) se encuentran sometidos a múltiples manipulaciones y procedimientos que pueden producir dolor, estrés y alteración de la vigilia. Concretamente, los recién nacidos de la UCINN experimentan entre 14-16 procedimientos dolorosos al día, la mayoría de los cuales se realizan sin medidas eficaces de control del dolor y sólo el 20,3% reciben tratamiento analgésico específico1,8. Entre estos procedimientos dolorosos se encuentran la aspiración de secreciones, la venopunción, la punción del talón, el cambio de apósitos adhesivos, inserción de catéter central, intubación endotraqueal…5,7,8.
Por todo esto, es fundamental realizar una adecuada evaluación, prevención y un correcto tratamiento del dolor.
En cuanto a la evaluación del dolor, debe hacerse con herramientas validadas y adecuadas, escalas, que tengan en cuenta la patología, la edad gestacional (EG) y que puedan ser incorporadas a la práctica clínica diaria.
Existen medidas ambientales fundamentales dirigidas a disminuir el estrés así como diversas medidas conductuales entre las que destacan las soluciones edulcoradas, el método madre canguro, la succión no nutritiva, lactancia materna, Swaddling3,4,8. En relación a las soluciones edulcoradas: consiste en la administración de sacarosa o glucosa vía oral a través de una jeringa o chupete, minutos antes de la intervención dolorosa y durante la misma.
El tratamiento no farmacológico tiene como objetivo reducir el dolor, y ha demostrado ser eficaz para prevenir y aliviar el dolor asociado a procedimientos sistemáticos en los cuidados del recién nacido hospitalizado, incluyendo aquellos dirigidos a disminuir el número de estímulos nociceptivos a los que están expuestos los neonatos mediante medidas preventivas, disminuir el estrés ambiental con medidas ambientales y modular la percepción del dolor a través de medidas conductuales. Todo esto con el fin de incrementar la comodidad y la estabilidad del neonato, así como reducir el grado de estrés. Estas intervenciones no farmacológicas han sido recomendadas por el International Evidence-based Group of Neonatal Pain y ofrecen la ventaja de que carecen de efectos adversos y son eficaces a corto plazo. Además, su eficacia es mayor si se combinan varias medidas no farmacológicas3,4.
La administración de sacarosa es la medida no farmacológica más utilizada y estudiada para el tratamiento del dolor en neonatos a término y en prematuros. Existe evidencia de que su uso disminuye la puntuación del dolor, la duración total del llanto, disminuye la respuesta fisiológica al dolor y las expresiones faciales de dolor9.
El objetivo del estudio es revisar la evidencia disponible sobre la eficacia y la seguridad de la sacarosa oral como tratamiento no farmacológico del dolor en neonatos durante los procedimientos dolorosos más frecuentes que se realizan a los neonatos en la UCINN de un hospital terciario.
MATERIAL Y MÉTODOS
El estudio presente consistió en una revisión bibliográfica. La búsqueda bibliográfica de la evidencia sobre la efectividad y seguridad de sacarosa oral en la literatura científica se realizó en las bases de datos de PUBMED y Cochrane Library.
En PUBMED, la búsqueda bibliográfica realizada se basó en términos MESH con la siguiente estructura: ("Infant, Newborn" [Mesh]) AND "Sucrose" [Mesh]) AND "Pain/therapy" [Mesh]. En Cochrane Library la búsqueda se realizó con los siguientes términos PICO: Sucrose (intervention) AND pain (outcome) AND term infant (population).
De los resultados obtenidos en la búsqueda bibliográfica, se seleccionaron ensayos clínicos (EC), metaanálisis y revisiones sistemáticas, al ser los estudios que mayor evidencia científica aportan, publicados en los últimos 10 años (2010 y 2020) con el fin de conocer la evidencia más reciente sobre la sacarosa oral en neonatos. En el término neonatos se engloban prematuros (<36 semanas de edad gestacional), recién nacidos a término (37-42 semanas) y lactantes.
Se incluyeron todos aquellos artículos cuyo procedimiento doloroso consistía en punción del talón, venopunción o extracción de sangre capilar/arterial, inyección intramuscular o vacunación y colocación de sonda o catéter. Se excluyeron de la revisión aquellos artículos donde se combinó o comparó la administración de sacarosa oral con medidas ambientales, con tratamiento farmacológico tópico como analgesia o con glucosa, debido a que en la práctica clínica habitual de nuestro hospital no se llevan a cabo este tipo de combinaciones. También se excluyeron los estudios que no incluían que no eran realizados en neonatos o que no incluían sacarosa como tratamiento no farmacológico. Todos los artículos que resultaron de interés en la selección realizada se revisaron manualmente y se recogió la siguiente información: autor, año de publicación y país en el que se realizó el estudio, tipo de estudio, población incluida en el estudio detallando el número de pacientes del mismo, brazos de tratamiento y resultados de eficacia.
En los brazos de tratamiento, concretamente, en el brazo de sacarosa se detalló concentración de sacarosa y dosis en ml que recibieron los pacientes del estudio.
En cuanto a los resultados de eficacia, se detalló cómo evaluaron el dolor, detallando las escalas del dolor utilizadas en cada estudio siempre que fuese posible y el valor de P del estudio estadístico si se realizó en los ensayos.
RESULTADOS
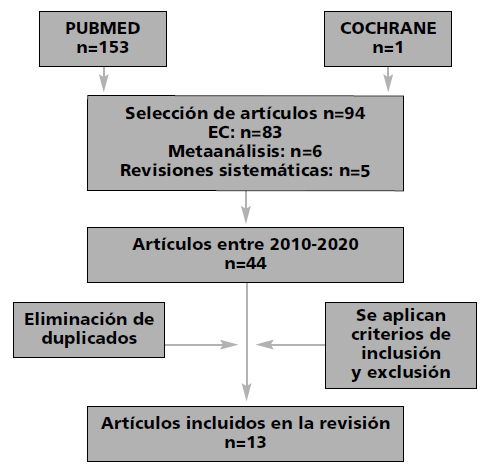
En la revisión realizada inicialmente había 154 artículos y, tras aplicar la selección de EC, metaanálisis y revisiones sistemáticas, además de eliminar duplicados y aplicar los criterios de inclusión, finalmente se revisaron 13 artículos publicados en los últimos 10 años. De estos 13 artículos, destacar que 11 eran ensayos clínicos, 1 revisión sistemática y 1 metaanálisis.
En la figura 1 se detalla el diagrama de flujo de los criterios de selección de los artículos incluidos en la revisión realizada.
Eficacia
Las características y los resultados de los EC en los que se evaluó la eficacia de la sacarosa oral como tratamiento no farmacológico del dolor en neonatos hospitalizados se detallan en la tabla 1.
La combinación de distintos tratamientos no farmacológicos para el dolor neonatal es una práctica habitual ya que existe evidencia de que la combinación tiene un efecto sinérgico para reducir el dolor en los neonatos5,7,8,10. Los artículos (EC y metaanálisis) en los que se estudió la eficacia de la combinación de tratamientos no farmacológicos se muestran en la tabla 2.
Tabla 2. Artículos que evalúan la eficacia de la administración de sacarosa oral en combinación con otros tratamientos no farmacológicos.

DM: diferencia de medias; IC: intervalo de confianza
1SNN: succión no nutritiva: estimulación del reflejo de succión a través de chupetes, dedo o pezón no lactante, en combinación o no con soluciones edulcoradas
2En los EC incluidos en el metaanálisis tanto la concentración como la dosis de sacarosa eran diferentes (24% 0,5 ml/kg o 0,1 ml o 0,2 ml, 33% 1 ml, 30% 2ml)
3SS: swaddling: consiste en envolver al recién nacido en mantas generando una presión y abrigo que asemejan el vientre materno y con esto se logra un efecto relajante prolongando el periodo de sueño.
Al analizar los artículos seleccionados y expuestos en la tabla 1 y 2, en cuanto a la población de los estudios observamos que en 4 de ellos la población diana eran RN prematuros y en 6 recién nacidos a término. En cambio, en el metaanálisis de Liu et al.7, la población era tanto recién nacidos a término como recién nacidos prematuros.
La dosis de sacarosa que recibieron los recién nacidos era diferente según el estudio. En 7 estudios, la dosis de sacarosa que recibían los pacientes era fija, en cambio en 1 ensayo la dosis que recibían dependía de la edad gestacional y en 2 ensayos la dosificación era según el peso de los neonatos. En el metaanálisis de Liu et al.7 no se detalla ni concentración de sacarosa que reciben ni la concentración de la misma. Respecto a la concentración de sacarosa, también existe variabilidad en los estudios al igual que vemos con la dosis, aunque la mayoría de los estudios, concretamente en 7, la concentración de sacarosa era del 24% pero en 3 estudios la concentración es distinta, 20%, 25% y 30%, respectivamente.
Las escalas para valorar el dolor en los neonatos y los indicadores para evaluar la respuesta al dolor coinciden en varios estudios. En 5 ensayos se utilizó la escala Neonatal Facil Coding System, en 3 la escala Premature Infant Pain Profile (PIPP) y en 2 Neonatal Infant Pain Scale (NIPS). Como indicadores, observamos que es frecuente el uso de frecuencia cardiaca, tiempo de llanto y saturación de oxígeno ya que la frecuencia cardiaca estaba presente en 6 ensayos, el tiempo de llanto en 5 y la saturación de oxígeno en 5. Destacar que, en los ensayos se utilizaban varios indicadores para evaluar la respuesta al dolor.
Los procedimientos dolorosos más estudiados son tanto la venopunción como la punción del talón, presente en 3 ensayos cada uno.
En la revisión de la Cochrane realizada por Stevens et al.9 en 2016, se incluyeron 74 estudios, 38 de los cuales examinaron el dolor asociado a la punción del talón. Esta revisión incluye 7.049 neonatos, la mayoría de los estudios con un tamaño de muestra comprendido entre 15-671 neonatos, y 48 estudios con menos de 100 neonatos incluidos en cada estudio. Los resultados de estos estudios proporcionaron más evidencia para apoyar la efectividad de la sacarosa. Los estudios incluidos en esta revisión informaron sobre el uso de sacarosa para venopunción, inyección intramuscular, punción arterial, inyecciones subcutáneas, inserción de sonda nasogástrica u orogástrica, cateterismo vesical en neonatos hospitalizados. Sin embargo, a excepción de la venopunción, punción del talón y la inyección intramuscular, para las cuales hubo evidencia de alta calidad para el uso de sacarosa en el tratamiento del dolor, en el resto hay estudios donde la evidencia es contradictoria. Hay que destacar que la sacarosa reduce el dolor de procedimientos menores con mínimos o ningún efecto adverso reportado. Pequeñas dosis de sacarosa al 24% (0,01-0,02 g) son efectivas en neonatos prematuros, mientras que dosis mayores (0,24-0,50 g) reducen la proporción de tiempo de llanto de los neonatos a término. Por otro lado, hay evidencia de calidad moderada de que la sacarosa en combinación con otros tratamientos no farmacológicos como la succión no nutritiva es más eficaz que la sacarosa en monoterapia. Es cierto que, es necesario evaluar la dosis óptima de sacarosa ya que aún no se ha establecido.
Como conclusión de esta última actualización de la revisión sistemática de la Cochrane, se sigue recomendando el uso de sacarosa debido a su efectividad en la reducción del dolor en la punción del talón, la inyección intramuscular y la venopunción en recién nacidos pretérmino o a término. Además destacar que el uso de sacarosa comparado con agua estéril reduce las puntuaciones totales de la escala NIPS (Neonatal Infant Pain Scales) de valoración del dolor durante la punción9,11.
Seguridad
La seguridad de la sacarosa oral en ninguno de los EC detallados en las tablas 1 y 2 fue el objetivo primario, y en ninguno de ellos se notificó ningún efecto adverso relacionado con su uso, considerándose un tratamiento seguro en neonatos.
En un ensayo clínico aleatorizado y controlado con placebo, realizado por Banga et al.12 en la unidad de UCINN de un hospital de tercer nivel, se comparaba el uso de sacarosa 24% (0,5 ml) con placebo (agua destilada) durante procedimientos dolorosos repetidos realizados en la práctica habitual de dicha unidad con el fin de evaluar su seguridad como objetivo principal del estudio. En este ensayo, se incluyeron 93 neonatos prematuros con una edad gestacional comprendida entre 32-37 semanas y concluyeron que el uso de analgesia de sacarosa oral en comparación con el agua destilada como placebo, no produce alteraciones de la conducta cerebral ni estados de conducta deficientes en recién nacidos prematuros cuando se evalúa mediante NAPI (Neurobehavioral Assesment of Preterm Infant) a las 40 semanas de edad gestacional. Por lo tanto, afirman que el uso de sacarosa en procedimientos dolorosos durante 7 días parece libre de efectos adversos inmediatos y a largo plazo.
En esta última revisión de la Cochrane9, los investigadores revisaron más detalladamente la presencia de efectos adversos con el fin de informar sobre los mismos pero la proporción de efectos adversos menores sigue siendo muy bajo y no se informaron de efectos adversos importantes en ningún caso. Concretamente, en dicha revisión, se detalla que 29 estudios informaron sobre efectos adversos y en ningún estudio se notificaron efectos adversos graves. El atragantamiento y las náuseas, son efectos adversos presentes en todos los grupos estudiados, de modo que no se relacionó con la administración de sacarosa.
En la revisión de la Cochrane9, detallan los procedimientos dolorosos incluidos en su revisión siendo los detallados en nuestros criterios de inclusión y la dosificación según los estudios son dosis altas y dosis bajas al tratarse de una revisión de estudios, pero en el ensayo clínico de Banga et al.12 cuyo objetivo primario fue evaluar la seguridad de la sacarosa, el procedimiento doloroso no está definido, sino que detallan que son procedimientos dolorosos de la práctica clínica de la UCINN. En este ensayo, la dosis de sacarosa que recibían los pacientes era dosis fija de 24%, que es la dosis más frecuente en los ensayos clínicos detallados en las tablas 1 y 2.
DISCUSIÓN
La presente revisión ha recopilado los estudios (EC, metaanálisis y revisiones sistemáticas) publicadas en los últimos 10 años sobre el tratamiento no farmacológico del dolor en neonatos, al ser cada vez más frecuente su uso en la práctica clínica diaria de las UCINN.
La sacarosa es un glúcido, concretamente, un disacárido compuesto por glucosa y fructosa. Se cree que el mecanismo de acción de la sacarosa como analgésico para el dolor en neonatos se debe a la activación/liberación de opioides endógenos, de modo que se produce una reducción de los indicadores fisiológicos y de conducta del dolor en los neonatos4,5,11.
En estos estudios, se observa que la administración de sacarosa como tratamiento no farmacológico del dolor neonatal reduce significativamente el dolor asociado con distintos procedimientos dolorosos, concretamente, se observa reducción de los indicadores fisiológicos del dolor y mejoría en distintas escalas validadas para el dolor10. Además de los ensayos mencionados en nuestra revisión, esto se avala en la revisión sistemática de Stevens et al.9
Como hemos detallado, a pesar de la efectividad de la sacarosa por sí sola, muchos estudios coinciden en los beneficios de asociarla con otras intervenciones no farmacológicas como la succión no nutritiva.
La succión no nutritiva es recomendada por las guías internacionales para el manejo del dolor neonatal durante los procedimientos dolorosos ya que existe evidencia de que reduce significativamente la puntuación del dolor de las distintas escalas que lo evalúan, y también reduce los comportamientos del dolor cuando se realiza la punción del talón, la venopunción y los exámenes oculares en neonatos7.
Existe evidencia de que el mecanismo de acción de la succión no nutritiva podría atribuirse a la activación de receptores táctiles y a la reducción del dolor a través de mecanismos de control de inhibición del dolor, mientras que la sacarosa estimula receptores gustativos y reduce la percepción del dolor al liberar opioides endógenos en el sistema nervioso central10. Por lo tanto, con la combinación de ambos tratamientos no farmacológicos se activan al mismo tiempo mecanismos opioides y no opioides, potenciando el efecto analgésico final7.
En el estudio de Leng HY et al., concluyeron que la combinación de los tres tratamientos no farmacológicos (sacarosa, succión no nutritiva y swaddling) demostró ser más efectivo que cuando se utilizan en monoterapia, aunque, cuando la punción no es muy profunda, podría utilizarse sacarosa en monoterapia ya que demostró ser efectiva13.
Según la evidencia disponible, cuando sea posible, se recomienda la combinación del tratamiento no farmacológico para el dolor en procedimientos dolorosos menores para lograr una analgesia óptima en neonatos7,9,10,13.
En cuanto a la dosificación de la sacarosa, a pesar de ser el tratamiento no farmacológico más utilizado en el dolor neonatal, la concentración y la dosis más eficaz en cada caso no está clara y existe variabilidad en la evidencia disponible, como se observa en las tablas 1 y 2. En muchos estudios utilizan dosis fijas de sacarosa, pero en otros, como hemos detallado en resultados, la dosis es por peso del paciente o por edad gestacional, en cambio, la concentración del 24% es la más utilizada en los estudios.
En la literatura, hay EC en los que se ha evaluado cuál podría ser la dosis mínima eficaz de sacarosa ante la variabilidad existente en la práctica clínica. En el ensayo clínico aleatorizado y doble ciego de Tanyeri-Bayraktar14, compararon la eficacia de dos dosis distintas de sacarosa al 24% durante la venopunción en 129 recién nacidos. A un grupo (n=65) le administraron 0,2 ml/kg de sacarosa 24% y al otro grupo (n=64) 0,5 ml/kg. Para evaluar las puntuaciones del dolor antes, durante y después del procedimiento utilizaron la Escala del Dolor de Berna para Neonatos (BPSN). No se observaron diferencias estadísticamente significativas en la puntuación BPSN entre los grupos (p>0,05), por lo que concluyeron que la dosis mínima eficaz para aliviar el dolor de la venopunción podría ser 0,2 ml/kg de sacarosa al 24%. En otro ensayo clínico, realizado por Stevens et al.15, en el que también querían determinar la dosis mínima eficaz de sacarosa al 24% para reducir el dolor en recién nacidos hospitalizados sometidos a la punción del talón, se incluyeron 245 recién nacidos con edad gestacional comprendida entre 24-42 semanas ingresados en 4 unidades de UCINN. Se aleatorizaron en 3 grupos con distinta dosis de sacarosa al 24% más succión no nutritiva o chupete, 2 minutos antes de la punción del talón. El primer grupo (n=81) recibía 0,1 ml de sacarosa 24%, el segundo grupo (n=81) 0,5 ml y el tercer grupo (n=83) 1 ml. Se midió la intensidad del dolor a los 30 y 60 segundos después de la punción utilizando el perfil del dolor del lactante prematuro revisado (PIPP-R). No se observaron diferencias estadísticamente significativas en las puntuaciones PIPP-R entre los grupos de tratamiento a los 30 segundos (p=0,97) y a los 60 segundos (p=0,93), concluyendo que la dosis mínima eficaz de sacarosa 24% necesaria para tratar el dolor asociado a la punción del talón fue de 0,1 ml pero se necesitaría una evaluación adicional para determinar la efectividad sostenida de esta dosis para reducir la intensidad del dolor en procedimientos dolorosos repetidos.
Por otro lado, en la revisión de la Cochrane de Stevens et al.9, recomiendan una dosificación comprendida en el rango de 0,05-0,5 ml de sacarosa al 24%, que corresponde a 0,012-0,12 g, 2 minutos antes del procedimiento doloroso. Esta dosificación coincide con la guía para la evaluación y el tratamiento del dolor en el recién nacido de Witt et al.10 donde se recomienda una dosis que varía de 12 a 120 mg de sacarosa al 24%. En el Hospital de Melbourne, la dosificación de la sacarosa oral se realiza según la edad corregida del paciente y el rango de dosificación también está comprendido entre 0,05 a 0,5 ml de sacarosa 24%16.
Por lo tanto, el rango de dosificación de la sacarosa ha sido estudiado y existe evidencia de uso en la práctica clínica, pero sería necesario realizar más estudios futuros con el objetivo principal de conocer cuál sería la dosificación más óptima en cada procedimiento doloroso con el fin de establecer un consenso.
Respecto a la seguridad, en la práctica clínica diaria de un hospital, se realizó un estudio de casos y controles cuyo objetivo fue examinar los posibles efectos secundarios de la sacarosa para el alivio del dolor en recién nacidos prematuros evaluando la alimentación y el aumento de peso durante la hospitalización. Se incluyeron 43 nacidos prematuros divididos en dos grupos: grupo sacarosa (sacarosa oral al 25% 0,5 ml/kg durante 2 minutos antes de todos los procedimientos dolorosos agudos como venopunción, aspiración traqueal o inserción de sonda nasogástrica durante 3 días consecutivos). Los patrones de alimentación de los recién nacidos y el aumento de peso no se vieron afectados después del uso a corto plazo de sacarosa para aliviar el dolor. Se concluyó que esa administración no sólo fue útil para el alivio del dolor, sino que no tuvo efectos adversos ni en la progresión de la dieta ni en su peso durante la hospitalización17, por lo que en vida real según este estudio se confirma lo que concluyen los EC de la ausencia de efectos adversos con el tratamiento de sacarosa oral.
Tras la revisión realizada, se concluye que la sacarosa es efectiva y segura para el tratamiento del dolor en prematuros y neonatos a término, siendo una opción de tratamiento en las unidades de UCI neonatos y neonatología cada vez más utilizada en nuestro medio.
Destacar que, la combinación de sacarosa con otros tratamientos no farmacológicos tiene efecto sinérgico y potencia el efecto analgésico en el neonato, por lo que debería valorarse la combinación en procedimientos más dolorosos o en neonatos con un umbral más bajo del dolor.
En cambio, sería interesante realizar un estudio para evaluar los efectos a largo plazo de su uso ya que los neonatos en ocasiones se encuentran hospitalizados largos periodos de tiempo en torno a 2-3 meses y son sometidos constantemente a procedimientos dolorosos.