Mi SciELO
Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Ene
versión On-line ISSN 1988-348X
Ene. vol.9 no.3 Santa Cruz de La Palma dic. 2015
https://dx.doi.org/10.4321/S1988-348X2015000300009
Vacunación del paciente pediátrico receptor de progenitores hematopoyéticos
Paloma Martínez Amigo
Enfermera. Centro de Salud de Monterrozas
RESUMEN
Introducción: El niño en programa de trasplante de progenitores hemopoyéticos presenta un estado de inmunosupresión que le hace más susceptible a padecer enfermedades infecciosas. Nos encontramos ante la necesidad de establecer recomendaciones de vacunación específicas para cubrir sus necesidades inmunitarias.
Método: El método utilizado ha sido una revisión bibliográfica, se ha utilizado como principal recurso Internet, realizando búsquedas en bases de datos científicas y páginas web de organismos oficiales.
Resultados: La inmunidad adquirida previamente al trasplante se pierde generalmente, siendo necesaria la reinmunización del paciente y, la elección del momento más adecuado para ello es fundamental para obtener una respuesta óptima.
Palabras clave: Trasplante de progenitores hemopoyéticos, inmunización, vacunación, leucemia, paciente inmunodeprimido.
ABSTRACT
Introduction: The child in program hematopoietic stem cell transplantation presents a state of immunosuppression that makes you more susceptible to infectious diseases. We are faced with the need to establish specific recommendations to meet your immune vaccination needs.
Method: The method used was a literature review has been used as the main Internet resource, by searching in scientific databases and websites of official agencies.
Results: The previously acquired immunity to the transplant is usually lost, the patient still needed reimmunization and choosing the right time for it is essential.
Key words: stem cell transplantation, immunization, vaccination, leukemia, immunocompromised patient.
Introducción
El sistema hemopoyético es un órgano líquido, formado por células jerarquizadas con capacidad para regenerar las células linfoides y mieloides del organismo. El trasplante de progenitores hemopoyéticos es una técnica terapéutica utilizada para regenerar el tejido hemopoyético con función insuficiente por una enfermedad primaria de la médula ósea o por haber recibido un tratamiento quimioterápico y/o radioterápico intensivo. En la segunda mitad del siglo XX este tipo de trasplante se convirtió en un tratamiento curativo para miles de pacientes con neoplasias hematológicas y otras enfermedades. La sangre periférica y el cordón umbilical han sustituido a la médula ósea como fuentes principales de obtención de células progenitoras, disminuyendo las complicaciones y simplificando el proceso de extracción.(1)
Podemos clasificar los trasplantes de células hemopoyéticas en distintos tipos según el donante y la fuente de la que provengan las células progenitoras. Según el donante pueden ser: Singénico (el realizado entre hermanos gemelos univitelinos; es poco frecuente); Alogénico (el realizado entre dos personas diferentes genéticamente pero con un grado de similitud alta en los antígenos del sistema HLA); Autólogo (en el que se extraen y conservan células progenitoras del paciente, que se reinfundirán tras someterle a un tratamiento erradicativo de su enfermedad; es el tratamiento de elección en el caso de algunas neoplasias hematológicas). (1)
La fuente de obtención de las células progenitoras puede ser: médula ósea (es la fuente original, la única técnica de obtención de progenitores hasta hace pocos años; es necesario realizarla en quirófano, bajo anestesia general o epidural), sangre periférica ( normalmente existe una cantidad mínima de células madre, pero se ven aumentadas tras tratamientos con factores de crecimiento hemopoyético) y cordón umbilical ( obtención de células madre hemopoyéticas a partir de la sangre del cordón umbilical; la forma más novedosa, y con auge en los últimos años).
Previamente al trasplante, es necesario realizar un tratamiento de acondicionamiento. Hasta hace unos años, se trataba de un tratamiento bastante agresivo que pretendía eliminar toda la enfermedad, si se trataba de una neoplasia, y permitir que injertaran las células trasplantadas al suprimir la médula y el sistema inmunitario del paciente. Actualmente existe otro tipo de tratamiento menos tóxico que cada vez se utiliza más, que pretende lograr la suficiente inmunosupresión del paciente de manera que no se produzca rechazo del injerto pero sin erradicar toda la enfermedad para que se produzca un efecto "injerto contra tumor". (1)
Una de las complicaciones más importantes tras el trasplante son las infecciones, causando la mayor parte las muertes que se producen en estos pacientes en la fase temprana. Las infecciones son consecuencia de la neutropenia y el daño a la barrera mucosa y cutánea producido por el tratamiento de acondicionamiento y otras medidas invasoras como la colocación de catéteres endovenosos, además de la inmunodeficiencia producida por la enfermedad de base y el uso de inmunosupresores.(1)
La vacunación sistemática pretende la protección de la población de enfermedades infecciosas prevalentes y graves que suponen una amenaza para la salud individual y comunitaria. La inmunización de estos pacientes busca además de su protección individual, mantener la protección inmune de la comunidad para que no se produzcan brotes de enfermedades inmunoprevenibles. (1) Debido a esa inmunosupresión, es fundamental conocer en qué momento se debe realizar la vacunación y si existen contraindicaciones para la vacunación del paciente.
Los trasplantes de progenitores hemopoyéticos, constituyen una medida terapéutica eficaz para enfermedades hemopoyéticas primarias (inmunodeficiencias, anemia aplásica, enfermedades congénitas,...) y enfermedades tumorales susceptibles de curación con tratamiento radio o quimioterápico a altas dosis y que precisen de rescate de la función hemopoyética (leucemias, linfomas, mielomas,...) (2). Tras el trasplante, la recuperación de la función inmune es lenta en mayor o menor medida dependiendo del tipo de trasplante que se realice, la enfermedad de base, el tratamiento de acondicionamiento que se realice y la existencia de Enfermedad injerto contra huésped crónica o el tratamiento inmunosupresor al que se le someta al paciente. Puede ser frecuente presentar déficits humorales o celulares hasta uno o dos años después del trasplante. (3)
Aunque en la última memoria publicada por la Organización Nacional de Trasplantes, del total de los Trasplantes de Progenitores hemopoyéticos sólo el 10% se realizaron en niños menores de quince años (3), es interesante el estudio de la vacunación en esta etapa por ser el momento en que se realiza la administración del calendario de vacunación sistemático en niños, y por ende, la mayor cantidad y concentración de vacunas a lo largo de la vida.
Asimismo, el profesional de enfermería es el contacto directo con los pacientes pediátricos y sus familiares al ser el encargado de la administración de las vacunas. Por este motivo es fundamental localizar y recuperar información relevante que responda a cualquier duda que como profesional pueda surgir sobre la vacunación ante un paciente pediátrico receptor de progenitores hemopoyéticos en la práctica clínica, tanto antes como después del trasplante.
Hipótesis y objetivos
Hipótesis:
¿Existen recomendaciones de vacunación específicas para el paciente pediátrico receptor de progenitores hemopoyéticos?
Objetivo general:
El propósito del trabajo es establecer recomendaciones para la vacunación de los receptores de progenitores hemopoyéticos.
Objetivos específicos:
• Establecer recomendaciones de vacunación, previas y posteriores a la realización del trasplante.
• Señalar las contraindicaciones para la vacunación, previas y/o posteriores, a la realización del trasplante.
• Establecer cuál es el momento idóneo para realizar la vacunación antes y después del trasplante.
• Determinar si existe la necesidad de recomendar la vacunación en los convivientes y en los profesionales sanitarios que tratan a los receptores de progenitores hemopoyéticos.
• Determinar si existe la necesidad de realizar una vacunación de refuerzo en los donantes de progenitores hemopoyéticos.
Metodología
El presente trabajo se trata de un estudio de tipo descriptivo y se ha realizado entre los meses de Marzo y Abril de 2015. La técnica empleada para la realización del este trabajo es la revisión bibliográfica. Se ha utilizado como principal recurso Internet, a través del cual se ha podido acceder a distintas bases de datos científicas: Dialnet, Cuiden, Pubmed, Medline, Scielo, Fisterra y Google Académico; así como la consulta de revistas y manuales de pediatría y vacunación "en línea", y páginas web de organismos oficiales, referentes en vacunación infantil, como la Asociación Española de Pediatría, que cuenta con un Comité Asesor de Vacunas, u otras entidades científicas que cuentan con estudios propios.
Se comenzó con una búsqueda bibliográfica en bases de datos en castellano como Dialnet y Scielo, para tomar un primer contacto con el tema a investigar. Posteriormente se emplearon bases de datos con un volumen elevado de documentación en otros idiomas para una mayor profundidad en el tema a investigar. Se utilizaron palabras clave como "vacunación", "vacuna", "inmunodeprimido", "receptor de progenitores hemopoyéticos", "médula ósea", "cancer", "leucemia", "vaccination", "vaccine", immunocompromised", "leukemia", "hemopoietic stem cell" o "transplantation". Se utilizaron distintas combinaciones de las palabras clave, separándolas por la preposición "&" para conseguir documentación de relevancia para el estudio de investigación. Se acotaron las búsquedas filtrando por la fecha de publicación a los últimos cincos años, ampliándola hasta diez años dependiendo de la cantidad y relevancia de los resultado obtenidos, para conseguir una documentación lo más actual posible. Se acotó la búsqueda por idioma, seleccionando el castellano, inglés y francés, idiomas de los que más volumen de artículos aparecían publicados. Para facilitar el acceso a la documentación se filtró la búsqueda por documentos disponibles gratuitamente en Internet con el texto completo.
Tras realizar la búsqueda bibliográfica, y contar con toda la documentación, se realizó la lectura comprensiva de la misma para decidir el enfoque del tema y formular la pregunta de investigación, así como plantear el objetivo general y los específicos. Se encontró en este momento, en algunos puntos, documentación contradictoria que se describe en la "discusión" del estudio. Se han seleccionado ante cualquier divergencia en las recomendaciones de vacunación en el paciente pediátrico receptor de progenitores hemopoyéticos, los documentos de consenso de los expertos en vacunación de la Asociación de Pediatría, ya que en España, suponen un referente; teniendo en consideración que serían necesarios más estudios de investigación para poder sacar conclusiones más firmes.
Para la elaboración de un calendario vacunal específico para estos pacientes, se realizaron búsquedas bibliográficas sobre las vacunas recomendadas, para determinar cuál es el momento propicio de inicio de la inmunización, en qué dosis y a qué intervalo entre dosis.
Resultados
El transplante de progenitores hemopoyéticos es una medida terapéutica que conlleva una pérdida de inmunidad humoral y celular frente a antígenos adquiridos previamente al trasplante tanto de manera natural como artificial. El déficit en el sistema inmunitario puede deberse a factores como la enfermedad de base, el tratamiento de acondicionamiento previo, el tipo de trasplante, la fuente de obtención de los progenitores hemopoyéticos, el grado de disparidad entre del HLA del donante y el receptor, el grado de aceptación del injerto, el tiempo transcurrido desde el trasplante y la presencia o no de enfermedad de injerto contra huésped y la necesidad de iniciar un tratamiento inmunosupresor posterior al trasplante (2)(3). La duración de la inmunosupresión depende de la enfermedad que ha requerido el trasplante y del tipo de trasplante que se realice; puede ser de meses e incluso años si existe enfermedad de injerto contra huésped (4). Por tanto, debido a esa situación de inmunodeficiencia, existe una mayor susceptibilidad a padecer infecciones, con una alta morbimortalidad en la fase inicial (1)(2)(4). El déficit inmune es, a su vez, la causa de una respuesta alterada a las vacunas, observándose porcentajes de seroconversión menores y títulos de anticuerpos más bajos que en el resto de la población. (2)
Se debe realizar la puesta al día de los calendarios vacunales tanto del receptor como del donante antes de realizar el trasplante. Los títulos de anticuerpos por vacunación del virus del tétanos, el de la poliomielitis, el sarampión, las paperas, la rubéola y otras bacterias encapsuladas disminuyen de uno a cuatro años después del trasplante de progenitores hemopoyéticos autólogos o alogénicos si el receptor no está vacunado (5). Las vacunas de microorganismos vivos pueden administrarse hasta cuatro semanas antes de iniciar el tratamiento de acondicionamiento, posteriormente no se debe por riesgo de enfermedad por el agente vacunal. Las inactivas pueden administrarse hasta dos semanas previas al inicio del tratamiento de acondicionamiento al trasplante. En niños mayores de doce meses, no inmunocomprometidos, se recomienda administrar dos dosis de la vacuna de la Varicela antes de cuatro semanas de iniciarse el tratamiento de acondicionamiento. (6)
Existe una pérdida de inmunidad específica que requiere inmunización post trasplante. Una vez realizado el injerto, se asume que el paciente es susceptible a contraer todo tipo de infecciones por lo que sería necesario realizar una vacunación completa con todas las vacunaciones del calendario sistemático; se recomienda iniciar a los seis meses de haber realizado el injerto en el caso de las vacunas de microorganismos inactivados e iniciar la administración de vacunas atenuadas entre los 1824 meses postinjerto, siempre y cuando no exista enfermedad de injerto contra huésped o el paciente esté recibiendo tratamiento inmunosupresor. (3)(5)(6)(7)(8)(9)
En el caso de la Varicela y la Triple Vírica, vacunas de microorganismos vivos, para poder recibirlas, el paciente no tiene que haber sido tratado con inmunoglobulinas y si las ha recibido que haya sido hace 811 meses; que sean seronegativos, no tengan enfermedad de injerto contra huésped, que no estén en tratamiento con antiherpéticos y que su recuento de Linfocitos T sea igual o mayor de 200/mm. (3)(7). Se administrarán dos dosis de cada vacuna, con un intervalo de cuatro semanas (si hubiera un brote epidémico) hasta 12 semanas (intervalo recomendado en el caso de los niños menores de 13 años) con una dosis de refuerzo a los tres años post trasplante si tras realizar una determinación serológica posterior, se obtiene seronegatividad. (4)(10)(11)
La vacuna contra la Fiebre Amarilla, para aquellos pacientes que viven en un país endémico, evaluando el riesgobeneficio obtenido con la vacunación del paciente, se debe realizar la vacunación, no antes de los 24 meses posttrasplante y siempre y cuando no se esté administrando un tratamiento inmunosupresor durante al menos tres meses y no exista enfermedad de injerto contra huésped.(11)
Existe una mayor susceptibilidad a Neumococo, Haemophilus Influenzae tipo b y Meningococo (2)(5), siendo por tanto, especialmente importante la vacunación frente a éstos. En España, dada la situación epidemiológica actual, se recomienda la administración a partir de los 36 meses posttrasplante, la vacuna conjugada de Neumococo, por observarse en ella una mayor respuesta y tener mayor capacidad de inducir memoria inmunológica. Se recomienda la vacunación con tres dosis y un intervalo de un mes entre ellas. Si el receptor tiene enfermedad injerto contra huésped crónico, se recomienda una cuarta dosis de refuerzo a los 12 meses del trasplante. La vacuna no conjugada, 23 valente, aunque tiene una mayor cobertura, los serotipos que cubre son poco frecuentes en niños y sólo puede administrarse a partir de los 24 meses de edad. Es posible la utilización de esquemas vacunales mixtos con la vacuna 13 y 23 valente, administrándose ésta última a los 12 meses del injerto, en una sola dosis si no hay enfermedad de injerto contra huésped, como la dosis de refuerzo. (6)(7)(11)(12)(16)
Las infecciones pulmonares son frecuentes en los receptores de progenitores hemopoyéticos entre los tres y doce meses tras el trasplante. La vacunación con Haemophilus influenzae tipo b puede inducir inmunidad protectora independientemente de la terapia inmunosupresora que se utilice, la existencia o no de enfermedad de injerto contra huésped y el tiempo de administración post trasplante (11). Se recomienda administrar tres dosis, con un intervalo de al menos un mes, a partir de los 612 meses tras el trasplante de progenitores hemopoyéticos de vacuna de Haemophilus Influenzae tipo b (4)(5)(7)(10)(17), con una dosis de refuerzo a los 18 meses de la realización del injerto en niños menores de cinco años (11). En cuanto al Meningococo C, no hay datos sobre la epidemiología de las infecciones meningocócicas en este tipo de pacientes en España, pero el riesgo de aparición de la infección podría ser mayor en comparación con la población sana debido a la asplenia funcional existente tras el trasplante. Se debe iniciar la vacunación a los 612 meses posttrasplante, con dos dosis, con un intervalo entre ellas de 48 semanas (10)(11), si el paciente es menor de un año de edad, y una dosis de refuerzo a partir de los 12 meses, y una sola dosis en mayores de un año, para conseguir una respuesta inmunizara satisfactoria. (11)
Si el niño no se ha vacunado en el primer año de vida, se administran dos dosis únicamente. (4)
Se observa una menor respuesta a los toxoides diftéricos y tetánicos, aunque se alcanza una protección suficiente. La respuesta a la vacuna de la tos Ferina es inferior si se administra como Tdpa, por lo que sería conveniente la administración de DTPa en todos pacientes receptores de progenitores hemopoyéticos aunque no esté indicada en niños mayores de 7 años. El esquema de vacunación recomendado es de tres dosis con intervalo entre ellas de un mes, que debe iniciarse a los 612 meses de realizarse el trasplante y con una dosis de refuerzo a los 1824 meses. (7)(11)
El virus de Gripe produce un 23% de mortalidad en estos pacientes, aunque la respuesta a la vacuna se ve disminuida, se alcanzan niveles de protección aceptables, por lo que se recomienda la vacunación anual a partir de los seis meses del trasplante, con dos dosis separadas 46 semanas el primer año, de vacuna inactivada, fraccionada o de subunidades. Los años posteriores, se vacunará con una dosis anual única (4)(5)(6)(7)(11). En determinadas situaciones de riesgo epidemiológico, como un brote nosocomial o epidemia declarada, puede administrarse la vacuna a los tres meses posttrasplante. En este caso, se recomienda la administración de una segunda dosis contra Influenza, cuatro semanas después de la primera dosis. En niños menores de nueve años, que reciban la vacuna por primera vez, con dos dosis espaciadas por cuatro semanas, es suficiente. En niños mayores de nueve años, o menores de nueve que hayan recibido la vacuna contra Influenza, se recomienda una sola dosis de vacuna de la gripe. Es recomendable la administración de esta vacuna de por vida en estos pacientes. Está contraindicada la administración de la vacuna de virus vivos intranasal, tanto en el paciente, como en los convivientes. (11)
Aunque no existen datos sobre la vacunación contra el virus del Papiloma Humano en estos pacientes, debido a la alta prevalencia y a la aparición frecuente de complicaciones tardías de la infección por el virus del papiloma humano en estos pacientes, observándose en por lo menos un tercio de ellos, se recomienda la vacunación a todos los niños sometidos a un trasplante de células progenitoras (4)(11). Expertos estadounidenses, recomiendan la vacunación rutinaria de niños y niñas a partir de 11 a 12 años, a los seis meses posttrasplante, con tres dosis de vacuna tetravalente, o, únicamente en niñas con dos o tres dosis de la vacuna bivalente. (13)(18)
Tras el trasplante se produce una pérdida rápida de inmunidad contra la Poliomielitis. El esquema de vacunación recomendado es de tres dosis con un intervalo de un mes entre ellas, iniciándolo a los 612 meses después del trasplante, con una dosis de refuerzo a los 1824 meses. La vacuna de virus vivos, oral, está contraindicada. (11)(14)
La Hepatitis B supone un riesgo para cualquier paciente trasplantado, ya que puede suponer la cronificación de la enfermedad y además puede producirse la reactivación viral con más frecuencia que en la población sana. Se recomienda un calendario de vacunación de todos los pacientes con tres dosis de vacuna, iniciándolo a los 612 meses, con un intervalo de un mes entre dosis. Se debe realizar un recuento serológico al mes de finalizar la pauta, si éste no fuera adecuado, se administrará una dosis de refuerzo a los 1824 meses. (10)(11)(19)
La Asociación Española de Pediatría no recomienda la vacunación rutinaria de Hepatitis A en estos pacientes. Aconseja la administración de la vacuna de la hepatitis A en los receptores de progenitores hemopoyéticos que padecen hepatitis A de forma crónica o en los que padecen enfermedad injerto contra huésped crónico. Se deben administrar dos dosis separadas por un intervalo de 612 meses. (3)(4)
El donante transfiere inmunidad a través del injerto, produciéndose lo que se conoce como inmunidad de adopción. La mayor parte de las células T circulantes en el paciente meses después del trasplante, son células T de memoria que probablemente provengan del injerto. Esta inmunidad es de corta duración. Es recomendable la actualización de las inmunizaciones del donante entre tres y cuatro semanas antes del trasplante, para mejorar la inmunidad y aumentar la respuesta a las vacunaciones posteriores en el receptor (2)(3)(4)(7). Se aconseja la administración de dosis de refuerzo de vacunas inactivadas, 20 días antes del trasplante, tanto al donante como al receptor, para conseguir que el receptor adquiera más rápidamente los títulos de anticuerpos protectores frente a antígenos vacunales (3). Es recomendable la administración de dosis de refuerzo de la vacuna de la hepatitis B, dos semanas antes de realizar la donación, tras realizar una serología previa; completar la vacunación con tres dosis tras realizar la donación con un intervalo de un mes entre ellas. Tras la realización de la donación es recomendable la administración de la vacuna anual de la gripe, por lo menos durante 2 años. Y también la administración de la vacuna de difteria y tétanos, con 3 dosis, la primera tras realizar la donación, la segunda 1 mes después y la tercera a los 6 meses. (5)
Como en cualquier otro paciente inmunodeprimido, es primordial proteger al paciente mediante la puesta al día de los calendarios vacunales de los convivientes y el personal sanitario encargado de los cuidados del receptor, siendo muy recomendable la vacunación anual de la Gripe así como la vacunación frente a Varicela en el caso de aquellos miembros de la familia que sean susceptibles, es decir aquellos no inmunizados que sean seronegativos (4)(6)(7)(10). Se recomienda la administración de la vacuna con dos dosis y un intervalo de cuatro semanas entre dosis; es necesario evitar el contacto con el paciente inmunodeprimido si apareciera una erupción secundaria a la vacunación hasta la resolución completa de la misma (10)(11). Deben administrarse tres dosis de la vacuna de la Hepatitis B en los convivientes, administradas en el momento que se realiza el trasplante, al mes y a los seis meses del mismo (10). Se indica la vacunación de convivientes por existencia un brote epidémico de Poliomielitis, debiendo administrarse la vacuna inactivada. Deben completarse las pautas vacunales de Triple Vírica si no estuvieran actualizados los calendarios; la vacunación completa requiere la administración de dos dosis incluso también en los adultos. (7)
Discusión y conclusiones
Se han encontrado resultados contradictorios en algunos aspectos como ya se ha mencionado con anterioridad. La principal complicación es la falta de estudios de investigación específicos para este tipo de paciente en este rango de edad, aunque muchas recomendaciones de vacunación son comunes a las generales del paciente inmunodeprimido.
Existen diferentes documentaciones con respecto de la Inmunidad de adopción o inmunidad que el donante transfiere al receptor a través del injerto. No se han llevado a cabo hasta el momento, un volumen de estudios de investigación suficiente que demuestre la eficacia de dicha inmunidad transferida por el donante. La Asociación Española de Pediatría documenta que la mayor parte de las Linfocitos T circulantes, se convierten en Linfocitos T de memoria con posterioridad al trasplante, que esos linfocitos T provienen del injerto y contienen el repertorio frente al antígeno con el que el donante tuvo contacto (4). Otros autores documentan que la inmunización de los donantes con vacunas como Hepatitis B, Haemophilus influenzae tipo b, difteria tétanos y tos ferina y Neumocócica antes de la recolección de las células progenitores hemopoyéticas aunque ha demostrado mejorar la respuesta de anticuerpos en los receptores, debido a la falta de evidencia científica, apoyan la existencia de consideraciones prácticas y éticas que limitan el uso de la inmunización en ellos. (8)(11)
Se han encontrado también divergencias en cuanto a la vacuna del virus del Papiloma Humano, debido a la falta de datos sobre la vacuna en estos pacientes, algunos autores proponen la administración de la vacuna de forma sistemática a todos los pacientes receptores de progenitores hemopoyéticos, sin realizar distinción por sexo o edad (4). Expertos estadounidenses matizan más esta recomendación, sugiriendo la vacunación rutinaria de niños y niñas a partir de los 11 a 12 años, edad media de inicio de las relaciones sexuales y recomendación en cuanto a franja etaria común a la del niño sano (15). Otros autores recomiendan la administración de la vacuna únicamente en niñas de entre 9 y 19 años, siguiendo las recomendaciones para la población infantil sana. (11)
La Asociación Española de Pediatría no recomienda la vacunación rutinaria de Hepatitis A en estos pacientes. Aconseja la administración de la vacuna de la hepatitis A en los receptores de progenitores hemopoyéticos que padecen hepatitis A de forma crónica o en los que padecen enfermedad injerto contra huésped crónico. Se deben administrar dos dosis separadas por un intervalo de 612 meses (3)(4). Sin embargo se han encontrado recomendaciones de otros autores sobre la administración rutinaria de dos dosis de vacuna para la Hepatitis A en todos los pacientes receptores de progenitores hemopoyéticos, iniciando la pauta a los 612 meses post trasplante, con un intervalo de 48 semanas entre dosis. (15)
El receptor de progenitores hemopoyéticos tiene unas necesidades vacunales adicionales al paciente pediátrico sano que debemos satisfacer debido al déficit inmunitario previo y posterior al trasplante, ya que la protección frente a enfermedades infecciosas prevenibles influirá en la morbimortalidad de estos pacientes. Antes de la recepción de las células progenitoras se deben poner al día los calendarios vacunales en las cuatro semanas previas al trasplante, tanto del donante como del receptor, en el caso de las vacunas atenuadas, y en las dos semanas previas en el de las de microorganismos inactivados. Una vez realizado el trasplante, y recuperada la función inmune, se debe revacunar al paciente administrando todas las vacunas del calendario sistemático infantil. Para conseguir una inmunidad óptima y sin riesgo, debe iniciarse la inmunización a los seis meses para las vacunas de microorganismos inactivados (en el caso de que hubiera un brote de gripe o Neumococo, se pueden administrar estas vacunas antes, a los tres o cuatro meses posttrasplante, ya que aunque no se consiga un título de anticuerpos óptimo, se consigue mayor protección y el riesgo para el paciente es menor que no administrando dichas vacunas). Para las vacunas de microorganismos atenuados, el inicio de la vacunación es a los 1824 meses postinjerto, siempre y cuando no exista enfermedad de injerto contra huésped.
Los familiares, el personal sanitario y cuidadores de los receptores de progenitores hemopoyéticos deben tener actualizados sus calendarios vacunales; y deben administrarse determinadas vacunas como la de la gripe, anualmente, Neumococo o poliomielitis en caso de la existencia de un brote epidémico, o la vacuna de la varicela en aquellos convivientes con alto riesgo de contraerla, es decir aquellos que no estén inmunizados y sean seronegativos.
Bibliografía
1. Rifón JJ. (2006). Trasplante de progenitores hemopoyéticos. An Sist Sanit; 29(2): 137-152. (Consultado el 21 de marzo 2015). Disponible en: http://recyt.fecyt.es/index.php/ASSN/article/view/2205/1614. [ Links ]
2. Ruiz Contreras J, Hernández Merino A. (2005). Vacunaciones en niños con enfermedades de riesgo. Información Terapéutica del Sistema Nacional de Salud; 29(5): 113-132. (Consultado el 23 de marzo 2015). Disponible en: http://www.msssi.gob.es/biblioPublic/publicaciones/docs/vol29_5VacunacionesNinosEnfRiesgo.pdf. [ Links ]
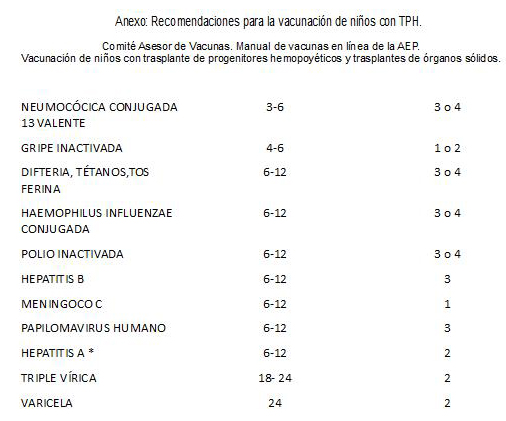
3. Sierrasesúmaga L, Martín I. (2004). Vacunación en trasplantes de progenitores hematopoyéticos. Recomendaciones de vacunación en niños con patologías de base. Manual de vacunas en línea. Asociación Española de Pediatría. (Consultado 23 de marzo 2015). Disponible en:http://vacunasaep.org/manual/Cap13_6_Vacunacion_txt_progenitores_hematopoyeticos.pdf. [ Links ]
4. Mellado MJ, MorenoPérez D, Ruis J, Hernández Sampelayo T y Navarro ML. (2012). Documento de consenso de la Sociedad Española de Infectología Pediátrica y el Comité Asesor de Vacunas de la Asociación Española de Pediatría para la vacunación en inmunodeprimidos. An Pediatra; 75 (6): 413.e1413.e22. (Consultado el 23 de marzo 2015). Disponible en: http://vacunasaep.org/sites/vacunasaep.org/files/Vacunacion_en_inmunodeprimidos_SEIP_CAVAEP_2011.pdf. [ Links ]
5. Tomblyn M, Chiller T, Einsele H, Gress R, Sepkowitz K, Storek J, et al. (2009). Guidelines for preventing infectious complications among hematopoietic cell transplantation recipients: a global perspective. Biol Blood Marrow Transplant; 15: 1143-1238. (Consultado el 21 de Abril 2015). Disponible en: http://www.cdc.gov/vaccines/pubs/downloads/hematocelltransplits508.pdf. [ Links ]
6. Rubin LG, Levin MJ, Ljungman P, Davies EG, Avery R, Tomblyn M and Kang I. (2013). IDSA clinical practice guideline for vaccination of the immunocompromised host. Clin Infect Dis; cit. 684. (Consultado el 9 de abril 2015). Disponible en: http://cid.oxfordjournals.org/content/early/2013/11/26/cid.cit684.short. [ Links ]
7. Asociación Española de Pediatría. (2014). Comité Asesor de Vacunas. Manual de vacunas en línea de la AEP. Vacunación de niños con trasplante de progenitores hemopoyéticos y trasplantes de órganos sólidos. Asociación española de pediatría Madrid: AEP. (Consultado el 10 de marzo 2015). Disponible en: http://vacunasaep.org/documentos/manual/cap16. [ Links ]
8. Australian Government. (2015). The Australian Immunisation Hand Book. 10 th Edition 2015. (Consultado el 21 de Abril 2015). Disponible en: http://www.health.gov.au/internet/immunise/publishing.nsf/Content/Handbook10home~handbook10part3~handbook1033. [ Links ]
9. Ljungman P, Cordonnier C, Einsele H, Englund J, Machado CM, Storek J, et al. (2009). Vaccination of hematopoietic cell transplant recipients. Bone Marrow Transpl; 44(8): 521-526. (Consultado el 15 de Abril 2015). Disponible en: http://www.nature.com/bmt/journal/v44/n8/full/bmt2009263a.html. [ Links ]
10. Zubizarreta R, Rego E, Nartallo V. (2008). Guía Clínica de Vacunas en el paciente en programa de trasplante de progenitores hemopoyéticos. Fisterra.com Atención Primaria en la Red. La Coruña: fisterra.com. (Actualizado el 15 de julio de 2008; Consultado el 21 de abril de 2015). Disponible en: https://www.fisterra.com/ayudaenconsulta/vacunas/hemato.asp. [ Links ]
11. Haut Conseil de la Santé Publique. (2012). Vaccinations des personnes immunodérimées Recommandations. (Consultlado el 23 de Abril 2015). Disponible en: http://www.hcsp.fr/explore.cgi/avisrapportsdomaine?clefr=322. [ Links ]
12. Ljungman P, Small TN. (2011). Vaccination of SCT recipients. Bone Marrow Transpl; 46(4): 621 (Consultado el 21 de Abril 2015). Disponible en: http://www.nature.com/bmt/journal/v46/n4/full/bmt2010274a.html. [ Links ]
13. Shetty AK, Winter MA. (2012). Immunization of children Receiving Immunosuppressive Theraphy for Cancer or Hematopoietic Stemm Cell Transplantation. The Ochsner Journal; 12(3): 228-243. (Consultado el 9 de abril 2015). Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3448245/. [ Links ]
14. Patel SR, Ortiz M, Cohen BJ, et al. (2007). Revaccination with measles, tetanus, poliovirus, Haemophilus influenzae type B, meningococcus and pneumococcus vaccines in children after hematopoietic stem cell transplantation. Colin Infect Dis.; 44: 625-634. (Consultado el 23 de Abril 2015). Disponible en: http://cid.oxfordjournals.org/content/44/5/625.full.pdf+html. [ Links ]
15. NIHPA. (2009). Guidelines for preventing infectious complications among Hemotopoietic Cell Transplant Recipients: A global perspective. Biol Blood Marrow Transpl.: 15 (10): 1143-1238. (Consultado el 17 de Abril 2015). Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3103296/. [ Links ]
16. Meisel R, Kuypers L, Dirksen U, Schubert R, Gruhn B, Strauss G, et al. (2009). Pneumococcal conjugate vaccine provides early protective antibody responses in children after related and unrelated allogenic hematopoietic stem cell transplantation. Blood; 109 (6): 2322-2326. (Consultado el 21 de Abril 2015). Disponible en: http://www.bloodjournal.org/content/109/6/2322.long?ssochecked=true. [ Links ]
17. Ljungman P, Avetisyan G. Influenza vaccination in hematopoietic SCT recipients. Bone Marrow Transpl. (Internet). 2008; 42: 637-641. (citado el 15 de Abril 2015). Disponible en: http://www.nature.com/bmt/journal/v42/n10/full/bmt2008264a.html. [ Links ]
18. Savani BN, Stratton P, Shenoy A, Kozanas E, Goodman S, Barrett AJ. (2008). Increased risk of cervical dysplasia in longterm survivors of allogenic stem cell transplantation implications for screening and HPV vaccination. Biol Blood Marrow Transpl.; 14(9): 1072-1075. (Consultado el 21 de Abril 2015). Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2946417/. [ Links ]
19. Knöll A, Boehm S, Hahn J, Holler E, Jilg W. (2007). Longterm surveillance of hematopoietic stem cell recipients with resolved hepatitis B: high risk of viral reactivation even in a recipient with a vaccinated donor. J Virol Hepat.; 14: 478-483. (Consultado el 21 de Abril 2015). Disponible en: http://onlinelibrary.wiley.com/doi/10.1111/j.13652893.2006.00830.x/abstract;jsessionid=51A82791FC17CA47D6D4FC6BC5EBBD7D.f01t04. [ Links ]