Introducción
La hemodiálisis (HD) es la terapia de reemplazo renal mayormente utilizada en los pacientes con enfermedad renal crónica (ERC) a nivel mundial y en Chile1. A pesar de que permite prolongar la vida de la persona, impacta en diferentes ámbitos de la vida del paciente: cambios de alimentación, dinámica familiar, económicas, trastornos del sueño, presencia de síntomas físicos, entre otros2), (3.
El sueño es una necesidad biológica prioritaria para todo ser, en los pacientes con ERC los problemas relacionados con el sueño se consideran de importancia clínica, dado que generan estrés y afectan negativamente la calidad de vida3), (4. De los múltiples problemas a los que se ven enfrentados los pacientes en diálisis, los más reportados son los trastornos del sueño, que alcanzan una prevalencia entre el 60% y 80%3. Una revisión sistemática con 17 estudios, reveló que los problemas del sueño eran uno de los problemas más comunes en esta población5. Frente a este escenario, surge el interés de conocer cuáles son los problemas de sueño más prevalentes y qué estrategias de abordaje son efectivas para enfermería.
El objetivo de esta revisión es conocer las principales alteraciones del sueño en pacientes con ERC en tratamiento dialítico, los factores que influyen en su aparición y los cuidados de enfermería.
Material y Método
Se realizó una revisión narrativa de la literatura. Los criterios de inclusión fueron estudios primarios y revisiones sistemáticas, sobre alteraciones del sueño en pacientes adultos con ERC en terapia dialítica.
Para la revisión, se consultaron las bases de datos Medline, Scielo, Cochrane y Epistemonikos. La estrategia de búsqueda fue (“sleep disturbances” OR“dyssomnias”) AND “renal dialysis”, acotada a los últimos 10 años (del 01/01/2006 al 31/12/2016), sin restricción de idioma. Además, se agregó una búsqueda dirigida a terapias cognitiva-conductual de las alteraciones del sueño, cuya estrategia de búsqueda fue (“non-pharmacological interventions”) AND (“insomnia” OR “dyssomnias”).
Se realizó un primer cribado de los registros de los artículos devueltos por las bases de datos, con una lectura de título y abstract, para detectar duplicidades y realizar una primera selección. Tras la misma, se accedió al texto completo de los artículos seleccionados y se realizó su lectura para determinar su idoneidad, descartándose 2 por no tener acceso real y 2 por presentar resultados no concluyentes.
Resultados
Finalmente se seleccionaron 43 artículos para realizar la síntesis narrativa (la Figura 1 muestra el diagrama de flujo de la selección de artículos y en las tablas 1 a 5 los documentos revisados clasificados por tema). De cada artículo se realizó una ficha resumen, donde se organizó la información de acuerdo a las alteraciones del sueño, considerando su descripción, manifestaciones, prevalencia, factores de riesgo, diagnóstico y complicaciones.
Tabla 1 Artículos revisados sobre síndrome de piernas inquietas.

SPI: síndrome de piernas inquietas, EP: estudio primario, ERC: enfermedad renal crónica, HD: hemodiálisis; IMC: índice de masa corporal, IRC: insuficiencia renal crónica, MPE: movimiento periódico de extremidades, RL: revisión de la literatura, SAOS: síndrome de apnea obstructiva del sueño, SDE: somnolencia diurna excesiva.
Tabla 2 Artículos revisados sobre síndrome de apnea obstructiva del sueño.
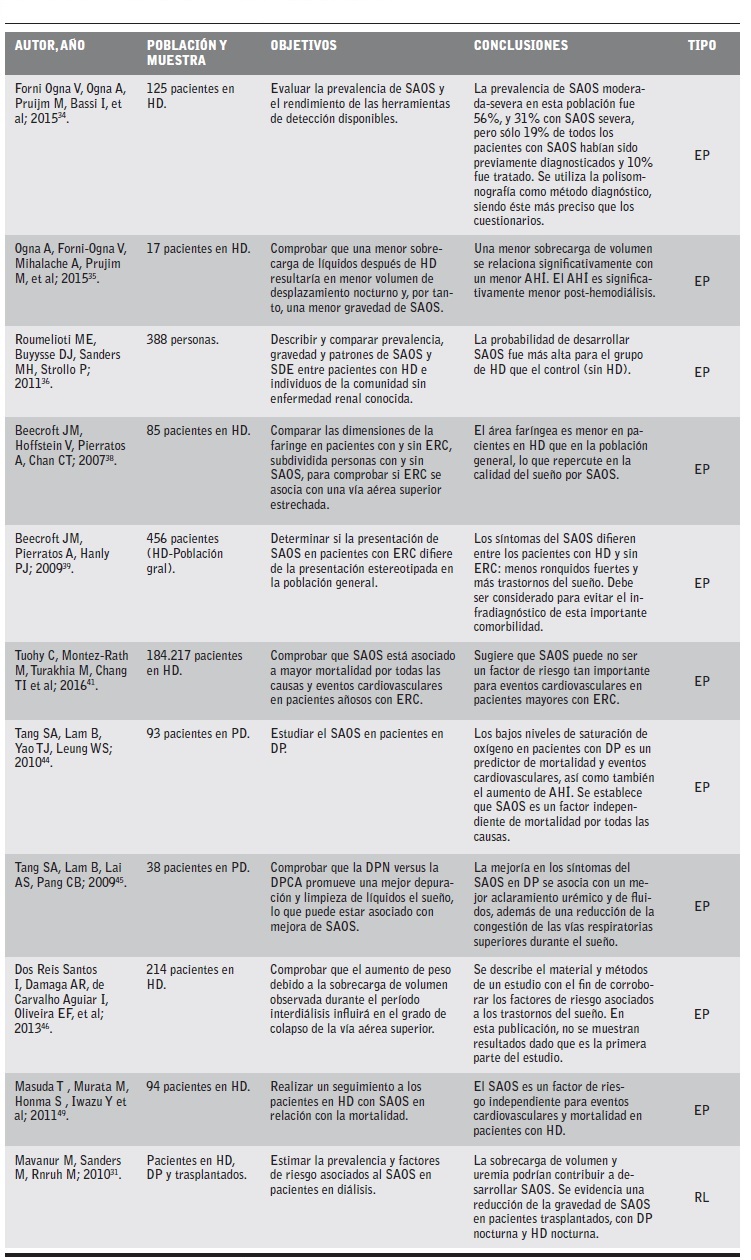
SAOS. Síndrome de apnea obstructiva del sueño, AHÍ: índice de apnea-hipoapnea, DP: diálisis peritoneal, DPCA: diálisis peritoneal contínua ambulatoria, DPN: diá lisis peritoneal nocturna, EP: estudio primario, ERC: enfermedad renal crónica, HD: hemodiálisis, RL: revisión de la literatura, SDE: somnolencia diurna excesiva.
Tabla 4 Artículos revisados sobre somnolencia diurna excesiva.

EP: estudio primario; HD: hemodiálisis.
Tabla 5.Estudios revisados sobre de mas de una alteración del sueño.
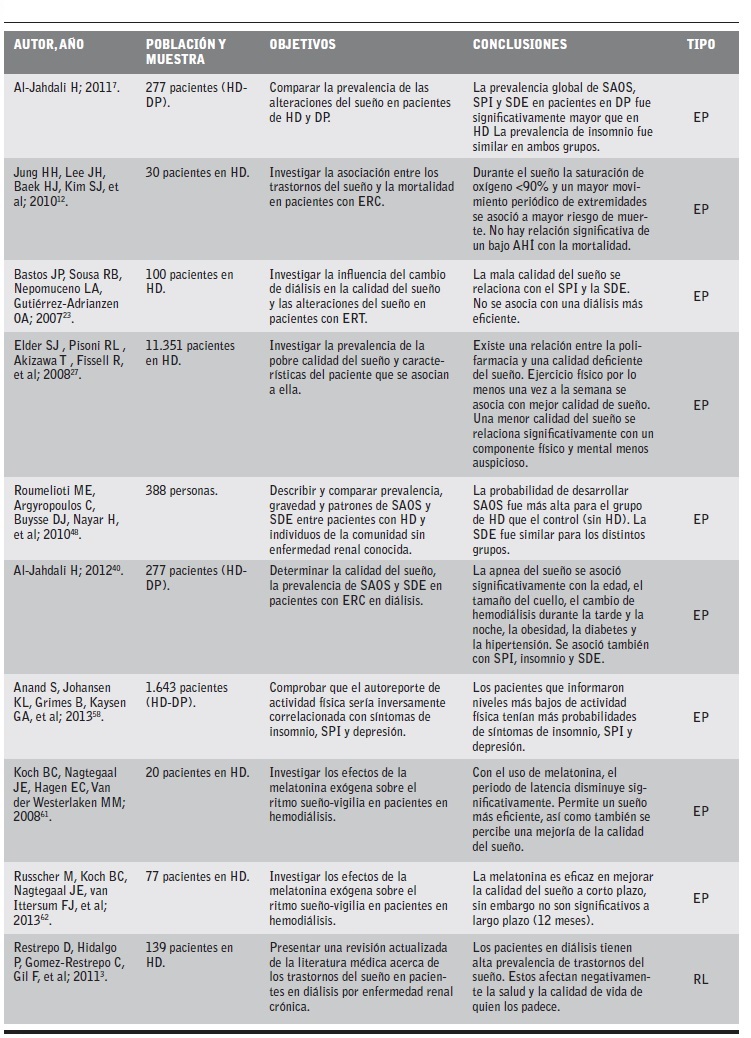
AHÍ: índice de apnea-hipoapnea; DP: diálisis peritoneal; EP: estudio primario; ERC: enfermedad renal crónica; ERT: enfermedad renal crónica; HD: hemodiálisis; RL: revisión de la literatura; SAOS: síndrome de apnea obstructiva del sueño; SDE: somnolencia diurna excesiva; SPI: síndrome de piernas inquietas.
A partir de la información compilada se realizó una síntesis narrativa, agrupada por los siguientes aspectos.
Síndrome de piernas inquietas y movimiento periódico de las extremidades.
Apnea obstructiva del sueño.
Somnolencia diurna excesiva.
Insomnio.
Síndrome de piernas inquietas y movimiento periódico de extremidades
El síndrome de piernas inquietas (SPI) es una alteración neurosensitiva-motora asociada al sueño, afecta esencialmente a las piernas, cuando se intensifica también puede afectar brazos y otras partes del cuerpo6)-(11.
Por otra parte, el movimiento periódico de extremidades (MPE) es la agitación estereotipada e involuntaria de las extremidades durante el sueño, predominando en las extremidades inferiores12.
La diferencia radica en que el movimiento del SPI se expresa en el periodo de vigilia, mientras que el MPE se evidencia en las primeras etapas del sueño (I y II de no REM) (13), (14.
En relación a los síntomas, el SPI se caracteriza por sensaciones dolorosas en las piernas, simultáneo a una intensa necesidad de moverlas, particularmente durante la noche, aumentan con el reposo y mejora con la actividad, al menos transitoriamente10), (11), (15), (16. Mientras que el MPE genera una actividad frecuente y repetitiva del músculo tibial anterior que resulta en el movimiento del ortejo mayor y/o del tobillo, durante el sueño17.
La prevalencia de SPI va de 6% hasta un 60% en pacientes dializados16)-(18, sin embargo, sus cifras varían según la población, es así que en hemodializados las cifras son cercanas al 40%, mientras que en la población en diálisis peritoneal (DP) van de un 33% a 50%5), (17, la que varía si la modalidad es automática (APD) o manual (CAPD), encontrando una prevalencia mayor con APD17. En cambio, el MPE podría afectar a la población con ERC entre un 40 y 70%12), (17. Cabe destacar que cerca del 80% de las personas que tienen SPI, también padecen MPE3), (13), (14), (20.
Autores mencionan que la etiología del SPI es desconocida aún11), (20)-(23. Sin embargo, existen factores de riesgo que estarían asociados a su aparición, tales como, el déficit de hierro o alteración en su metabolismo, frecuente en embarazadas y en los pacientes con ERC13), (14), (21, lo anterior hace suponer que la anemia desempeña un papel relevante en el desarrollo de SPI11. Mortazavi y cols exponen que los síntomas mejoran con agonistas de la dopamina y empeorado con antagonistas dopaminérgicos, por lo que proponen que se relaciona con la disfunción de la dopamina en el sistema nervioso (SN) central14), (21.
En los últimos años se han realizado estudios con el objetivo de encontrar factores de riesgo bioquímicos relacionados con SPI, se estudiaron niveles de ferritina, calcio, fósforo, urea y creatinina; sin embargo, no fueron predictores estadísticamente significativos8), (15), (24. Stefanidis y cols refieren que mujeres, pacientes jóvenes y aquellos con niveles elevados de ß2-microglobulina y PTH presentan mayor riesgo de SPI16. La duración de cada sesión de HD se asocia a SPI, según Beladi-Mousavi y cols, a mayor tiempo mayor es la intensidad de los síntomas8.
El MPE tiene mayor riesgo a mayor edad de la persona y puede relacionarse con otras comorbilidades, según la guía elaborada por las Sociedades Españolas de Neurología (SEN) y la de Sueño (SES), los síntomas podrían intensificarse con fármacos antidepresivos, situación respaldada por un estudio que incluía polisomnografía en pacientes con antidepresivos frente a pacientes controles, que evidenció que el riesgo de tener MPE era 5 veces mayor en pacientes que tomaban antidepresivos13.
Se diagnostica en base de al menos 4 criterios según la guía de “International Restless Legs Syndrome Study Group”, entre ellos el deseo de mover los miembros, usualmente asociados con parestesias o disestesias; agitación motora; agravamiento o presentación exclusiva de los síntomas en reposo con alivio total o parcial por actividad y; por último el agravamiento de los síntomas por la noche8)-(10), (16. Considerando que el uso de los criterios podrían causar confusión en el momento de evaluar y aportar falsos positivos, se utilizan métodos diagnósticos complementarios como la polisomnografía y el test de inmovilización sugerida13.
En relación al tratamiento farmacológico, está enfocado a los síntomas y no a la causa ni su curso. Entonces, ante la falta de adherencia al fármaco los síntomas no desaparecen. La guía realizada por las SEN-SES, sugiere iniciar con monoterapia en una sola dosis en la más mínima cantidad, 2 o 3 horas antes del comienzo de los síntomas, la dosis podría ir aumentando progresivamente hasta conseguir control sintomático13. La evidencia muestra que la primera línea de tratamiento de SPI son los agentes dopaminérgicos y anticonvulsivantes25), (26. Sin embargo, una revisión de Cochrane concluyó que existe un efecto impreciso de las intervenciones farmacológicas18. Por otra parte, existe el tratamiento no farmacológico: masajes, ejercicio, yoga, técnicas de relajación, baños de agua fría o caliente, entre otras.
Además, en ambos es necesario complementarlo con una adecuada higiene del sueño, tomar medidas como dormir lo justo y necesario, evitar siestas y en el caso de pacientes con SPI, retrasar la hora de acostarse para prevenir los movimientos de las extremidades durante el inicio del sueño13.
Un estudio con más de 10.000 pacientes, mostró que la actividad física al menos una vez por semana mejoraba la calidad del sueño27, sin embargo, a nivel de mejoría de síntomas del SPI en pacientes en diálisis, otros autores no encontraron diferencias estadísticamente significativas si la comparaban con el grupo control. A pesar de los resultados, recomiendan la actividad física aeróbica21, así mismo una revisión de Cochrane sugiere que el ejercicio aeróbico podría ser efectivo18.
En la misma línea, Giannaki y sus colegas, estudiaron la eficacia de los agonistas dopaminérgicos ante la actividad física, donde ambos fueron efectivos para disminuir la sintomatología del SPI (46% para el ejercicio y 54% para el fármaco) y ambas intervenciones mejoraron significativamente la calidad de vida, aunque sólo los agonistas de dopamina mejoraron la calidad del sueño significativamente28. Razazian y cols, estudiaron la efectividad de levodopa y de gabapentina en la reducción de síntomas de SPI, éste último mostró ser más efectivo dada la mejora de los síntomas sensitivo-motores del SPI y MPE, con aumento de la calidad del sueño en general29.
Respecto a las complicaciones producto del SPI, se mencionan menor supervivencia y disminución en la calidad de vida6), (8), (30), (31. Algunos autores refieren que existen mecanismos fisiopatológicos en los que este síndrome predispone a desarrollar enfermedad cardiovascular en el paciente en terapia dialítica32), (33, uno de ellos es el incremento de la actividad del SN simpático y la consecuente hipertensión y taquicardia32. Giannaki y cols, sugieren que una menor calidad de vida en pacientes con SPI puede ser por un sueño poco reparador y salud mental alterada30. Las complicaciones del MPE se relacionan con un aumento del riesgo cardiovascular en la población dializada versus la general, Lindner refiere que existe una asociación entre el MPE e hipertensión, así como con insuficiencia cardíaca congestiva17.
Síndrome de apnea obstructiva del sueño (SAOS)
El SAOS es una alteración crónica grave provocada por el colapso frecuente de las vías aéreas superiores que causa asfixia nocturna reiterada e interrupción del sueño. Los repetidos descensos de saturación de oxígeno, incrementan el estrés oxidativo y la activación del SN simpático, esto ocasiona considerables cambios de la presión arterial y ritmo cardiaco7), (34)- (36. Las apneas se clasifican en obstructivas, centrales o mixtas; las primeras son causadas por la oclusión intermitente de las vías aéreas, mientras que en las centrales la causa es la ausencia de movimientos respiratorios, producto de una alteración del centro respiratorio. En tanto que la apnea mixta es una mezcla de ambas37. En pacientes con ERC predominan las apneas obstructivas, con un leve porcentaje de mixtas o centrales38.
Entre sus manifestaciones destaca la interrupción del sueño, que desencadena síntomas durante el día, como la somnolencia diurna excesiva (SDE). Autores refieren que la presentación del SAOS en pacientes con ERC se distingue de la población general por síntomas clásicos, como ronquidos fuertes menos concurrentes, mientras que la hipertensión y fatiga son más frecuentes en pacientes en HD34), (39.
Al igual que el SPI, la prevalencia del SAOS en los pacientes dializados es variable y depende de la población estudiada y método diagnóstico utilizado34), (40. La prevalencia en HD oscila entre un 6% y 86%6), (7), (34), (40)-(43. En tanto que en DP la prevalencia es de un 16% a un 92%, y si se compara APD y CAPD, los porcentajes son mayores en este último grupo6), (7), (41), (44), (45.
Las personas con ERC tienen mayor riesgo de presentar SAOS que la población general, la etiología en el primer grupo se describe como multifactorial y entre los agentes causales se mencionan la sobrecarga de volumen, estrechez de las vías aéreas superiores, inestabilidad de la ventilación, edades avanzadas y otras patologías concomitantes como diabetes31), (46.
Su diagnóstico es difícil de establecer y el mejor método no parece estar definido47. Actualmente el gold estándar es la polisomnografía, su alto costo económico limita su implementación en pacientes potencialmente afectados con SAOS31), (34), (48. El criterio diagnóstico también es controvertido, algunas instituciones lo diagnostican con un Índice de apnea e hipoapnea (AHÍ) > a 5/h49, mientras la Academia de Medicina del Sueño la considera si es > a 15/h31), (34), (35), (43)-(45. Además, se utilizan cuestionarios que apoyan el diagnóstico, como la escala de somnolencia de Epworth para evaluar la SDE y el Índice de calidad del sueño Pittsburgh para determinar la calidad subjetiva del sueño6), (7), (23), (40), (43. Existen escalas de screening del SAOS para complementar la evaluación, entre los que se destacan “Cuestionario de Berlín”, “STOP-BANG Score” y “circunferencia de cuello ajustada” 6), (34), (40), (48.
La primera línea de tratamiento para el SAOS incluye la modificación del estilo de vida del paciente, pérdida de peso y terapia con presión positiva continua en la vía aérea (CPAP) (48. Esta última ha mostrado ser efectiva para resolverlo, reduciendo la SDE y mejorando la calidad de vida. Sin embargo, sólo la mitad de los pacientes con indicación de CPAP continúan usándolo a largo plazo, dado que no tienen buena tolerancia o lo rechazan. Sin embargo, una cantidad de personas permanecen con somnolencia a pesar del tratamiento48.
Entre las complicaciones del SAOS, se mencionan la SDE, hipertensión, hipertrofia ventricular izquierda, mayor riesgo cardiovascular y por ende, aumento de mortalidad7), (46), (49. Al respecto, Masuda y cols estudiaron el SAOS como factor de riesgo independiente de mortalidad y sus resultados así lo comprueban50.
Somnolencia diurna excesiva
Es la tendencia de la persona a quedarse dormida durante la vigilia, se reconoce también como la propensión a dormirse o la habilidad de transición de la vigilia al sueño. Es una alteración que evidencia la dificultad de mantenerse en alerta y puede presentarse como manifestación de cualquiera de las patologías mencionadas anteriormente43), (51), (52.
La prevalencia de la SDE varía dependiendo del tipo de diálisis aplicada: en HD oscila entre un 31% a 77%, en tanto que en DP varía de 13% a 37%7), (24. Si se realiza un día de diálisis versus un día de no-diálisis, las cifras son mayores en los días de diálisis7.
Es causada por alguna deficiencia del sueño, en calidad o cantidad de éste, las más encontradas son el SAOS, insomnio y SPI. Además, se describen factores que determinan su aparición: trastornos neurológicos, psicológicos, pulmonares, presencia de obesidad y/o depresión, edades extremas, anemia, entre otros45), (51), (52.
Para su diagnóstico se utiliza la Escala de Epworth, escala subjetiva de somnolencia, que considera la probabilidad percibida de quedarse dormido en situaciones cotidianas45), (48), (52. Es una prueba fácil de administrar y rápida, sin embargo, depende de la interpretación del evaluador y podría verse afectada por factores sociales, culturales y psicológicos (como ansiedad o depresión), además, puede ser no tan fiable en pacientes muy somnolientos52.
El tratamiento de la SDE está enfocado en la causa, complementándose con la promoción de la adecuada cantidad de horas de sueño y en la educación sobre higiene del sueño52. Es importante considerar todos los factores que pudieran influir negativamente en la calidad y cantidad de sueño, esto es fundamental para dar un manejo correcto51.
Dentro de las complicaciones se menciona que las actividades cotidianas y calidad de vida son afectadas. Igualmente se asocia a mayores niveles de mortalidad y eventos cardiovasculares10), (53), (54, también contribuye a una disminución cognitiva y alteración de estados anímicos. En pacientes afectados por SDE, existe mayor riesgo de accidentes de tránsito y de trabajo40. Algunos autores declaran que existe una reducción en la supervivencia si la calidad del sueño de los pacientes se altera durante el primer año de tratamiento55.
Insomnio
Es la sensación subjetiva de sueño insatisfactorio e insuficiente, aunque se tenga la capacidad para dormir56. Puede implicar dificultades para conciliar el sueño, comportamientos infrecuentes del sueño o que éste sea excesivo3)-(57. La Asociación Americana de Centros de Estudio y Tratamientos del Sueño lo define como: “la latencia mayor a 30 minutos y/o dos o más despertares nocturnos y/o vigilia nocturna mayor a una hora y/o tiempo de sueño total menor a 6 horas” (57.
Existen diferentes tipos de insomnio: el insomnio primario o idiopático y el insomnio secundario, que aparece en respuesta a la presencia de un problema médico o mental, abuso de sustancias, alteraciones del sueño o higiene del sueño inadecuada58.
Cuando el insomnio está presente, por lo general, el paciente manifiesta problemas para conciliar el sueño, despertares frecuentes en la noche o SDE.
Puede clasificarse de acuerdo al momento de presentación: inicial o de conciliación (incremento en latencia del sueño), de mantenimiento (despertares nocturnos con imposibilidad de volver a dormir) o despertar temprano (más temprano que la hora habitual con imposibilidad de volver a dormir) (57.
Existen diversas variables, incluso por definición y clasificación, que dan origen al amplio rango de prevalencia del insomnio49. En HD las cifras van de un 36% a 85%6), (56)-(58, entretanto en DP se describe que CAPD es cercana al 81% y en DPA es 84%6. En un estudio realizado por El Harraqui, la prevalencia de insomnio en sus pacientes fue de 67,7%, lo que demuestra su alta prevalencia58.
En particular, los factores de riesgo asociados con el insomnio referidos en la literatura no son pocos y dan cuenta que los pacientes en diálisis tienen más posibilidades de presentarlo, además de objetivarse, mediante polisomnografía, un sueño más corto y poco reparador59. Se menciona que la duración de HD mayor a un año es estadísticamente significativa en la aparición del insomnio. Asimismo, existe mayor riesgo en los pacientes de sexo femenino, de edad avanzada, con depresión y/o hipertensión, comorbilidades que impidan el inicio/mantención del sueño (dolor, disnea, nicturia, etc), BUN alto pre-diálisis, bajos flujos dialíticos, inflamación, poca actividad física y anemia56), (58.
Los criterios para el insomnio primario son: periodo de latencia >30 minutos, tiempo total de vigilia nocturna >30 minutos, tiempo total de sueño nocturno menor a 6½ horas, efectos diurnos (SDE/disminución de rendimiento cognitivo), presentación más de 3 veces semanales, por al menos un mes60. El diagnóstico se fundamenta en una anamnesis completa, considerando hábitos de sueño, auto-informe del sueño e información concedida por un tercero. Se deben estudiar características del insomnio: duración, gravedad, causas, características del sueño-vigilia (hora de levantada, periodo de latencia, uso de fármacos o drogas, etc). También es importante realizar un completo examen físico y psicológico, se puede complementar con polisomnografía, actigrafía y test de latencia del sueño múltiple56), (58.
El tratamiento del insomnio fue el objeto de estudio de un meta-análisis, con referencia al insomnio primario, ya que en insomnio secundario la resolución radica en tratar la causa principal. Los resultados muestran que terapias cognitivo-conductuales fueron las más utilizadas y las más efectivas. El tratamiento farmacológico es efectivo, aunque su uso es complicado dado que las personas suelen auto-medicarse y quienes acuden al médico, no siempre reciben una prescripción adecuada61. Algunos estudios afirman que el uso de melatonina trae beneficios a corto plazo mejorando parámetros del sueño62), (63, sin embargo, no se evidencian estos resultados a largo plazo63.
El control de estímulos, restricción del sueño, higiene del sueño y la relajación son consideradas terapias conductuales. Mientras que la imaginación guiada o distracción cognitiva, terapia cognitivo-conductual, aurículo-terapia, biblioterapia y la terapia luminosa son categorizadas como terapias cognitivas61.
Las medidas de higiene del sueño se relacionan con el control de factores ambientales y hábitos de salud favorables con el sueño. Por ejemplo, acostarse sólo cuando tenga sueño, levantarse todos los días a la misma hora, no dormir siestas, no consumir cafeína/nicotina de 4 a 6 horas previas a ir a la cama, no beber alcohol en dos horas previas, realizar ejercicio físico siempre y cuando no sea en horas cercanas al acostarse, tener un ambiente cómodo: reducir niveles de luminosidad, de ruido y tener una temperatura agradable60), (61.
De las intervenciones no farmacológicas, la primera línea son las terapia conductuales, las cuales tienen alta efectividad con cifras que van del 50% al 80% de respuesta. Es importante destacar que no se lleva a cabo por sí sola, por lo que se requiere intervenciones combinadas, considerando aspectos del ambiente y la persona61.
De acuerdo a los resultados más relevantes del meta-análisis, se categorizaron los diferentes tipos de terapia61:
Intervención combinada: todas estas intervenciones obtuvieron buenos resultados, que se mantuvieron durante el seguimiento.
Monoterapias: en esta categoría, los resultados no fueron consistentes: estudios que usaron alguna de las técnicas cognitivas arrojaron leves mejoras, en tanto si se utilizaban otras técnicas como “supresión de pensamientos” o “automonitorización” se aumentaba la latencia de sueño o hubo mayor percepción de deterioro en el funcionamiento.
Terapia luminosa: todos los estudios que lo aplicaron arrojaron resultados positivos.
Terapia auricular: es discordante, un estudio mostró leves mejoras que no perduraron en el tiempo y en el otro estudio continuaron hasta seis meses posteriores.
Zou y colaboradores realizaron un ensayo clínico randomizado comparando la acupuntura auricular en puntos específicos versus no específicos para el insomnio en pacientes en HD, los resultados fueron favorables para la acupuntura en puntos específicos64. En esta línea, Cochrane llevó a cabo una revisión que estima que la evidencia disponible debe ser de mayor calidad para poder recomendar la acupuntura en esta población65.
Si se comparan intervenciones farmacológicas versus no farmacológicas, los resultados favorecen a esta última y al combinar ambos tipos de terapia es más efectivo que fármacos por sí solos66.
La reducción en la calidad de vida es uno de los efectos del insomnio más mencionados en la literatura58. También está asociado con un mayor riesgo de morbi-mortalidad53)-(54, tiene implicancias en diferentes aspectos de la vida: familiar, social y laboral56. La depresión y ansiedad pueden ser consideradas causa o efecto del insomnio52.
Discusión
En las personas con ERC que se someten a alguna de las modalidades de diálisis, la prevalencia de trastornos del sueño es alta. Se describen cinco alteraciones que son las más reportadas por la literatura: síndrome de piernas inquietas, movimiento periódico de extremidades, insomnio, síndrome de apnea obstructiva del sueño y somnolencia diurna excesiva. A grandes rasgos, todas influyen negativamente en la calidad de vida del paciente y aumentan la morbimortalidad.
Esta revisión es útil para el equipo de salud y principalmente para enfermeras, ya que acompañan por más tiempo al paciente. Se destaca dentro de sus responsabilidades el cuidado “integral y holístico”, es decir, es imprescindible considerar el ámbito físico, espiritual, psicológico y social de cada una de las personas a su cuidado. Así, a través de la valoración de la persona, reconocer sus necesidades, tomando en cuenta el sueño como una necesidad básica que repercute en su cotidianidad66. Ha quedado demostrado que las alteraciones del sueño son un aspecto fundamental en el diario vivir del paciente y que, sin duda, repercute en el deterioro de su calidad de vida. Por ende, es un elemento que el equipo de salud no debiese pasar por alto.
En muchas ocasiones, durante la entrevista inicial el paciente manifiesta que tiene sueño, que no pasó buena noche o que está cansado. Enfermeras tienen la oportunidad de visibilizar esta situación, acoger al paciente y buscar alternativas de solución. Ahora que son conocidas las manifestaciones, los factores de riesgo asociados y el tratamiento farmacológico y no-farmacológico de cada una de las alteraciones del sueño presentes en estos pacientes, es entonces, parte de la responsabilidad de enfermería indagar en la existencia de alteraciones del sueño, sintomatología e intensidad y detectar los signos de los trastornos del sueño. Así como también, sugerir al médico la indicación de fármacos si corresponde, también es relevante que enfermeras puedan recomendar medidas no farmacológicas y educar respecto a ellas, además de los efectos esperados y secundarios de los medicamentos recetados.
Finalmente, con el objetivo de lograr una correcta detección y tratamiento de las alteraciones del sueño, sería importante que instituciones educacionales acreditadas instauren e impartan un programa de capacitación formal sobre higiene del sueño y terapias cognitivo-conductual para la resolución de estos trastornos. Además, es imprescindible que enfermería participe de estas instancias y la aplique en su quehacer cotidiano.
Proyecto: Estudio Independiente de la Escuela de Enfermería, Pontificia Universidad Católica de Chile
















