My SciELO
Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Ars Pharmaceutica (Internet)
On-line version ISSN 2340-9894
Ars Pharm vol.57 n.2 Granada Apr./Jun. 2016
https://dx.doi.org/10.30827/ars.v57i2.4965
ARTÍCULO ORIGINAL
Especies de Ulva del Golfo San Jorge, Patagonia Argentina: variaciones bioquímicas estacionales - espaciales y su relación con la producción de metabolitos bioactivos
Ulva species from San Jorge Gulf, Patagonia argentina: seasonal and spatial biochemical variation and their relation with the production of bioactive metabolites
Analía Verónica Uhrich1, Osvaldo León Córdoba2 y María Luján Flores3
1 Farmacología II,
2 Química Biológica II y
3 Farmacognosia, GQBMRNP-CRIDECIT, Facultad de Ciencias Naturales, Universidad Nacional de la Patagonia San Juan Bosco.
El trabajo fue financiado por los proyectos de investigación competitivos PNUD ARG 02/018 BB-34; PICTO Golfo San Jorge 36871; PROMFYB FARMACIA FCN, UNPSJB; IRSES FP7 ChemBioFight.
Dirección para correspondencia
RESUMEN
Objetivos: Investigar especies de Ulva del Golfo San Jorge, Patagonia Argentina, integrando aspectos bioquímicos, actividad biológica y variaciones estacionales/habitacionales que permitan determinar su potencial aplicación en Salud.
Métodos: Las algas se colectaron estacionalmente en playas con y sin contaminación antrópica; se secaron, molieron y extrajeron con etanol. Los extractos se fraccionaron mediante solventes de distinta polaridad. Cada fracción fue caracterizada mediante reacciones químicas cualitativas y cromatografía. Las fracciones ricas en flavonoides se analizaron por HPLC-DAD y los lípidos, por TLC. La actividad biológica se ensayó mediante el test de citotoxicidad de Artemia salina, inhibición de la elongación radicular, inhibición de la xantino oxidasa, actividad antioxidante y antibacteriana.
Resultados: Se identificaron Ulva rigida y Ulva lactuca. Ambas evidenciaron flavonoides, taninos, quinonas, lípidos, carbohidratos, esteroides. Los flavonoides resultaron mayoritarios en U. rigida (otoño e invierno) y en U. lactuca (primavera e invierno), destacándose kayaflavona. Se detectaron alcaloides en Ulva rigida (verano). Los lípidos fueron mayoritarios en verano; U. lactuca en invierno mostró monogalactosildiacilglicérido y en otoño, digalactosilacilglicérido y fosfatidilcolina. La actividad inhibitoria de la elongación radicular, que presume actividad antitumoral, fue importante y dosis dependiente, destacándose U. rigida de otoño y primavera (DE50= 480 y 520 µg/ml, respectivamente). Las demás bioactividades resultaron escasas o negativas.
Conclusiones: Las variaciones metabólicas observadas muestran la importancia de considerar las condiciones espacio - temporales al planificar una colecta de ejemplares para su estudio y/o aplicación. Este primer análisis integral de especies de Ulva de la Patagonia Argentina, evidencia su potencialidad como antitumoral.
Palabras claves: Ulva. Fenoles. Antitumoral.
ABSTRACT
Aim: To study species of Ulva from San Jorge Gulf, Patagonia Argentina, integrating biochemical aspects, biological activity and seasonal and spatial variations, to determine their potential application in health.
Methods: Algae were collected seasonally on beaches with and without anthropogenic pollution, then dried and ground and the bioactive compounds extracted with ethanol. Extracts were fractionated using solvents with different polarity. Each fraction was characterized using qualitative chemical reactions and chromatography. Fractions rich in flavonoids were analyzed using HPLC-DAD, and lipids were analyzed using TLC. Biological activity was assayed by using the Artemia salina cytotoxicity test and the xanthine oxidase inhibition assay and by studying the inhibitory effect on root elongation, antioxidant activity and antibacterial activity.
Results: Ulva rigida and Ulva lactuca were identified. Flavonoids, tannins, quinones, lipids, carbohydrates, and steroids were identified in both species. U. rigida showed a much greater amount of flavonoids in autumn and winter, whereas U. lactuca did so in spring and winter, especially kayaflavone. Alkaloids were detected in U. rigida (summer). Lipids were high in summer. U. lactuca showed monogalactosyldiacylglycerol in winter and digalactosylacylglyceride and phosphatidylcholine in autumn. The inhibitory effect on root elongation (assumed as antitumor activity) was significant and dose-dependent, U. rigida showed the highest values in autumn and spring (ED50 = 480 and 520 µg/ml, respectively). Other bioactivities were low or negative.
Conclusions: Metabolic differences showed the importance of considering the seasonal-spatial conditions to plan collection of specimens for their study and/or application. This works is the first integral analysis of Ulva species from Patagonia Argentina and shows their potential to exert antitumor activity.
Key words: Ulva. Phenols. Antitumoral.
Introducción
El ambiente marino presenta una biodiversidad considerable, poco explorada aún en diversas regiones del mundo. Los organismos bentónicos deben competir por la luz, los nutrientes y el espacio en el que habitan, no sólo con especies propias del lugar sino también con organismos invasores que presentan una gran capacidad de colonización y asentamiento. Además deben hacer frente a depredadores, microorganismos patógenos y alteraciones ambientales que los lleva a desarrollar diferentes estrategias de supervivencia1.
Como parte de tales estrategias, se destaca la biosíntesis de una gran variedad de sustancias de defensa, tanto metabolitos primarios como secundarios, los cuales son muy estudiados para un potencial aprovechamiento en la industria farmaceutica2. Se ha descrito una importante diversidad de estructuras químicas, destacándose polisacáridos, proteínas, terpenos, alcaloides, cumarinas, flavonoides y otros polifenoles3,4.
Las algas representan una importante fuente de compuestos bioactivos, destacándose su potencialidad para aplicaciones farmacológicas. En este contexto, se han descrito propiedades antitumoral, antimicrobiana, anticoagulante, antiinflamatoria y antioxidante, entre otras4,5. Por otra parte, en las algas marinas se ha observado una variación importante en la biosíntesis de compuestos, relacionada con factores ambientales tales como temperatura del agua, salinidad, luz y disponibilidad de nutrientes. Gran parte de los parámetros ambientales varían de acuerdo a la estación del año, por lo que resulta probable que los cambios en las condiciones ecológicas puedan estimular, inhibir y/o modificar la biosíntesis de determinados compuestos6.
Las costas patagónicas de la República Argentina presentan una gran diversidad algal. El Golfo San Jorge posee características particulares dada su ubicación geográfica, mostrando zonas con fuerte impacto antrópico además de la presencia de hidrocarburos como ocurre en la zona central, en donde se sitúa la ciudad de Comodoro Rivadavia. Sin embargo, son escasos los estudios que integren análisis bioquímicos de algas verdes de esta región en relación a variaciones estacionales y habitacionales; menos aún que determinen una potencialidad de aplicación.
El género Ulva (División Chlorophyta, Clase Ulvophyceae, Orden Ulvales, Familia Ulvaceae), es uno de los más abundantes en nuestra región, mostrando además una amplia distribución mundial3,7. No obstante, poco se conoce de nuestras especies en cuanto a la composición química relacionada con la bioactividad y al contexto espacio temporal que habitan.
Teniendo en cuenta los aspectos señalados, para el presente estudio se seleccionaron dos especies de Ulva presentes en todas las estaciones del año en las costas de la zona central del Golfo San Jorge, a fin de analizar variaciones bioquímicas y actividad biológica, en relación a variaciones estacionales y habitacionales de las especies.
Materiales y Métodos
Materiales
DPPH (2,2'-difenil-1-picrilhidracilo) y xantino oxidasa, ambos de Sigma-Aldrich Inc; acetonitrilo y ácido acético calidad HPLC, de Merck; los demás reactivos fueron de calidad analítica.
Colecta del material algal y área de estudio
Las algas se colectaron de forma manual y aleatoriamente, durante las cuatro estaciones del año, en el intermareal de dos playas situadas en la zona central del Golfo San Jorge, Patagonia Argentina: Punta Borja, con fuerte contaminación antrópica (45o 52'S, 67o 28'O), y Punta Maqueda, libre de contaminación antrópica (46o 01'S, 67o 35'O) (Figura 1a y 1b). Los ejemplares se limpiaron manualmente para eliminar restos de arena, epífitas y fauna acompañante. Para la clasificación, se emplearon las claves de identificación sistemática7. Una muestra de cada especie de cada colecta estacional se depositó en el Herbario Regional Patagónico (Facultad de Ciencias Naturales, Universidad Nacional de la Patagonia San Juan Bosco) bajo los números de registro 7083 a 7090, correspondientes a ULMV, URMO, ULMP, URMP, URMI, ULMO, URMV, ULMI, respectivamente y 7317 a 7324, correspondientes a URBO, ULBO, URBI, ULBI, URBP, ULBP, URBV, ULBV, respectivamente; en donde, U corresponde a Ulva, L a lactuca, R a rigida, M indica playa Punta Maqueda, B indica playa Punta Borja, mientras que V, O, P, I, se refieren a las estaciones del año verano, otoño, primavera e invierno, respectivamente. El resto del material colectado fue secado a temperatura ambiente, bajo techo y al abrigo de la luz, reducido a polvo en un molinillo de paletas provisto de un tamiz de malla No 20 y pesado.
Obtención y análisis de los extractos alcohólicos
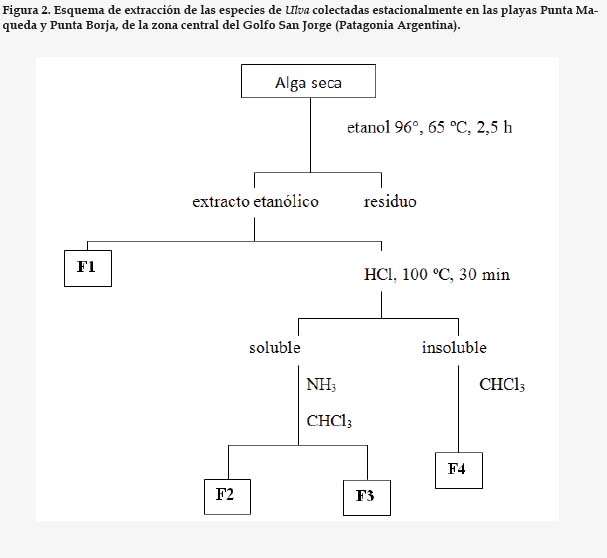
Cada especie colectada (50 g) fue sometida a una extracción con etanol de 96o durante dos horas y media, a 65oC en un baño de agua termostatizado. Los extractos crudos fueron fraccionados mediante cambios de pH y partición con un solvente de menor polaridad (cloroformo), obteniéndose distintas fracciones (Figura 2). Todas las fracciones obtenidas fueron analizadas mediante reacciones cualitativas de identificación de grupos químicos8,9 y perfiles cromatográficos.
Extracción de lípidos y determinación de perfiles cromatográficos
La extracción de lípidos totales se realizó siguiendo la metodología descrita por Folch (1957)10. Cada especie colectada (1 g) fue sometida a una extracción con cloroformo-metanol (2:1), a temperatura ambiente, por 24 h con agitación.
Para la determinación de los perfiles lipídicos se efectuaron cromatografias planares bidimensional (fase estacionaria: Sílicagel G60 F254; fases móviles: 1. cloroformo - metanol - hidróxido de amonio, 65:25:5; 2. cloroformo - acetona - metanol - ácido acético - agua, 50:20:10:10:5; en ambas se utilizó ácido palmítico como estándar) y monodimensional (fase estacionaria: Sílicagel G60 F254 saturada con sulfato de amonio al 2 %; fase móvil: acetona - benceno - agua, 91:30:8). En todos los casos, los cromatogramas se revelaron bajo luz visible, luz UV (365 nm) y con vapores de yodo.
Análisis de flavonoides y derivados
Las fracciones ricas en flavonoides se analizaron mediante cromatografías planares monodimensionales sobre papel Whatman No 1, utilizando como fases móviles: forestal (ácido clorhídrico - ácido acético - agua, 3:30:10); BAW (butanol - ácido acético - agua; 4:1:5) y fenol - agua (3:1), empleando en todos los casos rutina como estándar. Los revelados se efectuaron bajo luz visible, UV (365 nm) sin y con tratamiento previo con vapores de amoníaco; además se empleó el revelador químico FeCl3.
Para la cromatografía líquida de alta performance se utilizó un equipo Waters 1525 equipado con un detector de arreglo de diodos (HPLC-DAD), empleando como referencias un extracto alcohólico de ginkgo, Ginkgo biloba (Ginkgoaceae) y una solución patrón de rutina. La muestra se disolvió en etanol de 96o, se centrifugó a 10000 r.p.m. durante 5 min y se filtró por membrana de 0,20 mm de poro. El volumen de inyección fue de 20 ml. Se utilizó una columna de fase reversa C18 de 250 x 4,6 mm y 5 mm de tamaño de partícula, empleando un gradiente de dos solventes (A, acetonitrilo; B, ácido acético al 0,3 % en agua), mediante el siguiente esquema: 0 a 18 min, 25 % de A; 18 a 55 min, 25 a 46 % de A; 55 a 60 min, 46 a 80 % de A; 60 a 75 min, 80 a 25 % de A. Se trabajó a un flujo constante de 0,8 ml/min.
Ensayos de actividad biológica
Los estudios de actividad biológica comprendieron el bioensayo de citotoxicidad de la Artemia salina11 y determinación de la DE50 mediante el programa propuesto por Finney (1978)12; el ensayo de inhibición de la elongación de raíces de trigo (que presume actividad antitumoral), siguiendo la metodología de Van Puyvelde (1988)13; la actividad antioxidante, utilizando el método de inhibición del DPPH14; el ensayo de inhibición de la xantino oxidasa15; y la actividad antibacteriana mediante la técnica de difusión en ágar16, utilizando cepas tipificadas de Escherichia coli (ATCC 25922), Enterococcus faecalis (ATCC 29212), Staphylococcus aureus (ATCC 29213) y Pseudomonas aeruginosa (ATCC 27853).
Resultados
Las especies determinadas por clasificación sistemática fueron Ulva rigida (C. Agardh) Thuret y U. lactuca L., para ambas playas y en todas las estaciones anuales. En ambos casos se observó que las algas se desarrollan preferentemente sobre sustrato rocoso y piletas de marea de fondo rocoso. La especie más abundante en ambas zonas de colección y durante los cuatro períodos estudiados, resultó ser Ulva rigida. Durante el estudio, la temperatura del agua osciló entre 2 oC (invierno) y 13 oC (verano); con una salinidad de 24 mg/ml y un pH entre 8,1 - 8,3 en ambas playas. Las características morfoanatómicas observadas para ambas especies coincidieron en general con las descritas en bibliografía7.
Los rendimientos de los extractos etanólicos obtenidos se muestran en la Tabla 1. Se destacan los rendimientos correspondientes a U. rigida de otoño colectada en ambas playas, así como el de la misma especie de primavera de Punta Borja. El screening cualitativo reveló la presencia de flavonoides, taninos, lípidos, carbohidratos y esteroides como los principales constituyentes (Tabla 2).
Los flavonoides mostraron una importante distribución, destacándose en U. rigida de Punta Borja colectada en otoño, y en U. lactuca de Punta Maqueda colectada en primavera, así como en ambas especies obtenidas durante el invierno en la playa Punta Maqueda. En general se observaron variaciones entre especies de la misma playa (Tabla 2). Los polifenoles diversos, así como los hidratos de carbono y los esteroides, resultaron presentes en todas las muestras estudiadas. En ningún caso se detectaron triterpenos, cardenólidos ni leucoantocianinas.
El análisis químico cualitativo evidenció también diferencias respecto de las quinonas. Se pudo observar que durante el otoño, sólo U. rigida de ambas playas biosintetizaba sustancias de este grupo químico. Durante el invierno, ambas especies resultaron positivas en Punta Maqueda. En cambio en primavera y en verano, en todos los casos se observó muy baja proporción.
Los alcaloides, otro grupo químico muy activo, pero con menor presencia en algas verdes, fueron detectados sólo en Ulva rigida colectada en Punta Borja en verano. Además en U. rigida de ambas playas en otoño, en U. rigida de Punta Maqueda en invierno y en U. rigida de Punta Borja de verano, se pudo apreciar la probable presencia de sales de amonio cuaternario (Tabla 2).
En cuanto a los lípidos, los rendimientos de las extracciones mediante la técnica de Folch evidenciaron una importante variabilidad. Así, para ambas especies, se evidenció un mayor porcentaje de lípidos en verano, siendo mayores para las especies colectadas en Punta Borja (Tabla 1). Al analizar los perfiles cromatográficos planares para este grupo químico, fue posible observar la presencia de lípidos neutros en todas las especies; sólo U. lactuca de invierno evidenció monogalactosildiacilglicérido, y de otoño, digalactosilacilglicérido y fosfatidilcolina.
Respecto de los flavonoides, al analizar los perfiles cromatográficos planares, se destacaron dímeros de flavonas tipo kayaflavona. Mediante HPLC-DAD, se corroboró este resultado, coincidiendo con el perfil obtenido para el extracto de ginkgo, una planta medicinal rica en este tipo de sustancias que fuera utilizada como referencia.
Por otra parte, la mayoría de los extractos no mostraron citotoxicidad frente al test de la Artemia salina. La viabilidad en el grupo control fue del 100 % y no se observaron alteraciones en el comportamiento de los nauplios. El valor promedio de la DE50 fue superior a 1000 mg/ml en casi todos los extractos ensayados, excepto en aquellos obtenidos de Ulva rigida y de U. lactuca colectadas en Punta Borja en verano, los cuales evidenciaron una DE50 de 249 y 355 µg/ml, respectivamente. En cambio la actividad inhibitoria de la elongación radicular, que presume actividad antitumoral, fue importante en todos los casos y de tipo dosis dependiente, destacándose U. rigida de otoño y primavera con DE50 de 480 y 520 µg/ml, respectivamente. En Punta Borja, las dos especies colectadas durante el invierno, presentaron una DE50 > 1000 µg/ml. En todos los casos analizados existieron diferencias en el crecimiento de las raíces de trigo al aplicar las dos concentraciones utilizadas (0,5 y 0,05 %) de los extractos crudos de ambas especies.
En cuanto a la actividad antioxidante, no resultó relevante en ninguna de las muestras ensayadas. Las únicas que evidenciaron esta actividad, aunque muy baja, fueron U. rigida de Punta Maqueda colectada en otoño (18,3 % de inhibición) y la misma especie colectada en Punta Borja en otoño (16,9 % de inhibición).
En la Tabla 3 se exhiben los resultados de las actividades biológicas mencionadas.
Con respecto a las restantes actividades biológicas, ninguno de los extractos mostró capacidad para inhibir la enzima xantino oxidasa, ni actividad antibacteriana frente a las cepas utilizadas.
Discusion
Las especies presentes en las cuatro estaciones fueron Ulva lactuca y U. rigida. Ambas presentan una amplia distribución mundial. Para Argentina, la primera ha sido descrita en las costas de Buenos Aires, Chubut, Santa Cruz, Tierra del Fuego e Islas Malvinas, en piletas de marea en niveles medios y bajos del intermareal, sobre rocas en niveles bajos del intermareal. U. rigida, por su parte, se extiende en las costas de Santa Cruz, Tierra del Fuego e Islas Malvinas; en general se la encuentra en piletas de marea del intermareal medio y bajo, y sobre Brachydontes purpuratus y Corallina officinalis17.
El screening de las especies colectadas reveló la presencia de flavonoides, polifenoles diversos, hidratos de carbono, lípidos y esteroides como los principales constituyentes. La diversidad de estructuras químicas que pueden biosintetizar las algas marinas varía dependiendo de la especie, el hábitat, la época y las presiones ecológicas a las que están sometidas6. Los lípidos presentaron una gran variabilidad estacional y geográfica, siendo mayores en verano en Punta Borja, playa con fuerte contaminación antrópica. Tales metabolitos resultan importantes como marcadores quimiotaxonómicos y por su relación con la presencia de contaminantes ambientales como lo son los hidrocarburos en nuestras costas. Este tipo de comportamiento ha sido identificado por otros autores18.
Los flavonoides mostraron una importante distribución en las especies estudiadas. Estos compuestos son derivados fenólicos altamente distribuidos en las plantas superiores, pero poco descritos para las algas marinas. Se ha informado la presencia de rutina, hesperidina, morina y otros compuestos semejantes en algas verdes19.
El análisis químico cualitativo evidenció también diferencias estacionales respecto de las quinonas, grupo químico de importancia farmacológica. Se ha descrito la presencia de estos metabolitos en Ulva lactuca colectada en las costas del Mar de Ramanathapuram de la India20. Otros autores informaron sobre estos compuestos para Ulva fasciata de las costas de Tuticorin de la India21. Nuestros resultados son importantes desde el punto de vista de la salud y deben ser considerados especialmente al momento de decidir o proponer la utilización de estas especies para alimentación, debido al riesgo que implica la presencia de quinonas para niños, ancianos y personas con patologías crónicas. Cabe recordar que las quinonas y sus derivados actúan acelerando el peristaltismo intestinal.
Otros metabolitos que deben ser considerados fundamentalmente por su potencial toxicidad, son los alcaloides. Nuestros estudios evidenciaron la presencia de sales de amonio cuaternario en algunas de las muestras. Se ha informado la presencia de alcaloides en Ulva lactuca colectada en verano en Baja California Sur, México22. En nuestro caso, para dicha estación esta especie no mostró este grupo químico, pero si lo hizo U. rigida colectada en verano en Punta Borja; U. lactuca sólo fue positiva para invierno.
Distintos autores23 han descrito baja toxicidad de extractos algales frente al ensayo de la Artemia salina; esto concuerda con los resultados alcanzados en este estudio. Nuestros resultados sugieren una posible actividad antitumoral, ejercida fundamentalmente por mecanismos de acción que no afectan la intercalación en el ADN. Dicha actividad se puede atribuir a los fenoles presentes en los extractos, ya que existen evidencias que indican que compuestos de esa naturaleza química poseen actividad antitumoral, citotóxica y antiproliferativa24. Por otra parte, se ha descrito que la combinación de los ensayos de la Artemia salina (citotoxicidad) y de la inhibición del desarrollo de las raíces de trigo (efecto citostático), permite detectar prácticamente el 100 % de los agentes antitumorales que se evalúan25. En nuestro estudio, Ulva lactuca colectada en verano en Punta Borja evidenció valores de DE50 en ambos ensayos que sugieren una potencialidad interesante como antitumoral.
La baja actividad antioxidante puede atribuirse a la probable ausencia de un sistema o-dihidroxilado en el anillo B de los flavonoides presentes en las especies investigadas, uno de los componentes estructurales responsables de la mencionada actividad26 y a la presencia de dímeros de flavonas. Otros autores27 han descrito como antioxidantes a polisacáridos sulfatados obtenidos de estas especies, los cuales en nuestro trabajo no fueron extraídos ya que las extracciones se realizaron con etanol de 96o a fin de conocer la composición química cualitativa general, y por Folch10 para caracterizar los lípidos.
En cuanto a la capacidad para inhibir la enzima xantino oxidasa, los resultados fueron negativos. Existen algunos estudios que indican que flavonoides tales como apigenina, quercetina, miricetina, isovitexina y genisteína inhiben esta enzima28. Tales flavonoides no se identificaron en nuestro estudio.
Por otra parte, ninguno de los extractos resultó activo frente a las cepas bacterianas utilizadas. Bansemir et al. (2006)29 estudiaron entre otras, a Ulva rigida de las costas de Portugal y de España, no obteniendo actividad antibacteriana importante en coincidencia con nuestros resultados. Sin embargo otros autores observaron diferencias significativas en esta actividad, encontrando que era muy importante en muestras colectadas durante primavera y verano en las costas de Tunez30.
Conclusiones
Es sabido que el hábitat puede modificar los patrones biosintéticos de las especies como una respuesta de supervivencia. Las costas del Golfo San Jorge presentan espacios en donde intervienen las corrientes marinas subtropicales y las subantárticas, a lo cual se suman los cambios que suceden ante la intensa explotación petrolera. En este contexto, nuestros resultados muestran variaciones metabólicas, fundamentalmente para fenoles y lípidos, relacionadas con la estación del año y el hábitat de las especies, así como también de la capacidad inhibitoria sobre el desarrollo radicular y por ende de una potencial actividad antitumoral. De esta forma se pone en evidencia la importancia de considerar tales variaciones espacio - temporales al momento de planificar una colecta de ejemplares para su estudio y/o aplicación, dado que tales diferencias serán determinantes en la puesta en valor del recurso para su utilización racional. Este trabajo es el primero que integra todos los parámetros mencionados para las algas del género Ulva de la Patagonia Argentina.
Conflicto de interés
Los autores del presente trabajo, declaran no tener ningún tipo de relación económica o de otra naturaleza que puedan haber influido en la realización del proyecto y en la preparación de este manuscrito para su publicación.
Referencias
1. Attaway DH, Zaborzky OR. Marine Biotechnology. Pharmaceutical and Bioactive Natural Products. New York: Plenum; 1993. 503 p. [ Links ]
2. De La Calle F. Fármacos de origen marino. Treballs de la SCB. 2007; 58: 141-155. [ Links ]
3. Suleria HAR, Gobe G, Masci P, Osborne SA. Marine bioactive compounds and health promoting perspectives; innovation pathways for drug Discovery. Trends Food Sci Tech. 2016; 50: 44-55. [ Links ]
4. De Lara-Isassi G, Alvarez-Hernámndez S, Lozano-Ramirez C. Actividad antibacteriana de algas marinas de Oaxaca, Pacífico Tropical Mexicano. Rev Nat Mex. 2002; 8(6): 895-898. [ Links ]
5. Marinho-Soriano E, Fonseca PC, Carneiro MAA, Moreira WSC. Seasonal variation in the composition of two tropical seaweeds. Bioresource Technol. 2006; 97: 2402-2406. [ Links ]
6. Boraso A. Elementos para el estudio de las macroalgas de Argentina. Comodoro Rivadavia: Editorial Universitaria de la Patagonia EDUPA; 2013. 207 p. [ Links ]
7. Rondina RVV, Coussio JD. Estudio fotoquímico de plantas medicinales Argentinas (1). Rev Invest Agropec. 1969; VI: 351-366. [ Links ]
8. Harbone JB. Phytochemical Methods. Londres: Chapman and Hall; 1991. 288 p. [ Links ]
9. Folch J, Lees M, Sloane-Stanley G. A simple method for the isolation and purification of total lipids. J Biol Chem. 1957; 226: 497-504. [ Links ]
10. McLaughlin JL. Crown gall tumours on potato disc and brine shrimp lethality: two simple bioassays for higher plants screening and fractionation. En: Hostettmann K, editor. Methods in plant biochemistry. Londres: Academic Press; 1991. p. 1-32. [ Links ]
11. Finney DJ. 1978. Statistical method in biological assay. Londres: Charles Griffin Ltd; 1978. 508 p. [ Links ]
12. Van Puyvelde L, Dekimple N, Ayobaringa F, Costa J, Nshimyukiza P, Boily Y, Schamp N. Wheat rootlet growth inhibition test of Rwandese medicinal plants: active principles of Tetradinia riparia and Diplolophium africanum. J Ethnopharmacol. 1988; 24: 233-246. [ Links ]
13. Koleva II, Van Beek TA, Linssen JPH, Groot A, Evstatleva L. Sreening of Plant Extract for Antioxidant Activity: a comparative Study of Three Testing Methods. Phytochem Anal. 2002; 13: 8-17. [ Links ]
14. Noro T, Oda Y, Toxhio M, Ueno A, Fukushima S. Inhibition of xantina oxidase from the flowers and buds of Daphene genkwa. Chem Pharm Bull. 1983; 31: 3984-3987. [ Links ]
15. Martínez MJ, Molina N, Boucourt E. Evaluación de la actividad antimicrobiana del Psidium guajava L. (Guayaba). Rev. Cubana Plant Med. 1997; 2(1): 12-14. [ Links ]
16. Khairy HM, El-Shafay SM. Seasonal variations in the biochemical composition of some common seaweed species from the coast of Abu Qir Bay, Alexandria, Egypt. Oceanologia. 2013; 55: 435-452. [ Links ]
17. Boraso de Zaixso A. Chlorophytas Marinas de la Argentina. Historia Natural. 2004; 3: 95-119. [ Links ]
18. Kumbhar RD, Rode SP, Sabale AB. Phycochemical Screening of Seaweeds from Sindhudurg District of Maharashtra. Int J Pharm Sci Rev Res. 2014; 29: 77-81. [ Links ]
19. Abirami RG, Kowsalya S. Nutrient and nutraceutical potencials of seaweeds biomass Ulva lactuca and Kappaphycus alvarezii. J Agr Sci Tech. 2011; 5(1): 109-115. [ Links ]
20. Radhika D, Veerabahu C, Priya R, Mohaideen A. A comparative study of biopotential of crude and fractionated extracts of some seaweeds from Tuticorin Coast. Int. J Phytopharmacol. 2014; 5(1): 27-30. [ Links ]
21. Castro-González MI, Pérez-Gil RF, Pérez-Estrella S, Carrillo-Dominguez S. Composición química del alga verde Ulva lactuca. Cienc. Mar. 1996; 22(2): 205-213. [ Links ]
22. Guedes EAC, de Carvalho CM, Lisboa-Ribeiro KA., Lisboa Ribeiro TF, Barros LD, Ferreira de Lima MR, et al. Larvicidal Activity against Aedes aegypti and Molluscicidal. [ Links ]
23. Activity against Biomphalaria glabrata of Brazilian Marine Algae. J Parasitol Res. 2014; 501328. doi:10.1155/2014/501328. [ Links ]
24. Dellai A, Laajili S, Le Morvan V, Robert J, Bouraoui A. Antiproliferative activity and phenolics of the Mediterranean seaweed Laurencia obtusa. Ind Crop Prod. 2013; 47: 252-255. [ Links ]
25. Ticona VR, Nieva TM, Irahola SP, Gimenez TA. Pruebas biológicas destinadas a evaluar citotoxicidad como indicadores de potentes antitumorales. Biofarbo. 1998; 6: 11-16. [ Links ]
26. Van ASA, Van BDJ, Tromp MN, Griffioen DH, Van BWP, Van VWJ. Structural aspects of antioxidant activity of flavonoids. Free Rad Biol Med. 1996; 20: 331-342. [ Links ]
27. Qi H, Zhao T, Zhang Q, Li Z, Zhao Z , Xing R. Antioxidant activity of different molecular weight sulfated polysaccharides from Ulva pertusa Kjellm (Chlorophyta). Appl Phycol. 2005; 17: 527-534. [ Links ]
28. Lin CM, Chem CS, Chem CT, Liang YC, Lin JK. Molecular modeling of flavonoids that inhibits xanthine oxidase. Biochem Biophy Res Commun. 2002; 294(1):167-172. [ Links ]
29. Bansemir A, Blume M, Schröder S, Lindequis U. Screnning of cultivated seaweeds for antibacterial activity against fish pathogenic bacteria. Aquaculture. 2006; 252: 79-84. [ Links ]
30. Trigui, M, Gasmi L, Zouari I, Tounsi S. Seasonal variation in phenolic composition, antibacterial and antioxidant activities of Ulva rigida (Chlorophyta) and assessment of antiacetylcholinesterase potential. Appl Phycol. 2012; 1: 319-328. [ Links ]
31. Rico A, Pérez L, Perales S. Especies del género Enteromorpha (Chlorophyta) en los alrededores de Comodoro Rivadavia, Chubut, Argentina. Naturalia Patagónica. 1993; 1: 103-107. [ Links ]
![]() Dirección para correspondencia:
Dirección para correspondencia:
Osvaldo León Córdoba
Química Biológica II,
GQBMRNP-CRIDECIT,
Facultad de Ciencias Naturales,
Universidad Nacional de la Patagonia San Juan Bosco,
Km 4, s/No, 9000, Comodoro Rivadavia,
Chubut, Argentina.
+54-297-4550339
okylola@gmail.com
Received: 07-04-2016
Accepted: 02-06-2016