INTRODUCCIÓN
El complejo Burkholderia cepacia (cBc) está formado por al menos 20 especies de microorganismos que se encuentran ampliamente distribuidos en el medio ambiente y desde la década del 80 han sido reportados como patógenos oportunistas para el ser humano1,2. El grupo poblacional más afectado por estos microorganismos son los pacientes con fibrosis quística (FQ), a los que pueden causar desde infecciones respiratorias crónicas hasta el llamado ¨síndrome cepacia¨ caracterizado por un rápido deterioro de la salud, muchas veces con consecuencias fatales3. También se han reportado en forma cada vez más frecuente, infecciones intrahospitalarias por el uso de productos contaminados 4,5,6. Los miembros del cBc son resistentes a un gran número de antibióticos por lo que la prevención de las infecciones con estos microorganismos es una constante preocupación 7.
La distribución de especies del cBc es variable según la región y el nicho estudiado. En Canadá, EEUU y parte de Europa, B. multivorans y B. cenocepacia son prevalentes en pacientes FQ 8,9,10. Sin embargo en otros países como Argentina, España y Portugal, B. contaminans está emergiendo como la especie más frecuentemente aislada 11,12,13. Esta última especie, junto a B. lata, integran un subgrupo dentro del cBc denominado Taxón K 14.
Paralelamente a la situación clínica descrita anteriormente, otro aspecto negativo del cBc es la capacidad de sobrevivir y contaminar productos industriales. La presencia de estos microorganismos ha sido reportada en productos de limpieza, cosméticos, desinfectantes, y fármacos 15,16. En este aspecto, los miembros del Taxón K son detectados habitualmente como contaminantes y B. lata ha sido tomada como referencia en estudios sobre efectividad de conservadores y mecanismos de resistencia a los mismos 2,14,17. Por otro lado se han reportado infecciones con B. contaminans asociadas al uso de productos contaminados en países como Alemania y EEUU 4,18,19.
A pesar del potencial riesgo sanitario que implica el cBc como contaminante, la búsqueda de estos microorganismos en el control microbiológico de fármacos, cosméticos y desinfectantes no es obligatoria y no existe una metodología validada para tal fin 20.
Existen diversos medios selectivos para el aislamiento del cBc. Uno de los más usados, especialmente en clínica, es el agar selectivo para Burkholderia cepacia (BCSA) 21. Existe además, una versión comercial de este medio (BCSA modificado), que posee una menor concentración de colorantes que el medio original. Otro medio es el Agar Trypan Blue- Tetraciclina (TB-T) que ha sido empleado en investigaciones del cBc en ambientes naturales 22,23.
Los medios de cultivo para el aislamiento del cBc fueron desarrollados previamente a la definición del Taxón K, y si bien está aceptado que los mismos son adecuados para la recuperación de B. contaminans y B. lata, existe muy poca documentación al respecto. Además, tampoco existen estudios que indiquen la efectividad de tales medios de cultivo en la búsqueda del cBc en el ámbito industrial.
En este trabajo evaluamos la utilidad de los medios TB-T, BCSA y BCSAm para la recuperación de microorganismos del Taxón K mediante un análisis comparativo en términos de productividad, selectividad y especificidad frente a cepas de referencia del cBc, una colección de aislamientos del Taxón K y especies ajenas al cBc.
Para estudiar la posible influencia del origen de los aislamientos en la capacidad de recuperación de los medios de cultivo, incluimos aislamientos de B. contaminans y B. lata obtenidos de pacientes FQ, no FQ y del ámbito industrial. El estudio se realizó utilizando el método ecométrico, que es ampliamente empleando en los laboratorios microbiológicos de diferentes industrias para el control de medios de cultivo 24.
MÉTODOS
Cepas
Se utilizaron cepas de referencia del cBc y aislamientos de B. contaminans y B. lata obtenidos de diversos orígenes. Además, se emplearon cepas de Achromobacter spp., Acinetobacter baumanii, Burkholderia gladioli, distintas especies de Pseudomonas, Proteus vulgaris, Serratia marsecens, Staphylococcus aureus y Stenotrophomonas maltophilia. Los aislamientos del cBc fueron identificados mediante reacción en cadena de la polimerasa (PCR) del gen recA usando los primers BCR1 y BCR2 en las condiciones descriptas originalmente 25. La asignación de especie fue realizada mediante secuenciación del amplicón del gen recA obtenido en la reacción de PCR y la comparación de dichas secuenciascon secuencias depositadas en GenBank utilizando el Basic Local Alignment Tool (BLAST) disponible en: https://blast.ncbi.nlm.nih.gov/Blast.cgi.
Medios de cultivo
Se analizaron tres medios de cultivo selectivos para el aislamiento del cBc: el Agar Selectivo para Burkholderia cepacia (BCSA: cloruro de sodio 5g/L, sacarosa 10g/L, lactosa 10g/L, tripteina 10g/L, extracto de levadura 1,48g/L, bacto-agar 16g/L, solución de cristal violeta 0,02% 10ml/L, solución de rojo fenol 0,8% 10 ml/L, polimixina B 600.000U/L, gentamicina 10mg/L, vancomicina 2,5mg/L) 21; el Agar Selectivo para Burkholderia cepacia comercial modificado (BCSA m - Laboratorio Britania S.A., Argentina). Este medio posee igual composición que el BCSA pero con menor concentración de colorantes (solución de cristal violeta 0,02% 1ml/L, solución de rojo fenol 0,25ml/L); y el Agar Trypan Blue Tetraciclina (TB-T: glucosa 2g/L, bacto-agar 20g/L, L-asparagina 1g/L, bicarbonato de sodio 1g/L, fosfato monobásico de potasio 0,5g/L, sulfato de magnesio heptahidratado 0,1g/L, trypan blue 0,05g/L, tetraciclina 0,02g/L) 22.
Se emplearon además, Agar Tripteína Soja (TSA) (Laboratorio Britania S.A., Argentina) y Caldo Cerebro Corazón (Merck Química Argentina S.A.).
Comparación de medios de cultivo
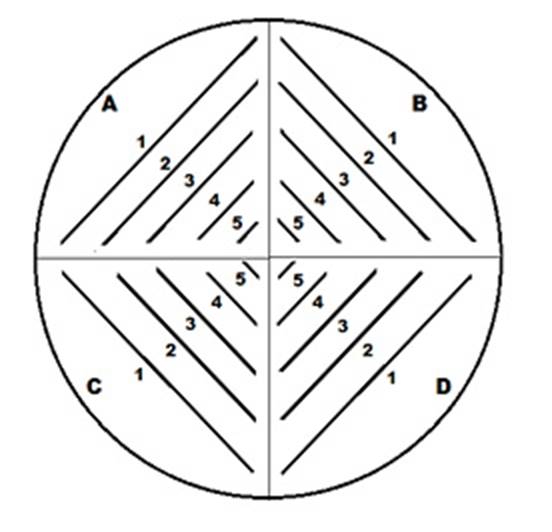
Se utilizó el método ecométrico de Mossel 24. A partir de repiques frescos de las cepas a estudiar, se inocularon con una anzada, tubos con 5 mL de caldo cerebro corazón y se incubaron a 30ºC durante 6 hs. Las placas preparadas con los medios a ensayar se dividieron en cuatro; cada cuarto se rotuló con una letra (A, B, C, D) y se trazaron líneas paralelas (Figura 1). Con anza calibrada, se sembraron 5 uL de la suspensión microbiana crecida en el caldo cerebro corazón sobre las líneas marcadas, siguiendo el orden A1, A2, A3, A4, B1, B2, ..... hasta D4 y finalmente un trazo en el centro de la placa. La misma operación se realizó con todas las cepas a ensayar en los tres medios de cultivo descritos anteriormente (BCSA, BCSAm y TB-T) y en TSA. Las placas se incubaron durante 48 hs a 30ºC, registrándose datos a las 24 hs y a las 48 hs de incubación.
El registro del último trazo en donde se observó crecimiento en cada una de las placas se usó para determinar los índices de crecimiento absoluto (ICA) según valores expresados en Tabla 1 y los índices de crecimiento relativo (ICR) según la siguiente ecuación:
ICR = ICA (en placa de ensayo)x 100/ ICA (en placa control)
El ICA en placa control corresponde al índice de crecimiento absoluto obtenido en las placas de TSA.
Tabla 1: Índices de crecimiento absoluto
| Sector | ICA | Sector | ICA | Sector | ICA | Sector | ICA |
|---|---|---|---|---|---|---|---|
| A1 | 5 | B1 | 10 | C1 | 15 | D1 | 20 |
| A2 | 25 | B2 | 30 | C2 | 35 | D2 | 40 |
| A3 | 45 | B3 | 50 | C3 | 55 | D3 | 60 |
| A4 | 65 | B4 | 70 | C4 | 75 | D4 | 80 |
| A5 | 85 | B5 | 90 | C5 | 95 | D5 | 100 |
ICA: Indice de Crecimiento Absoluto.
Valor asignado al último trazo de crecimiento bacteriano según el método ecométrico de Mossel
Los ensayos se realizaron en duplicado por operadores diferentes. Cuando se obtuvieron más de tres trazos de diferencia en el crecimiento de los duplicados, el ensayo fue descartado y realizado nuevamente.
Criterios de evaluación de los medios: se tuvieron en cuenta tres parámetros utilizados en el control de calidad de medios de cultivo según criterios previamente establecidos26:
i) Productividad: definida como la capacidad de recuperación de los microorganismos de interés. Para este estudio consideramos productividad apropiada, cuando se obtuvieron valores de ICR superiores a 70. ii) Selectividad: dada por la inhibición del crecimiento de microorganismos que no son de interés. Se consideró selectividad adecuada cuando el ICR de aislamientos no pertenecientes al cBc fue inferior a 25. iii) Especificidad: se asocia a la diferenciación de las colonias de los microorganismos de interés por alguna característica determinada (morfología tamaño, color, etc). Dado que muchos aislamientos de B. contaminans presentan pigmentación amarillo verdoso en ciertas condiciones de crecimiento, se evaluó el color de las colonias y la facilidad de observación del mismo.
Tratamiento estadístico de los resultados
Se utilizó el Método no Paramétrico de muestras apareadas de Wilcoxon para comparar el desarrollo de las cepas en estudio en cada uno de los medios y el método de Análisis de la varianza no paramétrico de Kruskal-Wallis para evaluar si existen diferencias en la performance de los medios de cultivo entre los tres grupos de cepas (de referencia, industriales y clínicas).
RESULTADOS
En la mayoría las cepas se observó adecuado crecimiento en TSA, evidenciado por valores de ICA superiores a 70 a las 24hs de incubación y de 90 a las 48 hs. Sólo dos aislamientos de B. contaminans (FFH 2050 obtenido de un paciente FQ y FFH 2026 aislado del ambiente hospitalario) mostraron bajo ICA en TSA con valores inferiores a 60 a las 24 hs y de 80 a las 48 hs de incubación.
El crecimiento en los medios BCSA, BCSAm y TB-T se analizó a través del ICR (Tabla 2). En todos los casos, el crecimiento en los medios analizados arrojó ICAs inferiores o iguales al ICA obtenido en TSA.
Productividad:
En los tres medios de cultivo la productividad resultó mayor a las 48 hs que a las 24 hs de incubación (p<0.001). Asimismo se observó mejor recuperación en los medios BCSA y BCSAm que en el medio TB-T (p<0.001). Los dos medios BCSA mostraron similar productividad tanto con cepas de referencia como con aislamientos del Taxón K. Con 24 hs. de incubación 50% de las cepas ensayadas fueron adecuadamente recuperadas en BCSA; mientras que en BCSAm el mismo resultado se obtuvo en 50% y 57,7% de las cepas de referencia y aislamientos del Taxón K respectivamente. Al incubar durante 48hs, los ICRs de todas las cepas del cBc fueron mayores a 70 en ambos medios.
En la mayoría de los aislamientos del cBc, el ICR obtenido en TB-T resultó significativamente inferior a los alcanzados en los dos medios BCSA. Sólo una cepa (B. cenocepacia B) alcanzó un ICR de 75 en el medio TB-T a las 24 hs de incubación. En tanto que a las 48 hs, en el 66,7% de las cepas de referencia y en 77% de los aislamientos se verificó una productividad adecuada. Con la cepa de referencia de B. pyrrocinia y con cinco aislamientos de B. contaminans los ICRs obtenidos en TB-T fueron menores a 25 aún a las 48 hs de incubación. Dentro del taxón K, con todos los aislamientos de B. lata se obtuvo adecuada productividad a las 48 hs, en contraste con B. contaminans que arrojó valores de ICR inferiores a 70 en el 55% de las cepas estudiadas.
Teniendo en cuenta si el origen de los aislamientos es de pacientes o de otra fuente (productos industriales, agua, ambiente hospitalario), no hubo diferencias de productividad a las 48hs.de incubación en cada uno de los medios ensayados (p>0.45).
Selectividad:
A las 48 hs de incubación, los tres medios evaluados evidenciaron selectividad frente a las cepas ensayadas de Acinetobacter baumannii, Staphylococcus aureus y Pseudomonas fluorescens. Sin embargo, el medio TB-T resultó el menos selectivo debido a los ICRs con valores mayores a 25 obtenidos en mayor cantidad de cepas de otras especies (Achromobacter sp., Burkholderia gladioli, Pseudomonas aeruginosa, Pseudomonas putida, Pseudomonas stutzeri, Proteus vulgaris, Serratia marcescens y Stenotrophomonas maltophilia) (Tabla 2).
Por otro lado, los medios BCSA mostraron selectividad similar entre sí. Dicha selectividad no fue completa ya que se observaron valores de ICR superiores a 25 con los aislamientos ensayados de Achromobacter sp., Burkholderia gladioli, Pseudomonas stutzeri, Proteus vulgaris y Serratia marcescens.
Especificidad:
La cepa de B. cepacia ATCC25416T y el 90,5% de los aislamientos de B. contaminans estudiados desarrollaron pigmentación amarillo verde cuando crecieron en TSA. Este mismo pigmento fue observado en los medios evaluados aunque en menor cantidad de cepas (B. cepacia ATCC25416T y 66,6% de los aislamientos de B. contaminans en los medios BCSA; B. cepacia ATCC25416T y 61,9% de los aislamientos de B. contaminans en TB-T). En este aspecto, si bien es un dato subjetivo que depende de los operadores, cabe señalar que la visualización del pigmento en el medio BCSAm resultó más evidente que en el medio BCSA.
Tabla 2: Índice de crecimiento relativo de las cepas empleadas en este estudio
| Especie | Cepa | Origen | BCSA | BCSA m | TB-T | |||
|---|---|---|---|---|---|---|---|---|
| 24hs | 48hs | 24hs | 48hs | 24hs | 48hs | |||
| B. cepacia | ATCC25416T | Cebolla | 65,0 | 95,0 | 62,5 | 95,0 | 12,5 | 75,0 |
| B. multivorans | LMG13010 T | PFQ | 40,6 | 87,5 | 31,3 | 87,5 | 12,5 | 72,5 |
| B. cenocepacia A | LMG18863 | PFQ | 85,8 | 100,0 | 77,3 | 97,5 | 11,4 | 45,0 |
| B. cenocepacia B | LMG16654 | PFQ | 69,5 | 97,5 | 72,2 | 100,0 | 83,3 | 100,0 |
| B. stabilis | LMG18870 | PFQ | 71,8 | 100,0 | 64,1 | 100,0 | 12,9 | 100,0 |
| B. vietnamiensis | LMG10929 T | Suelo | 77,5 | 100,0 | 67,7 | 100,0 | 12,9 | 73,9 |
| B. dolosa | LMG21820 | PFQ | 67,7 | 100,0 | 70,6 | 100,0 | 8,8 | 75,0 |
| B. ambifaria | LMG19467 | PFQ | 94,6 | 100,0 | 92,0 | 100,0 | 24,4 | 95,0 |
| B. anthina | LMG20983 | PFQ | 56,7 | 100,0 | 64,8 | 100,0 | 8,1 | 37,5 |
| B. pyrrocinia | ATCC15958T | Suelo | 66,7 | 92,5 | 58,3 | 97,5 | 2,8 | 10,0 |
| B. ubonensis | LMG20358T | Suelo | 79,4 | 97,5 | 70,6 | 100,0 | 20,6 | 50,0 |
| B. contaminans | LMG23361T | Oveja con mastitis | 72,8 | 100,0 | 75,7 | 97,5 | 21,3 | 90,0 |
| FFI-6 | Agua purificada | 63,6 | 97,5 | 63,8 | 100,0 | 6,1 | 72,5 | |
| FFI-10 | Agua destilada | 95,0 | 97,5 | 87,5 | 97,5 | 12,5 | 57,5 | |
| FFI-15 | Limpiador desinfectante | 56,7 | 90,0 | 62,3 | 87,5 | 5,4 | 25,0 | |
| FFI-28 | Producto farmacéutico | 25,0 | 94,9 | 16,7 | 92,4 | 13,9 | 25,7 | |
| FFI-29 | Producto farmacéutico | 24,1 | 100,0 | 24,3 | 100,0 | 12,1 | 15,0 | |
| FFI-30 | Producto farmacéutico | 87,5 | 100,0 | 93,8 | 102,6 | 6,3 | 43,6 | |
| FFI-33 | Crema cosmética | 78,9 | 100,0 | 82,0 | 97,5 | 27,2 | 87,5 | |
| FFI-34 | Producto farmacéutico | 65,8 | 100,0 | 60,5 | 100,0 | 39,5 | 82,5 | |
| FFI-35 | Agua purificada | 97,2 | 100,0 | 94,4 | 100,0 | 8,5 | 60,0 | |
| FFI-40 | Agua purificada | 83,8 | 100,0 | 89,2 | 100,0 | 37,9 | 100,0 | |
| FFI-41 | Agua purificada | 58,8 | 100,0 | 67,6 | 100,0 | 29,4 | 62,5 | |
| FFH-1026 | PNFQ | 69,4 | 100,0 | 83,3 | 100,0 | 11,1 | 82,5 | |
| FFH-1050 | PNFQ | 76,4 | 100,0 | 91,7 | 100,0 | 0,0 | 7,8 | |
| FFH-2026 | Ambiente hospitalario | 84,5 | 100,0 | 94,1 | 100,0 | 12,5 | 57,5 | |
| FFH-2004 | PFQ | 77,7 | 100,0 | 90,4 | 100,0 | 35,6 | 85,0 | |
| FFH-2022 | PFQ | 43,9 | 100,0 | 44,2 | 96,7 | 44,2 | 83,3 | |
| FFH-2050 | PFQ | 19,2 | 100,0 | 11,5 | 100,0 | 3,8 | 16,7 | |
| FFH-2053 | PFQ | 82,5 | 100,0 | 87,5 | 100,0 | 20,0 | 70,0 | |
| FFH- 2057 | PFQ | 50,0 | 100,0 | 63,2 | 97,5 | 28,9 | 100,0 | |
| FFH-6002 | Gel de ecografía | 45,6 | 100,0 | 27,4 | 100,0 | 6,1 | 25,0 | |
| B. lata | FFI-17 | Limpiador desinfectante | 96,9 | 100,0 | 100,0 | 100,0 | 31,3 | 97,4 |
| FFI-18 | Limpiador desinfectante | 71,9 | 100,0 | 77,9 | 100,0 | 15,6 | 92,5 | |
| FFI-20 | Limpiador desinfectante | 97,1 | 100,0 | 100,0 | 100,0 | 8,8 | 70,0 | |
| FFI-21 | Limpiador desinfectante | 62,1 | 100,0 | 73,0 | 100,0 | 10,8 | 97,5 | |
| FFH-2067 | PFQ | 55,6 | 97,5 | 61,1 | 100,0 | 33,3 | 87,5 | |
| FFH-2074 | PFQ | 82,4 | 100,0 | 76,1 | 100,0 | 64,7 | 95,0 | |
| Achromobacter spp. | FFH-Ac2001 | PFQ | 5,9 | 50,0 | 5,9 | 52,5 | 26,5 | 67,5 |
| Acinetobacter baumanii | FFH-Ab2002 | PNFQ | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 12,5 |
| Burkholderia gladioli | FFH-2071 | PNFQ | 85,3 | 95,0 | 50,0 | 95,0 | 14,7 | 75,0 |
| Pseudomonas aeruginosa | ATCC9027 | Infección oído | 0,0 | 0,0 | 0,0 | 0,0 | 30,6 | 85,0 |
| ATCC27853 | Hemocultivo | 0,0 | 0,0 | 0,0 | 0,0 | 13,2 | 87,5 | |
| FFI-157 | Limpiador desinfectante | 0,0 | 0,0 | 0,0 | 0,0 | 19,4 | 82,5 | |
| Pseudomonas fluorescens | FFI-178 | Limpiador desinfectante | 0,0 | 22,5 | 2,9 | 25,0 | 11,8 | 22,5 |
| Pseudomonas putida | FFI-180 | Agua purificada | 3,1 | 17,5 | 0,0 | 17,5 | 0,0 | 67,5 |
| Pseudomonas stutzeri | FFA-13 | Agua de río | 10,5 | 80,0 | 10,5 | 72,5 | 5,3 | 80,0 |
| Proteus vulgaris | FFA-22 | Agua de río | 27,8 | 72,5 | 22,2 | 67,5 | 11,1 | 62,5 |
| Serratia marsecens | FFH-S2003 | PNFQ | 0,0 | 77,5 | 6,3 | 80,0 | 21,9 | 97,5 |
| Staphylococcus aureus | ATCC658 | PNFQ | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| Stenotrophomas maltophilia | FFH-Sm2011 | PFQ | 0,0 | 0,0 | 0,0 | 0,0 | 35,3 | 95,0 |
ATCC: American Type Culture Collection, Manassas (USA); LMG: Bacteria Collection, Laboratorium voor Microbiologie, Universiteit Gent (Belgium); PFQ: Paciente Fibroquístico; PNFQ: Paciente No Fibroquístico
DISCUSIÓN
La elección de medios de cultivo selectivos es fundamental en la búsqueda de microorganismos, tanto en clínica como en la industria. Teniendo en cuenta la prevalencia que posee B. contaminans en pacientes FQ en diversas partes del mundo y la frecuencia con que son detectadas las bacterias del Taxón K en productos industriales, realizamos este estudio con el fin de aportar fundamentos teóricos para la elección de un medio de cultivo adecuado para el aislamiento de estos microorganismos. Si bien en el ámbito clínico el medio BCSA es utilizado para la recuperación del cBc, no existen trabajos que fundamenten esta elección para las bacterias del Taxón K. Por otro lado, no existen recomendaciones sobre qué medio usar en el ámbito industrial; y según nuestro conocimiento es el primer estudio donde se evalúa la efectividad de estos medios con aislamientos de dicho origen.
El método ecométrico utilizado en este estudio, a pesar de ser una técnica semicuantitativa desarrollada hace aproximadamente tres décadas, continúa siendo usado para el control de calidad de medios de cultivo en diversas industrias y además es empleado para evaluar y comparar la utilidad de nuevos medios de cultivo 24,27,28,29. Una de sus principales desventajas es que pueden existir diferencias de resultados cuando el análisis es realizado por distintos operadores 27. En nuestro caso, para reducir esta clase de error los ensayos fueron realizados por duplicado por operadores diferentes. Se descartaron y repitieron aquellos ensayos con más de tres trazos de diferencia en el crecimiento observado. Sólo debieron ser repetidos cuatro ensayos: tres cepas del cBc (dos en medio BCSA y una en TB-T) y una cepa de Pseudomonas aeruginosa en TB-T (datos no mostrados).
La composición de los medios estudiados podría explicar las diferencias observadas entre los medios BCSA y TB-T. En el trabajo que describe el medio TB-T se señala que el uso de arginina como única fuente de nitrógeno y trypan blue como inhibidor probablemente afecte el desarrollo de ciertas especies del cBc 22. En este sentido es interesante señalar que con todos los aislamientos de B. lata, el medio de TB-T mostró adecuada productividad, mientras que con B. contaminans sólo se obtuvo con el 47,6% de las cepas ensayadas, por lo cual no es adecuado para la recuperación de dicha especie. Considerando los tiempos de un laboratorio de microbiología, evaluamos los medios de cultivo dentro de las 48hs de incubación. No fue del alcance del estudio analizar si mayores tiempos de incubación hubieran mejorado la productividad del TB-T.
Por otro lado, al igual que otros trabajos donde se evalúan medios de cultivo, estudiamos la selectividad de los medios mediante la inclusión de especies ajenas al cBc aisladas de distintos orígenes 30. Si bien el medio TB-T resultó menos selectivo, la selectividad de los medios BCSA y BCSAm no es completa ya que permiten el desarrollo de diferentes especies, entre ellas B. gladioli. Esta especie, si bien no pertenece al cBc, comparte con estos microorganismos gran número de características31.
En cuanto a especificidad, solamente fue evaluada la posibilidad de observar el pigmento amarillo verdoso producido por B. cepacia y B. contaminans, dado que ninguno de los medios estudiados fue diseñado para producir colonias del cBc con características diferenciales del resto de los microorganismos. Consideramos que para el estudio este parámetro no fue determinante, ya que la producción de pigmentos es variable entre cepas de la misma especie y aún con la misma cepa en distintas condiciones de incubación 2. Sin embargo, gran parte de las cepas de B. contaminans produjeron pigmentos en todos los medios pudiéndose observar mejor en el BSCAm debido a la menor concentración de colorantes. La disminución de concentración de cristal violeta en el BCSAm, podría permitir el crecimiento de microorganismos Gram positivos y afectar la selectividad, esto no fue observado con la cepa de Staphylococcus aureus empleada en el estudio.
Dada la combinación de antibióticos en el medio BCSA, este medio es ampliamente usado para la detección del cBc en muestras clínicas no sería de utilidad para el aislamiento de cepas de origen ambiental32. Recientemente fueron reportados mayor cantidad de genes involucrados en la resistencia a antibióticos en cepas clínicas que ambientales; lo cual avalaría esta idea33. En este sentido, cabe preguntarse a cuál de los dos orígenes (clínico o ambiental) se asemejan los aislamientos obtenidos de la industria. Los aislamientos de agua purificada, podrían tener comportamiento similar a las cepas ambientales; y los aislamientos de productos que por su exposición continua a conservadores y otros agentes biocidas podrían asemejarse a las cepas clínicas. Sin embargo, no se observó diferencia de productividad en relación con el origen de las cepas.
CONCLUSIÓN
Los resultados obtenidos fundamentan la elección de medios BCSA (tanto formulado como el comercial modificado) para el aislamiento de las especies del Taxón K, en condiciones de incubación a 30° C durante al menos 48hs. Los mismos pueden ser empleados no sólo en clínica sino también en la recuperación estas especies a partir de muestras industriales.