Introducción
Antecedentes
La tuberculosis (TB) es una enfermedad infecciosa transmisible de declaración obligatoria en España, causada por el Mycobacterium tuberculosis, que se presenta habitualmente en su forma pulmonar, aunque también puede manifestarse de forma extrapulmonar1,2. Según la Organización Mundial de la Salud (OMS) se estima que una cuarta parte de la población mundial ha sido infectada con M. tuberculosis, siendo este dato equivalente a unos 2 mil millones de personas y una de las principales causas de muerte en adultos1.
Según la Red Nacional de Vigilancia Epidemiológica (RENAVE) el 90% de las personas infectadas son asintomáticas y clasificadas como portadoras de infección tuberculosa latente (ITL)3,4, definida según la OMS como un estado de respuesta inmunitaria persistente a la estimulación por antígenos de Mycobacterium tuberculosis que no se acompaña de las manifestaciones clínicas de una TB activa o infección tuberculosa(4). Se estima que alrededor del 5 al 10 % de las personas con ITL desarrollarán la enfermedad en algún momento de sus vidas3,4,5, siendo el riesgo máximo los 2 primeros años tras la infección, de ahí la importancia del manejo de ITL para la prevención de la enfermedad tuberculosa activa6. Es por ello, que el objetivo del tratamiento de ITL es reducir el riesgo de reactivación7, que a su vez disminuye el riesgo de desarrollar la enfermedad hasta en un 90% y, por lo tanto, a reducir las posibles fuentes de infección8.
La OMS cataloga al tratamiento preventivo de la TB, como una estrategia clave para poner fin a la TB4. Sin embargo, la eficacia de ciertos tratamientos se ha visto limitada por la mala tolerabilidad, la larga duración y baja adherencia9, debido a ello, en los últimos años se han ido haciendo numerosos estudios en relación con diferentes pautas de tratamiento para hacer frente a la ITL.
Diferentes organismos como la OMS en sus Directrices Unificadas sobre TB 20224, los Centros para el Control y Prevención de Enfermedades (CDC)10 y El Plan para la Prevención y Control de la TB en España 201911, recomiendan el uso de los siguientes fármacos: Isoniacida por 6 - 9 meses, Rifampicina (R) 3-4 meses, Rifampicina + Isoniacida (R+H) por 3-4 meses, Rifapentina + Isoniacida (RPT+H) 1-3 meses; que varían en cuanto número de dosis e intervalo pero promueven pautas tratamiento de corta duración.
Según los CDC, las personas con alto riesgo a desarrollar la enfermedad tuberculosa están divididas en dos categorías: 1) las personas que han sido infectadas recientemente con TB, incluidas aquellas que trabajan en instituciones tales como hospitales5 y las personas con condiciones médicas que afectan a su sistema inmunológico; convirtiendo la transmisión de TB en los centros sanitarios de salud, en un importante problema de salud pública12.
Además, es importante señalar que los trabajadores de la salud tienen 2 veces más riesgo de padecer TB en comparación con la población general13, siendo responsables de la transmisión de nosocomial de la TB en los Centros Sanitarios (CS), de ahí que el tratamiento de la ITL sea una estrategia clave para poner fin a la TB. Ello convierte a los Servicios de Prevención de Riesgos Laborales (SPRL) de los CS en un pilar básico, al ser los responsables de la vigilancia de la salud de este grupo de trabajadores.
En consecuencia, los objetivos en la presente revisión sistemática fueron planteados teniendo en cuenta ensayos clínicos aleatorizados que permitan analizar las distintas pautas de tratamiento en los últimos 5 años.
Como objetivos secundarios:
Material y Métodos
Se ha realizado una búsqueda sistemática de artículos científicos publicados entre 2017 y 2022 (última fecha consultada: 24/08/2022) que versan sobre el tratamiento de la ITL, focalizando principalmente en aquellos aspectos relacionados con las pautas de tratamiento y factores relacionados con la adherencia.
La búsqueda de artículos científicos se llevó a cabo en las siguientes bases de datos: MEDLINE (a través de Pubmed), Scopus, WOS (Web of Science), EMBASE (Excerpta Medica dataBASE), IBECS (Índice Bibliográfico Español de Ciencias de la Salud), Cochrane Library Plus, LILACS (Literatura Latinoamericana y del Caribe en Ciencias de la Salud) y CISDOC (Base de Datos de Salud y Seguridad en el trabajo). Se utilizaron los descriptores y ecuaciones de búsqueda que se muestran en la Tabla 1.
Para la elaboración de esta revisión fueron aplicados los criterios PRISMA14. Los artículos fueron, en primer lugar, seleccionados a partir de sus títulos y resúmenes, de acuerdo con los criterios de inclusión y exclusión establecidos previamente (Tabla 2).
La selección se realizó de forma independiente por los autores, revisando en sesión conjunta las controversias y llegando a consenso de su inclusión en la colección a estudio.
Tras este primer cribado se procedió a la recuperación de los artículos a texto completo, a través de la biblioteca del Hospital Universitario Fundación Alcorcón (m-hufa c.17/net).
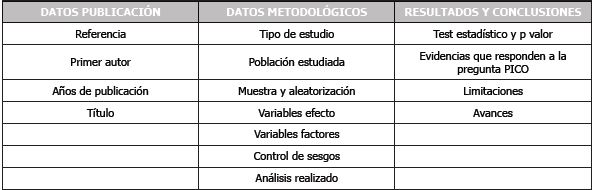
Posteriormente, se realizó una tabla de síntesis de información para la lectura sistemática de los artículos, en la que se recogió información referente a datos de publicación, datos metodológicos, resultados, conclusiones y discusión (Tabla 3).
La evaluación de la calidad metodológica de los artículos seleccionados se realizó utilizando las pautas de las declaraciones de CONSORT15. En la evaluación se puntuó con el valor 1 por cada parámetro cumplido, en caso contrario el valor 0 y en caso de no ser aplicable no se asignaba ningún valor. En aquellos casos en los que existe una subdivisión de parámetros, se realizó una evaluación de forma independiente, otorgando el mismo peso específico a cada uno de ellos, para posteriormente calcular un valor promedio y se asignó el nivel de evidencia de cada estudio mediante los criterios SIGN.
Resultados
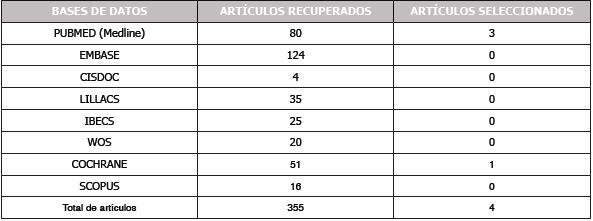
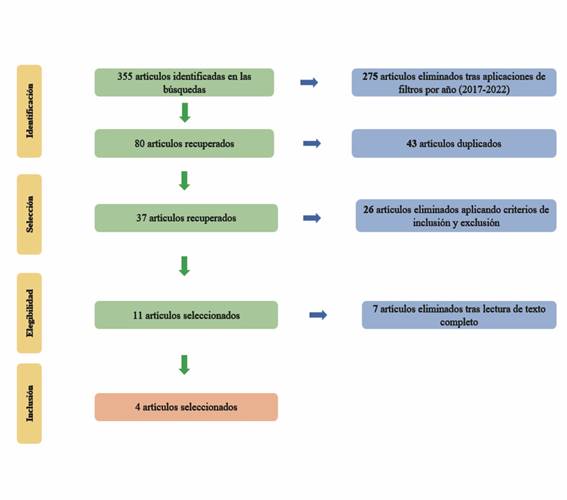
Después de aplicar las estrategias de búsqueda en las distintas bases de datos anteriormente mencionadas (Tabla 1), se recuperaron 354 artículos. Una vez seleccionado el filtro de año (restringiendo a aquellos publicados entre 2017 y 2022), el número de artículos fue de 80. Se identificaron 43 artículos duplicados, obteniéndose 37 artículos de los cuales, 26 fueron eliminados tras aplicar criterios de elegibilidad, obteniéndose 11 artículos. Posteriormente, se procedió a la lectura exhaustiva de los artículos en texto completo en donde se eliminaron 7 artículos al no cumplir con los criterios de elegibilidad, arrojando un total de 4 artículos que fueron incluidos en la presente revisión (Tabla 4 y Figura 1).
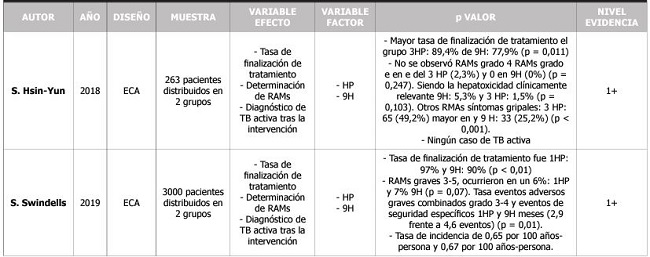
Análisis de estudios contrastados que incluyen pautas con Rifapentina + Isoniazida vs Isoniazida en monoterapia (Tabla 5)
S. Hsin-Yun (2018)
Realizó un ensayo clínico aleatorizado en 263 pacientes, distribuidos en 2 grupos según el tratamiento administrado para la ITL, 3HP (Rifapentina con Isoniazida por 3 meses) y el otro grupo 9H (Isoniacida 9 meses). Se compararon las tasas de finalización de tratamiento y se analizaron en las poblaciones por intención de tratar, además de la determinación de reacciones adversas medicamentosas (RAMs). Hubo diferencias estadísticamente significativas en cuanto a una mayor tasa de finalización de tratamiento el grupo 3 HP: 89,4% respecto al grupo 9H: 77,9% (p = 0,011). La tasa de finalización fue del 69,0 % y 82,1 % para 9H y 3 HP, respectivamente. En cuanto a RAMs se determinó que: 1) la hepatotoxicidad fue clínicamente relevante (elevación por 5 de enzimas hepáticas), al ser más frecuente en 9H que en 3 HP (5,3 % frente a 1,5 %; p = 0,103) y 2). Respecto a otros RAMs (síntomas gripales): 3 HP: 65 (49,2 %) mayor en y 9 H: 33 (25,2 %) (p < 0,001) siendo estadísticamente significativos. No se observó RAMs grado 4. RAMs grado 3 en 3 (2,3%) y 0 (0%) participantes en los grupos de 3 HP y 9H, respectivamente (p = 0,247). Ninguno de los participantes del estudio desarrolló TB activa16.
S. Swindells (2019)
Llevó a cabo un ensayo clínico aleatorizado de 3000 pacientes con VIH, dividido en dos grupos con tratamiento para la ITL: el primer grupo con tratamiento de 1 mes de Rifapentina con Isoniazida diaria (grupo de 1 mes) y el segundo grupo 9 meses de isoniazida (grupo de 9 meses). Al autor buscaba comparar la eficacia y la seguridad de los tratamientos en ambos grupos, siendo el objetivo primario el diagnóstico de tuberculosis, muerte por tuberculosis o causa desconocida, encontrando en el grupo de 1 mes: 32 casos de 1488 pacientes (2 %) y en el grupo de 9 meses: 33 casos de 1498 pacientes (2 %), con una tasa de incidencia de 0,65 por 100 años-persona y 0,67 por 100 años-persona, respectivamente. En cuanto a los objetivos secundarios, el porcentaje de finalización de tratamiento fue del 97% para el grupo de 1 mes y 90% en el grupo de 9 meses, siendo estadísticamente significativo (p<0,001). Los eventos adversos graves 3-5, ocurrieron en un 6% del grupo 1 HP y un 7% en el grupo 9H, no siendo estadísticamente significativo (p=0.07). Sin embargo, la tasa de eventos adversos graves combinados de grado 3-4 y eventos de seguridad específicos (dentro de los que se encuentra niveles elevados de enzimas hepáticas) en 1HP en comparación con 9H meses (2,9 frente a 4,6 eventos) (p=0,01)17.
Análisis de estudios contrastados que incluyen pautas con Rifampicina + Isoniazida vs Isoniazida en monoterapia (Tabla 6)
L. Apriani (2021)
Realizó un ensayo clínico aleatorizado, abierto de Fase 3, por intención de tratar en Indonesia. La muestra estuvo conformada por 1017 participantes, de los cuales 860 eran adultos con ITL, que se asignaron al azar a los grupos: Rifampicina durante 4 meses (4R) e isoniazida durante 9 meses (9H). Como objetivo primario, los autores se plantearon determinar la tasa de finalización del tratamiento (definida como ≥ 80% de las dosis tomadas), que arrojó un resultado significativamente mayor para el grupo 4R, respecto a 9H (78,7 % frente a 65,5 %), con una diferencia de tasas del 13,2 % (IC del 95 %: 7,1-19,2) (p<0.001). Respecto a los objetivos secundarios: los eventos adversos (EA) de grado 3 a 5 en adultos, fueron menores en 4R (0,4%) frente a 9H (2,8%) con una diferencia % de -2.2 (IC al 95%: -3.6 a -0.7) (p=0.004). Respecto al diagnosticó TB activa; se obtuvo 1 participante en el grupo 4R, siendo la tasa de 0,09/100 persona-años, equivalente a 0,21 durante los 28 meses el seguimiento y 4 participantes en el grupo 9H, con una tasa de: 0,36/100 persona-años, equivalente a 0,83 durante los 28 meses el seguimiento, con una ratio de diferencia de: -0,36/100 persona- año, para un IC 95% -0,72 a -0,007 respectivamente. Es decir, que el número total de participantes desarrollaron TB activa, fue significativamente menor en 4R que en 9H18.
En relación con el coste por paciente, L. Apriani determinó fue menor para la pauta 4R que para la 9H (USD 151,9 frente a USD 179,4 en adultos)18.
D. Menzies (2018)
Llevó a cabo un ensayo clínico aleatorizado fase II/III, por intención de tratar abierto realizado en 9 países (Australia, Benín, Brasil, Canadá, Ghana, Guinea, Indonesia, Arabia Saudita y Corea del Sur), en el que se incorporaron 6859 adultos con ITBL, distribuidos en un grupo intervención: Rifampicina por 4 meses (4R: 10 mg/kg. Max 600 mg) y grupo estándar: Isoniacida 9 meses (9H: 5 mg/kg. Max 300 mg). En cuanto al objetivo primario, los autores se plantearon comparar la tasa de infección tuberculosa activa en los 2 grupos durante los 28 meses después de la aleatorización, fue de −0,02 casos por 100 años-persona, determinando que no hubo diferencias significativas entre ambos grupos, IC al 95% −0.4 (−1.5 al 0.8) (p=0.53). Respecto a los objetivos secundarios, se evaluó el porcentaje y tasa de finalización del tratamiento (≥ 80% de las dosis tomadas), en donde se obtuvo que el grupo 4R cumplió con el 78,8% y grupo 9H un 63,2%, es decir con una diferencia de tasa de finalización del 15,1% IC al 95%: (12.7 - 17.4) (p<0,001). En cuanto al número total de los efectos adversos, se observó una menor cantidad en el grupo 4R, en donde se notificaron 80 (2.8%), en comparación con el grupo 9H que obtuvo 162 notificaciones (5.8%), con un IC del 95%: −3.0 (−4.1 to −2.0) (p< 0.001) y en relación con los efectos hepatotóxicos (Grado 3 o 4), estos fueron menores en el grupo de la 4R con 8 (0.3%) notificaciones, en comparación con el grupo 9H con 49 notificaciones (1.7%) IC: −1.2 (−1.7 a −0.7) (p<0.001)19.
Discusión y Conclusiones
Habitualmente se ha usado la monoterapia con Isoniacida durante 6- 9 meses en el tratamiento de la ITL. Sin embargo, en los últimos años la evidencia científica se ha inclinado hacia el uso de pautas más cortas empleando la Rifampicina y Rifapentina.
Los ECA de los autores; S. Hsin-Yun la pauta de Isoniacida + Rifapentina por 3 meses (3HP) vs Isoniazida por 9 meses (9H) y S. Swindells la pauta de Isoniacida + Rifapentina por 1 mes (1 HP) vs Isoniazida por 9 meses (9H), coinciden en que las pautas de HP tienen una mayor tasa de finalización de tratamiento con respecto a 9H. En relación con las RAMs, S. Hsin-Yun no observó RAMs grado 4 en ninguno de los grupos (HP vs H). Sin embargo, al analizar la hepatotoxicidad (elevación x 5 de enzimas hepáticas) obtuvo resultados clínicamente relevantes, siendo este dato concordante con S. Swindells, que obtuvo resultados estadísticamente significativos en relación con los efectos adversos graves 3-5 (elevación x 5 de enzimas hepáticas). Otro aspecto analizado por S. Hsin-Yun fueron síntomas gripales, siendo mayores en 3HP respecto del 9H, con resultados estadísticamente significativos. No obstante, estos fueron bien tolerados. Por otro lado, ambos autores S. Hsin-Yun y S. Swindells, coinciden en que no hubo diferencias entre las pautas de tratamiento en cuanto a la aparición de TB activa.
Asimismo, los autores L. Apriani y D. Menzies, que contrastaron las pautas de Rifampicina 4 meses (4R) vs Isoniazida 9 meses (9H), coinciden en que la pauta 4R tiene una mayor tasa de finalización de tratamiento con respecto a 9H. Además, L. Apriani demostró que la pauta 4R fue no inferior para la prevención de TB activa en relación con la 9H, al encontrar una menor tasa de TB activa en la pauta 4R durante el periodo de seguimiento. Por otra parte, D. Menzies no encontró diferencias estadísticamente significativas entre las pautas analizadas para el desarrollo de TB activa durante el seguimiento. Pese a ello, D. Menzies encontró diferencias estadísticamente significativas respecto a las RAMs, siendo menores en el grupo 4R, dato coincidente con L. Apriani. Respecto a la hepatotoxicidad, D. Menzies encontró menor porcentaje en el grupo 4R respecto al 9H, siendo estos datos estadísticamente significativos.
Si bien es cierto que los estudios en la presente revisión analizan pautas diferentes, todos contrastan una pauta corta combinada respecto a la pauta 9H, siendo estos coincidentes en que las pautas cortas combinadas o en monoterapia, sugieren una mayor tasa de finalización del tratamiento, ausencia TB activa durante el período de seguimiento y menos efectos adversos respecto a la monoterapia con 9H. Estos datos obtenidos en la presente revisión se asemejan a las recomendaciones de la OMS para el tratamiento preventivo de la TB, en donde se incluyen pautas cortas con Rifapentina más Isoniazida durante 1 o 3 meses (1-3 HP) y Rifampicina durante 4 meses (4R)2. Además, la OMS en sus directrices del 2022 espera para un futuro próximo dosis fijas combinadas del esquema de 3HP que facilitarán la administración y el cumplimiento de los esquemas acortados4. Igualmente, los CDC recomiendan 3 HP y 4R20.
En un estudio reciente de modelos transaccionales el autor K.K. Radtke, propone que las pautas basadas en monoterapia con Rifapentina durante 6 semanas podrían tener igual o mejor eficacia que aquellos tratamientos que emplean Isoniazida en monoterapia o combinada, sin sus potenciales efectos tóxicos21.
Sin embargo, se necesitan más investigaciones para contrastar estas pautas y así poder establecer resultados más concluyentes, que garanticen una mejor adherencia al tratamiento de la ITL.