ESTUDIOS EXPERIMENTALES
Como hemos comentado anteriormente (1), los estudios analíticos son aquellos en los que hay grupos de comparación que nos permiten el estudio de asociación de factores de estudio con eventos finales o resultados, como, por ejemplo, el tabaquismo y el desarrollo de AAA.
Dijimos (1) que los estudios analíticos se dividían en observacionales y experimentales. Los primeros ya han sido tratados previamente (2). Trataremos ahora los estudios analíticos experimentales, o simplemente experimentales, ya que podemos considerar siempre que los experimentales son analíticos al existir 2 grupos de comparación, por ejemplo, supervivencia de dos tipos diferentes de tratamiento.
Un diseño experimental es un estudio en el que el investigador asigna el factor de estudio a un grupo de pacientes u otro. Es el investigador el que decide qué sujetos recibirán el fármaco A o el fármaco B. Esta asignación, si es aleatoria (determinada por el azar), reduce notablemente la probabilidad de sesgos, es decir, mejora la validez interna de nuestro estudio. Lo único que garantiza la aleatorización es que los sujetos reciben un tratamiento u otro al azar, pero si la aleatorización funciona correctamente tendremos la ventaja de que los grupos de comparación serán muy parecidos en cuanto a variables que puedan influir en el resultado, así que las diferencias que nosotros encontremos entre los grupos serán atribuibles a la intervención, pues el resto de variables estarán “equiparadas” entre los diferentes grupos.
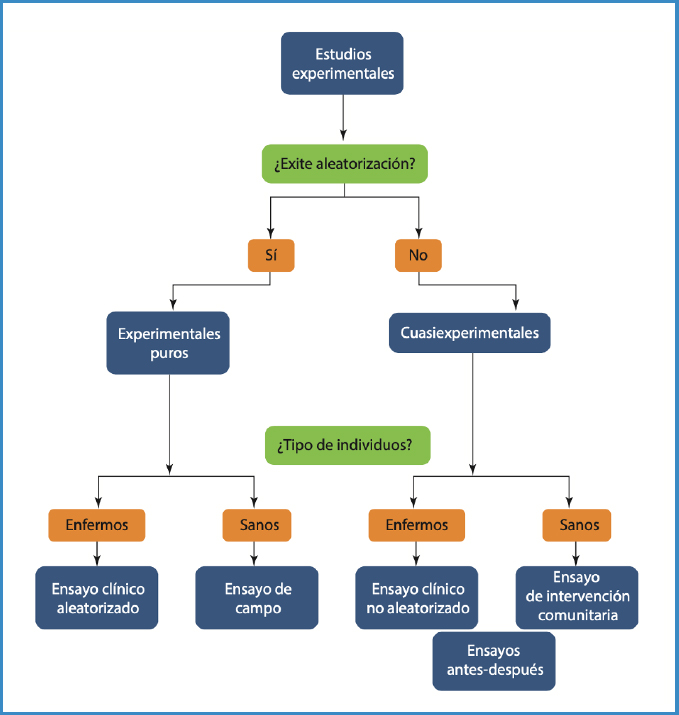
Los estudios experimentales, por tanto, pueden dividirse en dos grandes ramas en función de si existe aleatorización o no, tal y como se muestra en la figura 1.
Para no hacer muy extensa la exposición que nos ocupa, nos centraremos a continuación en desarrollar el estudio experimental que más frecuentemente encontramos en la literatura. El ensayo clínico.
ENSAYO CLÍNICO
Denominamos ensayo clínico (EC) a los estudios prospectivos y experimentales en los que, una vez seleccionada la muestra, se divide aleatoriamente en dos grupos de pronóstico comparable que, idealmente, solo se diferencian en la intervención terapéutica que van a recibir.
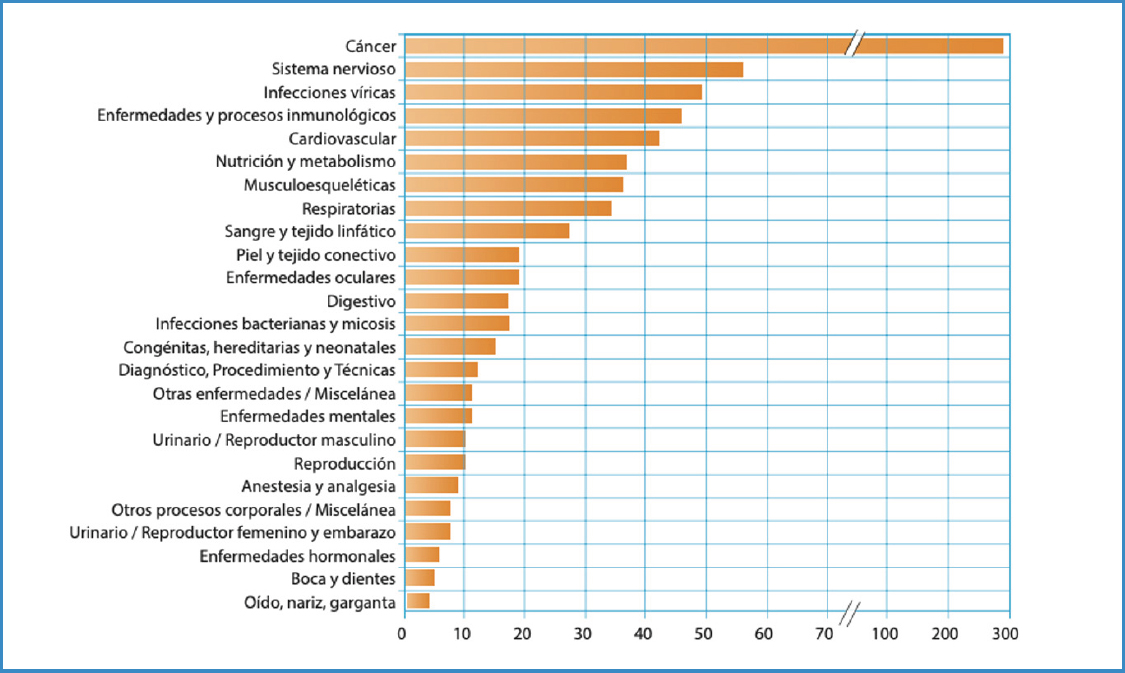
Alejándonos de los argumentos teóricos, ¿el ensayo clínico es una metodología en auge? La Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) señala que la investigación clínica en España, en lo relativo a estos diseños, es considerablemente buena (Fig. 2). Lamentablemente, la parte de estos estudios que es exclusiva de nuestra especialidad es escasa; es la cardiología la especialidad que aglutina la mayoría de los estudios dentro del ítem cardiovascular.
Etapas en la realización de un ensayo clínico
Muchas de las etapas que encontramos en el desarrollo de un ensayo clínico son comunes a otros diseños. Además, apreciaréis cómo son pasos muy lógicos y evidentes dentro del método epidemiológico. Para garantizar una explicación ordenada, van a respetarse las etapas señaladas por Hulley y cols. (1988):
-
- Selección de la cohorte de estudio. Mediante la formulación de los criterios de inclusión, se establecen las características clínicas y sociodemográficas de los pacientes en los que se empleará el fármaco. Los criterios de exclusión se utilizan para rechazar a aquellos pacientes con criterios de inclusión pero que presentan alguna contraindicación, condiciones que pueden afectar a la variable-resultado o a alguna característica que haga complicado su estudio.
En esta etapa también hay que determinar el tamaño muestral. Este ha de ser suficiente para obtener un IC del 95 % de la eficacia, cuyos límites sean clínicamente relevantes.
- Medición de variables basales. Consiste en determinar una serie de variables en los sujetos que cumplen los criterios de inclusión y que han aceptado participar en el estudio (consentimiento informado). Pretendemos aportar una serie de datos que permitan verificar posteriormente que la aleatorización ha sido eficaz y hacer el análisis.
-
- Aleatorización. La aleatorización consiste en asignar por azar, sin que influya ningún factor, los pacientes de la muestra a los dos grupos de intervención, de modo que, si el tamaño muestral es suficientemente grande, se consiga una distribución homogénea de las variables predictoras en ambos grupos. Puede realizarse de tres formas diferentes:
Aleatorización simple. Cada paciente tiene la misma probabilidad de ser asignado a cualquiera de los grupos de tratamiento. Con este método existe riesgo de desigualdad numérica entre grupos. Para que lo entendamos, sería como lanzar una moneda al aire. Cada paciente tendría un 50 % de probabilidades de recibir uno u otro tratamiento, pero la desigualdad en el tamaño de los dos brazos de tratamiento puede ser un problema en el caso de estudios de tamaño muestral reducido.
Aleatorización por bloques. Se establecen bloques de aleatorización, de modo que, en cada uno de ellos, la mitad de los pacientes reciba el tratamiento experimental y la otra mitad, el control. Cada bloque contiene el mismo número de sujetos que reciben uno u otro tratamiento, lo que garantiza el mismo tamaño en los brazos de tratamiento.
Aleatorización estratificada. Los pacientes se dividen en grupos (estratos) homogéneos respecto a alguna variable de interés pronóstico y, posteriormente, se asignan aleatoriamente a uno de los dos grupos de intervención. Por ejemplo, si comparamos la supervivencia de EVAR y OR en el tratamiento de los AAA, sería adecuado estratificar por edad, ya que la edad per se podría justificar la diferente supervivencia entre los grupos de tratamiento.
-
- Aplicación de la intervención. Es importante evitar que tanto investigadores como otros proveedores de cuidados traten de forma diferente a los dos grupos de intervención. Para obviar este hecho, llamado sesgo de cointervención, y que la medición de la variable-resultado pueda estar sesgada por el mismo motivo, se utiliza el enmascaramiento. Los tipos de enmascaramiento son:
- Simple ciego. El paciente desconoce el grupo de tratamiento al que está asignado.
- Doble ciego. Paciente y personal sanitario-evaluador de la variable-resultado lo desconocen.
- Triple ciego. Además de los anteriores, el analista de los datos no sabe el tipo de tratamiento de cada uno de los grupos.
- Análisis de los datos. Debemos tener en cuenta dos aspectos fundamentales. En primer lugar, las pérdidas de sujetos incluidos en el EC ocurridas antes de la aleatorización van a afectar a la capacidad de generalización de los resultados, mientras que las pérdidas posaleatorización pueden afectar a la validez interna. Además, no nos encontramos ante una metodología novedosa para nosotros: el análisis estadístico de los EC es muy parecido al de los estudios de cohortes (2), aunque es más frecuente el uso de métodos no paramétricos y, al tener importancia cuándo ocurre la variable resultado, el empleo de análisis de supervivencia (3).
Fases en la realización de un EC
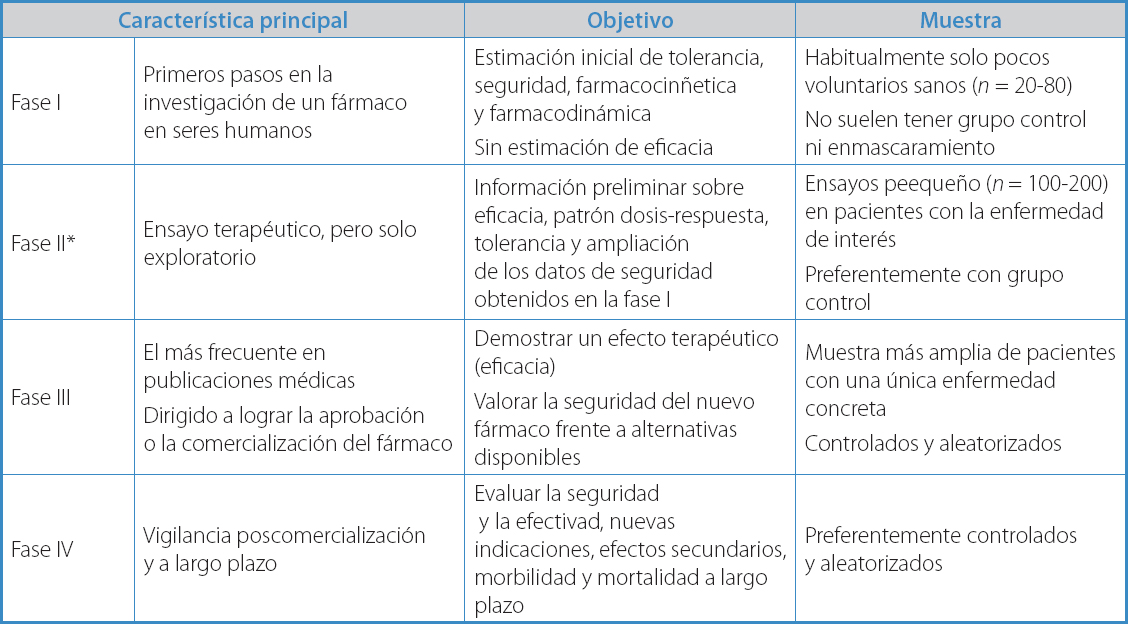
Teniendo en cuenta los objetivos perseguidos en el desarrollo de un medicamento, se distinguen cuatro fases, como figura en la tabla I.
- Ensayo en fase I. Es la primera vez que un fármaco se administra a humanos. Generalmente se realiza con voluntarios sanos (20-80 sujetos) y sin grupo control. Suelen ser EC abiertos, no aleatorizados y, muchas veces, no comparativos. El principal objetivo es evaluar la toxicidad y conocer la dosis única aceptable no tóxica. Se limitan al terreno experimental o a sus efectos farmacocinéticos y farmacodinámicos. Por ejemplo, los estudios de bioequivalencia con genéricos estarían incluidos en esta fase.
- Ensayo en fase II. El principal objetivo es aportar información sobre la relación dosis-respuesta, proporcionando una información preliminar acerca de la eficacia. Se lleva a cabo en pacientes con la enfermedad de interés (n = 100-200). No necesariamente tienen que ser comparativos. Generalmente, este tipo de EC es controlado y con asignación aleatoria del tratamiento.
- Ensayo en fase III. Es el prototipo del EC. Suele ser comparativo con la terapéutica de referencia o con un placebo. Es la investigación clínica más extensa y rigurosa sobre un tratamiento médico. Sirve para establecer la eficacia de un nuevo fármaco y la existencia de efectos adversos frecuentes. Se realiza habitualemente en un grupo mayor de pacientes seleccionados con unos criterios de inclusión/exclusión más laxos, que normalmente se encuentran polimedicados y que permitan hacer una extrapolación de los resultados al resto de la población (validez externa).
- Ensayo en fase IV. Consiste en la realización de un ensayo clínico con fármacos o procedimientos para los que ya existe una indicación aprobada. Esto implica la realización de EC con pacientes de la rutina clínica, lo que permite sacar conclusiones sobre los efectos adversos, ls efectividad e incluso nuevas indicaciones.
Tipos de ensayo clínico
Aunque hemos visto las características generales del EC, algunos de ellos tienen características propias. Los enumeramos a continuación en la tabla II.
- EC por protocolo. Incluye únicamente a aquellos pacientes que han cumplido los requisitos del protocolo o han finalizado el estudio. Tienen el inconveniente de que los sujetos que finalizan los estudios suelen ser aquellos que responden bien al tratamiento. Si solo analizamos a estos sujetos, daremos una imagen sesgada que favorece al tratamiento con más abandonos.
- EC por intención de tratar. El análisis incluye a todos los pacientes que han sido seleccionados y en el grupo en el que fueron asignados, aunque no hayan finalizado el estudio o hayan cambiado de grupo. Es un diseño que se aproxima a la rutina clínica. Infraestiman las diferencias entre los brazos de tratamiento y simulan la realidad clínica.
- EC paralelo. El grupo control recibe el tratamiento a la vez que el grupo experimental, con el fin de controlar el efecto de factores pronósticos que pudieran cambiar a lo largo del tiempo. El análisis de los datos consiste en comparar la diferencia en la variable resultado entre ambos grupos con la variabilidad esperable dentro de cada grupo por el mero efecto del azar. Es muy apropiado en los casos de enfermedades agudas.
-
- EC cruzado. Consiste en que un mismo paciente va a recibir los dos tratamientos objeto de comparación en dos momentos distintos, de modo que el propio paciente sirve de control a sí mismo, lo que permite llevar a cabo el estudio con un tamaño muestral menor al del diseño clásico al reducir la variabilidad. Sus inconvenientes son:
- Al observar el efecto de un tratamiento, se asume la ausencia de sus efectos residuales, anterior (carryover). Debe existir un periodo de blanqueo o de lavado suficientemente largo como para asegurar que no permanecen los efectos residuales del primer tratamiento asignado.
- La secuencia con la que se administran los diferentes tratamientos puede asociarse a respuestas diferentes (efecto periodo).
- Este diseño no es posible cuando la nueva terapia es quirúrgica o el primer tratamiento está dirigido a curar definitivamente la enfermedad (por ejemplo, en enfermedades agudas).
- Resulta difícil adjudicar los efectos secundarios tardíos.
- El análisis estadístico es más complejo que para grupos paralelos y requiere el uso de métodos apareados o de medidas repetidas.
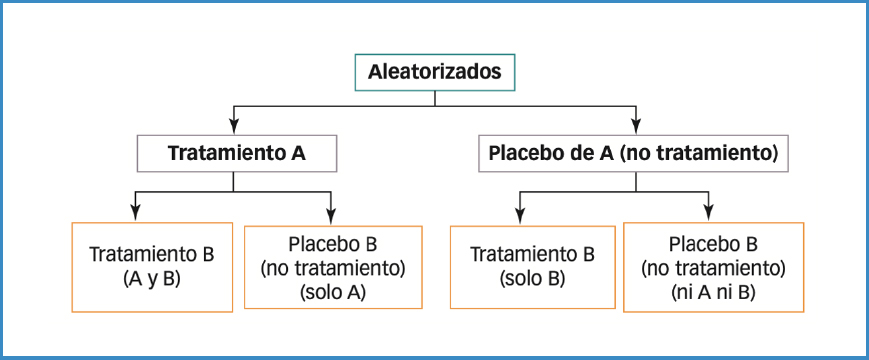
- EC factorial. En ese tipo de diseño se evalúan simultáneamente dos tratamientos distintos en una misma muestra de sujetos, asignándose aleatoriamente los sujetos a uno de los cuatro grupos posibles: A, B, A + B y placebo. En los ensayos factoriales, los placebos que se utilizan tienen que parecerse externamente al tratamiento activo asignado en cada secuencia. Es la razón por la que se habla de “placebo de A” y “placebo de B” para los dos tratamientos, A y B, respectivamente. El diseño factorial habitualmente se utiliza cuando se quiere estudiar la eficacia de terapias combinadas. En este caso, los medicamentos utilizados pueden tener efectos diferentes cuando se combinan, y al final interesará comparar por separado los tres grupos con algún tratamiento activo (Fig. 3).
- EC de no-inferioridad. Habitualmente los EC se realizan con el fin de demostrar la superioridad de un fármaco con respecto a otro. Sin embargo, puede ser útil probar que dos fármacos son al menos igualmente eficaces, con lo que podrá emplearse, por ejemplo, el más barato. Es decir, importa que no sea inferior, de manera que si es igual o superior se considera que el fármaco experimental es “no inferior” comparado con el grupo control. Los ensayos de no inferioridad intentan probar que la nueva terapia es igual, o si fuese peor que el tratamiento habitual, la diferencia entre ambos sería muy pequeña e inferior a delta.
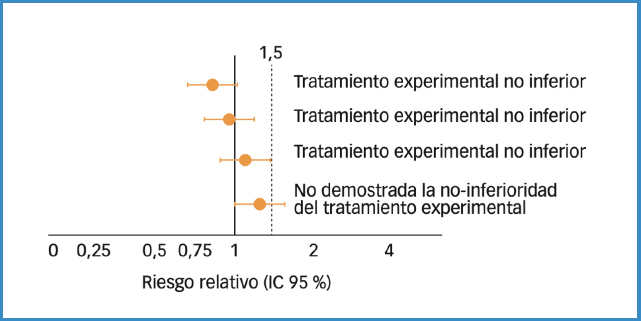
Tal y como se ha comentado, la equivalencia terapéutica se define a partir de los estudios de no inferioridad. En estos estudios es importante tener en cuenta dos aspectos (Fig. 4):
- Valor delta. Es la máxima diferencia clínica que se acepta para definir dos tratamientos con un margen tolerable a peor a cambio de otros beneficios. Por ejemplo, una quimioterapia puede ser levemente inferior a otra, pero si la primera carece de efectos secundarios, diremos que el primer fármaco es no inferior.
- Análisis de las variables. El análisis que suele realizarse es “por protocolo”. Este análisis permite aumentar las diferencias entre los tratamientos, lo que dificulta poder concluir que dos tratamientos son equivalentes, manteniendo la posición más cauta en la interpretación de los resultados.
En la figura 4 se observa un ejemplo de diagrama de no inferioridad con las diferentes posibilidades. El fármaco experimental es mejor que el control si el RR es inferior a 1. Sin embargo, en los estudios de no inferioridad, aunque el RR sea levemente mayor, si no sobrepasa delta, diremos no inferior. Es decir, a cambio de que el experimental no sea tan bueno como el control, ofrece ventajas, como, por ejemplo, menos efectos secundarios, administración oral o administración cada 24 horas en vez de cada 6 horas, entre otros.
Como vemos, el EC es un estudio que puede ser tan simple o tan complejo como queramos hacerlo. Conviene conocer en qué consiste y las opciones de diseño que ofrece para que, como investigadores, sepamos elegir el que más se adecúa a nuestro estudio.